文档内容
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
1.1.2 有机化合物中的共价键
一、选择题
1.下列不属于共价键成键因素的是( )
A. 形成共用电子对
B. 成键原子的原子轨道在空间重叠
C. 形成化学键,体系能量降低,趋于稳定
D. 两原子体积大小要适中
【答案】D
【解析】共价键的本质是在原子之间形成共用电子对。两原子形成共价键时原子轨道发生重叠,两
原子的原子轨道重叠越多,键越牢固,体系的能量也越低,但对成键原子体积的大小没有要求。综
上所述,D项错误。
2.下列说法正确的是( )
A. σ键强度小,容易断裂,而π键强度较大,不易断裂
B. 所有共价键都具有方向性
C. 含有共价键的化合物一定是共价化合物
D. 两个原子之间形成共价键时,最多有一个σ键
【答案】D
【解析】形成σ键的原子轨道的重叠程度比π键大,形成的共价键强,不易断裂,A项错误;s轨
道与s轨道重叠形成的共价键无方向性,B项错误;氢氧化钠是离子化合物,含有氢氧共价键,C
项错误;两个原子之间形成共价键时,单键为σ键,双键或三键中只有一个σ键,D项正确。
3.下列关于碳原子的成键特点及成键方式的理解中正确的是( )
A.饱和碳原子不能发生化学反应 B.碳原子只能与碳原子形成不
饱和键
C.具有六个碳原子的苯与环己烷的结构不同 D.五个碳原子最多只能形成四个碳碳单键
【答案】C
【解析】不饱和碳原子比饱和碳原子活泼,但并不是饱和碳原子不能发生化学反应,如甲烷可以发生
取代反应,A错;碳原子也可以与氧原子形成碳氧双键,与氮原子形成碳氮三键等,B错;苯环是平面结构,
而环己烷中的六个碳原子为饱和碳原子,碳原子之间呈折线结构不能共面,C对;五个碳原子可以呈环,
环状结构为5个碳碳单键。4.下列关于丙烯 的说法错误的是( )
A.丙烯分子中有8个 键、1个 键 B.丙烯分子中3个碳原子都采取 杂化
C.丙烯分子中存在非极性键 D.丙烯分子中最多有7个原子在同
一平面
【答案】B
【解析】烯分子中含有6个C H键、1个C C键和1个 键,其中C C键、C H键均
为 键, 键中有1个 键和1个m键,则丙烯分子中有8个σ键和1个 键,A正确;甲
基C原子采取 杂化,双键C原子采取 杂化,B错误;同种非金属元素原子之间形成非极性
键,则丙烯分子中碳原子间存在非极性键,C正确;碳碳双键为平面结构,甲基为四面体结构,通
过单键旋转,丙烯分子中最多有7个原子在同一平面上,D正确。
5.下列关于苯乙炔的说法错误的是( )
A.该分子有8个 键和5个 键
B.该分子中碳原子有sp和 杂化
C.该分子中不存在非极性键
D.该分子中有8个碳原子在同一平面上
【答案】AC
【解析】苯乙炔分子中含有14个 键,苯环中有1个大 键, 键中有2个 键,故共含
有3个 键,故A错误;苯环中碳原子都采取 杂化,碳碳三键碳原子采取sp杂化,该分子中
碳原子有sp和 杂化,故B正确;同种原子间形成的共价键为非极性键,该分子中碳原子间形成
非极性键,故C错误;苯环是平面形结构,碳碳三键是直线形结构,因此该分子中有8个碳原子在
同一平面上,故D正确。6.对于分子式为 的有机化合物结构的说法中不正确的是( )
A.可能是分子中只有一个双键的链烃B.分子中可能有两个双键
C.分子中可能只含有一个三键 D.分子中含有一个双键的环烃
【答案】A
【解析】含5个碳原子的饱和烃应含有12个氢原子, 较饱和烃少了12-8=4个氢原子,每减少
2个氢原子就增加一个不饱和度,所以该分子结构有四种可能:①两个双键,②一个三键,③一个
双键和一个环,④两个环。故A项不合理。
7.下列关于σ键和π键的说法不正确的是( )
A. σ键能单独形成,π键不能单独形成
B. σ键可以绕键轴旋转,π键不能绕键轴旋转
C. 双键中一定有一个σ键,一个π键,三键中一定有一个σ键,两个π键
D. CH —CH 、CH ==CH 、CH≡CH中的σ键都是C—C键,所以键能都相同
3 3 2 2
【答案】D
【解析】单键中只有一个σ键,双键中有一个σ键,一个π键,三键中有一个σ键,两个π键,π
键不能单独形成,A、C项正确;σ键的电子云呈轴对称,π键的电子云呈镜面对称,π键不能绕键
轴旋转,B项正确;三种分子中还含有C—H σ键,D项错误。
8.下列说法不正确的是( )
A. π键是原子轨道以“肩并肩”方式相互重叠而形成的
B. 2个原子形成的多重共价键中,只能有一个是σ键,而π键可以是一个或多个
C. s电子与s电子间形成的键是σ键,p电子与p电子间形成的键是π键
D. 共价键一定有原子轨道的重叠
【答案】C
【解析】原子轨道以“头碰头”方式相互重叠形成的共价键为σ键;以“肩并肩”方式相互重叠形成的
共价键为π键。σ键是轴对称,而π键是镜面对称。分子中所有的单键都是 σ键,双键中有一个σ
键,一个π键,叁键中有一个σ键,两个π键。
9.下列有关σ键和π键的说法错误的是( )
A. 含有π键的分子在反应时,π键是化学反应的积极参与者
B. 当原子形成分子时,首先形成σ键,可能形成π键
C. 有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D. 在分子中,化学键可能只有π键而没有σ键
【答案】D
【解析】本题主要考查σ键和π键的形成。由于π键的键能小于σ键的键能,所以反应时易断裂,A正确;在分子形成时为了使其能量最低,必然首先形成 σ键,根据形成原子的核外电子排布来判
断是否形成π键,所以B正确;C正确,像H、Cl原子跟其他原子只能形成σ键,D错误。
10.下列化学反应中不属于取代反应的是( )
A. CH Cl +Br CHBrCl +HBr
2 2 2 2
B. CH OH+HCl―→CH Cl+H O
3 3 2
C. 2Na+2H O===2NaOH+H ↑
2 2
D. CH CH Br+H O CH CH OH+HBr
3 2 2 3 2
【答案】C
【解析】选项A是CH Cl 分子中的一个氢原子被溴原子所取代,属于取代反应;
2 2
选项B是CH OH分子中的原子团-OH被氯原子所取代,属于取代反应;
3
选项C是无机物之间的置换反应,不是取代反应;
选项D是CH CH Br分子中的溴原子被原子团-OH所取代,属于取代反应。
3 2
11.已知正四面体形分子E和单质分子G反应,生成四面体形分子L和分子M(组成E分子的元素的
原子序数小于10,组成G分子的元素为第三周期的元素),如图所示,则下列判断中不正确的是(
)
A. 常温常压下,E、L均为气态有机物
B. E是一种含有10个电子的分子
C. 上述反应的类型是置换反应
D. 上述4种物质中有3种为共价化合物
【答案】C
【解析】正四面体形分子E,组成E分子的元素的原子序数都小于10,E由两种元素组成,灰色球
只形成一个共价键,所以是H,黑色球表示C,所以E是甲烷;直线形分子G,组成G分子的元素
为第三周期的元素,且G是双原子分子,所以G是Cl ,该反应是甲烷和氯气发生取代反应生成一
2
氯甲烷和氯化氢,即L是一氯甲烷,M是氯化氢。常温常压下,甲烷、一氯甲烷均是气体,A项正
确;E是甲烷分子,含有10个电子,B项正确;甲烷中的氢原子被氯原子取代生成一氯甲烷,属于
取代反应,生成物中没有单质,不是置换反应,C项错误;四种物质中甲烷、一氯甲烷和HCl属于
共价化合物,所以4种物质中有3种为共价化合物,D项正确。
12.有下列三种物质①乙醇、②碳酸、③水,它们与钠反应产生氢气的速率由大到小的顺序是(
)
A. ①>②>③ B. ②>①>③ C. ③>①>② D. ②>③>①【答案】D
【解析】物质的酸性越强,越容易电离产生氢离子,与钠反应生成氢气的速率就越大。碳酸、水、
乙醇三种物质电离产生氢离子的能力依次减弱,它们与钠反应产生氢气的速率由大到小的顺序是
②>③>①。
13.有人认为化合物中数量、品种最多的是ⅣA族的碳的化合物(有机化合物),下列关于其原因的叙
述中不正确的是( )
A.碳原子既可以跟自身又可以跟其他原子(如氢原子)形成4个共价键
B.碳原子性质非常活泼,易跟多种原子形成共价键
C.碳原子之间既可以形成稳定的单键,又可以形成双键和三键
D.多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合
【答案】B
【解析】碳四价理论是有机化学中的基础理论,4次成键机会造成多种成键方式,使由碳形成的有机
物丰富多彩。
二、填空题
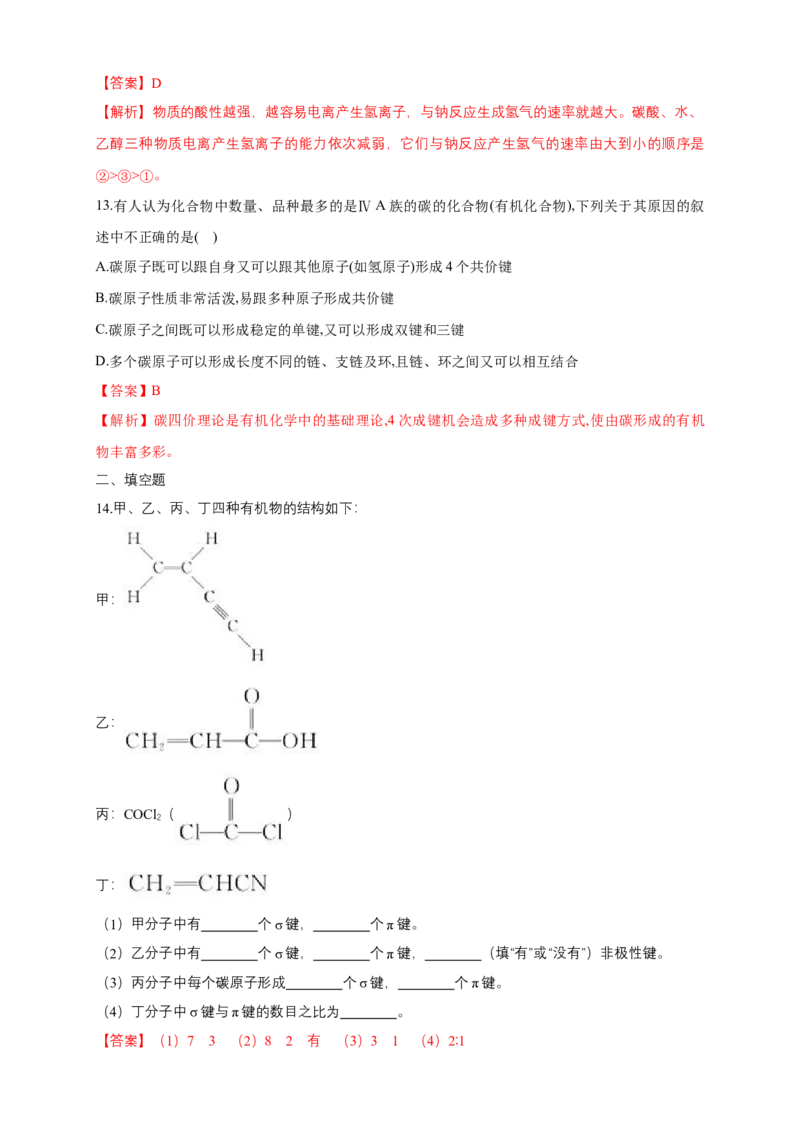
14.甲、乙、丙、丁四种有机物的结构如下:
甲:
乙:
丙:COCl ( )
2
丁:
(1)甲分子中有 个σ键, 个π键。
(2)乙分子中有 个σ键, 个π键, (填“有”或“没有”)非极性键。
(3)丙分子中每个碳原子形成 个σ键, 个π键。
(4)丁分子中σ键与π键的数目之比为 。
【答案】(1)7 3 (2)8 2 有 (3)3 1 (4)2∶1【解析】(1)甲分子中除5条单键全是σ键外,双键中1个是σ键,另1个是π键,三键中1个是
σ键,另2个是π键。故甲分子中σ键总数为7,π键总数为3。
(2)乙分子中有3个C—H σ键,2个C—C σ键,2个C—O σ键,1个O—H σ键;C===C
和C===O中分别有1个π键;有C===C、C—C非极性键。
(3)丙分子中C与O原子之间形成1个σ键和1个π键,C与两个Cl原子之间分别形成1个σ键。
(4)丁分子中含有1个C===C键,1个 键,3个C—H键和1个C—C键,故丁分子
中共有6个σ键和3个π键。
15.为了探究乙醇和钠反应的原理,做如下实验:
甲:向试管中加入3 mL乙醇,放入一小块钠,观察现象,并收集、检验产生的气体。
乙:向试管中加入3 mL乙醚(CHCHOCH CH),放入一小块钠,无气体产生。
3 2 2 3
回答以下问题:
(1)简述检验实验甲中产生的气体的方法及作出判断的依据:_____________________。
(2)从结构上分析,选取乙醚作参照物的原因是_____________________________。
(3)实验甲说明____________________________________________________________;
实验乙说明_______________________________________________________________;
根据实验结果,乙醇和金属钠反应的化学方程式应为____________________________
________________________________________________________________________。
【答案】(1)将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁
有水滴,则证明该气体是氢气
(2)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基
(3) 羟 基 氢 可 与 钠 发 生 置 换 反 应 乙 基 上 的 氢 不 能 与 钠 发 生 反 应 2CHCHOH +
3 2
2Na―→2CH CHONa+H↑
3 2 2
【解析】(1)试管中加入乙醇,放入一小块钠,二者会发生反应得到乙醇钠和氢气,氢气的检验方法:
将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则
证明该气体是氢气。
(2)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,故选取乙醚作参照物,说明与钠发生反应的
为羟基。
(3)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,向试管中加入 3 mL 乙醚
(CHCHOCH CH),放入一小块钠,不发生反应,故与钠反应的物质中需含有羟基氢,羟基中的氢
3 2 2 3
原子能和金属钠反应得到氢气。16.为了测定乙醇的结构式,利用乙醇和钠的反应,设计如图1装置进行实验,在烧瓶中放入足量的
钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体
积。
(1)实验前检验该装置的气密性的实验操作是____________________________________。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认
为___________(填“正确”或“不正确”)。
(3)若实验中所用乙醇含有少量水则实验结果将_______(填“偏大”或“偏小”),若实验开始
前b导管内未充满水则实验结果将________(填“偏大”或“偏小”)。
(4)若测得有1.15 g C HO参加反应,把量筒c中的水的体积换算成标准状况下H 的体积为280
2 6 2
mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确______。
【答案】(1)连接好装置,关闭分液漏斗的活塞,将右侧导管插入水槽,微热烧瓶,右侧导管若
有气泡冒出,冷却后形成一段水柱,且一段时间内水柱不变化,证明装置气密性良好
(2)不正确
(3)偏大 偏小
(4)Ⅰ
【解析】分析解题的基点:测定乙醇结构的实验原理、实验误差及原因分析、实验的相关问题。
①探究确定乙醇的结构
测定乙醇结构的实验原理是用一定量的乙醇与钠反应,测定产生氢气的体积,
由此计算出1 mol 乙醇分子中被置换氢原子的物质的量。
计算1.15 g C HO的物质的量n= = = 0.025 mol,
2 6
生成氢气的物质的量n=V/V = = 0.0125 mol,
m
即1 mol C HO~0.5 mol H~1mol H,
2 6 2
说明1 mol C HO分子中只有1mol 氢原子被钠置换,
2 6
也就是说C HO分子中有1个氢原子与其他5个氢原子不同,其结构应为Ⅰ。
2 6②实验误差分析(影响测定氢气体积大小的因素)。
等质量的水与钠反应产生氢气比乙醇与钠反应放出气体多,如果乙醇含有水,则导致实验结果偏大。
如果实验开始前b导管内未充满水时,排到量筒中的水的体积偏小,则导致实验结果偏小。
③实验相关问题与关键。
装置气密性良好(检查方法)、准确确定乙醇的用量(称其质量或量其体积)、金属钠要足量(若乙醇为
nmol则钠大于nmol)、准确测定氢气的体积(测定的方法)等。