文档内容
★秘密·2023年3月17日10:00前
重庆市 2022-2023 学年(下)3 月月度质量检测
高三化学
2023.3
3
【命题单位:重庆缙云教育联盟】
注意事项:
1.答题前,考生务必用黑色签字笔将自己的姓名、准考证号、座位号在答题卡上填写清楚;
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,在试卷上作答无效;
3.考试结束后,请将本试卷和答题卡一并交回;
4.全卷共6页,满分100分,考试时间75分钟。
一、选择题(共 14 小题,每题3 分,共42分)
1.下列过程中不发生化学变化的是
A.石油裂解 B.煤的液化 C.石油分馏 D.煤的干馏
2.化学与材料、生活和环境密切相关。下列有关说法中错误的是
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.大量使用化肥和农药,以提高农作物产量
C.“绿色化学”的核心是使原料尽可能全部转化为目标产物
D.不随意丢弃旧电池,生活垃圾分类放置
3.下列叙述正确的是
A.1molH O的质量为18g/mol
2
B.CH 的相对分子质量为16
4
C.11.2LNO与11.2LO 混合后的分子数目为N
2 A
D.标准状况下,1mol任何物质体积均为22.4L
4.下列离子方程式书写正确的是
A.Cl 与H O反应:Cl +H O=2H++Cl-+ClO-
2 2 2 2
B.碳酸氢钠溶液与稀硫酸反应:CO2+2H+=CO ↑+H O
3 2 2
C.Fe (SO ) 溶液与氨水反应:Fe3++3OH-=Fe(OH) ↓
2 4 3 3
D.Na与H O反应:2Na+2H O=2Na++2OH-+H ↑
2 2 2
5.下列电离方程式错误的是
A.HNO →H++NO B.CaCO Ca2++CO2
3 3 3 � 3
高三化学试卷 第 1 页 共 6 页
学科网(北京)股份有限公司C.NaHSO →Na++H++SO2 D.NH •H O NH+OH-
4 4 3 2 � 4
6.将一定浓度的硫酸钾溶液和氯化钡溶液混合后,已知其中氯离子的浓度为0.2mol·L-1,硫酸根离子浓度
为0.2mol·L-1,则混合后K+的物质的量浓度为
A.0.2mol·L-1 B.0.4mol·L-1 C.0.6mol·L-1 D.0.8mol·L-1
7.对于2A(g)+B(g)⇌4C(g) △H<0,假设反应处于恒容容器中的平衡状态,在此条件下,一定会增大气体
C浓度的措施是
A.增加A B.升高温度 C.增大压强 D.移出C
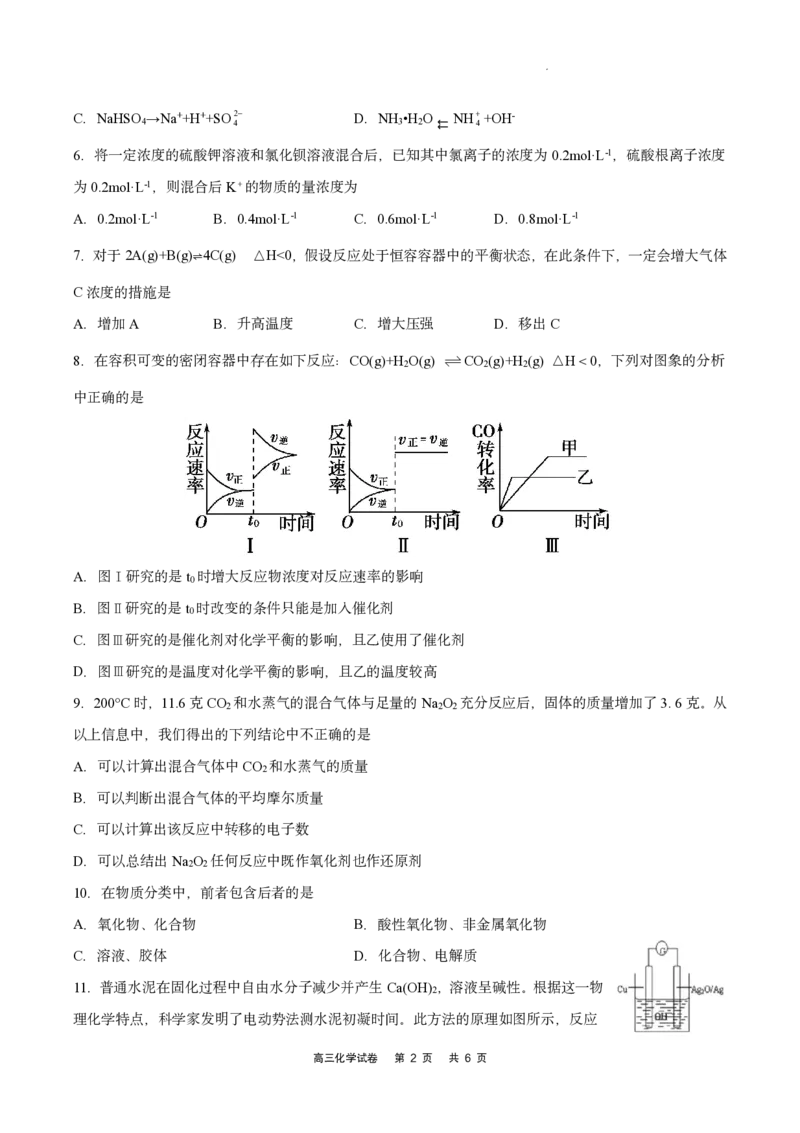
8.在容积可变的密闭容器中存在如下反应:CO(g)+H O(g) CO (g)+H (g) △H<0,下列对图象的分析
2 2 2
中正确的是
A.图 研究的是t 时增大反应物浓度对反应速率的影响
Ⅰ 0
B.图 研究的是t 时改变的条件只能是加入催化剂
Ⅱ 0
C.图 研究的是催化剂对化学平衡的影响,且乙使用了催化剂
Ⅲ
D.图 研究的是温度对化学平衡的影响,且乙的温度较高
Ⅲ
9.200°C时,11.6克CO 和水蒸气的混合气体与足量的Na O 充分反应后,固体的质量增加了3.6克。从
2 2 2
以上信息中,我们得出的下列结论中不正确的是
A.可以计算出混合气体中CO 和水蒸气的质量
2
B.可以判断出混合气体的平均摩尔质量
C.可以计算出该反应中转移的电子数
D.可以总结出Na O 任何反应中既作氧化剂也作还原剂
2 2
10.在物质分类中,前者包含后者的是
A.氧化物、化合物 B.酸性氧化物、非金属氧化物
C.溶液、胶体 D.化合物、电解质
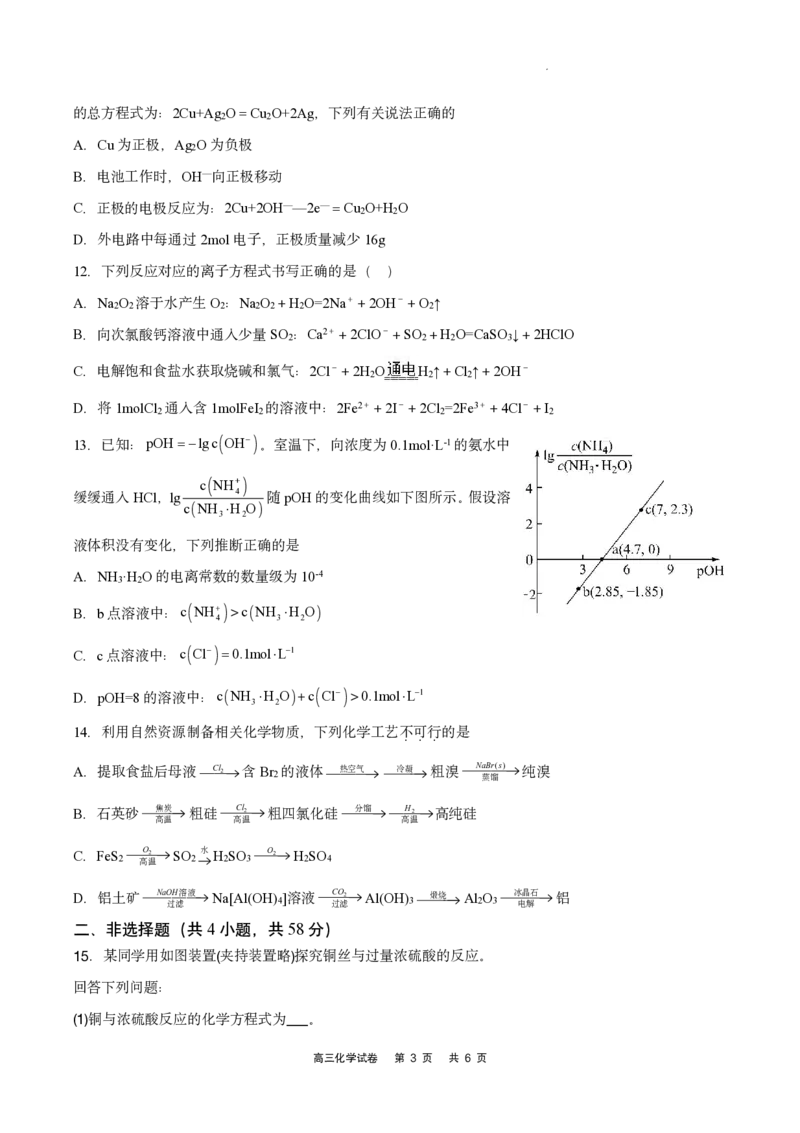
11.普通水泥在固化过程中自由水分子减少并产生Ca(OH) ,溶液呈碱性。根据这一物
2
理化学特点,科学家发明了电动势法测水泥初凝时间。此方法的原理如图所示,反应
高三化学试卷 第 2 页 共 6 页
学科网(北京)股份有限公司的总方程式为:2Cu+Ag O=Cu O+2Ag,下列有关说法正确的
2 2
A.Cu为正极,Ag O为负极
2
B.电池工作时,OH—向正极移动
C.正极的电极反应为:2Cu+2OH——2e—=Cu O+H O
2 2
D.外电路中每通过2mol电子,正极质量减少16g
12.下列反应对应的离子方程式书写正确的是( )
A.Na O 溶于水产生O :Na O +H O=2Na++2OH-+O ↑
2 2 2 2 2 2 2
B.向次氯酸钙溶液中通入少量SO :Ca2++2ClO-+SO +H O=CaSO ↓+2HClO
2 2 2 3
C.电解饱和食盐水获取烧碱和氯气:2Cl-+2H O H ↑+Cl ↑+2OH-
2 2 2
D.将1molCl 通入含1molFeI 的溶液中:2Fe2++2I-+2Cl =2Fe3++4Cl-+I
2 2 2 2
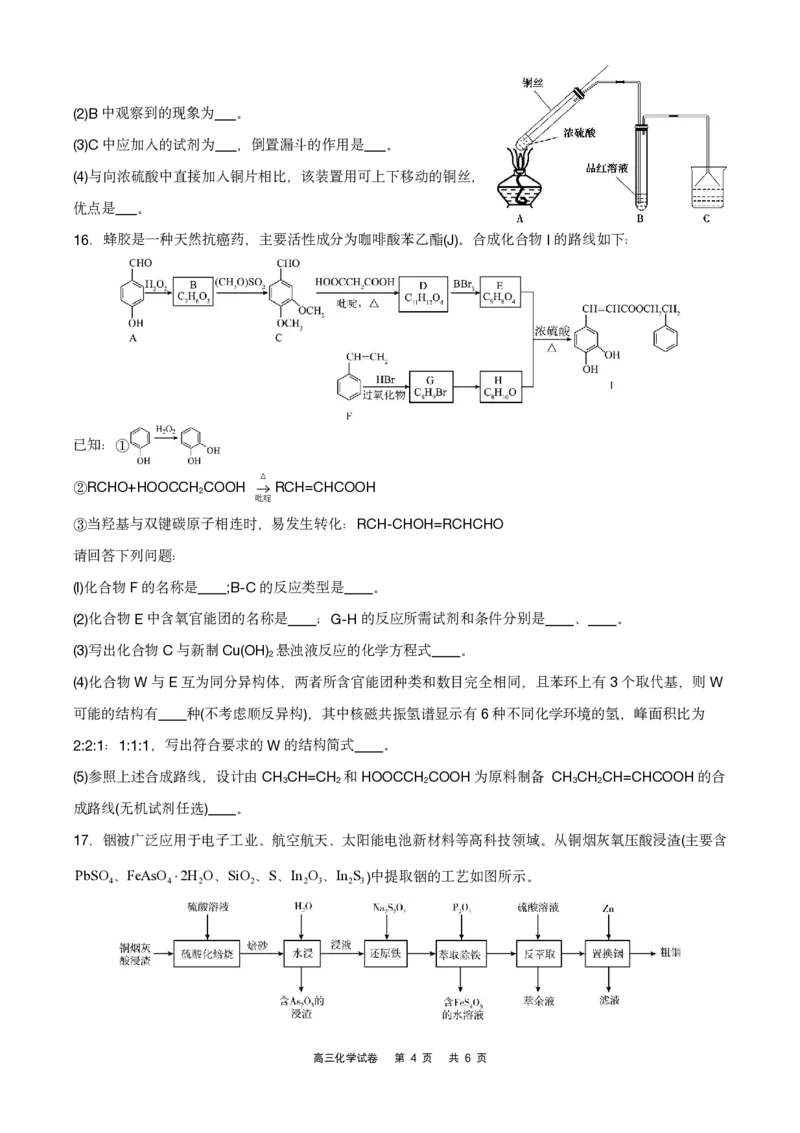
13.已知:pOHlgc
OH
。室温下,向浓度为0.1mol·L-1的氨水中
c
NH+
4
缓缓通入HCl,lg 随pOH的变化曲线如下图所示。假设溶
cNH H O
3 2
液体积没有变化,下列推断正确的是
A.NH ·H O的电离常数的数量级为10-4
3 2
B.b点溶液中:c NH cNH H O
4 3 2
C.c点溶液中:c Cl 0.1molL1
D.pOH=8的溶液中:cNH H Oc Cl 0.1molL1
3 2
14.利用自然资源制备相关化学物质,下列化学工艺不可行的是
...
A.提取食盐后母液Cl2含Br
2
的液体热空气 冷凝粗溴Na
蒸
B
馏
r(s)纯溴
B.石英砂焦炭粗硅Cl2粗四氯化硅分馏H2高纯硅
高温 高温 高温
C.FeS 2 高 O 温 2SO 2 水 H 2 SO 3 O2H 2 SO 4
D.铝土矿NaOH溶液Na[Al(OH) ]溶液CO2Al(OH) 煅烧Al O 冰晶石铝
过滤 4 过滤 3 2 3 电解
二、非选择题(共4小题,共58分)
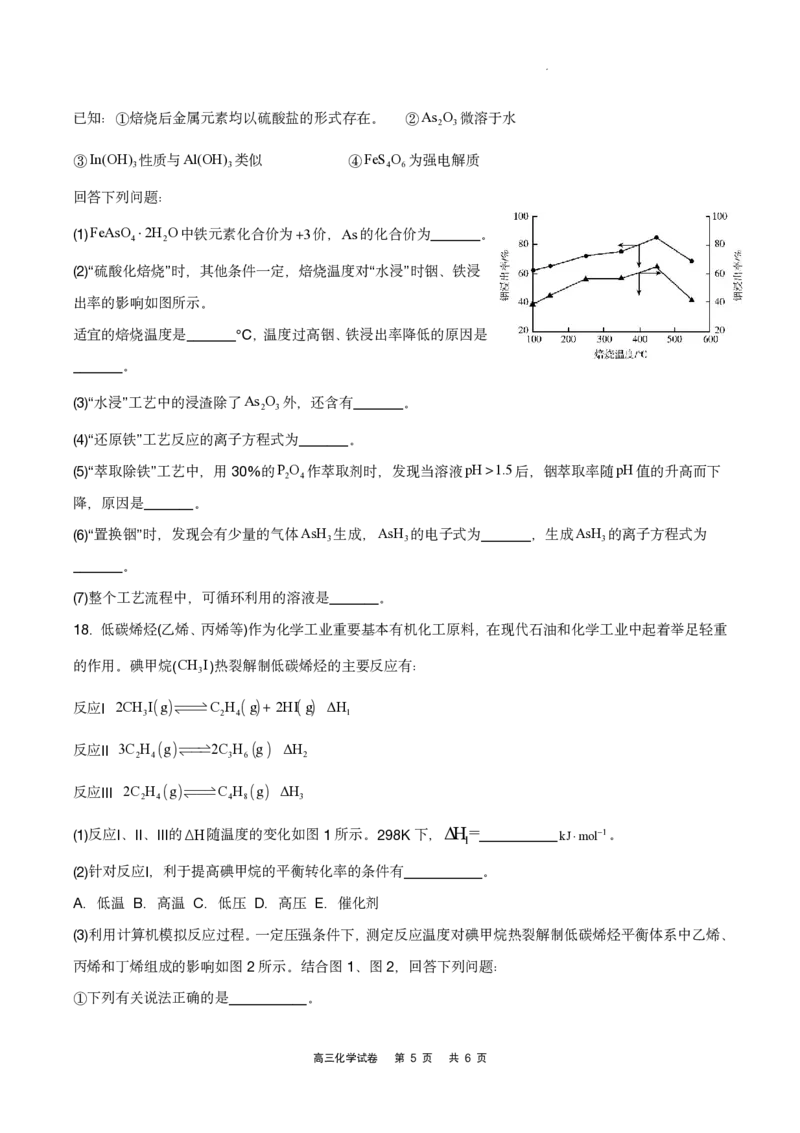
15.某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应。
回答下列问题:
(1)铜与浓硫酸反应的化学方程式为___。
高三化学试卷 第 3 页 共 6 页
学科网(北京)股份有限公司(2)B中观察到的现象为___。
(3)C中应加入的试剂为___,倒置漏斗的作用是___。
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,
优点是___。
16.蜂胶是一种天然抗癌药,主要活性成分为咖啡酸苯乙酯(J)。合成化合物I的路线如下:
已知:
①
②RCHO+HOOCCH
2
COOH RCH=CHCOOH
吡啶
③
当羟基与双键碳原子相连时,易发生转化:RCH-CHOH=RCHCHO
请回答下列问题:
(l)化合物F的名称是____;B-C的反应类型是____。
(2)化合物E中含氧官能团的名称是____;G-H的反应所需试剂和条件分别是____、____。
(3)写出化合物C与新制Cu(OH) 悬浊液反应的化学方程式____。
2
(4)化合物W与E互为同分异构体,两者所含官能团种类和数目完全相同,且苯环上有3个取代基,则W
可能的结构有____种(不考虑顺反异构),其中核磁共振氢谱显示有6种不同化学环境的氢,峰面积比为
2:2:1:1:1:1,写出符合要求的W的结构简式____。
(5)参照上述合成路线,设计由CH CH=CH 和HOOCCH COOH为原料制备 CH CH CH=CHCOOH的合
3 2 2 3 2
成路线(无机试剂任选)____。
17.铟被广泛应用于电子工业、航空航天、太阳能电池新材料等高科技领域。从铜烟灰氧压酸浸渣(主要含
PbSO
4
、FeAsO
4
2H
2
O、SiO
2
、S、In
2
O
3
、In
2
S 3)中提取铟的工艺如图所示。
高三化学试卷 第 4 页 共 6 页
学科网(北京)股份有限公司已知: 焙烧后金属元素均以硫酸盐的形式存在。 As O 微溶于水
① ② 2 3
In(OH) 性质与Al(OH) 类似 FeS O 为强电解质
③ 3 3 ④ 4 6
回答下列问题:
(1)
FeAsO
4
2H
2
O中铁元素化合价为3价,As的化合价为_______。
(2)“硫酸化焙烧”时,其他条件一定,焙烧温度对“水浸”时铟、铁浸
出率的影响如图所示。
适宜的焙烧温度是_______℃,温度过高铟、铁浸出率降低的原因是
_______。
(3)“水浸”工艺中的浸渣除了As
2
O
3
外,还含有_______。
(4)“还原铁”工艺反应的离子方程式为_______。
(5)“萃取除铁”工艺中,用30%的P
2
O
4
作萃取剂时,发现当溶液pH1.5后,铟萃取率随pH值的升高而下
降,原因是_______。
(6)“置换铟”时,发现会有少量的气体AsH
3
生成,AsH
3
的电子式为_______,生成AsH
3
的离子方程式为
_______。
(7)整个工艺流程中,可循环利用的溶液是_______。
18.低碳烯烃(乙烯、丙烯等)作为化学工业重要基本有机化工原料,在现代石油和化学工业中起着举足轻重
的作用。碘甲烷( CH
3
I )热裂解制低碳烯烃的主要反应有:
反应Ⅰ 2CH
3
Ig C
2
H
4
g 2HI g ΔH
1
反应Ⅱ 3C
2
H
4
g 2C
3
H
6
g ΔH
2
反应Ⅲ 2C
2
H
4
g C
4
H
8
g ΔH
3
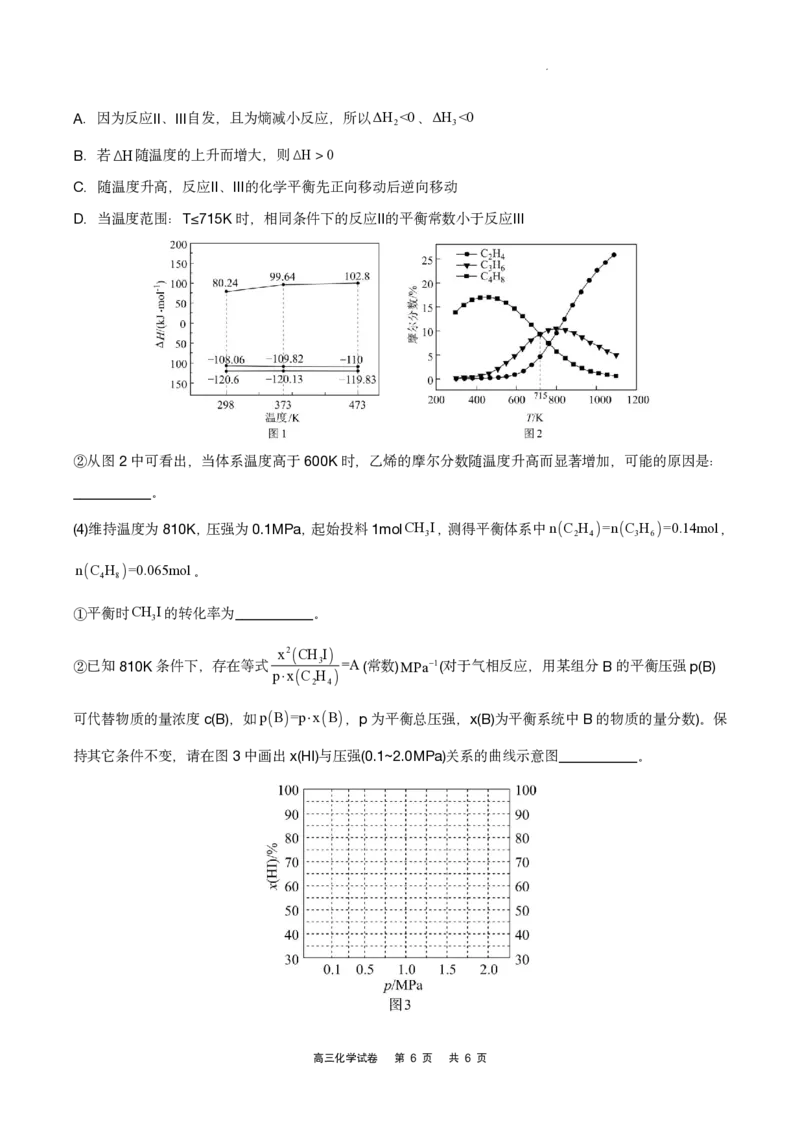
(1)反应Ⅰ、Ⅱ、Ⅲ的H随温度的变化如图1所示。298K下,ΔH= ___________kJmol1。
1
(2)针对反应Ⅰ,利于提高碘甲烷的平衡转化率的条件有___________。
A.低温 B.高温 C.低压 D.高压 E.催化剂
(3)利用计算机模拟反应过程。一定压强条件下,测定反应温度对碘甲烷热裂解制低碳烯烃平衡体系中乙烯、
丙烯和丁烯组成的影响如图2所示。结合图1、图2,回答下列问题:
①
下列有关说法正确的是___________。
高三化学试卷 第 5 页 共 6 页
学科网(北京)股份有限公司A.因为反应Ⅱ、Ⅲ自发,且为熵减小反应,所以ΔH
2
<0、ΔH
3
<0
B.若H随温度的上升而增大,则H 0
C.随温度升高,反应Ⅱ、Ⅲ的化学平衡先正向移动后逆向移动
D.当温度范围:T≤715K时,相同条件下的反应Ⅱ的平衡常数小于反应Ⅲ
②
从图2中可看出,当体系温度高于600K时,乙烯的摩尔分数随温度升高而显著增加,可能的原因是:
___________。
(4)维持温度为810K,压强为0.1MPa,起始投料1mol CH
3
I,测得平衡体系中nC
2
H
4
=nC
3
H
6
=0.14mol,
nC H =0.065mol。
4 8
①
平衡时CH
3
I的转化率为___________。
x2CH I
②
已知810K条件下,存在等式
pxC H
3
=A (常数)MPa1(对于气相反应,用某组分B的平衡压强p(B)
2 4
可代替物质的量浓度c(B),如pB=pxB
,p为平衡总压强,x(B)为平衡系统中B的物质的量分数)。保
持其它条件不变,请在图3中画出x(HI)与压强(0.1~2.0MPa)关系的曲线示意图___________。
高三化学试卷 第 6 页 共 6 页
学科网(北京)股份有限公司