文档内容
荆州中学 2021 级高三下学期 5 月第三次适应性考试
化学试卷
命题: 审题:
可能用到的相对原子质量 H-1 C-12 N-14 O-16 Ca-40 Zr-91
一、单选题(每小题3分,共45分)
1.湖北省是中华文明的重要发祥地之一,大批考古发掘成果展示了湖北悠久而辉煌的历史。
下列文物的材质与另外三种不同的是( )
A.凤舞九天木雕 B.石家河玉人像 C.睡虎地秦简 D.漆木虎座鸟架鼓
2.下列化学用语表达正确的是( )
A.次氯酸钠的电子式: B.CCl 分子的空间填充模型为
4
C.Cl 分子中共价键电子云轮廓图: D.2-丁烯的键线式:
2
3.生产、生活中蕴藏着丰富的化学知识。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 用活性炭清除冰箱中的异味 活性炭具有吸附性
B 用FeS除去工业废水中的Cu2 FeS具有还原性
C 用纯碱溶液清洗抽油烟机上的油渍 油脂在碱性条件下易水解
D 盐碱地(含较多Na CO 等)施用适量石膏,降低土壤碱性 盐与盐能发生复分解反应
2 3
4.实验室制取SO 并回收CuSO 的实验原理及装置不能达到实验目的是( )
2 4
A、制取SO2 B、干燥SO2 C、吸收尾气中的SO2 D、将硫酸铜溶液蒸发浓缩
5.科研人员开发了一种生产药物中间体三氟甲苯的方法:
设N 为阿伏加德罗常数的值,已知三氟乙酸的pKa=0.23,下列叙述正确的是( )
A
A.1mol三氟甲苯中碳碳双键数目为3N
A
B.氢气和二氧化碳组成的混合物共1mol ,其中氢、氧原子总数为2N
A
高三化学第1页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}C.生成22.4L H 时,需消耗1mol苯
2
D.1L1molL1三氟乙酸溶液中,H的数目为N
A
6.NH 分子的空间结构是三角锥形结构而不是平面正三角形结构,最充分的理由是( )
3
A.NH 分子内3个N—H键长均相等
3
B.NH 分子内3个价键的键角和键长均相等
3
C.NH 分子内3个N—H的键长相等,键角都等于107°
3
D.NH 分子内3个N—H的键长相等,键角都等于120°
3
7.作为“血迹检测小王子”,鲁米诺反应在刑侦中扮演了重要的角色,其一种合成原理如图
所示。下列有关说法正确的是( )
A.鲁米诺的化学式为C H N O
8 6 3 2
B.一定条件,A可以和甘油发生聚合反应
C.B中处于同一平面的原子最多12个
D.(1)、(2)两步的反应类型分别为加成反应和取代反应
8.某抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族
元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。下列叙述错
误的是( )
A.简单气态氢化物的稳定性:X>W B.简单离子半径:Z>W>X
C.第一电离能:Y>W>X D.Z的最高价氧化物对应的水化物为强酸
9.下列叙述对应的离子方程式正确的是( )
A.向饱和NaOH溶液中通入过量CO 析出白色晶体:OHCO HCO
2 2 3
B.白色沉淀CuCl溶于NH Cl-NH 溶液得到深蓝色溶液:
4 3
4Cu 4NH
4
O
2
12NH
3
4·H
C 2 Ou NH
3
4
2 2H
2
O
C.向NaHSO 溶液中滴入酸化的BaNO 溶液产生白色沉淀:
3 3 2
2HSOBa2 H OSO BaSO
3 2 2 3
D.向KMnO 溶液中滴入H O 溶液产生黑色沉淀和气泡:
4 2 2
2MnO3H O 2MnO 3O 2OH2H O
4 2 2 2 2 2
10.研究表明许多疾病,包括基因突变(癌变、动脉硬化等)和生物机体中毒等,可能是一氧
化氮的释放或调节不正常引起的。用间接电化学法可对NO进行无害化处理,其原理如图所
示(质子膜允许H和H O通过),下列相关判断错误的是( )
2
试卷第2页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}A.该装置工作时,可视Pb为惰性电极
B.电极I接电源负极,电极反应式为:
2HSO2H 2e S O22H O
3 2 4 2
C.吸收塔中每消耗2molNO,有4molH通
过质子膜
D.每处理1molNO,电解池将产生11.2LO
2
11.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
选项 性质差异 结构因素
A 键角:NH >H O 孤电子对数目
3 2
B 碱性:Mg(OH) >Al(OH) 第一电离能
2 3
C 熔点:金刚石>晶体硅 共价键键能
D 酸性:CF COOH>CH COOH 羟基极性
3 3
12.乙烯水化法制乙醇的反应机理如下,能量与反应进程关系如图。下列叙述不正确的是( )
A.第①步反应是吸热反应,第②③步反应是放热反应
B.总反应速率由第①步反应决定
C.第①步反应过程中,只有碳碳键断裂和碳氢键形成
D.第③步的反应为
13某兴趣小组用CaS与MgCl 反应制备高纯H S,实验装置如图所示(装置A内产生的H S
2 2 2
气体中含有酸性气体杂质)
高三化学第3页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}下列说法不正确的是( )
...
A.装置A中的反应利用了水解原理
B.为了简化装置,B可以省略
C.装置C中的Ba(OH) 可以换成NaHS
2
D.为了快速排除体系内的空气,可先断开装置F和装置G的连接
14.科研工作者合成了低温超导化合物M,再利用低温去插层法,获得了一个新化合物N。
二者的晶体结构如图所示,下列说法正确的是( )
A.去插层过程中Cs元素均转化为Cs单质
B.N的化学式为VSe O
2 2
C.M中与Cs原子最临近的Se原子有2个
D.N中V原子填充了Se原子构成的正八面体空隙
15.常温下,分别在Mn(NO ) 、Zn(NO ) 、HNO 溶液中滴加NaOH溶液,溶液pX[pX=-lgc(X),
3 2 3 2 2
c
NO
X代表Mn2+、Zn2+、OH-、 2 ]与pH关系如图所示。已知:
cHNO
2
K MnOH K ZnOH 。下列叙述错误的是( )
sp
2
sp
2
c
NO
A.图中L 代表 2 ,L 代表Zn2+
2 cHNO 3
2
c
Mn2
B.同时产生两种沉淀时, 103.45
c
Zn2
C.MnOH 2HNO MnNO 2H O的平
2 2 2 2 2
衡常数K 108.7
D.室温下,K
sp
MnOH
2
的数量级为1013
试卷第4页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}二、解答题
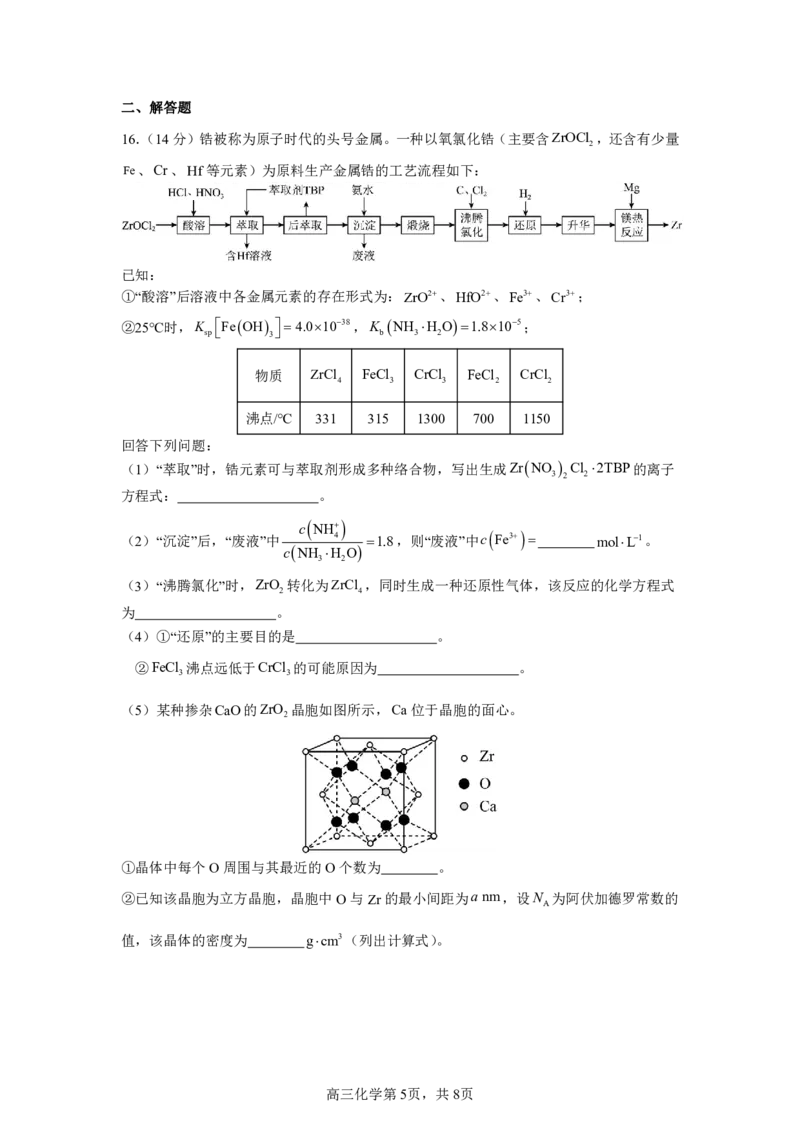
16.(14分)锆被称为原子时代的头号金属。一种以氧氯化锆(主要含ZrOCl ,还含有少量
2
Fe、Cr、Hf等元素)为原料生产金属锆的工艺流程如下:
已知:
①“酸溶”后溶液中各金属元素的存在形式为:ZrO2、HfO2、Fe3、Cr3;
②25℃时,K
sp
FeOH
3
4.01038,K
b
NH
3
H
2
O1.8105;
物质 ZrCl FeCl CrCl FeCl CrCl
4 3 3 2 2
沸点/℃ 331 315 1300 700 1150
回答下列问题:
(1)“萃取”时,锆元素可与萃取剂形成多种络合物,写出生成ZrNO Cl 2TBP的离子
3 2 2
方程式: 。
c
NH
(2)“沉淀”后,“废液”中 4 1.8,则“废液”中c Fe3 molL1。
cNH H O
3 2
(3)“沸腾氯化”时,ZrO 转化为ZrCl ,同时生成一种还原性气体,该反应的化学方程式
2 4
为 。
(4)①“还原”的主要目的是 。
②FeCl 沸点远低于CrCl 的可能原因为 。
3 3
(5)某种掺杂CaO的ZrO 晶胞如图所示,Ca位于晶胞的面心。
2
①晶体中每个O周围与其最近的O个数为 。
②已知该晶胞为立方晶胞,晶胞中O与Zr的最小间距为anm,设N 为阿伏加德罗常数的
A
值,该晶体的密度为 gcm3(列出计算式)。
高三化学第5页,共8页
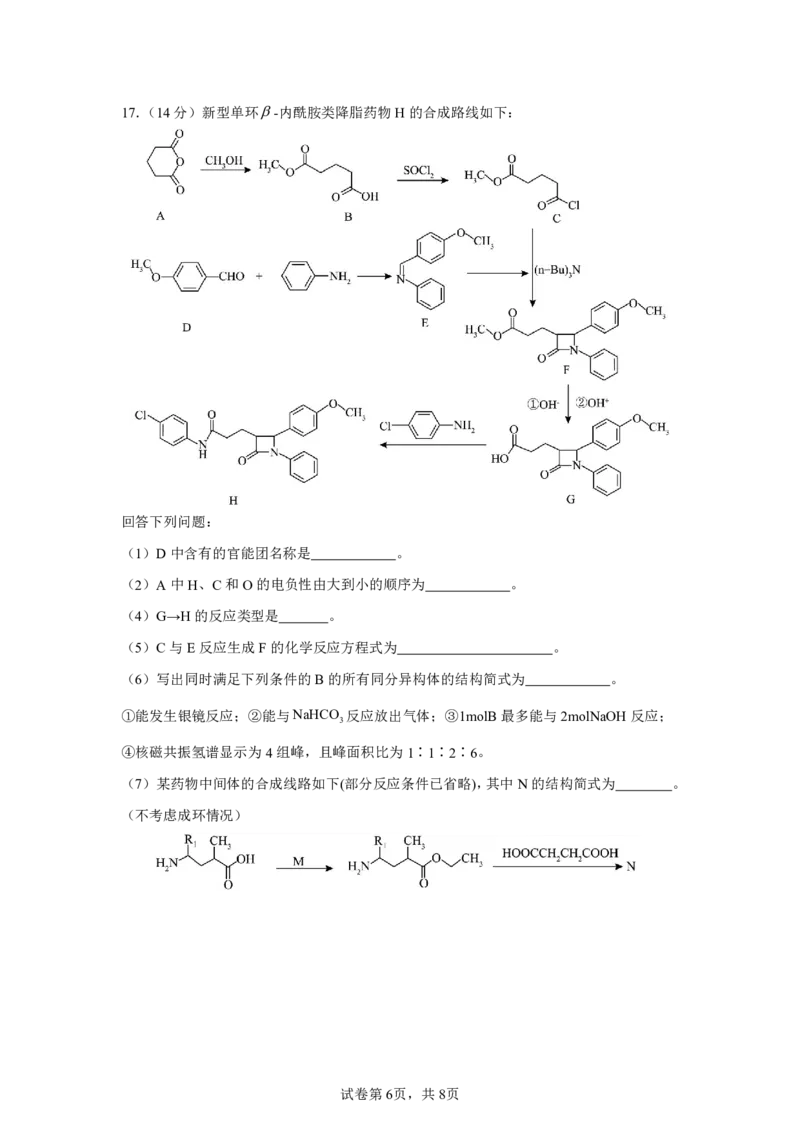
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}17.(14分)新型单环-内酰胺类降脂药物H的合成路线如下:
回答下列问题:
(1)D中含有的官能团名称是 。
(2)A中H、C和O的电负性由大到小的顺序为 。
(4)G→H的反应类型是 。
(5)C与E反应生成F的化学反应方程式为 。
(6)写出同时满足下列条件的B的所有同分异构体的结构简式为 。
①能发生银镜反应;②能与NaHCO 反应放出气体;③1molB最多能与2molNaOH反应;
3
④核磁共振氢谱显示为4组峰,且峰面积比为1∶1∶2∶6。
(7)某药物中间体的合成线路如下(部分反应条件已省略),其中N的结构简式为 。
(不考虑成环情况)
试卷第6页,共8页
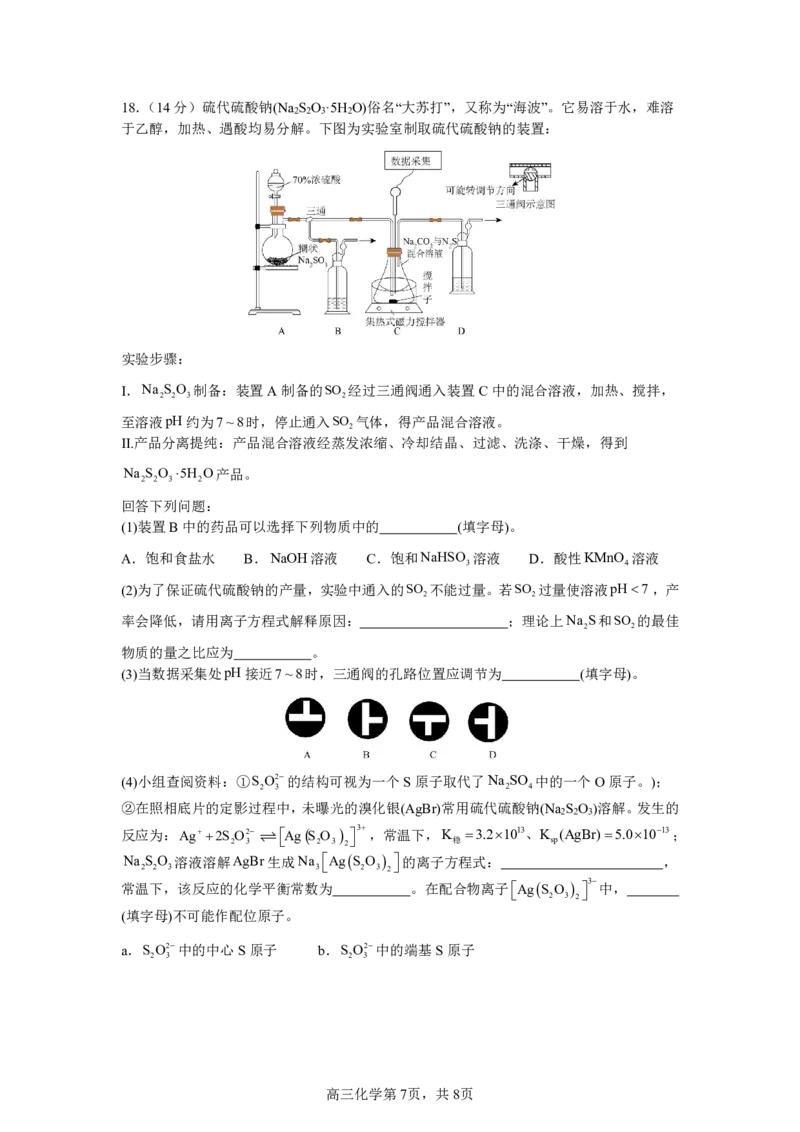
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}18.(14分)硫代硫酸钠(Na S O ·5H O)俗名“大苏打”,又称为“海波”。它易溶于水,难溶
2 2 3 2
于乙醇,加热、遇酸均易分解。下图为实验室制取硫代硫酸钠的装置:
实验步骤:
I.Na S O 制备:装置A制备的SO 经过三通阀通入装置C中的混合溶液,加热、搅拌,
2 2 3 2
至溶液pH约为7~8时,停止通入SO 气体,得产品混合溶液。
2
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
Na S O 5H O产品。
2 2 3 2
回答下列问题:
(1)装置B中的药品可以选择下列物质中的 (填字母)。
A.饱和食盐水 B.NaOH溶液 C.饱和NaHSO 溶液 D.酸性KMnO 溶液
3 4
(2)为了保证硫代硫酸钠的产量,实验中通入的SO 不能过量。若SO 过量使溶液pH7,产
2 2
率会降低,请用离子方程式解释原因: ;理论上Na S和SO 的最佳
2 2
物质的量之比应为 。
(3)当数据采集处pH接近7~8时,三通阀的孔路位置应调节为 (填字母)。
(4)小组查阅资料:①S O2的结构可视为一个S原子取代了Na SO 中的一个O原子。);
2 3 2 4
②在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na S O )溶解。发生的
2 2 3
反应为:Ag 2S
2
O
3
2
AgS
2
O
3
2
3 ,常温下,K
稳
3.21013、K
sp
(AgBr)5.01013;
Na S O 溶液溶解AgBr生成Na AgS O 的离子方程式: ,
2 2 3 3 2 3 2
常温下,该反应的化学平衡常数为 。在配合物离子AgS O 3 中,
2 3 2
(填字母)不可能作配位原子。
a.S O2中的中心S原子 b.S O2中的端基S原子
2 3 2 3
高三化学第7页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}19.(15分)血红蛋白(Hb)和肌红蛋白(Mb)分别存在于血液和肌肉中,都能与氧气结合,与
氧气的结合度α(吸附O 的Hb或Mb的量占总Hb或Mb的量的比值)和氧气分压 pO 密切
2 2
相关。请回答下列问题:
(1)人体中的血红蛋白(Hb)能吸附O 、H+,相关反应的热化学方程式及平衡常数如下:
2
I.HbaqHaq HbHaq ΔH K
1 1
II.HbHaqO g HbO aqHaq ΔH K
2 2 2 2
III.HbaqO g HbO aq ΔH K
2 2 3 3
ΔH = (用ΔH 、ΔH 表示),K = (用K 、K 表示)。
3 1 2 3 1 2
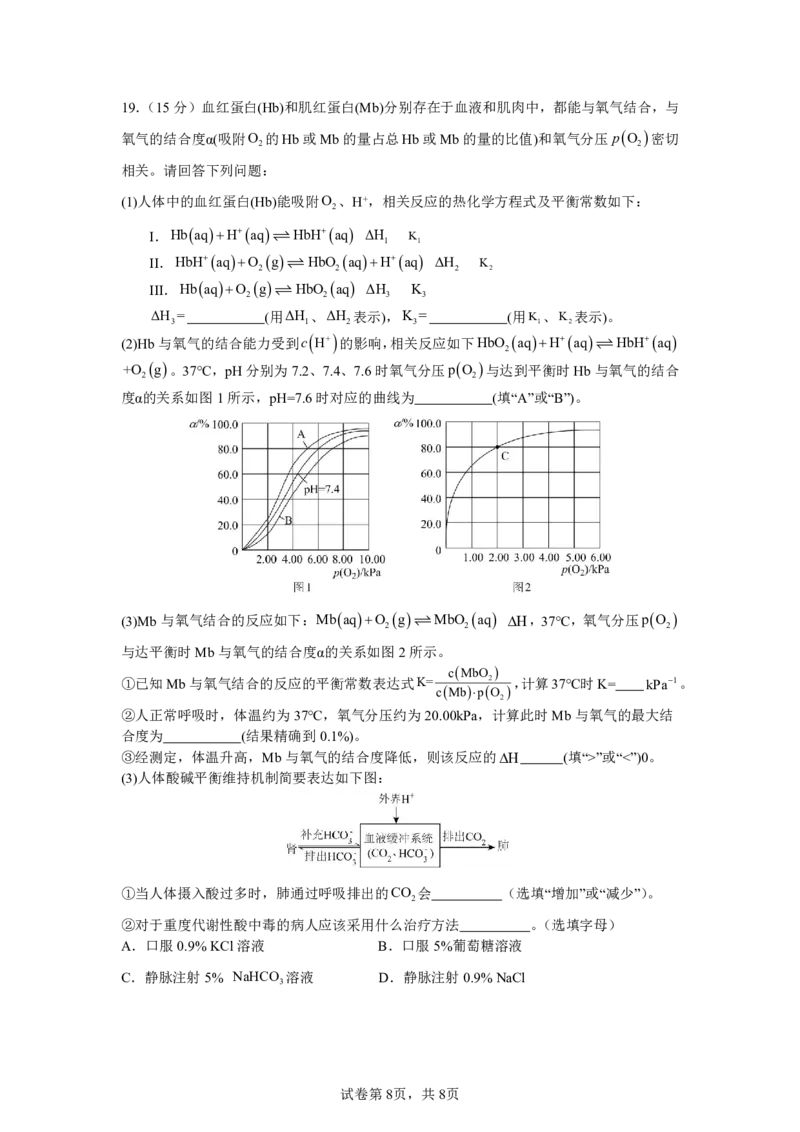
(2)Hb与氧气的结合能力受到c H 的影响,相关反应如下HbO aqHaq HbHaq
2
+O g。37℃,pH分别为7.2、7.4、7.6时氧气分压pO 与达到平衡时Hb与氧气的结合
2 2
度α的关系如图1所示,pH=7.6时对应的曲线为 (填“A”或“B”)。
(3)Mb与氧气结合的反应如下:MbaqO g MbO aq H,37℃,氧气分压pO
2 2 2
与达平衡时Mb与氧气的结合度α的关系如图2所示。
cMbO
①已知Mb与氧气结合的反应的平衡常数表达式K= 2 ,计算37℃时K= kPa1。
cMbpO
2
②人正常呼吸时,体温约为37℃,氧气分压约为20.00kPa,计算此时Mb与氧气的最大结
合度为 (结果精确到0.1%)。
③经测定,体温升高,Mb与氧气的结合度降低,则该反应的H (填“>”或“<”)0。
(3)人体酸碱平衡维持机制简要表达如下图:
①当人体摄入酸过多时,肺通过呼吸排出的CO 会 (选填“增加”或“减少”)。
2
②对于重度代谢性酸中毒的病人应该采用什么治疗方法 。(选填字母)
A.口服0.9%KCl溶液 B.口服5%葡萄糖溶液
C.静脉注射5% NaHCO 溶液 D.静脉注射0.9%NaCl
3
试卷第8页,共8页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}参考答案
1-15 BABCB CBCDD BCBBC
16(1)ZrO2++2TBP+2NO-+2Cl-+2H+=Zr(NO ) Cl 2TBP+2H O (2分)
3 3 2 2 2
(2)4.01023(2分)
高温
(3)2C+2Cl +ZrO ZrCl +2CO(2分)
2 2 4
(4)把FeCl 还原为FeCl ,避免升华时ZrCl 含有FeCl 杂质(2分)
3 2 4 3
FeCl 是分子晶体,CrCl 是离子晶体(2分)
3 3
91340816
(5)6 (2分)
(
4a
107)3
(2分)
3
17、(1)醚键、醛基(2分)
(2)O>C>H(2分)
(3)取代反应(2分)
(4) +HCl(2分)
(5)HCOOCH CCH COOH(2分)、HCOOCCH CH COOH (2分)
2 3 2 3 2 2
(6) (2分)
18.
(1) BD (2分) (2) S O2+2H+=SO +S+H O(2分) 1:2(2分)
2 3 2 2
(3) D (2分) (4) AgBr+2S O2=[Ag(S O ) ]3-+Br-(2分) 16(2分) a(2分)
2 3 2 3 2
19.
(1) ΔH +ΔH (2分) K K (2分) (2) A(2分)
1 2 1 2
(3) 2(2分) 97.6%(2分) < (1分) (4) 增加(2分) C(2分)
答案第1页,共1页
{#{QQABCQKAggAgAIIAAQhCEwUQCAIQkBAACagGBBAIIAIBgRFABAA=}#}