文档内容
2024 年高考适应性考试(一)
化 学 试 题
总分:100分考试时间:75分钟
本卷可能用到的相对原子质量:H1 C12 N14 O16 Co59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.形成正确的化学观念有助于学习。下列有关化学观念正确的是
A.组成相同的物质其性质相同
B.化学反应中既有物质变化也有能量变化
C.化学反应的限度大小是不可改变的
D.晶体类型一定是纯粹的,不存在过渡晶体
高温 高温
2.电石可通过如下反应制得:CaCO=====CaO+CO 、CaO+3C=====CaC +CO。下列说法
3 2 2
正确的是
A.基态Ca2+的电子排布式:[Ar]4s2 B.CO2-的空间构型为四面体形
3
C.CaC 的电子式为 D.二氧化碳晶体属于共价晶体
2
3.臭氧(O )在[Fe(H O) ]2+催化下能将烟气中的 SO 、NO 分别氧化为SO2-和NO-。下列关
3 2 6 2 x 4 3
于 N、O、S、Fe 元素及其化合物的说法正确的是
A.原子半径:N>O>S B.第一电离能:I (N)>I (O)>I (S)
1 1 1
C.沸点:H
2
S>H
2
O>NH
3
D.电负性:χ(Fe)<χ(O)<χ(N)
4.下列物质的结构与性质或性质与用途具有对应关系的是
A.N 中化学键非常牢固,可用作保护气
2
B.乙醇易溶于水,可用于消毒杀菌
C.浓硫酸具有强氧化性,可用于与CaF 反应制HF
2
D.SO 是极性分子,可用于漂白纸浆
2
阅读下列资料,完成5~8题:
氨用于生产硝酸、铵盐、纯碱、配合物等,液氨可以和金属钠反应产生H 。NH 中的一
2 3
个H原子被OH取代可形成羟胺(NH OH),被-NH 取代可形成肼(N H ),OH吸电子能
2 2 2 4
力比-NH 强。N H 的燃烧热为622kJ·mol-1,具有强还原性,可由尿素[CO(NH ) ]、NaClO
2 2 4 2 2
和NaOH溶液一起反应制得。
5.实验室利用下列装置进行氨气或氨水的有关实验,能够达到实验目的的是
A.制取NH B.干燥NH C.收集NH D.制[Cu(NH ) ](OH) 溶液
3 3 3 3 4 2
6.下列说法正确的是
A.NH 的键角比H O小 B.1mol[Cu(NH ) ]2+中含12mol σ键
3 2 3 4
C.NH OH难溶于水 D.NH OH中N结合H+的能力比N H 弱
2 2 2 4
第1页,共6页
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}7.下列化学反应的表示正确的是
A.金属钠和液氨反应:NH +Na=NaNH +H ↑
3 2 2
B.过量氨水和SO 反应:SO +2NH ·H O=(NH ) SO +H O
2 2 3 2 4 2 3 2
C.尿素、NaClO、NaOH溶液制取N H 的离子方程式:
2 4
CO(NH ) +ClO-=CO ↑+N H +Cl-
2 2 2 2 4
D.肼燃烧的热化学方程式:N H (l)+O (g)=N (g)+2H O(g) ΔH=-622kJ·mol-1
2 4 2 2 2
8.下列说法正确的是
A.侯氏制碱的原理可表示为
B.氨气催化氧化制取NO属于氮的固定中的一种
C.由尿素、NaClO和NaOH溶液制N H 时,应将NaClO溶液滴加到尿素溶液中
2 4
D.浓氨水与浓硫酸靠近时会有白烟生成
9.工业上用CH 催化还原NO 可以消除氮氧化物的污染,反应原理为:CH (g)+
4 2 4
2NO (g) N (g)+CO (g)+2H O(g)ΔH=-867.0kJ·mol-1。不同的催化剂催化该反应的
2 2 2 2
最佳活性温度不同。下列说法正确的是
c(CO )·c(N )
A.上述反应平衡常数K= 2 2
c2(NO )·c(CH )
2 4
B.其他条件不变时,反应单位时间,NO 去除率随温度升高而增大的原因可能是平衡常
2
数变大
C.其他条件不变,在低温下使用高效催化剂可提高CH 的平衡转化率
4
D.反应中若采用高分子分离膜及时分离出水蒸气,可以使反应的平衡常数增大
10.有机物W可发生如图所示的反应,下列说法正确的是
A.为促进M的生成,试剂Q可用硫酸
B.Y中所有碳原子均可能共平面
C.M、X、Y都存在顺反异构体
D.X中sp2杂化和sp3杂化的碳原子的比例是8∶1
11.室温下,下列实验方案能达到探究目的的是
选项 探究方案 探究目的
测定等体积CH COONa 和NaNO 溶液 比较CH COOH和HNO 的酸性强
3 2 3 2
A
的pH 弱
将石油裂解产生的气体通入Br 的CCl
2 4
B 验证石油裂解产物中是否含乙烯
溶液,观察溶液颜色变化
向Na S溶液中通入SO 至过量,观察是
2 2
C SO 是否具有氧化性
2
否有沉淀生成
将卤代烃与NaOH水溶液混合加热,待
D 确定卤代烃中卤原子种类
冷却后加入硝酸银溶液,观察沉淀颜色
第2页,共6页
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}12.室温下,用含少量ZnSO 杂质的1mol·L-1MnSO 溶液制备MnCO 的过程如下图所示。
4 4 3
下列说法正确的是
已知:K (MnS)=2×10-10、K (ZnS)=2×10-24、K (NH ·H O)=2×10-5
sp sp b 3 2
K (H CO )=4×10-7、K (H CO )=5×10-11
a1 2 3 a2 2 3
A.“除锌”后所得上层清液中,c(Zn2+)一定小于1×10-5mol·L-1
B.0.1mol·L-1NH HCO 溶液中存在:c(H+)+c(H CO )=c(OH-)+c(CO2-)
4 3 2 3 3
C.氨水、NH HCO 溶液中存在:c(NH+)<2c(CO2-)+c(HCO-)
4 3 4 3 3
D.“沉锰”后的滤液中存在:c(NH+)+c(NH ·H O)=2c(SO2-)
4 3 2 4
13.利用H 和CO反应生成CH 的过程中主要涉及的反应如下:
2 4
反应Ⅰ CO(g)+3H (g)=CH (g)+H O(g) ΔH =-206.2kJ·mol-1
2 4 2 1
反应Ⅱ CO(g)+H O(g)=CO (g)+H (g) ΔH =-41.2kJ·mol-1
2 2 2 2
向密闭容器中充入一定量H 和CO发生上述反应,保持温度和容器体积一定,平衡时CO
2
n(H )
和H 的转化率、CH 和CO 的产率及随起始 2 的变化情况如下图所示。
2 4 2
n(CO)
n(CH ) n(CH )
4 生成 4 生成
[CH 的产率= ×100%,CH 的选择性= ×100%]。
4 4
n(CO) n(CO ) +n(CH )
投料 2 生成 4 生成
下列说法不 . 正 . 确 .的是
A.当容器内气体总压强保持不变时,反应Ⅰ、Ⅱ均
达到平衡状态
n(H )
B.曲线c表示CH 的产率随 2 的变化
4
n(CO)
n(H )
C. 2 =0.5,反应达平衡时,CH 的选择性为50%
4
n(CO)
n(H )
D.随着 2 增大,CO 的选择性先增大后减小
2
n(CO)
第3页,共6页
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}二、非选择题:共4题,共61分
14.(14分)全钒液流电池正极废液中含有的离子是VO+、VO2+、H+、SO2-。以该废液为原料
2 4
经过氧化、调pH、沉钒、煅烧可以制取V O 。
2 5
⑴氧化:向正极废液中加入 NaClO 将 VO2+转化为 VO+,写出该反应的离子方程式:
3 2
▲ 。
⑵调pH:向氧化后的溶液中加入NaOH调节溶液pH,溶液中V(+5价)会以V O4-、V O3-、
2 7 3 9
V 10 O6 2 - 8 等形式存在。随pH的升高,溶液中- c c - ( ( V V --2 3 - O O -- 4 7 3 9 - - -- ) ) 的值将 ▲ (填“增大”“减小”
或“保持不变”),判断的方法是 ▲ 。
⑶沉钒:不同pH时,向溶液中加入(NH ) SO ,可得到不同类型的含钒沉淀。
4 2 4
①其他条件一定,控制溶液pH在2~5之间,向溶液中加入(NH ) SO ,沉钒率和沉淀
4 2 4
的X射线衍射图分别如题14图-1和题14图-2所示。pH>3时,pH越大,溶液的沉
钒率越低的原因是 ▲ 。
②向pH=8的溶液中(此时V主要以VO-存在)加入过量(NH ) SO 溶液,生成NH VO
3 4 2 4 4 3
沉淀。加入过量(NH ) SO 溶液的目的是 ▲ 。已知:K (NH VO )=1.7×10-3。
4 2 4 sp 4 3
题14图-1 题14图-2 题14图-3
⑷煅烧:煅烧NH VO 固体制取V O 时,需在有氧条件下进行,原因是 ▲ 。
4 3 2 5
⑸VO 是一种相变材料,其一种晶胞(部分O原子未标出)的结构如图题14图-3所示,
2
在图中合适位置补充其余O原子。
15.(15分)一种药物中间体G的合成路线如下:
已知:Ⅰ.
Ⅱ.
第4页,共6页
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}⑴转化①除物质B外,还有另一含苯环的有机产物生成。则A的结构简式为 ▲ 。
⑵X的结构简式为 ▲ 。
⑶已知F与E互为同分异构体,则E→F的反应类型为 ▲ 反应。
⑷写出满足下列条件的D的一种同分异构体的的结构简式: ▲ 。
①能与FeCl 溶液发生显色反应;
3
②水解后可得到三种有机产物,其中一种是最简单的α-氨基酸,另两种产物酸化后均只
含两种化学环境不同的氢。
⑸写出以CH BrCH CH Br、CH COOH、2-丁烯为原料制备
2 2 2 3
的合成路线流程图。(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
16.(18分)CoO可用于制取催化剂,可以由含钴废料(主要成分为Co O ,还含有少量SiO 、
2 3 2
Fe O 、Al O 和MgO)经过如下过程进行制取:
2 3 2 3
⑴含钴废料用硫酸和Na SO 溶液浸出后,溶液中含有的阳离子是Na+、H+、Co2+、Fe2+、
2 3
Fe3+、Al3+和Mg2+。
①写出“浸取”时Co O 所发生反应的离子方程式: ▲ 。
2 3
②“浸取”时含钴废料、硫酸和Na SO 溶液混合的方式为 ▲ 。
2 3
⑵已知:①氧化性Co3+>H O ;
2 2
②K (MgF )=6.4×10-11;CoF 可溶于水;Fe3+、Al3+与F-可生成配合物难以沉
sp 2 2
淀;
③实验条件下金属离子转化为氢氧化物时开始沉淀及沉淀完全的pH如下表所示:
Fe3+ Al3+ Fe2+ Co2+ Mg2+
开始沉淀pH 1.9 3.4 6.9 6.6 9.1
沉淀完全pH 3.2 4.7 8.9 9.2 11.1
补充完整由“浸取液”制取CoC O ·2H O的实验方案:取一定量的浸取液, ▲ ,
2 4 2
过滤,向滤液中滴加2mol·Lˉ1(NH ) C O 溶液,……,得到CoC O ·2H O晶体,(实
4 2 2 4 2 4 2
验中可选用的试剂是2mol·L-1的氨水、5%的H O 溶液、K [Fe(CN) ]溶液、1mol·L-1
2 2 3 6
的NH F溶液)。
4
⑶已知:K (CoC O )=4×10-8、K (H C O )=5×10-2、K (H C O )=5×10-5。
sp 2 4 a1 2 2 4 a2 2 2 4
①反应Co2++H C O CoC O ↓+2H+的平衡常数为 ▲ 。
2 2 4 2 4
②制取CoC O ·2H O时使用(NH ) C O 溶液而不是Na C O 溶液的原因是 ▲ 。
2 4 2 4 2 2 4 2 2 4
⑷为测定草酸钴样品的纯度,进行如下实验:
①取草酸钴样品3.000g,加入100.00mL0.1000mol·L-1酸性KMnO 溶液,加热充分反
4
应至不再有CO 气体产生(该条件下Co2+不被氧化,杂质不参与反应)。
2
②将溶液冷却,加水稀释定容至250mL。
③取25.00mL溶液,用0.1000mol·L-1FeSO 溶液滴定过量的KMnO ,恰好完全反应
4 4
时消耗18.00mLFeSO 溶液。计算样品中CoC O ·2H O的质量分数,并写出计算过
4 2 4 2
程。
第5页,共6页
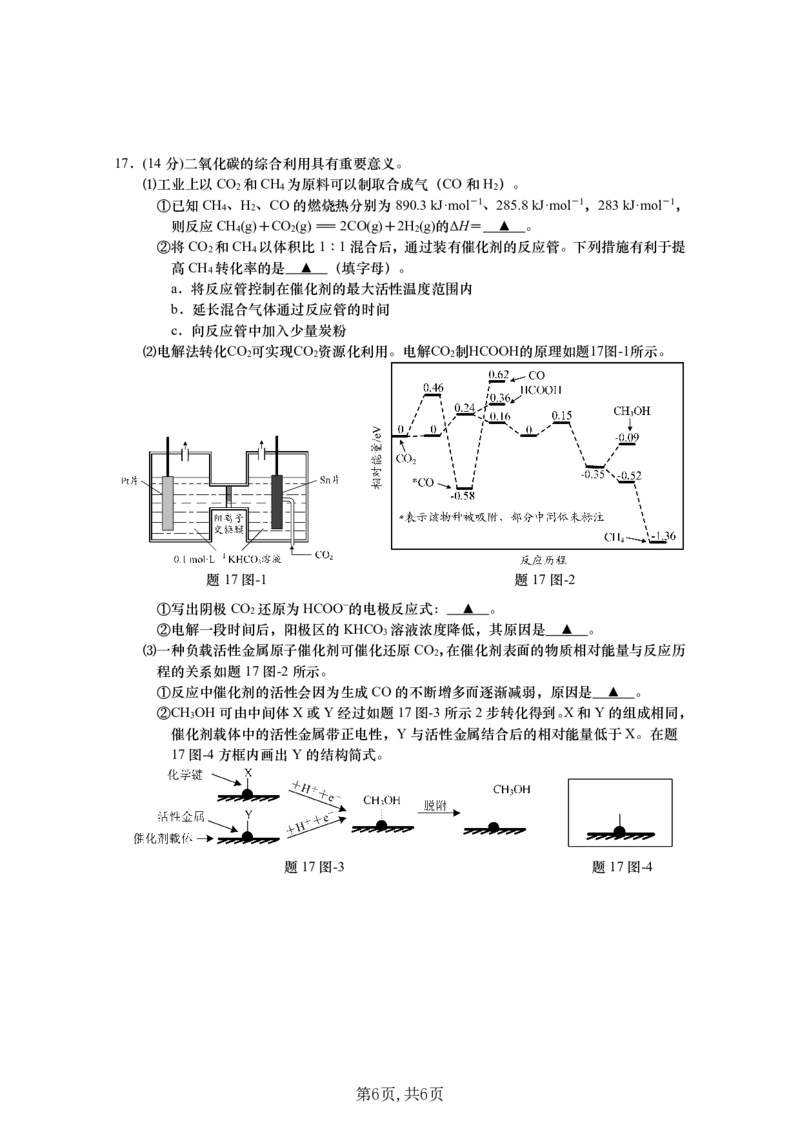
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}17.(14分)二氧化碳的综合利用具有重要意义。
⑴工业上以CO 和CH 为原料可以制取合成气(CO和H )。
2 4 2
①已知CH 、H 、CO的燃烧热分别为890.3kJ·mol-1、285.8kJ·mol-1,283kJ·mol-1,
4 2
则反应CH (g)+CO (g)=2CO(g)+2H (g)的ΔH= ▲ 。
4 2 2
②将CO 和CH 以体积比1∶1混合后,通过装有催化剂的反应管。下列措施有利于提
2 4
高CH 转化率的是 ▲ (填字母)。
4
a.将反应管控制在催化剂的最大活性温度范围内
b.延长混合气体通过反应管的时间
c.向反应管中加入少量炭粉
⑵电解法转化CO 可实现CO 资源化利用。电解CO 制HCOOH的原理如题17图-1所示。
2 2 2
题17图-1 题17图-2
①写出阴极CO 还原为HCOO−的电极反应式: ▲ 。
2
②电解一段时间后,阳极区的KHCO 溶液浓度降低,其原因是 ▲ 。
3
⑶一种负载活性金属原子催化剂可催化还原CO ,在催化剂表面的物质相对能量与反应历
2
程的关系如题17图-2所示。
①反应中催化剂的活性会因为生成CO的不断增多而逐渐减弱,原因是 ▲ 。
②CH OH可由中间体X或Y经过如题17图-3所示2步转化得到。X和Y的组成相同,
3
催化剂载体中的活性金属带正电性,Y与活性金属结合后的相对能量低于X。在题
17图-4方框内画出Y的结构简式。
题17图-3 题17图-4
第6页,共6页
{#{QQABKYaQggggAAAAAQhCQwGqCEIQkACACKoOwBAAsAABSQFABAA=}#}