文档内容
第三章 第一节 第2课时 铁盐和亚铁盐 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 在一些高档茶叶、点心等的包装盒中有一个小袋,将小袋打开,可以看到灰黑色粉末,其中有
些已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加 KSCN溶液,
原溶液立即变为红色。下列说法不正确的是( )
A.小袋中原来装有氧化铁
B.小袋中原来装有铁粉
C.该灰黑色粉末不可食用
D.该灰黑色粉末用作抗氧化剂
2. 除去FeCl 溶液中少量的FeCl ,最好的办法是( )
2 3
A.加入氢氧化钠溶液 B.通入氯气
C.加入铜粉 D.加入铁粉
3. 下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
2
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只
含有Fe2+,不含有Mg2+
4. 下列离子方程式中,正确的是( )
A.铁与盐酸反应:2Fe+6H+===2Fe3++3H↑
2
B.氯气与氯化亚铁溶液反应:2FeCl +Cl===2FeCl
2 2 3
C.氯化铁溶液与铁反应:Fe3++Fe===2Fe2+
D.氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-===Fe(OH) ↓
3
5. 要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③②
C.③① D.①②③
6. 证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变为灰绿色,最后呈红褐色
D.只需滴加KSCN溶液
7. 为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计错误的
是( )
1
学科网(北京)股份有限公司A.只有④ B.只有③
C.③④ D.③④⑤
8. 下列离子方程式正确的是( )
A.将氨水滴入到FeCl 溶液中:Fe3++3OH−===Fe(OH) ↓
3 3
B.氧化铁与盐酸反应:Fe O+6H+===2Fe3++3H O
2 3 2
C.向FeCl 溶液中加入铁粉:Fe+Fe3+===2Fe2+
3
D.向氯化亚铁溶液中通入Cl:Fe2++Cl===Fe3++2Cl−
2 2
9. 下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 实验操作及现象 实验结论
A 向某溶液中加入NaOH溶液,立即产生红褐色沉淀 该溶液中一定含有Fe3+
B 向某溶液中加入KSCN溶液,溶液变为红色 该溶液中一 定含有Fe2+
C 向某溶液中滴加酸性高锰酸钾溶液,溶液褪色 该溶液中一定含有Fe2+
向某溶液中通入Cl,然后加入KSCN溶液,溶液变
2
D 该溶液中一定含有Fe2+
为红色
10.下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧
②FeSO 溶液中滴入NaOH溶液,并在空气中放置一段时间
4
③FeCl 溶液中滴入KSCN溶液
3
④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④
C.③①②④ D.①②③④
11.将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+物质的量相等。则已反应
的Fe3+和未反应的Fe3+的物质的量之比是( A )
A.2∶3 B.3∶2
C.1∶2 D.1∶1
12.用FeCl 溶液腐蚀印刷电路板上的铜,所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分
3
析合理的是( )
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出
2
学科网(北京)股份有限公司13.将铁粉放入HCl、MgCl 、FeCl 、CuCl 组成的混合液中,充分反应后,铁粉有剩余,则此时
2 3 2
溶液中含有的大量阳离子是( )
A.Cu2+和Fe2+ B.Fe2+和Mg2+
C.Fe3+和Fe2+ D.H+和Cu2+
14. a g铁粉与含有HSO 的CuSO 溶液恰好完全反应后,得到a g铜,则参与反应的CuSO 与
2 4 4 4
HSO 的物质的量之比为( )
2 4
A.7∶1 B.1∶7
C.7∶8 D.8∶7
15.将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
A.铁粉剩余,溶液呈浅绿色,Cl-基本不变
B.向溶液中滴入无色KSCN溶液,仍无色
C.Fe2+与Fe3+物质的量之比为6∶1
D.氧化产物与还原产物的物质的量之比为2∶5
二、填空题(本题包括3个小题,共40分)
16.(12分)由价类二维图写出相关的方程式。
(1)写出符合Ⅰ的离子方程式
①将HS气体通入FeCl 溶液中产生淡黄色沉淀: 。
2 3
②向FeCl 溶液滴入KI淀粉溶液,溶液变蓝: 。
3
③FeCl 可溶解铁片: 。
3
(2)写出符合Ⅱ的离子方程式
①向FeCl 溶液滴加氯水: 。
2
②向FeCl 溶液滴加HO: 。
2 2 2
③FeSO 可使酸性KMnO 溶液褪色: 。
4 4
17.(14分)菠菜营养丰富,素有“蔬菜之王”之称,从营养价值看是一种高效的补铁剂。 某化学
小组欲设计实验方案,探究菠菜中铁元素的化合价。
(1)甲同学查阅资料得知:草酸又名乙二酸,化学式为 HC O ,是一种二元有机弱酸,具有较
2 2 4
强的还原性。甲同学依据上述信息推测,菠菜中铁元素呈 价,其理由是
。
(2)甲同学设计实验方案,验证其推测是否正确。首先,他查阅了相关资料,得到以下信息:
①在少量含Fe3+的溶液中加入硫氰化钾(KSCN)溶液,溶液变为红色;②在少量含Fe2+的溶
液中加入酸性高锰酸钾溶液,酸性高锰酸钾溶液紫色褪去。然后,甲同学设计并动手做实验。
3
学科网(北京)股份有限公司实验步骤如下:
步骤一:
步骤二:分别取2 mL溶液B于三支试管中,实验操作和现象如表所示:
试管 加入适量检验药品 实验现象
甲 酸性高锰酸钾溶液 酸性高锰酸钾溶液紫色褪去
乙 硫氰化钾溶液 溶液不变红色
丙 先加入稀硝酸,再加入硫氰化钾溶液 溶液变红色
请回答下列问题:
①实验步骤一中的操作②和③的名称是 。
②此实验证明菠菜中含有 (填“Fe2+”或“Fe3+”)。Fe2+和Fe3+可以相互转化,其中稀
硝酸可以使两种离子间发生怎样的转化? 。
(3)拓展研究:除了食物补铁外,还可以通过药物补铁,目前有一种补铁剂的主要成分是硫酸亚
铁,以铁屑(主要成分是Fe和Fe O)为原料,如何制备硫酸亚铁?
2 3
(写出相关反应的化学方程式)。
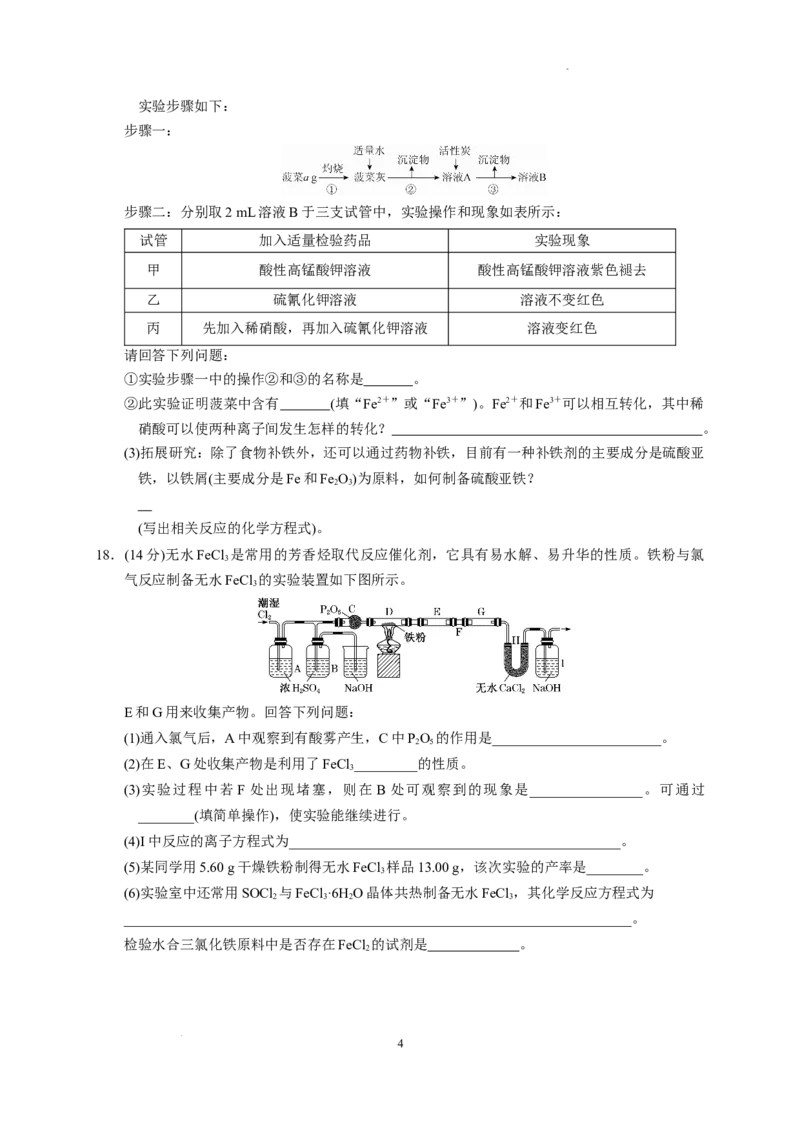
18.(14分)无水FeCl 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯
3
气反应制备无水FeCl 的实验装置如下图所示。
3
E和G用来收集产物。回答下列问题:
(1)通入氯气后,A中观察到有酸雾产生,C中PO 的作用是________________________。
2 5
(2)在E、G处收集产物是利用了FeCl _________的性质。
3
(3)实验过程中若 F 处出现堵塞,则在 B 处可观察到的现象是________________。可通过
________(填简单操作),使实验能继续进行。
(4)I中反应的离子方程式为_______________________________________________。
(5)某同学用5.60 g干燥铁粉制得无水FeCl 样品13.00 g,该次实验的产率是________。
3
(6)实验室中还常用SOCl 与FeCl ·6H O晶体共热制备无水FeCl ,其化学反应方程式为
2 3 2 3
________________________________________________________________________。
检验水合三氯化铁原料中是否存在FeCl 的试剂是 。
2
4
学科网(北京)股份有限公司1.答案:A
解析:从题中信息“滴入几滴氯水,再滴加KSCN溶液,原溶液立即变为红色”判断,黑色粉末中
含有铁元素。Fe O 为红棕色粉末,A项错误;该灰黑色粉末为还原铁粉,用于吸收包装盒中的氧
2 3
气,防止高档茶叶、点心等变质,B、C、D项正确。
2.答案:D
解析:要实现Fe3+―→Fe2+的转化,需要加入还原剂,且不引入新的杂质离子,最好的办法是加入
足量铁粉充分反应后过滤,发生的化学反应为2FeCl +Fe===3FeCl 。
3 2
3.答案:C
解析:选C A项,KSCN溶液不能直接检验Fe2+的存在,Fe2+是否存在不确定,检验方法不合理;
B项,Fe3+干扰Fe2+的检验,若原溶液中含有Fe3+且不含Fe2+,也会产生相同现象,检验方法不合
理;C项,Fe3+与OH-生成红褐色的Fe(OH) 沉淀,检验方法合理;D项,Mg(OH) 为白色沉淀,
3 2
易被红褐色沉淀掩盖,无法确定原溶液中是否含有Mg2+,检验方法不合理。
4.答案:D
解析:由于盐酸中H+的氧化性弱,故铁与盐酸反应时Fe只能被氧化为Fe2+,A项错误;B项是化
学方程式,不是离子方程式;C项中电荷不守恒,错误。
5.答案:C
解析:在该溶液中先加入少量NH SCN溶液,溶液不变红色,证明无 Fe3+存在,再加入氯水,将
4
Fe2+氧化成Fe3+,溶液变为红色。KMnO 溶液呈紫红色,溶液颜色变化不明显,所以不能用酸性
4
KMnO 溶液检验。
4
6.答案:B
解析:设计的步骤:先加KSCN溶液,无现象,可证明溶液中不含Fe3+,然后再滴加氯水,若溶液
呈红色,说明溶液中含有Fe2+。
7.答案:C
解析:实验③中现象错误,CuSO 溶液为蓝色,CuSO 与FeCl 不反应,混合后溶液不会变成无色;
4 4 3
实验④涉及反应的离子方程式为Ag++Cl-===AgCl↓,体现的是Cl-的性质。
8.答案:B
解析:A项,弱电解质NH ·H O不能拆写成离子的形式,A错误;C项,离子方程式中除遵循原子
3 2
守恒外,电荷也必须守恒,正确的离子方程式应为 Fe+2Fe3+===3Fe2+,C错误。D项,只符合原子
守恒,不符合电荷守恒,正确的离子方程式应为2Fe2++Cl===2Fe3++2Cl−,D错误。
2
9.答案:A
解析:A项,向某溶液中加入NaOH溶液,立即产生红褐色沉淀,说明溶液中一定含有Fe3+,正确;
B项,向某溶液中加入KSCN溶液,溶液变为红色,可知该溶液中一定含有Fe3+,不能确定是否存
在Fe2+,错误;C项,很多还原剂能使酸性高锰酸钾溶液褪色,Fe2+只是其中一种,错误;D项,
若溶液中只存在Fe3+,也能出现该现象,错误。
5
学科网(北京)股份有限公司10.答案:B
解析:①钠在纯氧中燃烧生成淡黄色的NaO;②FeSO 与NaOH反应生成Fe(OH) ,在空气中放置
2 2 4 2
一段时间后生成红褐色Fe(OH) ;③FeCl 与KSCN反应生成红色Fe(SCN) ;④CuSO 遇医用酒精
3 3 3 4
中的水变成蓝色。
11.答案:A
解析:设参加反应的Fe3+的物质的量为x, Fe+2Fe3+===3Fe2+
x 1.5x
完全反应后,溶液中的Fe3+和Fe2+物质的量相等,即溶液中剩余Fe3+的物质的量为1.5x,所以
已反应的Fe3+和未反应的Fe3+的物质的量之比为x∶1.5x=2∶3。
12.答案:B
解析:FeCl 溶液腐蚀印刷电路板上铜的反应为2FeCl +Cu===2FeCl +CuCl ,所得的溶液中存在
3 3 2 2
FeCl 和CuCl ,还可能有过量的FeCl 溶液,加入铁粉充分反应后,若无固体剩余,说明原溶液中
2 2 3
含有Fe3+,反应后不一定还含有Fe3+,A项错误;不管固体是铁粉还是铜粉,溶液中一定含有Fe2
+,B项正确;若溶液中有Cu2+,可能有部分铜固体析出,C项错误;若溶液中有Fe2+,不一定有
Cu析出,D项错误。
13.答案:B
解析:混合溶液中加入铁粉依次发生如下反应:2Fe3++Fe===3Fe2+、Cu2++Fe===Fe2++Cu、2H+
+Fe===Fe2++H↑,由于铁粉有剩余,故此时溶液中阳离子主要有Mg2+和Fe2+。
2
14.答案:A
解析:设参与反应的CuSO 与HSO 的物质的量分别为x、y。
4 2 4
Fe+Cu2+===Fe2++Cu
x x x
Fe+2H+===Fe2++H↑
2
y 2y 由题意得:56(x+y)=64x,解得:x∶y=7∶1。
15.答案:C
解析:n(Fe)=0.02 mol,n(FeCl )=0.05 mol,由Fe+2Fe3+===3Fe2+知,Fe3+过量0.01 mol,铁粉全
3
部溶解,反应生成Fe2+ 0.06 mol。由此可知A项错误,C项正确;Fe3+过量,滴入无色KSCN溶液,
溶液显红色,B项错误;氧化生成的Fe2+和还原生成的Fe2+的物质的量之比为1∶2,D项错误。
16.答案: (1) ①HS+2Fe3+===S↓+2Fe2++2H+
2
②2I-+2Fe3+===I +2Fe2+。
2
③2Fe3++Fe===3Fe2+。
(2) ①2Fe2++Cl===2Fe3++2Cl-。
2
②2Fe2++HO+2H+===2Fe3++2HO。
2 2 2
③5Fe2++MnO+8H+===5Fe3++Mn2++4HO。
2
17.答案:(1) +2 草酸类物质具有较强的还原性,与氧化性较强的Fe3+无法共存
6
学科网(北京)股份有限公司(2) ①过滤 ②Fe2+ 硝酸和Fe2+能发生氧化还原反应,把Fe2+氧化成Fe3+
(3) Fe+HSO ===FeSO+H↑、Fe O+3HSO ===Fe (SO )+3HO、
2 4 4 2 2 3 2 4 2 4 3 2
Fe+Fe (SO )===3FeSO
2 4 3 4
解析:(1)草酸类物质具有较强的还原性,Fe3+具有较强的氧化性,二者不能共存。(2)①过滤可以
将不溶性固体和液体分离,故实验步骤一中的操作②和③的名称是过滤。②甲中加入适量酸性高锰
酸钾溶液,酸性高锰酸钾溶液紫色褪去,说明溶液中可能含Fe2+;乙中加入适量硫氰化钾溶液,溶
液不变红,说明溶液中不含Fe3+;丙中先加入稀硝酸,再加入硫氰化钾溶液,溶液变红,故菠菜中
含有Fe2+。由于硝酸有强氧化性,Fe2+有还原性,所以硝酸和Fe2+能发生氧化还原反应,把Fe2+氧
化成Fe3+。(3)铁屑(主要成分是Fe和Fe O)与硫酸反应的化学方程式为 Fe+HSO ===FeSO +
2 3 2 4 4
H↑、Fe O+3HSO ===Fe (SO )+3HO、Fe+Fe (SO )===3FeSO。
2 2 3 2 4 2 4 3 2 2 4 3 4
18.答案:(1)除去酸雾 (2)易升华 (3)B处有气泡产生 适当加热F处
(4)Cl +2OH-===Cl-+ClO-+HO
2 2
(5)80.00%
(6)FeCl ·6H O+6SOCl ===FeCl +12HCl+6SO 铁氰化钾
3 2 2 3 2
解析:潮湿的氯气通过浓硫酸时,水与浓硫酸相遇放出大量的热使三氧化硫逸出,三氧化硫遇到瓶
内的空气中水蒸气形成酸雾,C中五氧化二磷的作用是除去酸雾,干燥的氯气和铁粉在D中反应生
成氯化铁,因氯化铁易升华,到达 E、G后重新凝华收集得到氯化铁,未反应完的氯气用 I中
NaOH溶液吸收,H中无水氯化钙防止I中水蒸气进入G中使氯化铁水解。
(3)实验过程中若F处出现堵塞,则氯气将到达B处,看到有气泡产生,然后进入NaOH溶液中与
NaOH反应;氯化铁易升华,则可通过适当加热 F处,使实验能继续进行。(4)I中未反应完的氯气
和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为 Cl +2OH-===Cl-+ClO-+
2
HO。
2
(5)由2Fe+3Cl=====2FeCl 可知,5.60 g(0.1 mol)干燥铁粉理论上可制得0.1 mol FeCl ,质量为0.1
2 3 3
mol×162.5 g·mol-1=16.25 g,因此该次实验的产率是×100%=80.00%。(6)若直接加热FeCl ·6H O,
3 2
氯化铁会水解得氢氧化铁和HCl,HCl挥发,促进氯化铁水解,最终得到氢氧化铁,实验室中常用
SOCl 与FeCl ·6H O晶体共热制备无水FeCl ,说明该过程产生了HCl抑制氯化铁水解,结合原子
2 3 2 3
守恒可知该反应的化学方程式为FeCl ·6H O+6SOCl ===FeCl +12HCl+6SO ;亚铁离子与铁氰化
3 2 2 3 2
钾相遇产生蓝色沉淀,因此检验水合三氯化铁原料中是否存在FeCl 的试剂是铁氰化钾溶液。
2
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司