文档内容
人教版(2019)必修一第三章第一节 铁及其化合物
强化训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1、铁是当前应用量最大的金属元素。下列说法错误的是( )
A.生铁与普通钢都是以铁为主的含碳合金
B.与铜质水龙头连接处的铁水管不容易发生腐蚀
C.红色涂料中的“铁红”,其主要化学成分是
D.食用富含维生素C的食物有助于人体对铁元素的吸收
2、载人潜水器的外壳是耐超高压的钛合金。下列有关合金的说法中正确的是( )
A.钛合金是一种新型的金属单质
B.钛合金的熔点比成分金属的低,硬度小
C.钛合金的化学性质与钛单质相同
D.青铜、碳素钢、合金钢和硬铝均是合金
3、某学生以铁丝和 为原料进行下列实验。
从分类角度分析,下列说法正确的是( )
A.实验①③反应制得的物质均为纯净物
B.实验②③均发生氧化还原反应
C.实验①中发生的反应是化合反应
D.实验①②所涉及的物质均为电解质或非电解质
4、向 的 溶液中加入足量的铁片并加热。充分反应后,溶液中溶质的成分和
所得气体的成分分别是( )
A.硫酸铁;二氧化硫
B.硫酸亚铁;二氧化硫、氢气
C.硫酸铁、硫酸亚铁;二氧化硫、氢气
D.硫酸铁;二氧化硫、氢气
5、下列物质反应后一定有+ 3价铁生成的是( )①过量的Fe与 反 应
② Fe与过量稀硫酸反应
③ 溶液中通入少量
④ Fe和 的混合物溶于盐酸中
A.只有① B.①③ C.①②③ D.全部
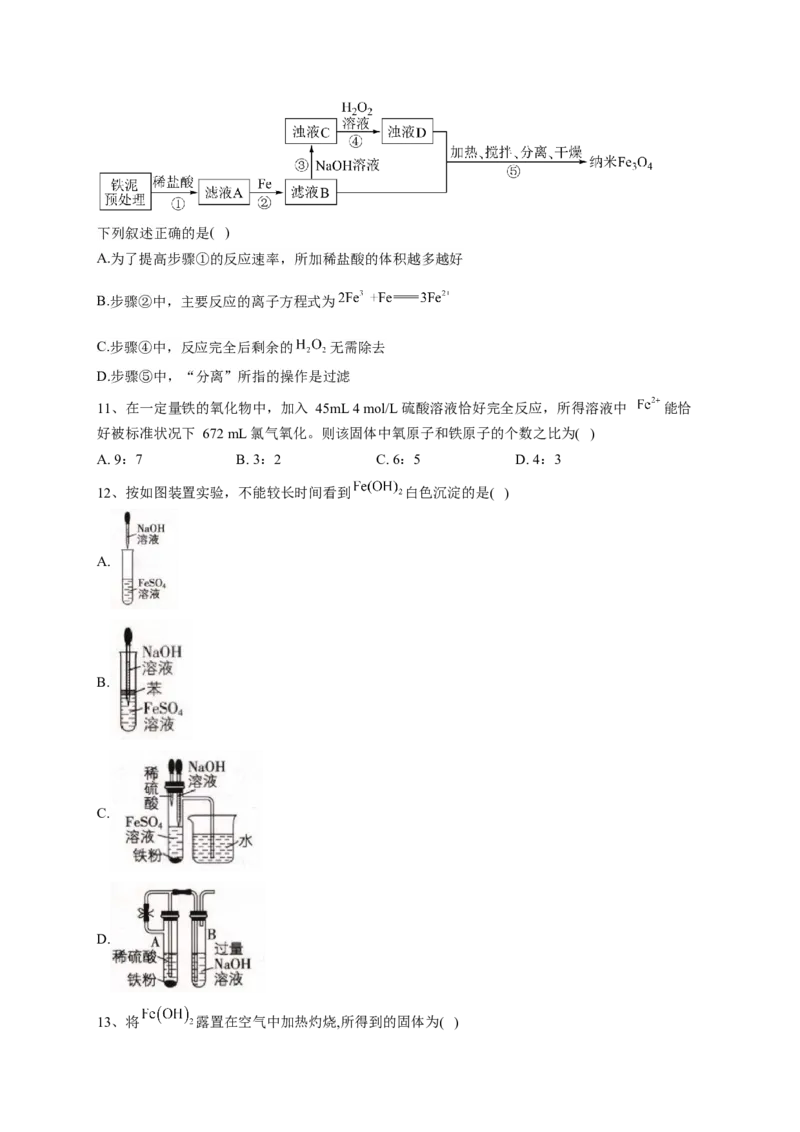
6、用如图所示装置进行Fe与水蒸气反应的实验,下列有关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中反应的化学方程式是
C.装置C中加入的固体干燥剂可以是碱石灰
D.点燃D处气体前必须检验气体的纯度
7、将1.12g铁粉加入到25mL 2 的氯化铁溶液中充分反应,下列说法正确的是( )
A.铁粉有剩余,反应后的溶液呈浅绿色
B.向反应后的溶液中滴入无色KSCN溶液,溶液仍呈无色
C.反应后的溶液中 和 的物质的量之比为6:1
D.氧化产物与还原产物的物质的量之比为2:5
8、2020年1月7日,文化和旅游部发布公告,正式确定甘肃省张掖七彩丹霞景区为国家5A级旅
游景区。丹霞地貌的岩层呈红色是因为含( )
A. B. C.FeO D.
9、关于铁的三种氧化物( )的下列叙述中正确的是( )
A.铁的三种氧化物中铁元素的化合价完全相同
B.都是碱性氧化物,都能与盐酸反应生成氯化铁和水
C.氧化亚铁在空气中加热可生成更稳定的四氧化三铁
D.四氧化三铁中铁元素有+2价和+3价,它是一种混合物
10、工业上用铁泥(主要成分为 和少量Fe)制备纳米 的流程图如下:下列叙述正确的是( )
A.为了提高步骤①的反应速率,所加稀盐酸的体积越多越好
B.步骤②中,主要反应的离子方程式为
C.步骤④中,反应完全后剩余的 无需除去
D.步骤⑤中,“分离”所指的操作是过滤
11、在一定量铁的氧化物中,加入 45mL 4 mol/L 硫酸溶液恰好完全反应,所得溶液中 能恰
好被标准状况下 672 mL 氯气氧化。则该固体中氧原子和铁原子的个数之比为( )
A. 9:7 B. 3:2 C. 6:5 D. 4:3
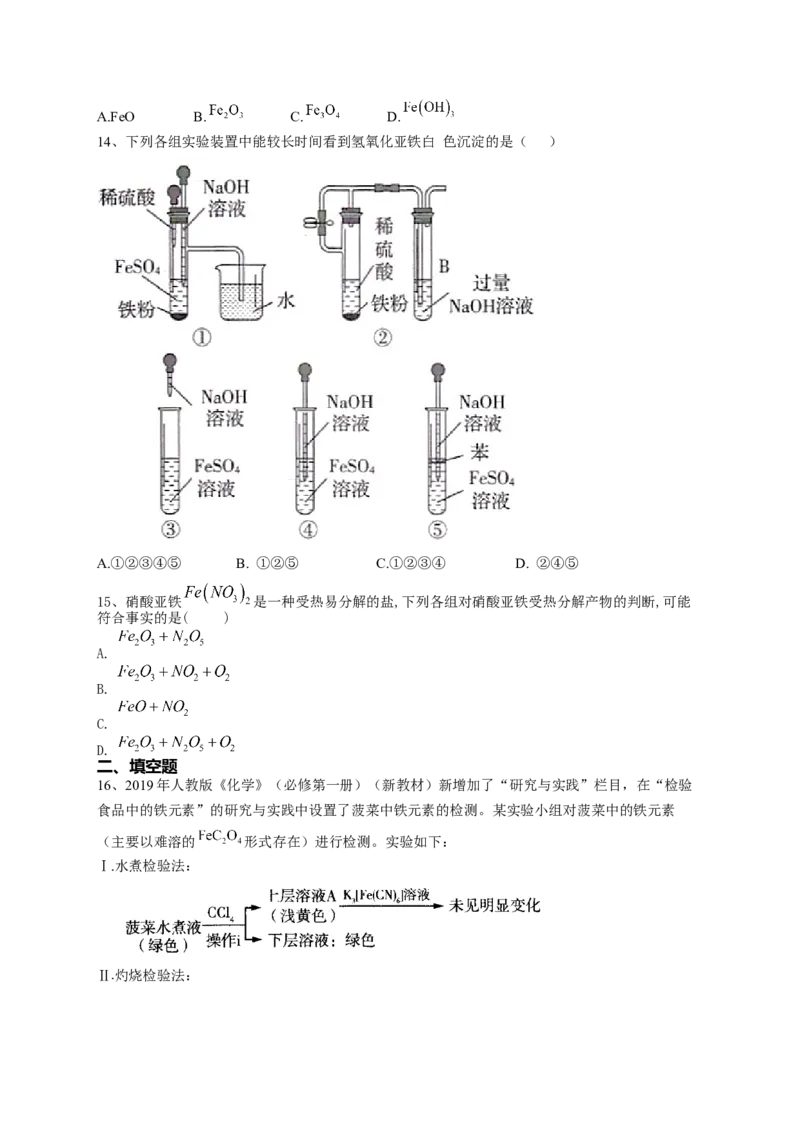
12、按如图装置实验,不能较长时间看到 白色沉淀的是( )
A.
B.
C.
D.
13、将 露置在空气中加热灼烧,所得到的固体为( )A.FeO B. C. D.
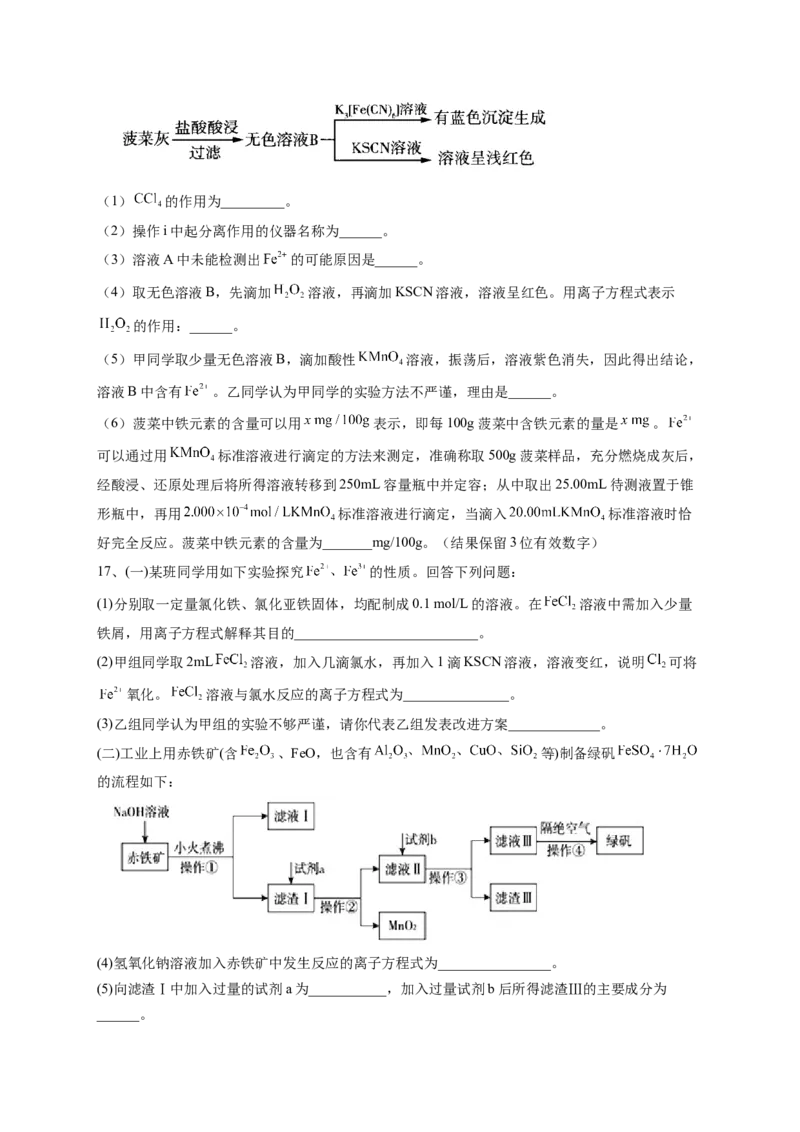
14、下列各组实验装置中能较长时间看到氢氧化亚铁白 色沉淀的是( )
A.①②③④⑤ B. ①②⑤ C.①②③④ D. ②④⑤
15、硝酸亚铁 是一种受热易分解的盐,下列各组对硝酸亚铁受热分解产物的判断,可能
符合事实的是( )
A.
B.
C.
D.
二、填空题
16、2019年人教版《化学》(必修第一册)(新教材)新增加了“研究与实践”栏目,在“检验
食品中的铁元素”的研究与实践中设置了菠菜中铁元素的检测。某实验小组对菠菜中的铁元素
(主要以难溶的 形式存在)进行检测。实验如下:
Ⅰ.水煮检验法:
Ⅱ.灼烧检验法:(1) 的作用为_________。
(2)操作i中起分离作用的仪器名称为______。
(3)溶液A中未能检测出 的可能原因是______。
(4)取无色溶液B,先滴加 溶液,再滴加KSCN溶液,溶液呈红色。用离子方程式表示
的作用:______。
(5)甲同学取少量无色溶液B,滴加酸性 溶液,振荡后,溶液紫色消失,因此得出结论,
溶液B中含有 。乙同学认为甲同学的实验方法不严谨,理由是______。
(6)菠菜中铁元素的含量可以用 表示,即每100g菠菜中含铁元素的量是 。
可以通过用 标准溶液进行滴定的方法来测定,准确称取500g菠菜样品,充分燃烧成灰后,
经酸浸、还原处理后将所得溶液转移到250mL容量瓶中并定容;从中取出25.00mL待测液置于锥
形瓶中,再用 标准溶液进行滴定,当滴入 标准溶液时恰
好完全反应。菠菜中铁元素的含量为_______mg/100g。(结果保留3位有效数字)
17、(一)某班同学用如下实验探究 的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在 溶液中需加入少量
铁屑,用离子方程式解释其目的__________________________。
(2)甲组同学取2mL 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
氧化。 溶液与氯水反应的离子方程式为_______________。
(3)乙组同学认为甲组的实验不够严谨,请你代表乙组发表改进方案_____________。
(二)工业上用赤铁矿(含 、FeO,也含有 等)制备绿矾
的流程如下:
(4)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为________________。
(5)向滤渣Ⅰ中加入过量的试剂a为___________,加入过量试剂b后所得滤渣Ⅲ的主要成分为
______。(6)操作③需要的玻璃仪器主要包括__________。
(7)操作④需要隔绝空气的主要原因可能是什么?_______________。
18、阅读下面科普信息,回答问题:
一个体重50kg的健康人体内含铁2g,亚铁离子易被人体吸收,给贫血者补充铁时,应给予含亚铁
离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸
收。
(1)以下为铁元素的几种常见微粒,其中既有氧化性又有还原性的是________(填序号)。
A.Fe
B.
C.
(2)工业盐的主要成分是 ,曾多次发生因误食工业盐而中毒的事件,中毒原因是
把人体内的 转化为 而使其失去与 结合的能力,这说明 具有________性。下列不
能实现上述转化的物质是________(填序号)。
A.
B.
C.
D.
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________性。
(4)在 的反应中, 表现了________性和
________性。
19、某同学为探究已保存较长时间的硫酸亚铁药品是否变质。设计了如下实验方案:
(1) 试剂①的主要成分的化学式是_____________。
(2) 加入新制氯水后溶液红色加深的原因是___________(用离子方程式表示)。
(3) 该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1: 溶液中的+3价铁被氧化为更高价态的铁;假设2: _______________。
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案___________。
(4) 应用拓展
写出实验室保存 固体的方法___________。20、实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料 。其主要
实验流程如下:
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使 完全转化为 。“还原”过程中除生
成 外,还会生成_______(填化学式);检验 是否还原完全的实验操作是_______。
三、实验题
21、硫酸亚铁铵[(NH ) Fe(SO ) ]是分析化学中的重要试剂:某学习小组为探究其分解产物设计如下
4 2 4 2
实验装置。
硫酸亚铁铵在500℃时隔绝空气加热完全分解,固体产物可能有FeO和Fe O ,气体产物可能有NH 、
2 3 3
SO 、SO 、N 和H O
3 2 2 2
1.A中固体充分加热较长时间后,通入氮气,目的是__________
2.能证明气体产物中有SO 的实验现象是__________
2
3.设计一个实验方案,用化学方法证明固体产物不含二价铁:__________
22、 和 是红色粉末,常作颜料。某校化学实验小组通过实验来探究红色粉末的成分是
、 或二者的混合物。
探究过程如下:
查阅资料
溶于稀硫酸生成Cu和 ,在空气中加热生成CuO。
提出假设
假设1:红色粉末是 ;
假设2:红色粉末是 ;
假设3:红色粉末是 和 的混合物。
设计实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN溶液。
(1)若假设1成立,则实验现象是__________;若假设2成立,发生反应的离子方程式为
__________。
(2)经实验分析,确定红色粉末为 和 的混合物,设计实验计算二者的物质的量:取一
定量的该固体粉末溶于500mL未知浓度的稀硫酸中,固体全部溶解,向反应后的溶液中加入Fe粉,
溶液中部分离子的物质的量随Fe粉加入的变化如图所示,则 和 的物质的量分别为
__________、__________。(3)硫酸溶液的物质的量浓度是__________。参考答案
1、答案:B
解析:A.生铁与普通钢都是以铁为主的含碳合金,生铁中的含碳量大于钢中的含碳量,故A正确;
B.铜、铁和自来水能构成原电池,铁做负极,所以与铜质水龙头连接处的铁水管容易发生吸氧腐
蚀,故B错误; C. 是红棕色粉末,红色涂料中的“铁红”,其主要化学成分是 ,故C
正确; D.维生素C具有还原性,人体吸收的是二价铁,而二价铁易被氧化,所以食用富含维生素
C的食物有助于人体对铁元素的吸收,故D正确;故选B。
2、答案:D
解析:合金是指两种或两种以上的金属或金属与非金属 熔合而成的具有金属特性的物质,不属于
新型金属单质,A 错误;合金的熔点一般比成分金属的熔点低但硬度大,B错误;合金的化学性质
与其成分金属的化学性质是相同的,钛合金除具备钛单质的化学性质外,还具有其他成分的化学
性质,C错误。
3、答案:C
解析:实验③得到的是氢氧化铁胶体,是混合物,A项错误;实验②是 的溶解,
是物理变化,实验③中的反应中无元素化合价变化,两实验均未发生氧化还原反应,
B项错误;实验①中发生反应的化学方程式为 ,是化合反应,
C项正确;实验①中的铁和氯气是单质,二者既不是电解质也不是非电解质,D项错
误。
4、答案:B
解析:浓硫酸与铁在加热的条件下反应生成硫酸铁、二氧化硫和水,当浓硫酸变稀后,过量的铁
将三价铁离子还原成亚铁离子,稀硫酸与铁反应生成硫酸亚铁和氢气,所以B项正确。
5、答案:B
解析:①中的 氧化性强,它能将铁氧化为+3 价,由于不是在溶液中反应,因此过量的
铁不会将氯化铁还原;②中 Fe与稀硫酸反应只能生成 ,③在溶液中 被 氧化生成
。④中依次发生:i ) Fe 0 与盐酸反应生成 的反应,ii ) Fe与 生成 的反
2 3
应,iii )Fe与盐酸反应生成 ,但题中未 给出反应物间相对量的关系,若铁是足量的,
则能将生成的 全部还原为 .
6、答案:B
解析:A.装置A是液态水在加热的条件下加热产生水蒸气的装置,作用是为实验提供持续不断的
水蒸气,故A正确;
B.Fe与水蒸气反应产物是四氧化三铁和氢气,B中反应的化学方程式是 ,
故B错误;C.氢气属于中性气体,可以用碱石灰做干燥剂,故C正确;
D.氢气在点燃之前应该先检验气体的纯度,防止发生爆炸,故D正确。
故选:B。
7、答案:C
解析:n(Fe)=0.02mol, 由 知,反应后 剩余0.01mol,铁粉全
部溶解,反应生成0.06mol ,A项错误,C项正确; 过量,滴入无色KSCN溶液,溶液显红色,B项
错误;氧化产物与还原产物的物质的量之比为1:2.D项错误。
8、答案:D
解析:根据题目所给的岩层是红色,可推测成分是 ; 虽也呈红褐色,但岩层长期风
吹日晒,不会是 ; ,故较稳定的红色岩石为 ;
不能稳定存在于空气中,它是白色沉淀, 是黑色固体,在空气中不能稳定存在。
9、答案:C
解析:A.氧化亚铁中铁元素得化合价为+2价,氧化铁中为+3价,四氧化三铁中为+2和+3价,故A
错误;B.氧化亚铁与盐酸反应生成氯化亚铁和水,为碱性氧化物。氧化铁与盐酸反应生成氯化铁和
水,为碱性氧化物。四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水,不符合碱性氧化物的概
念,故B错误;C.氧化亚铁在空气中加热能生成稳定性更好的四氧化三铁,故C正确; D.四氧化
三铁中铁元素有+2价和+3价,但它不是混合物,是化合物,故D错误;故选:C。
10、答案:B
解析:A.稀盐酸的量越多不能使反应速率加快,搅拌、适当升高温度可提高铁泥与盐酸的反应速率,
A错误;
B.滤液A的溶质为氯化铁、氯化亚铁、过量的稀盐酸,加入铁粉还原 ,即主要的离子反应为:
,B正确;
C.步骤④中,浊液C中的氢氧化亚铁被过氧化氢氧化成浊液D,为了提高 的产率需要控制浊
液D与滤液B中 的比例,为防止滤液B中 在步骤⑤中被 氧化,步骤④中反应完成后
需再加热一段时间除去剩余 ,C错误;
D.步骤⑤为浊液D与滤液B加热搅拌发生反应制得 ,使 分离出来需经过过滤、洗涤、
干燥,D错误;故答案选B。
11、答案:A
解析:铁的氧化物与硫酸反应生成硫酸盐和水,由H、O守恒可知, (氧化
物中的O),硫酸的物质的量为0.045 L ×4 mol/L=0.18 mol ,可知氧化物中含O为0.1 8mol; 能恰好被标准状况下672 mL 氯气氧化,由电子守恒可知 ,
;铁的氧化物中正负化合价的代数和为0,设 ,则
,解得 ,该固体中氧原子和铁原子的个数之比为
,故选项A符合题意。综上所述,本题正确答案为A。
12、答案:A
解析:空气中的氧气能迅速将生成的 氧化,因而不能较长时间看到 白色沉淀,A
符合题意;苯层能够隔绝空气,保证NaOH与 发生复分解反应生成的 白色沉淀不被
氧化,能够长时间观察到白色沉淀,B不符合题意;Fe与 反应产生 、 , 能够将
溶液及装置中的空气排出,使 处于 的惰性环境中,然后加入NaOH溶液,NaOH与
发生复分解反应产生 白色沉淀,能较长时间看到白色沉淀,C不符合题意;打开装
置A的止水夹,Fe与 反应产生 、 , 能够将A、B两个试管中的空气排出,
处于 的惰性环境中,然后关闭装置A的止水夹,反应产生的 将装置A中 溶液
压入装置B中的NaOH溶液,二者反应产生 白色沉淀,能较长时间看到白色沉淀,D不符
合题意。
13、答案:B
解析:因 极易被空气中的氧气氧化,当露置于空气中时, 首先转化为 ,
然后 受热分解生成 和 。
14、答案:B
解析:因为 在空气中很容易被氧化为红褐色 的 ,即发生
。因此要较长时间看到 白色沉淀,就 要排除装置中
的氧气或空气。
15、答案:B
解析:略
16、答案:(1)作萃取剂,萃取有机色素,排除对 检验的干扰
(2)分液漏斗
(3) 在水中的溶解度小;在加热水煮过程中二价铁被氧化为三价铁
(4)
(5)酸性条件下, 和 都可能将 还原
(6)2.24
解析:(1) 作萃取剂,萃取有机色素,排除对 检验的干扰。(2)操作i用来分离互不相溶的液体,名称是分液,操作中起分离作用的仪器是分液漏斗。
(3)铁元素主要以难溶的 形式存在, 的浓度小;或在加热水煮过程中二价铁被氧化
为三价铁,所以溶液A中未能检测出 。
(4) 把 氧化为 ,反应的离子方程式是 。
(5)用盐酸溶解菠菜灰得到的溶液B中含有 ,还可能含有少量 ,酸性条件下,
和 都可能将 还原,所以滴加酸性 溶液,振荡后,溶液紫色消失,不能证
明溶液B中含有 。
(6) 与酸性 的反应为 。设25.00mL待测
液中含 ,则有
,解得 ,则250mL待测液中含 的物质的量为
, ,所以菠菜中
铁元素的含量为 。
17、答案:(1)
(2) 、
(3)在 溶液的液面上覆盖一层煤油,就可以使溶液与空气隔离,排除氧气对实验的影响
(4) 、
(5)稀硫酸;铁和铜
(6)漏斗、玻璃棒、烧杯
(7)防止硫酸亚铁被氧化
解析:(1) 极易被空气中的 氧化成 ,加入铁屑后, 可与Fe发生反应
,就起到防止 被氧化的作用,故答案为: ;(2)氯气具有氧化性能氧化氯化亚铁为氯化铁 ,故答案为
;
(3)检验溶液中是否存在 时,应先排除溶液中 的干扰,故应先加入KSCN溶液,无明显
现象再加入氯水,若溶液变红色,则说明 可将 氧化,故答案为:先加入1滴KSCN溶液,
无现象,再加入几滴氯水,溶液变红,说明 可将 氧化
;
(4)赤铁矿中的 、 分别能与NaOH溶液发生如下反应 、
,故答案为 、
;
(5)滤渣的成分为赤铁矿中与NaOH溶液不反应的CO、 ,操作②后所得固体为 。所
得滤液Ⅲ为 溶液,最终欲得到 ,故试剂b为Fe,充分反应后过滤所得滤渣Ⅲ
为Fe和Cu的混合物。故答案为:稀硫酸,铁和铜。
(6)操作③后得到固体和溶液,为过滤操作,仪器有漏斗、玻璃棒、烧杯,答案为:漏斗、玻璃
棒、烧杯;
(7)操作④为 溶液蒸发结晶的操作,由于 易被空气中的 氧化成 ,故需
要隔绝空气进行蒸发结晶,答案为:防止硫酸亚铁被氧化。
18、答案:(1)B
(2)氧化;C
(3)还原
(4)氧化;酸
解析:(1)所含元素处于最低价态的粒子只有还原性,所以Fe只有还原性,故A不符合题意;
所含元素处于中间价态的粒子既有氧化性又有还原性,所以 既有氧化性又有还原性,故B符
合题意;所含元素处于最高价态的粒子只有氧化性,所以 只有氧化性,故C不符合题意。
(2)因为 发生了氧化反应,所以 具有氧化性。因为 具有强氧化性,能把
转化为 ,故A不符合题意; 能把 转化为 ,故B不符合题意; 与 不
能反应, 不能实现题述转化,故C符合题意; 具有强氧化性,能把 转化为
,故D不符合题意。(3)工业盐的主要成分是是 , 具有氧化性,把人体内的 转化为 而使其失
去与 结合的能力,为缓解中毒,应使 ,应加入具有还原性的物质。维生素C能缓解
中毒,所以具有还原性。
(4)在 的反应中,一部分 起氧化作用,生成
NO,另一部分则起酸性作用生成 ,所以 既表现了氧化性又表现了酸性。
19、答案:(1)KSCN
(2) 、
(3)① 被过量的氯水氧化
②取少量褪色后的溶液于试管中,滴加过量KSCN溶液,若出现红色,则说明假设2成立,若不出
现红色,则说明假设2不成立
(4)密封保存
解析: (1) 与KSCN溶液反应生成红色的 ,所以试剂1的主要成分为:KSCN,
(2)淡红色溶液中还含有较多的 ,向其中加入新制氯水时, 将 氧化成 ,溶液中
浓度增大,生成的 浓度也增大,发生的反应有: 、
,因此溶液红色加深,
(3)①实验中加入过量氯水,放置一段时间后,深红色褪去,说明 逐渐消失,而
的生成与 有关,假设1认为可能是溶液中的+3价的铁被 氧化为更高价态
的铁,溶液颜色褪去,分析 中各元素的化合价可知,S为-2价,C为+4价,N为-3价,所以
也具有还原性,故也可能是 被过量的氯水氧化导致深红色褪去,所以假设2为:
被过量的氯水氧化
②假设 没有被氧化,而是 被氧化,只要向褪色后的溶液中补充 ,若出现红色,说
明假设2成立,反之则假设2不成立,具体操作为:取少量褪色后的溶液于洁净的试管中,滴加过
量KSCN溶液,若出现红色,则说明假设2成立,若不出现红色,则说明假设2不成立,
(4) 容易被空气中的氧气氧化,所以保存硫酸亚铁固体时,密封保存
20、答案:(2) ;取少量清液,向其中滴加几滴KSCN溶液,观察溶液颜色是否呈血红色解析:(2)“酸浸”时酸过量,“酸浸”后的滤液中还含有大量 , 与铁粉反应生成 ;一
般用KSCN溶液检验 。
21、答案:1.使分解产生的气体在B、C中被吸收充分; 2.C中产生白色浑浊; 3.取少量固体样品,
加入稀硫酸溶解,加入酸性KMnO 溶液,不褪色(或加入K Fe(CN) 溶液,不产生蓝色沉淀)
4 3 6
解析:
22、答案:(1)固体全溶溶液变为棕黄色,滴加KSCN溶液后溶液变红;
(2)0.15mol;0.1mol
(3)
解析:(1)若假设1成立, 与稀硫酸反应生成 ,则实验现象为固体溶解,溶液变为棕
黄色,向所得溶液滴加KSCN溶液后溶液变红。由资料知 溶于稀硫酸生成Cu和 ,铜
为红色固体,不溶于水, 溶液为蓝色,因溶液中无 ,所以滴加KSCN溶液后溶液也不
变红,反应的离子方程式为 。
(2)发生反应的离子方程式为 , ,由
于固体全部溶解,则发生反应: ,溶液中剩余 ,可能含
有 。根据图像,向反应后的溶液中加入Fe粉后,三种离子物质的量减小到0,故溶液中一定
含有 ,加入铁之后,发生的反应依次为
。
设 的物质的量为 , 的物质的量为 ,根据铁离子守恒建立关系式: ,根据铜离子守恒建立关系式: ,解得
。
(3)由图像可知,当加入0.4mol铁粉时溶液恰好为 溶液,根据铁元素守恒,含有 的
物质的量为0.4mol+0.15mol×2=0.7mol,再根据硫元素守恒, ,所以
。