文档内容
高中化学人教版(2019)选择性必修1 第二章第三节 化学反应的方向
一、单选题
1.下列说法正确的是( )
A. 非自发反应一定不能实现
B. 同种物质气态时熵值最小,固态时熵值最大
C. 反应NH (g)+HCl(g)=NH Cl(s)在室温下可自发进行,则该反应的△H <0
3 4
D. 恒温恒压下,△H <0且△S>0的反应一定不能自发进行
21世纪教育网版权所有
2.25℃和1.01×105Pa时,反应2NO(g)=4NO (g)+O(g) ΔH=+56.76 kJ·mol-1 , 自发进行的原因是(
2 5 2 2
)
A. 吸热反应 B. 放热反应
C. 熵减少的反应 D. 熵增大效应大于热效应
3.下列反应中熵显著增加的是( )
A. 2NO(g)=4NO (g)+O(g) B. Cu(s)+Cl (g)=CuCl (s)
2 5 2 2 2 2
C. C(s)+O(g)=CO (g) D. 2H(g)+O(g)=2HO(1)
2 2 2 2 2 21cnjy.com
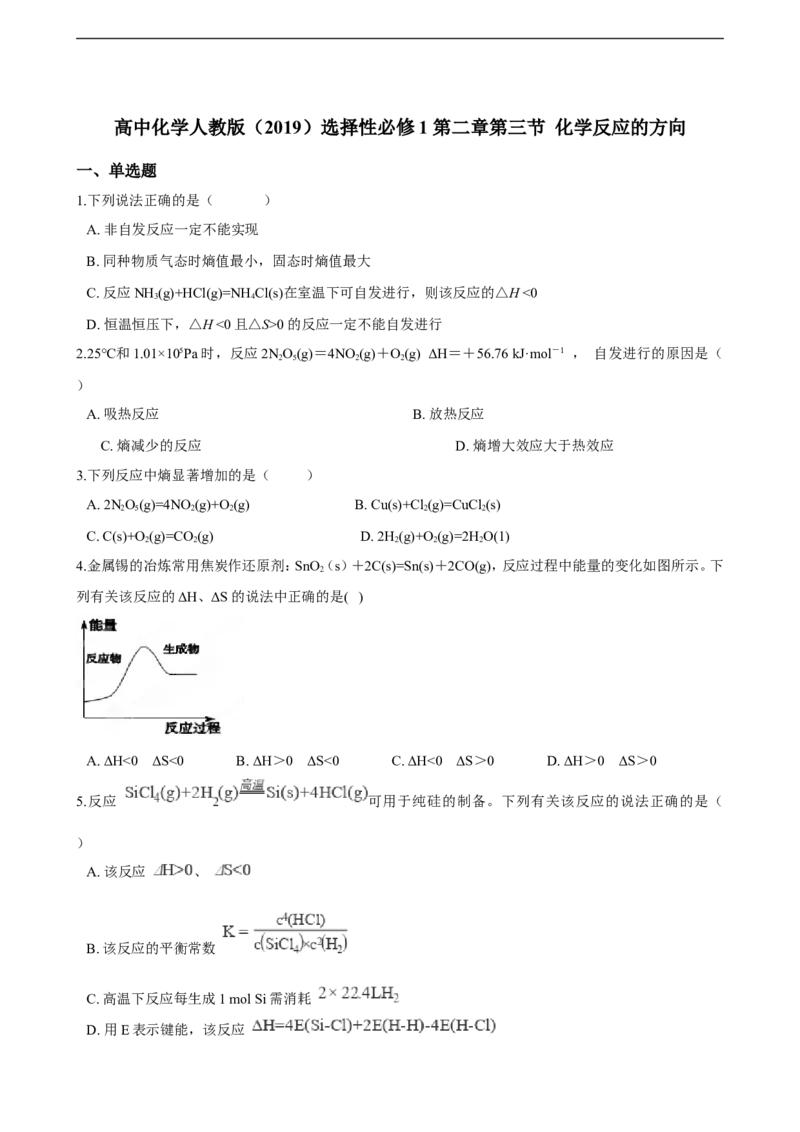
4.金属锡的冶炼常用焦炭作还原剂:SnO(s)+2C(s)=Sn(s)+2CO(g),反应过程中能量的变化如图所示。下
2
列有关该反应的ΔH、ΔS的说法中正确的是( )
www.21-cn-jy.com
A. ΔH<0 ΔS<0 B. ΔH>0 ΔS<0 C. ΔH<0 ΔS>0 D. ΔH>0 ΔS>0
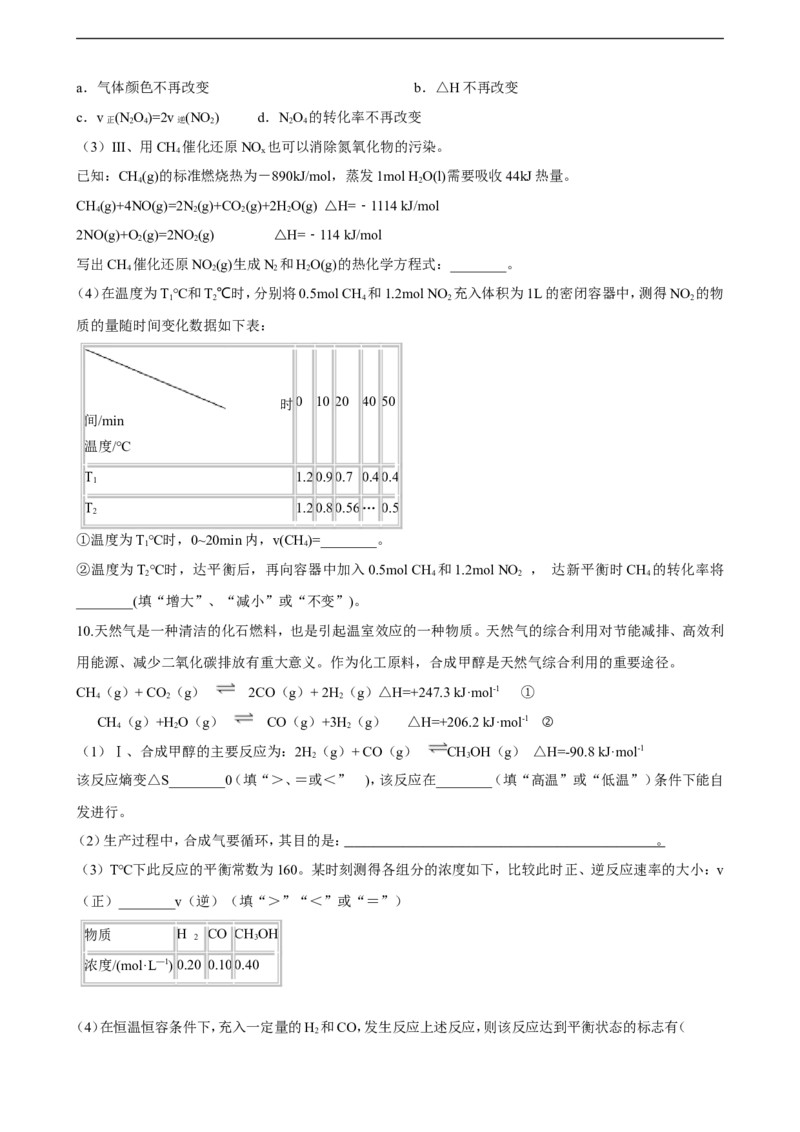
5.反应 可用于纯硅的制备。下列有关该反应的说法正确的是(
)
A. 该反应 、
B. 该反应的平衡常数
C. 高温下反应每生成1 mol Si需消耗
D. 用E表示键能,该反应
2·1·c·n·j·y6.对于温度与反应方向的关系,下列判断不正确的是( )
A. △H<0 ,△S>0,所有温度下反应自发进行 B. △H>0 ,△S>0,所有温度下反应自
发进行
C. △H<0 ,△S<0,低温下反应自发进行 D. △H>0 ,△S<0,所有温度
下反应不能自发进行
7.灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿。把白锡制成的器皿放在0℃ (T=
273K)和1.01×105Pa的室内保存,它能否变成灰锡(已知:该条件下白锡转化为灰锡的焓变和熵变分别是△H
=-2181 kJ·mol-1 , △S=-6.61J·mol-1·K-1;当△H-T△S<0时反应能自发进行)( )
A. 能 B. 不能
C. 不能确定
D. 升温后能
8.已知:在室温下有以下平衡:
编号平衡方程式 平衡常数
① HCN H++CN- K= 1×10 -10
a
② HO H++OH- K =1×10 -14
2 w
③ CN-+H O HCN+OH- K =?
2
则下列判断错误的是( )
A. ①的ΔS >0, ΔH>0
B. 用标准 NaOH 溶液滴定浓度约为 0.01mol•L-1HCN,可用甲基橙做指示剂
C. 0. 2mol•L-1 的 HCN 溶液中加入等体积的 0.1mol•L-1NaOH 溶液,则该溶液呈碱性
D. 0. 2mol•L-1 的HCN 溶液中加入等体积的 0.1mol•L-1NaOH 所得的混合溶液中: 2c(H+)+ c(HCN) =
2c(OH-)+c (CN- )
21·cn·jy·com
二、综合题
9.进入冬季北方开始供暖后,雾霾天气愈发严重,各地PM2.5、PM10经常“爆表”。引发雾霾天气的污染物
中,最为常见的是机动车尾气中的氮氧化物和燃煤产生的烟气。
2-1-c-n-j-y
I、用 NH 催化还原 NOx 可以消除氮氧化物的污染。反应原理为:NO(g)+NO(g)+2NH (g) 2N(g)
3 2 3 2
+3H O(g)。
2 21教育名师原创作品
(1)该反应的△S________0(填“>”、“=”或“<”)。
(2)II、已知反应NO(g) 2NO (g) △H,随温度升高,混合气体的颜色变深。将一定量NO 气体充入绝热
2 4 2 2 4
容器一段时间后,研究压缩和拉伸活塞过程中混合气体的气体的透光率(气体颜色越浅,透光率越大)随时间
变化情况。
21*cnjy*com
下列说法能说明透光率不再发生改变的有________。a.气体颜色不再改变 b.△H不再改变
c.v (N O)=2v (NO ) d.NO 的转化率不再改变
正 2 4 逆 2 2 4
(3)III、用CH 催化还原NO 也可以消除氮氧化物的污染。
4 x
已知:CH(g)的标准燃烧热为-890kJ/mol,蒸发1mol HO(l)需要吸收44kJ热量。
4 2 www-2-1-cnjy-com
CH(g)+4NO(g)=2N (g)+CO (g)+2HO(g) △H=﹣1114 kJ/mol
4 2 2 2
2NO(g)+O (g)=2NO (g) △H=﹣114 kJ/mol
2 2
写出CH 催化还原NO (g)生成N 和HO(g)的热化学方程式:________。
4 2 2 2
(4)在温度为T℃和T℃时,分别将0.5mol CH 和1.2mol NO 充入体积为1L的密闭容器中,测得NO 的物
1 2 4 2 2
质的量随时间变化数据如下表:
时0 10 20 40 50
间/min
温度/℃
T 1.20.90.7 0.40.4
1
T 1.20.80.56… 0.5
2
①温度为T℃时,0~20min内,v(CH)=________。
1 4
②温度为T℃时,达平衡后,再向容器中加入0.5mol CH 和1.2mol NO , 达新平衡时CH 的转化率将
2 4 2 4
________(填“增大”、“减小”或“不变”)。
21教育网
10.天然气是一种清洁的化石燃料,也是引起温室效应的一种物质。天然气的综合利用对节能减排、高效利
用能源、减少二氧化碳排放有重大意义。作为化工原料,合成甲醇是天然气综合利用的重要途径。
CH(g)+ CO(g) 2CO(g)+ 2H (g)△H=+247.3 kJ·mol-1 ①
4 2 2 【版权所有:21教育】
CH (g)+H O(g) CO(g)+3H (g) △H=+206.2 kJ·mol-1 ②
4 2 2
(1)Ⅰ、合成甲醇的主要反应为:2H(g)+ CO(g) CHOH(g) △H=-90.8 kJ·mol-1
2 3
该反应熵变△S________0(填“>、=或<” ),该反应在________(填“高温”或“低温”)条件下能自
发进行。
(2)生产过程中,合成气要循环,其目的是: 。
21*cnjy*com
(3)T℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下,比较此时正、逆反应速率的大小:v
(正)________v(逆)(填“>”“<”或“=”)
物质 H CO CHOH
2 3
浓度/(mol·L—1)0.20 0.100.40
(4)在恒温恒容条件下,充入一定量的H 和CO,发生反应上述反应,则该反应达到平衡状态的标志有(
2)
A.混合气体的密度保持不变
B.混合气体的总压强保持不变
C.甲醇的浓度保持不变
D.v (H)= v (CHOH)
正 2 逆 3
(5)在恒温恒容条件下,要提高反应2H(g)+ CO(g) CHOH(g)中CO的转化率,可以采取的措施是
2 3
( )
21·世纪*教育网
A.升温
B.加入催化剂
C.增加CO的浓度
D.增加H 的浓度
2
E.充入惰性气体
F.分离出甲醇
【出处:21教育名师】
(6)Ⅱ、合成甲醇的另一反应为:CO(g)+3H(g) CHOH(g)+HO(g) △H=-akJ·mol-1(a>0)。
2 2 3 2
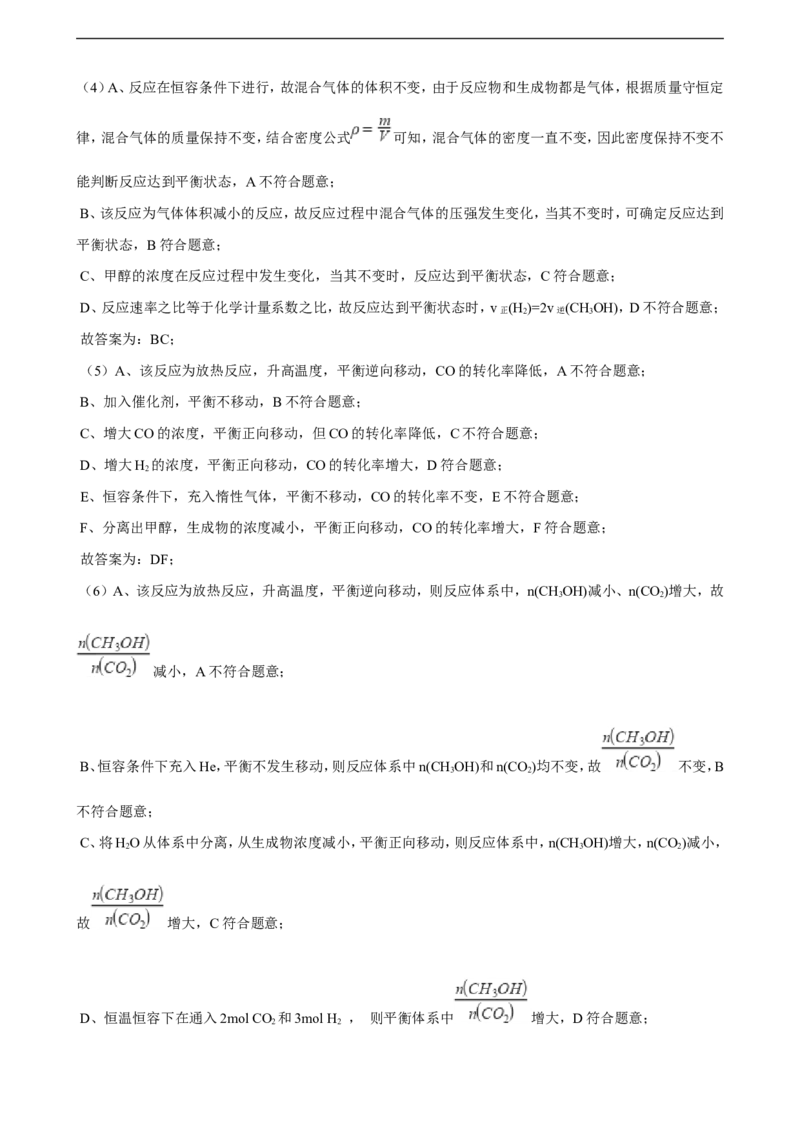
在一定温度下的2L固定容积的密闭容器中,通入2 molCO 和3mol H , 发生的反应为:测得CO(g)和
2 2 2
CHOH(g)的浓度随时间变化如图所示。
3
下列措施中能使 增大的是______(填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将HO(g)从体系中分离
2
D.恒温恒容再充入2 mol CO 和3 mol H
2 2
(7)经计算该温度下此反应的平衡常数K=0.20L2·mo l-2。若改变条件 (填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度 D.升高温度 E.加入催化剂
(8)10min内,用H 表示的该反应的化学反应速率为=________mol-1·L-1·min-1
2答案解析部分
一、单选题
1. C
解析:A.反应是否自发进行,由熵变、焓变、温度共同决定,非自发反应在改变条件下可以发生,A不符合题
意;
B.熵是指体系的混乱度,同种物质气态熵大于液态大于固态,即同种物质气态时熵值最大,固态时熵值最
小,B不符合题意;
C.反应能自发进行说明:△H-T△S<0,由方程式NH(g)+HC(l g)═NH C(l s)可知该反应的∆S<0,要使:
3 4
△H-T△S<0,所以必须满足△H<0,C符合题意
D.恒温恒压下,△H<0且△S>0的反应的△H-T△S<0,反应一定可以自发进行,D不符合题意。
故答案为:C
分析:判断反应能否自发进行由该公式确定:△G=△H-T△S,△G为吉布斯自由能变,△H为焓变,△S为
熵变,T为开氏温度。
在温度、压强一定的条件下,化学反应的判读依据为:
ΔH-TΔS<0 反应能自发进行;
ΔH-TΔS=0 反应达到平衡状态;
ΔH-TΔS>0 反应不能自发进行。
注意:(1)ΔH为负,ΔS为正时,任何温度反应都能自发进行;
(2)ΔH为正,ΔS为负时,任何温度反应都不能自发进行。
【来源:21·世纪·教育·网】
2. D
解析:该反应的ΔH>0,为吸热反应;该反应为气体分子数增大的反应,为熵增反应;该反应能自发进行,说
明熵增效应大于热效应,D符合题意;
故答案为:D
分析:根据反应自发进行的条件进行分析,反应自发进行,则该反应为焓减、熵增反应。
3. A
解析:A.该反应中,反应后气体分子数增多,熵显著增加,A符合题意;
B.该反应中,反应后气体分子数减少,熵显著减小,B不符合题意;
C.该反应中,反应前后气体分子数不变,熵不变,C不符合题意;
D.该反应中,反应后气体分子数减少,熵显著减小,D不符合题意;
故答案为:A分析:反应过程中熵显著增加,则反应后气体分子数增加,据此结合选项所给反应进行分析。
4. D
解析:反应物的总能量小于生成物总能量,该反应吸热;△H>0;SnO(s)+2C(s)=Sn(s)+2CO(g),反应由固
2
体生成部分气体,混乱度增大,△S>0;
故答案为:D。
分析:熵变和焓变是判断反应进行方向的两个判据。
5. B
解析:A.SiCl 、H、HCl为气体,且反应前气体系数之和小于反应后气体系数之和,因此该反应为熵增,即
4 2
△S>0,A不符合题意;
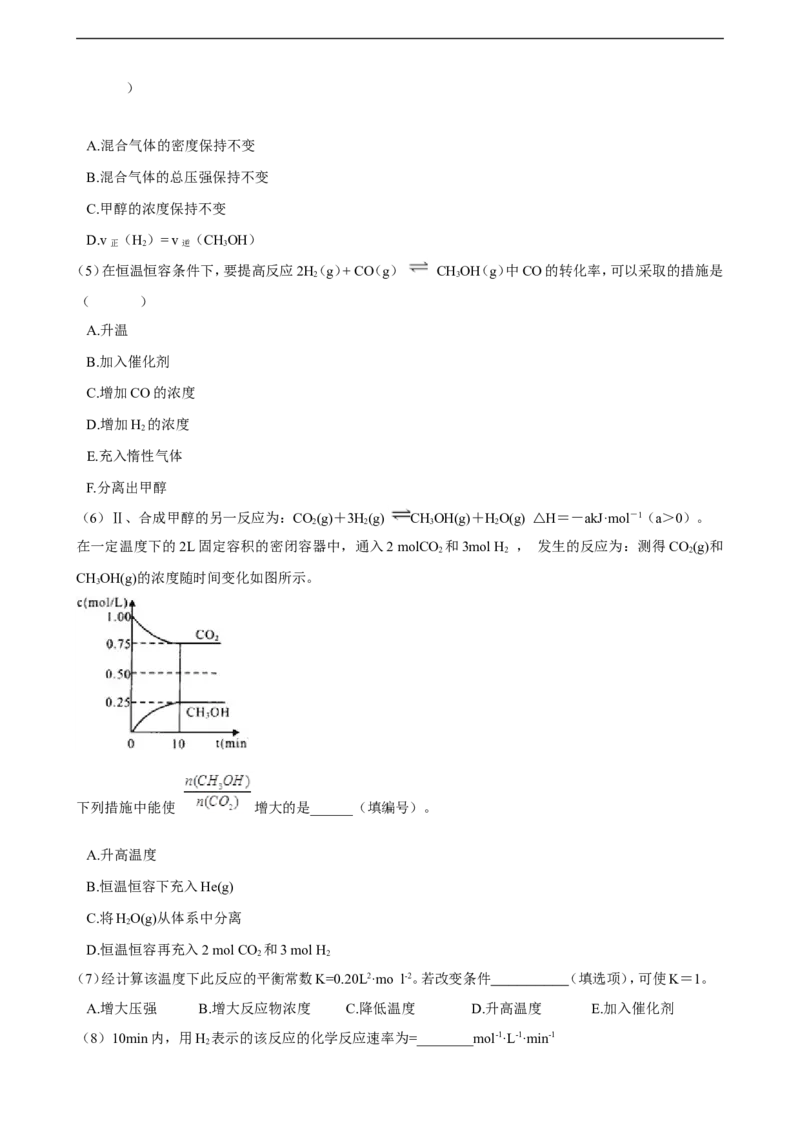
B.根据化学平衡常数的定义,该反应的平衡常数K= ,B符合题意;
C.题中说的是高温,不是标准状况下,因此不能直接用22.4L·mol-1计算,C不符合题意;
D.△H=反应物键能总和-生成物键能总和,即△H=4E(Si-Cl)+2E(H-H)-4E(H-Cl) -2E(Si-Si),D
不符合题意;
故答案为:B
分析:A.气体增加,所以混乱度增加,熵增加;
B.注意固体不考虑浓度;
C.标况下才能用气体摩尔体积衡量;
D.△H=反应物键能总和-生成物键能总和。
6. B
解析:A.当ΔH<0,ΔS>0时,任意温度下都能满足ΔH-TΔS<0,反应自发进行,选项正确,A不符合题意;
B.当ΔH>0,ΔS>0时,只有高温下才能满足ΔH-TΔS<0,反应自发进行,选项错误,B符合题意;
C.当ΔH<0,ΔS<0时,低温下满足ΔH-TΔS<0,反应自发进行,选项正确,C不符合题意;
D.当ΔH>0,ΔS<0,任意温度下都不能满足ΔH-TΔS<0,反应不能自发进行,选项正确,D不符合题意;
故答案为:B
分析:若反应自发进行,则ΔH-TΔS<0,据此结合选项进行分析。
7. A
解析:该反应中ΔH-TΔS=(-2181×103J/mol)-273×(-6.61J/(mol·K)<0,所以反应可自发进行,A符合题意;
故答案为:A
分析:根据反应自发进行的条件“ΔH-TΔS<0”进行计算分析即可。
8. B解析:A.弱电解质的电离过程是吸热过程,则HCN⇌H++CN-的ΔS>0、ΔH>0,A不符合题意;
B.用标准NaOH溶液滴定浓度约为0.01mol•L-1HCN,完全中和时生成NaCN,溶液显碱性,则应选择酚酞
做指示剂,B符合题意;
C.0.2mol•L-1的HCN溶液中加入等体积的0.1mol•L-1NaOH溶液,溶液中溶质HCN和NaCN的物质的量相
等,因CN-的水解常数Kh= =10-4>Ka,说明溶液中CN-的水解程度大于HCN的电离程度,即
该溶液呈碱性,C不符合题意;
D.0.2mol•L-1的HCN溶液中加入等体积的0.1mol•L-1NaOH溶液,溶液中溶质HCN和NaCN的物质的量相
等,溶液中的电荷守恒为c(H+)+c(Na+)=c(OH-)+c(CN-),物料守恒式为2c(Na+)=c(HCN)+c(CN-),则2c(H+)
+c(HCN)=2c(OH-)+c(CN-),D不符合题意。
故答案为:B
分析:A.电离过程是熵变增加的吸热过程;
B.NaCN强碱弱酸盐,溶液水解显碱性,则应选择酚酞做指示剂;
C.等浓度的HCN和NaCN混合溶液显碱性,说明溶液中CN-的水解程度大于HCN的电离程度;
D.根据溶液中的电荷守恒和物料守恒进行计算。
【来源:21cnj*y.co*m】
二、综合题
9. (1)>
(2)ad
(3)CH(g)+2NO (g)=N(g)+CO (g)+2HO(g) △H=-844kJ/mol
4 2 2 2 2
(4)0.0125mol/(L•min);减小
解析:(1)由于反应前后气体分子数增大,因此ΔS>0;
(2)a、气体颜色不再改变时,反应达到平衡状态,透光率不再改变,a符合题意;
b、ΔH是表示反应的热效应,只与物质具有能量的相对大小有关,ΔH不变,不能说明反应达到平衡状态,b
不符合题意;
c、根据反应速率之比等于化学计量系数之比可得,当反应达到平衡状态时,2v (N O)=v (NO ),c不符合
正 2 4 逆 2
题意;
d、当N2O4的转化率不再改变时,说明反应达到平衡状态,此时透光率不再改变,d符合题意;
故答案为:ad
(3)CH(g)燃烧热的热化学方程式为:CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890KJ/mol,HO(l)转化为
4 4 2 2 2 2
HO(g)的热化学方程式为:HO(l)=HO(g) ΔH=+44Kj/mol;
2 2 2
CH 催化还原NO 反应的化学方程式为CH(g)+2NO (g)=N(g)+CO(g)+2HO(g),根据盖斯定律可得,该
4 2 4 2 2 2 2反应的反应热 ,
因此该反应的热化学方程式为:CH(g)+2NO (g)=N(g)+CO(g)+2HO(g) ΔH=-844kJ/mol;
4 2 2 2 2
( 4)①由表格数据可知,0~20min内,参与反应的n(NO )=0.5mol,根据反应的化学方程式可知,参与反应的
2
n(CH)=0.25mol , 则 0~20min 内 , 用 CH4 表 示 的 反 应 速 率
4
;
②达到平衡后,再充入0.5molCH 和1.2molNO , 由于温度和容器的体积均不变,因此反应体系的压强增
4 2
大,平衡逆向移动,因此CH 的转化率减小;
4
分析:(1)根据反应前后气体分子数的变化确定ΔS的大小;
(2)透光率不再变化,则说明反应达到平衡状态,据此结合选项进行分析;
(3)根据题干信息确定反应物和生成,结合盖斯定律计算反应热,从而写出反应的热化学方程式;
(4)①根据公式 , 结合表格数据计算反应速率;
②根据平衡移动进行分析;
10. (1)<;低温
(2)提高原料利用率
(3)>
(4)B,C
(5)D,F
(6)C,D
(7)C
(8)0.075
解析:(1)该反应为气体分子数减小的反应,故ΔS<0;反应自发进行,则要求ΔH-TΔS<0,由于该反应的
ΔS<0,ΔH<0,故反应在低温条件下自发进行;
(2)合成气要循环,可增大原料的利用率;
( 3)该时刻下 , 故反应正向进行,因此正反应速率大于
逆反应速率;( 4)A、反应在恒容条件下进行,故混合气体的体积不变,由于反应物和生成物都是气体,根据质量守恒定
律,混合气体的质量保持不变,结合密度公式 可知,混合气体的密度一直不变,因此密度保持不变不
能判断反应达到平衡状态,A不符合题意;
B、该反应为气体体积减小的反应,故反应过程中混合气体的压强发生变化,当其不变时,可确定反应达到
平衡状态,B符合题意;
C、甲醇的浓度在反应过程中发生变化,当其不变时,反应达到平衡状态,C符合题意;
D、反应速率之比等于化学计量系数之比,故反应达到平衡状态时,v (H )=2v (CHOH),D不符合题意;
正 2 逆 3
故答案为:BC;
(5)A、该反应为放热反应,升高温度,平衡逆向移动,CO的转化率降低,A不符合题意;
B、加入催化剂,平衡不移动,B不符合题意;
C、增大CO的浓度,平衡正向移动,但CO的转化率降低,C不符合题意;
D、增大H 的浓度,平衡正向移动,CO的转化率增大,D符合题意;
2
E、恒容条件下,充入惰性气体,平衡不移动,CO的转化率不变,E不符合题意;
F、分离出甲醇,生成物的浓度减小,平衡正向移动,CO的转化率增大,F符合题意;
故答案为:DF;
(6)A、该反应为放热反应,升高温度,平衡逆向移动,则反应体系中,n(CHOH)减小、n(CO)增大,故
3 2
减小,A不符合题意;
B、恒容条件下充入He,平衡不发生移动,则反应体系中n(CHOH)和n(CO)均不变,故 不变,B
3 2
不符合题意;
C、将HO从体系中分离,从生成物浓度减小,平衡正向移动,则反应体系中,n(CHOH)增大,n(CO)减小,
2 3 2
故 增大,C符合题意;
D、恒温恒容下在通入2mol CO 和3mol H , 则平衡体系中 增大,D符合题意;
2 2故答案为:CD;
( 7)要使平衡常数增大,则反应应正向移动;且由于平衡常数只与温度有关,且该反应为放热反应,故应降
低温度,C符合题意;
故答案为:C
( 8 ) , 故 用 H2 表 示 的 速 率
;
分析:(1)气体分子数减少,ΔS<0;根据复合判据分析;
(2)反应物循环利用,可增大反应物的利用率;
(3)根据Q 与K的大小关系确定反应进行的方向,从而确定正逆反应速率的大小;
c
(4)分析反应过程中各物理量是否发生变化,若发生变化,当其不变时,反应达到平衡状态;
(5)增大CO的转化率,则平衡正向移动,根据平衡移动影响因素进行分析;
(6)根据平衡移动确定反应体系中CHOH、CO 的物质的量的变化,从而确定答案;
3 2
(7)平衡常数只与温度有关,结合温度对平衡移动的影响分析;
( 8)根据速率公式 计算CHOH的反应速率,结合速率之比等于化学计量系数之比确定H 的反应速
3 2
率;