文档内容
第 02 讲 电解质的电离
模块一 思维导图串知识 1.理解电解质的概念,了解常见的电解质和非电解
模块二 基础知识全梳理(吃透教材) 质,会正确判断电解质与非电解质、强电解质与弱电
模块三 教材习题学解题 解质。
模块四 核心考点精准练(6大考点) 2.理解酸、碱、盐在水溶液中或熔融状态下能发生电
模块五 小试牛刀过关测 离,并会用电离方程式表示。能从电离的角度认识
(基础练10题) 酸、碱、盐的概念及各自的通性。
(提升练6题) 3.能正确判断强电解质与弱电解质,并能正确书写电
离方程式。
一、电解质及其导电性
1.物质的导电性实验探究
(1)实验操作:将如图装置中的样品依次更换为NaCl固体、KNO 固体、蒸馏水、NaCl溶液、KNO 溶
3 3
学科网(北京)股份有限公司液。
(2)实验现象及结论
烧杯中物质 现象 结论
NaCl固体
NaCl固体、KNO 固体都
3
KNO 固体 灯泡
3
蒸馏水 导电能力非常弱,上述实验装置不能测出
NaCl溶液
灯泡 NaCl溶液、KNO 溶液都
3
KNO 溶液
3
(3)导电原因分析:物质导电必须具有能 、 的粒子。
①NaCl固体、KNO 固体不导电的原因是固体中含有阴、阳离子,但这些离子不能 。
3
②NaCl溶液、KNO 溶液导电的原因是 。
3
③NaCl固体受热熔化时,因温度升高,离子的运动加快,克服了离子间的相互作用,产生了能够
的Na+与Cl-,所以熔融状态的NaCl可以 。
结论:化合物在 或 下能产生自由移动的离子。
(4)电解质导电的两种模型认知
①电解质水溶液导电模型
②部分电解质熔融状态导电模型
2.电解质与非电解质
电解质 非电解质
在 或 能导电的 。 在 和 都不能导电的化合
概念
物。
学科网(北京)股份有限公司:HCl、HSO 、CHCOOH等
2 4 3
:CO、SO 、CO等
2 2
:NaOH、NH ·H O等
3 2
物质类型 :NH 等
3
:NaCl、NH Cl、NaHSO 等
4 4
:蔗糖、酒精、CH 等
4
:NaO、Al O 等
2 2 3
相同点 都是化合物
不同点 在水溶液或熔融状态下能 在水溶液和熔融状态下都不能
本质区别 自身 发生电离 自身 发生电离
思考与交流:NaCl晶体、液态HCl均不导电,则NaCl与HCl都不是电解质吗?
3.溶液的导电能力影响因素
溶液的导电能力与自由离子的浓度和离子所带的电荷有关:
主要原因
自由离子的浓度
溶液的导电能力
离子所带的电荷
次要原因
4.化合物的导电情况分析
类别 示例 导电情况
强碱和可溶性盐 NaOH、NaCl 水溶液和熔融状态都
酸 HCl、HSO 水溶液能
2 4
部分金属氧化物 CaO、NaO 熔融状态能
2
多数有机化合物 蔗糖、酒精 水溶液和熔融状态都
【归纳提升】
(1)电解质与导电性的关系
①有些电解质溶于水能导电,在熔融状态下不能导电,如HCl、HSO 等。
2 4
②有些电解质只在熔融状态下能导电,如BaSO、CaCO 等。
4 3
③能导电的物质不一定是电解质,如金属、石墨、盐酸等,电解质本身也不一定能导电,如NaCl固体、
HCl气体等。
④溶于水能导电的化合物本身不一定是电解质,如SO 、NH 等。
2 3
(2)电解质与溶解性的关系
电解质不一定易溶于水(如硫酸钡等),易溶于水的化合物不一定是电解质(如酒精等)。
学科网(北京)股份有限公司二、电解质的电离
1.电解质的电离
(1)电离:电解质 或 时,形成 的 的过程叫做电离。
2.电离方程式及其书写
(1)表示酸、碱、盐等电解质在水溶液里或熔融状态下电离成 的离子的式子叫做电离方程式。
(2)电离方程式的书写:左边为电解质的化学式,右边为电离生成的离子(离子数目写在离子符号之
前),中间用“=”(弱电解质用“⇌”)连接。
实例:HCl===H++Cl-;
NaCl===Na++Cl-;
Ba(OH) ===Ba2++2OH-。
2
【易错警示】电离方程式书写时注意:
①质量与电荷要守恒。
②原子团不能拆开,如HCO、SO、OH-等,但HSO在水溶液中拆开,在熔融状态下不拆开。
③正确标注离子所带的电荷及其数目。
3.从电离角度认识酸、碱、盐
分类 定义 实例
酸 电离时生成的阳离子全部是 的化合物是酸 HCl、CHCOOH
3
碱 电离时生成的阴离子全部是 的化合物是碱 NH ·H O、Ba(OH)
3 2 2
盐 电离时生成的 (或NH +)和 的化合物是盐 NaCl、NH Cl
4 4
【易错警示】
(1)理解酸、碱概念时注意“全部”两个字,如NaHSO 能电离产生Na+和H+,但属于盐不属于酸。
4
(2)盐中不一定含有金属元素,如NH Cl。
4
三、强电解质和弱电解质
强电解质 弱电解质
概念 在水溶液中能 的电解质 在水溶液中只能 的电解质
:HCl、HSO 、HNO 等 :HCO、CHCOOH、HClO等
2 4 3 2 3 3
所含物 :NaOH、KOH、Ca(OH) 等 :NH ·H O、Mg(OH) 等
2 3 2 2
质类型 :BaSO、(NH )SO 、NaCl等 :HO
4 4 2 4 2
:NaO、Al O 等 :(CHCOO) Pb等
2 2 3 3 2
相同点 都能电离、都是电解质、都是化合物
不同点 电离程度不同,溶质存在形式不同
用“⇋”表示,如:
电离方程式 用“=”表示,如:KNO=K++NO-
3 3
CHCOOH⇋CH COO-+H+
3 3
【易错警示】
1.CO、SO 、NH 等物质溶于水能导电,是因为溶于水后生成HCO、HSO 、NH ·H O等电解质导电,不
2 2 3 2 3 2 3 3 2
是其本身电离出离子,故应为非电解质。
学科网(北京)股份有限公司2.电解质的强、弱与其溶解性无关。难溶的盐如AgCl、CaCO 等,溶于水的部分能完全电离,是强电解
3
质。易溶的如CHCOOH、NH ·H O等在溶液中电离程度较小,是弱电解质。
3 3 2
3.溶液的导电能力与电解质的强弱无关。溶液的导电能力取决于溶液的离子浓度和离子所带的电荷,与电
解质的强弱无关。
教材习题01 解题思路
下列说法中不正确的有几个( )
①将碳酸钡放入水中不能导电,所以碳酸钡是非电解
质
②氨气溶于水得到的氨水能导电,所以氨水是电解质
③铜的导电性良好,所以铜是电解质
④ 电离时生成的阳离子有氢离子,所以是酸
⑤稀盐酸中 在电流的作用下电离出 和
A.2个 B.3个 C.4个 D.5个
教材习题02 解题思路
NaCl在熔融状态下和水溶液中的微观示意图如下图所
示。下列说法不正确的是( )
A.NaCl属于电解质
B.NaCl在水溶液中发生了电离
C.熔融NaCl能导电
D.固体NaCl中离子可自由移动
核心考点一:电解质及其导电性
【例1】下列叙述正确的是( )
A.凡能电离出H+的化合物均属于酸
学科网(北京)股份有限公司B.NaCl溶于水,在通电条件下才能发生电离
C.铜丝、石墨均能导电,所以它们都是电解质
D.熔融的MgCl 能导电,所以MgCl 是电解质
2 2
核心考点二:电解质和非电解质的判断
【例2】下列说法正确的是( )
A.蔗糖、酒精在水溶液里和熔融状态时均不导电,所以它们是非电解质
B.液态HCl、固态NaCl均不导电,所以HCl、NaCl 均是非电解质
C.NH 、CO 的水溶液均能导电,所以NH 、CO 均是电解质
3 2 3 2
D.铜、石墨均能导电,所以它们是电解质
核心考点三:电解质的电离
【例3】下表是常见的几种酸、碱、盐在水溶液中电离出来离子的情况,根据表中信息分析正确的是( )
酸 盐 碱
溶质
HCl HSO NaCl NaHSO NH Cl NaOH NH ·H O
2 4 4 4 3 2
电离出的离 H+、Cl Na+、Cl Na+、OH
H+、SO Na+、H+、SO NH、Cl- NH、OH-
子 - - -
A.在水溶液中电离出H+的物质一定是酸
B.在水溶液中电离出金属阳离子和酸根离子的物质一定是盐
C.盐溶液电离出来的阳离子一定是金属离子
D.碱溶液电离出的离子一定是金属阳离子和OH-
核心考点四:强电解质和弱非电解质的判断
【例4】下列物质属于强电解质的是 ( )
A.CO B.盐酸 C.冰醋酸 D.BaSO
2 4
核心考点五:电离方程式的书写
【例5】下列电离方程式错误的是 ( )
A.NaHCO ===Na++HCO
3
B.NaHSO===Na++H++SO
4
C.HSO ===2H++SO
2 4
D.KClO===K++Cl-+3O2-
3
学科网(北京)股份有限公司核心考点六:相关实验综合考查
【例6】滴有酚酞的 溶液显红色,在该溶液中分别滴加X溶液后有下列现象。下列说法不正确的
是 ( )
序号 装置 X溶液 现象
I 盐酸 溶液红色褪去,无沉淀,灯泡亮度没有明显变化
Ⅱ 溶液红色不变,有白色沉淀生成,灯泡亮度没有明显变化
Ⅲ 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗
A.实验I中溶液红色褪去,说明发生了反应
B.实验Ⅱ中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在有大量的 与
C.实验Ⅲ中溶液红色褪去,生成白色沉淀,灯泡逐渐变暗,说明发生了反应:
D.将实验Ⅱ中 溶液换成 溶液,现象与原实验Ⅱ中的现象相同
【基础练】
1.下列说法正确的是 ( )
A.电解质通电时才能发生电离 B.胶体和溶液的本质区别,是能否产生丁达尔效应
C.只含有一种元素的物质一定是纯净物 D.电离是电解质解离为自由移动离子的过程
2.下列物质属于电解质的是 ( )
A.固态NaCl B.葡萄糖 C.浓盐酸 D.铜丝
3.下列电离方程式正确的是 ( )
A.FeSO =Fe2++S6++4O2- B.MgCl =Mg2++Cl
4 2
C.NaHCO =Na++H++CO D.Ba(OH) =Ba2++2OH
3 2
4.将 固体溶解在水中,下列相关描述不正确的是 ( )
A.电离方程式是
B. 固体中不存在 、 ,所以 固体不导电
C.该过程中,水分子的作用是 溶液能够导电的重要原因
D. 溶液中存在自由移动的水合钠离子、水合氯离子
5.如图表示一些物质或概念间的从属关系正确的是 ( )
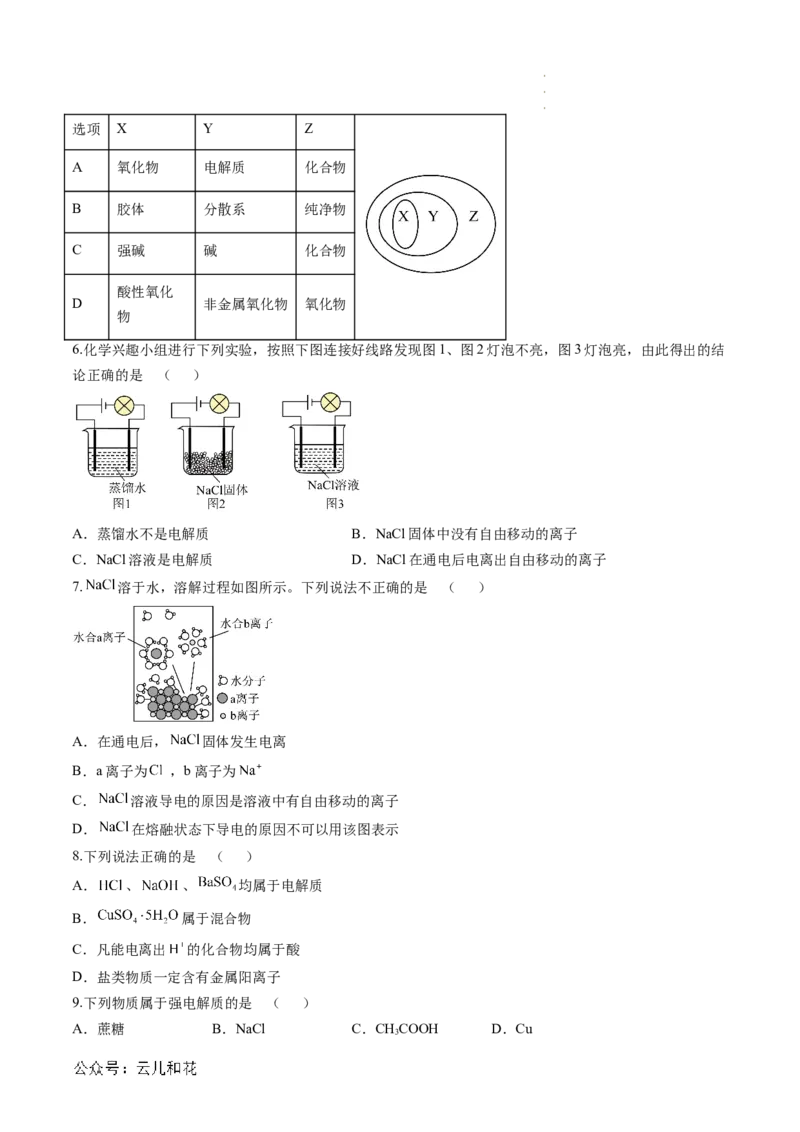
学科网(北京)股份有限公司选项 X Y Z
A 氧化物 电解质 化合物
B 胶体 分散系 纯净物
C 强碱 碱 化合物
酸性氧化
D 非金属氧化物 氧化物
物
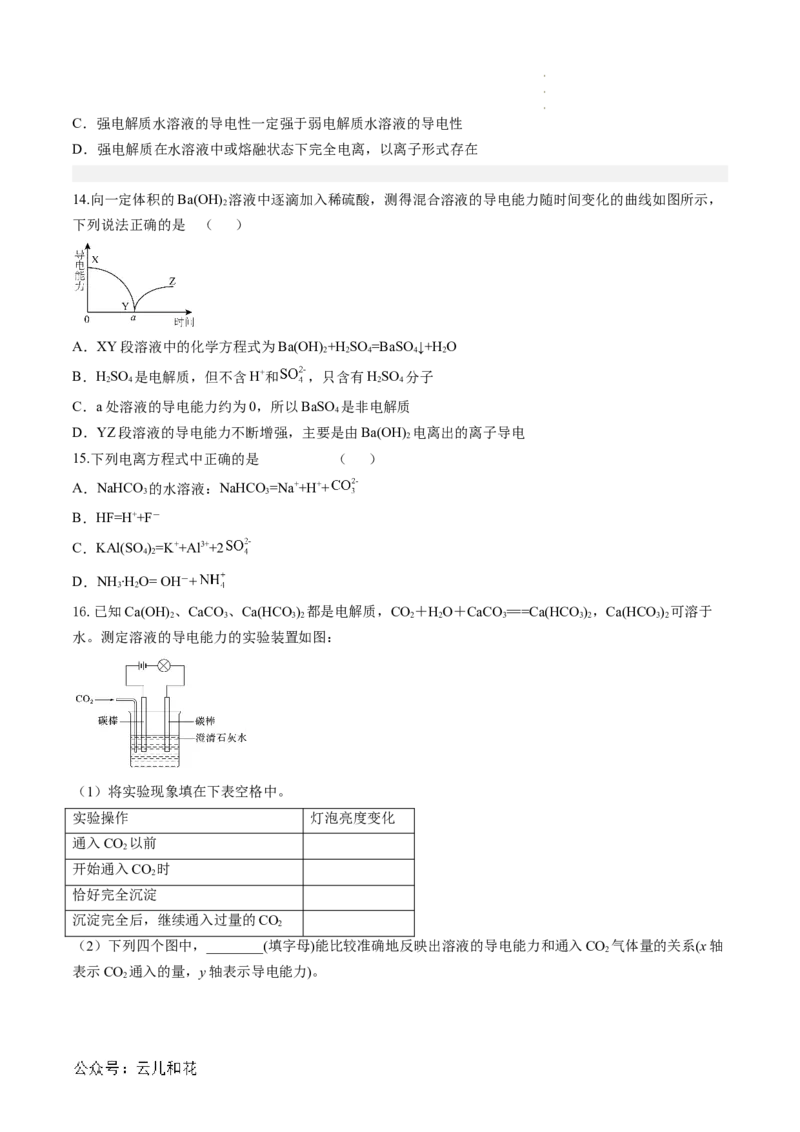
6.化学兴趣小组进行下列实验,按照下图连接好线路发现图1、图2灯泡不亮,图3灯泡亮,由此得出的结
论正确的是 ( )
A.蒸馏水不是电解质 B.NaCl固体中没有自由移动的离子
C.NaCl溶液是电解质 D.NaCl在通电后电离出自由移动的离子
7. 溶于水,溶解过程如图所示。下列说法不正确的是 ( )
A.在通电后, 固体发生电离
B.a离子为 ,b离子为
C. 溶液导电的原因是溶液中有自由移动的离子
D. 在熔融状态下导电的原因不可以用该图表示
8.下列说法正确的是 ( )
A. 、 、 均属于电解质
B. 属于混合物
C.凡能电离出 的化合物均属于酸
D.盐类物质一定含有金属阳离子
9.下列物质属于强电解质的是 ( )
A.蔗糖 B.NaCl C.CHCOOH D.Cu
3
学科网(北京)股份有限公司10.在常温常压下,有以下10种物质,请回答下列问题:
①干冰;②熔融氧化钠;③蔗糖;④稀硫酸;⑤ 溶液;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧雾
(1)上述物质中属于纯净物的是 (填序号,下同),能发生丁达尔效应的是 。
(2)其中能导电的是 ;属于电解质的是 ;属于非电解质的是 。
(3)上述物质相应状态下能够导电的且属于电解质的是 (填序号)。
(4)写出物质④和⑦反应的离子方程式: 。
(5)写出物质⑤和⑥在水中发生反应的离子方程式: 。
(6)请写出下列物质在水溶液中的电离方程式:
① 。
② 。
【提升练】
11.下图为NaCl在水中溶解和电离的示意图,关于该图的说法中正确的是 ( )
A.由图可知在HO分子中,H原子和O原子都不带电荷
2
B. 固体浴于水后,会形成水合钠离子和水合氯离子
C.氯化钠固体没有离子,所以干燥的氮化钠不导电
D.上述过程通常可表示为 ,该过程需要通电
12.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是 ( )
A B C D
强电解
Fe NaCl CaCO HNO
3 3
质
弱电解
CHCOOH NH HPO Fe(OH)
3 3 3 4 3
质
非电解
C H O (蔗糖) BaSO C HOH HO
12 22 11 4 2 5 2
质
13.下列说法正确的是 ( )
A.NaHCO 在水溶液中的电离方程式为NaHCO =Na++H++CO
3 3
B.在水中完全电离的可溶性盐是强电解质,在水中溶解度很小的难溶性盐是弱电解质
学科网(北京)股份有限公司C.强电解质水溶液的导电性一定强于弱电解质水溶液的导电性
D.强电解质在水溶液中或熔融状态下完全电离,以离子形式存在
14.向一定体积的Ba(OH) 溶液中逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化的曲线如图所示,
2
下列说法正确的是 ( )
A.XY段溶液中的化学方程式为Ba(OH) +H SO =BaSO ↓+H O
2 2 4 4 2
B.HSO 是电解质,但不含H+和 ,只含有HSO 分子
2 4 2 4
C.a处溶液的导电能力约为0,所以BaSO 是非电解质
4
D.YZ段溶液的导电能力不断增强,主要是由Ba(OH) 电离出的离子导电
2
15.下列电离方程式中正确的是 ( )
A.NaHCO 的水溶液:NaHCO =Na++H++
3 3
B.HF=H++F-
C.KAl(SO )=K++Al3++2
4 2
D.NH ∙H O= OH-+
3 2
16.已知Ca(OH) 、CaCO 、Ca(HCO ) 都是电解质,CO+HO+CaCO ===Ca(HCO ),Ca(HCO ) 可溶于
2 3 3 2 2 2 3 3 2 3 2
水。测定溶液的导电能力的实验装置如图:
(1)将实验现象填在下表空格中。
实验操作 灯泡亮度变化
通入CO 以前
2
开始通入CO 时
2
恰好完全沉淀
沉淀完全后,继续通入过量的CO
2
(2)下列四个图中,________(填字母)能比较准确地反映出溶液的导电能力和通入CO 气体量的关系(x轴
2
表示CO 通入的量,y轴表示导电能力)。
2
学科网(北京)股份有限公司学科网(北京)股份有限公司