文档内容
必修第二册 第五章 第一节 硫及其化合物 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
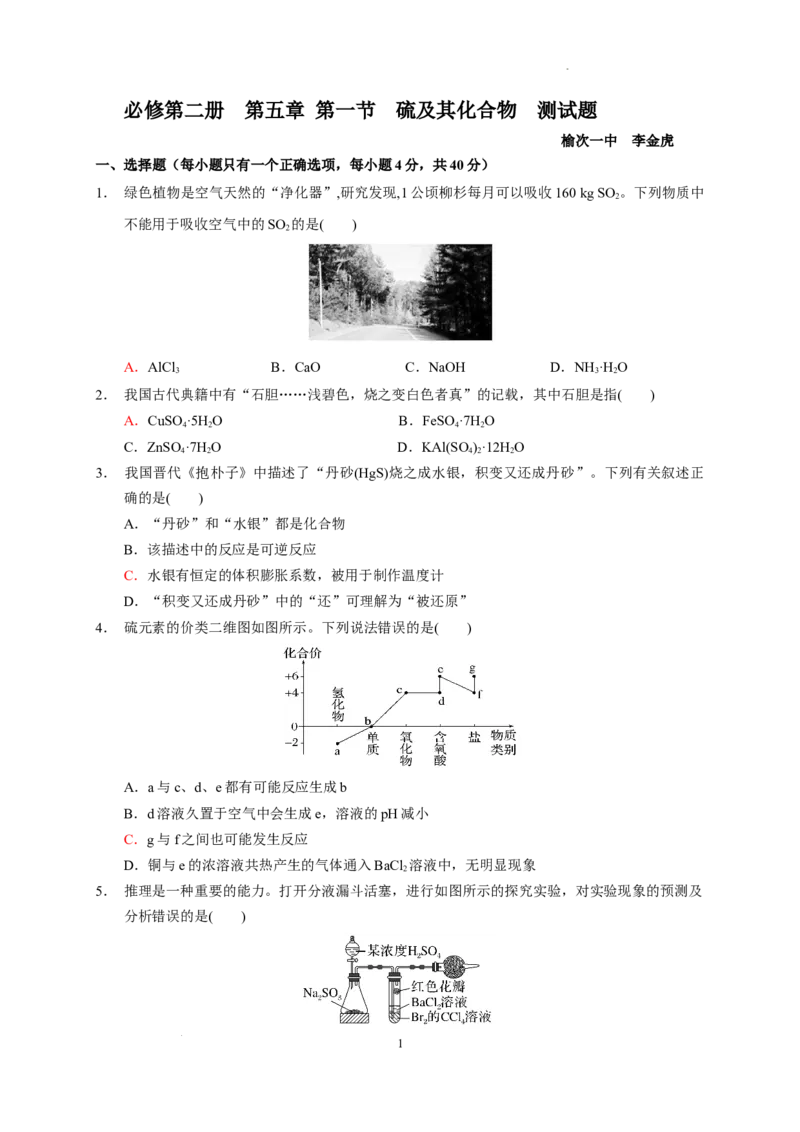
1. 绿色植物是空气天然的“净化器”,研究发现,1公顷柳杉每月可以吸收160 kg SO 。下列物质中
2
不能用于吸收空气中的SO 的是( )
2
A.AlCl B.CaO C.NaOH D.NH ·H O
3 3 2
2. 我国古代典籍中有“石胆……浅碧色,烧之变白色者真”的记载,其中石胆是指( )
A.CuSO ·5H O B.FeSO ·7H O
4 2 4 2
C.ZnSO·7H O D.KAl(SO )·12H O
4 2 4 2 2
3. 我国晋代《抱朴子》中描述了“丹砂(HgS)烧之成水银,积变又还成丹砂”。下列有关叙述正
确的是( )
A.“丹砂”和“水银”都是化合物
B.该描述中的反应是可逆反应
C.水银有恒定的体积膨胀系数,被用于制作温度计
D.“积变又还成丹砂”中的“还”可理解为“被还原”
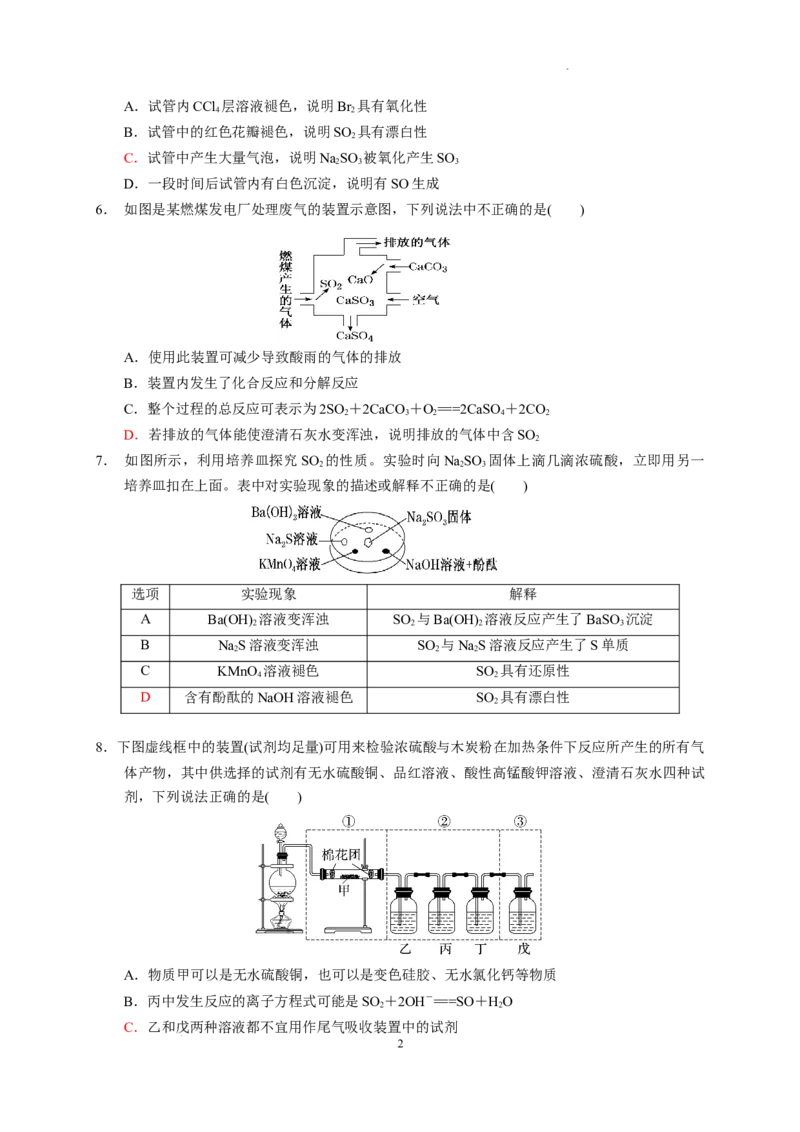
4. 硫元素的价类二维图如图所示。下列说法错误的是( )
A.a与c、d、e都有可能反应生成b
B.d溶液久置于空气中会生成e,溶液的pH减小
C.g与f之间也可能发生反应
D.铜与e的浓溶液共热产生的气体通入BaCl 溶液中,无明显现象
2
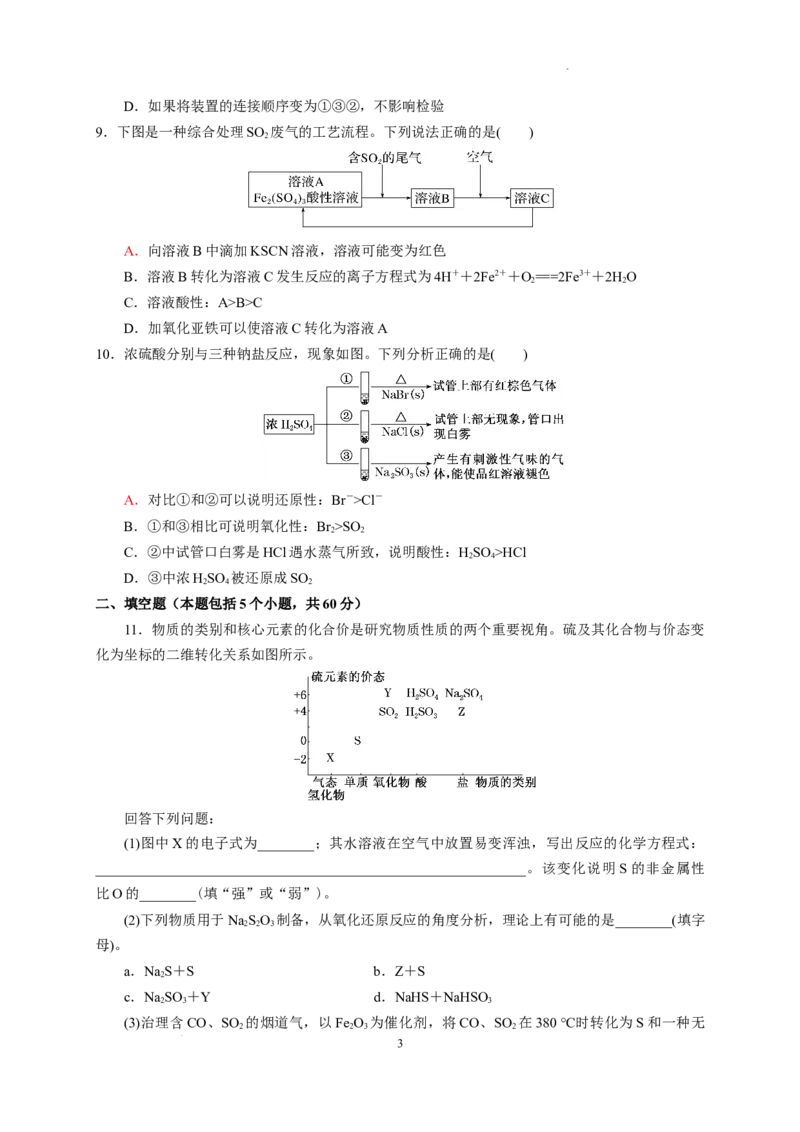
5. 推理是一种重要的能力。打开分液漏斗活塞,进行如图所示的探究实验,对实验现象的预测及
分析错误的是( )
1
学科网(北京)股份有限公司A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.试管中的红色花瓣褪色,说明SO 具有漂白性
2
C.试管中产生大量气泡,说明NaSO 被氧化产生SO
2 3 3
D.一段时间后试管内有白色沉淀,说明有SO生成
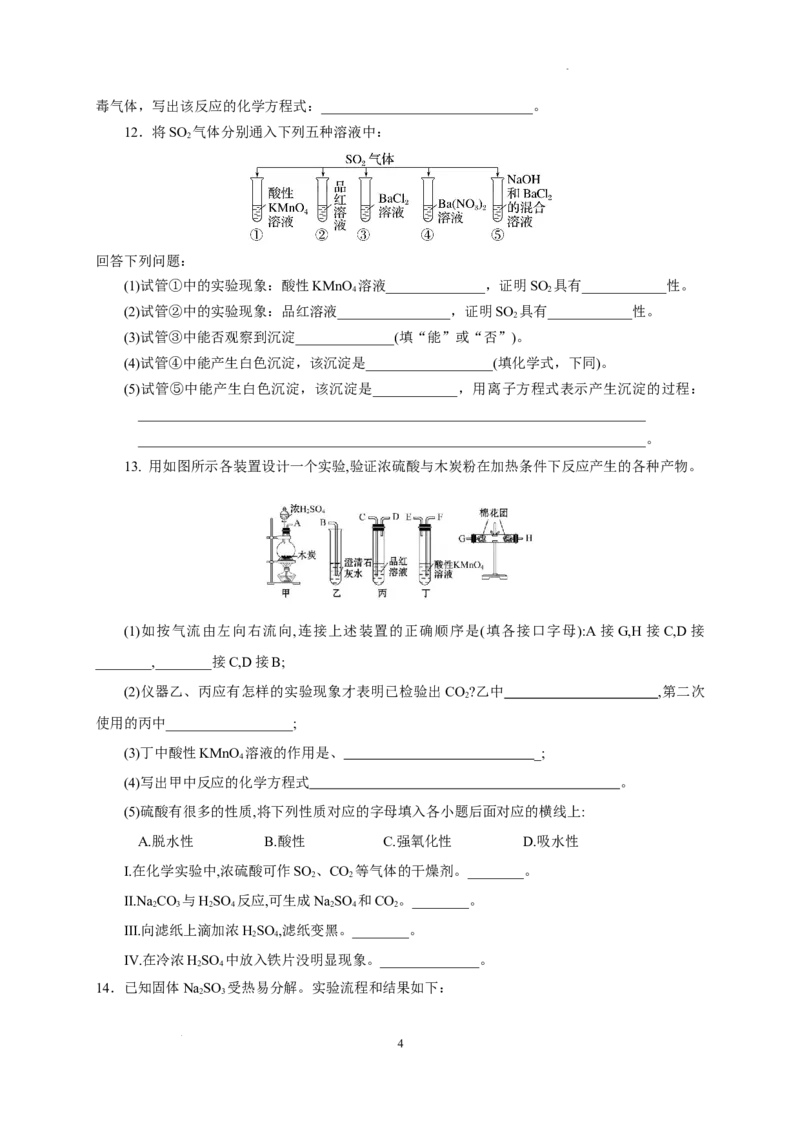
6. 如图是某燃煤发电厂处理废气的装置示意图,下列说法中不正确的是( )
A.使用此装置可减少导致酸雨的气体的排放
B.装置内发生了化合反应和分解反应
C.整个过程的总反应可表示为2SO +2CaCO +O===2CaSO +2CO
2 3 2 4 2
D.若排放的气体能使澄清石灰水变浑浊,说明排放的气体中含SO
2
7. 如图所示,利用培养皿探究SO 的性质。实验时向NaSO 固体上滴几滴浓硫酸,立即用另一
2 2 3
培养皿扣在上面。表中对实验现象的描述或解释不正确的是( )
选项 实验现象 解释
A Ba(OH) 溶液变浑浊 SO 与Ba(OH) 溶液反应产生了BaSO 沉淀
2 2 2 3
B NaS溶液变浑浊 SO 与NaS溶液反应产生了S单质
2 2 2
C KMnO 溶液褪色 SO 具有还原性
4 2
D 含有酚酞的NaOH溶液褪色 SO 具有漂白性
2
8.下图虚线框中的装置(试剂均足量)可用来检验浓硫酸与木炭粉在加热条件下反应所产生的所有气
体产物,其中供选择的试剂有无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石灰水四种试
剂,下列说法正确的是( )
A.物质甲可以是无水硫酸铜,也可以是变色硅胶、无水氯化钙等物质
B.丙中发生反应的离子方程式可能是SO +2OH-===SO+HO
2 2
C.乙和戊两种溶液都不宜用作尾气吸收装置中的试剂
2
学科网(北京)股份有限公司D.如果将装置的连接顺序变为①③②,不影响检验
9.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
10.浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )
A.对比①和②可以说明还原性:Br->Cl-
B.①和③相比可说明氧化性:Br >SO
2 2
C.②中试管口白雾是HCl遇水蒸气所致,说明酸性:HSO >HCl
2 4
D.③中浓HSO 被还原成SO
2 4 2
二、填空题(本题包括5个小题,共60分)
11.物质的类别和核心元素的化合价是研究物质性质的两个重要视角。硫及其化合物与价态变
化为坐标的二维转化关系如图所示。
回答下列问题:
(1)图中X的电子式为________;其水溶液在空气中放置易变浑浊,写出反应的化学方程式:
_____________________________________________________________。该变化说明S的非金属性
比O的________(填“强”或“弱”)。
(2)下列物质用于NaSO 制备,从氧化还原反应的角度分析,理论上有可能的是________(填字
2 2 3
母)。
a.NaS+S b.Z+S
2
c.NaSO +Y d.NaHS+NaHSO
2 3 3
(3)治理含CO、SO 的烟道气,以Fe O 为催化剂,将CO、SO 在380 ℃时转化为S和一种无
2 2 3 2
3
学科网(北京)股份有限公司毒气体,写出该反应的化学方程式:______________________________。
12.将SO 气体分别通入下列五种溶液中:
2
回答下列问题:
(1)试管①中的实验现象:酸性KMnO 溶液______________,证明SO 具有____________性。
4 2
(2)试管②中的实验现象:品红溶液________________,证明SO 具有____________性。
2
(3)试管③中能否观察到沉淀______________(填“能”或“否”)。
(4)试管④中能产生白色沉淀,该沉淀是__________________(填化学式,下同)。
(5)试管⑤中能产生白色沉淀,该沉淀是____________,用离子方程式表示产生沉淀的过程:
________________________________________________________________________
________________________________________________________________________。
13. 用如图所示各装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):A接G,H接C,D接
________,________接C,D接B;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO?乙中 ,第二次
2
使用的丙中__________________;
(3)丁中酸性KMnO 溶液的作用是、 _;
4
(4)写出甲中反应的化学方程式 。
(5)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的横线上:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可作SO 、CO 等气体的干燥剂。________。
2 2
Ⅱ.Na CO 与HSO 反应,可生成NaSO 和CO。________。
2 3 2 4 2 4 2
Ⅲ.向滤纸上滴加浓HSO ,滤纸变黑。________。
2 4
Ⅳ.在冷浓HSO 中放入铁片没明显现象。______________。
2 4
14.已知固体NaSO 受热易分解。实验流程和结果如下:
2 3
4
学科网(北京)股份有限公司气体Y是一种纯净物,在标准状况下的密度为1.518 g·L-1。请回答:
(1)气体Y分子的电子式为______________,白色沉淀的化学式为______________。
(2)该流程中NaSO 受热分解的化学方程式:________________________________________。
2 3
(3)另取固体X试样和NaSO 混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出产生
2 3
淡黄色沉淀的离子方程式:_____________________________________________ (不考虑空气的影
响)。
15.含硫化合物的种类很多,现有SO 、NaSO 、HSO 、CuSO 这4种常见的含硫化合物。
2 2 3 2 4 4
回答下列问题:
(1)为进一步减少SO 的污染并变废为宝,我国正在探索在一定条件下用 CO还原SO 的方法来
2 2
除去SO 。写出该反应的化学方程式:_______________________________。
2
(2)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
NaSO + KIO + HSO === NaSO + KSO + I+ HO。
2 3 3 2 4 2 4 2 4 2 2
①配平上面的氧化还原反应方程式。
②若反应中有5 mol电子转移,则生成的碘单质是________mol。
(3)向FeCl 和BaCl 的酸性混合溶液中通入SO 气体,有白色沉淀生成,此沉淀是________(填
3 2 2
字母)。
A.BaSO B.FeS C.BaSO D.S
4 3
(4)常温下,将铁棒置于浓硫酸中,课本上解释发生了钝化,但有人认为未发生反应。为验证此
过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于 CuSO 溶液中,若
4
铁棒表面____________,则发生了钝化。
1.答案 A
解析 SO 属于酸性氧化物,能够跟碱性氧化物或碱发生反应而被吸收。
2
2.答案 A
解析 在题给选项的四种物质中只有 CuSO ·5H O、FeSO ·7H O 晶体有色,而 ZnSO·7H O 和
4 2 4 2 4 2
KAl(SO )·12H O 均为无色晶体。CuSO ·5H O 加热分解生成 CuSO 和 HO,CuSO 呈白色,而
4 2 2 4 2 4 2 4
FeSO ·7H O加热发生分解反应,生成的Fe O 呈红棕色,A正确。
4 2 2 3
3.答案 C
解析 水银(Hg)是单质,属于纯净物,A错误;“丹砂(HgS)烧之成水银,积变又还成丹砂”,前
者需要加热,后者常温下反应,不是同一条件,故不是可逆反应,B错误;体积膨胀系数是表征物
体热膨胀性质的物理量,水银有恒定的体积膨胀系数,受热时体积变化均匀,可用于制作温度计,
5
学科网(北京)股份有限公司C正确;“积变又还成丹砂”,发生的反应是Hg+S===HgS,Hg发生了氧化反应,D错误。
4.答案 C
解析 根据化合价以及物质的类别可知a为HS、b为S、c为SO 、d为HSO 、e为HSO 、f含有
2 2 2 3 2 4
SO或HSO、g含有SO或HSO。a为HS,可以和SO 、HSO 、HSO 发生归中反应生成硫单质,
2 2 2 3 2 4
A正确;HSO 具有较强的还原性,在空气中久置会被氧气氧化成硫酸,硫酸酸性更强,pH更小,
2 3
B正确;g为硫酸盐,f为亚硫酸盐,硫元素化合价相邻,不反应,C错误;铜与浓硫酸共热产生气
体SO ,SO 通入BaCl 溶液中,不能发生反应,所以无明显现象,D正确。
2 2 2
5.答案 C
解析 锥形瓶内发生反应NaSO +HSO ===Na SO +SO ↑+HO ,产生的SO 进入到试管中,
2 3 2 4 2 4 2 2 2
CCl 层溶液褪色,发生反应SO +Br +2HO===H SO +2HBr,证明Br 具有氧化性,A项正确;
4 2 2 2 2 4 2
试管中花瓣褪色,说明SO 可以漂白花瓣中的有色物质,证明SO 具有漂白性,B项正确;试管中
2 2
产生大量气泡是锥形瓶中产生的SO 进入到试管中引起的,NaSO 与HSO 发生复分解反应,C项
2 2 3 2 4
错误;试管中Br 可将SO 氧化,生成HSO 和HBr,SO 可以和Ba2+结合成不溶于酸的白色沉淀,
2 2 2 4
D项正确。
6.答案 D
解析: A项,由图可知使用此装置可减少二氧化硫的排放;B项,该装置内,碳酸钙分解生成氧
化钙和二氧化碳,二氧化硫与氧化钙化合生成亚硫酸钙,亚硫酸钙再与氧气化合生成硫酸钙;C项,
反应的实质是二氧化硫与碳酸钙、氧气反应生成硫酸钙和二氧化碳;D项,二氧化碳也能使澄清石
灰水变浑浊。
7.答案 D
.解析: SO +Ba(OH) ===BaSO ↓+HO,A正确;SO 溶于水生成HSO ,进而与NaS溶液反应
2 2 3 2 2 2 3 2
生成S单质,B正确;SO 使KMnO 溶液褪色是因为SO 具有还原性,C正确;SO 中和了NaOH
2 4 2 2
使含有酚酞的NaOH溶液褪色,不是因为SO 具有漂白性,D错误。
2
8.答案 C
解析 装置①是检验混合气体中是否含有水蒸气,应该用无水硫酸铜或变色硅胶,不能用无水氯化
钙,A错误;二氧化碳也能被强碱溶液吸收,丙中试剂应该是酸性高锰酸钾溶液,B错误;品红溶
液可以检验二氧化硫,但一般不能用来除去二氧化硫,澄清石灰水浓度太小,不能用来吸收二氧化
硫,C正确;如果将仪器的连接顺序变为①③②,气体产物通过①中的无水硫酸铜,无水硫酸铜由
白色变成蓝色,能说明有水生成,通过③中的澄清石灰水,二氧化硫、二氧化碳都能使澄清石灰水
变浑浊,不可以检验出二氧化碳,D错误。
9.答案 A
解析 SO 与Fe3+发生氧化还原反应生成Fe2+,若二氧化硫足量,则溶液中无Fe3+,加入KSCN溶
2
液,溶液不变红色;若二氧化硫不足,则溶液中有Fe3+,加入KSCN溶液,溶液变红色,A正确;
离子方程式中电荷不守恒,B错误;溶液A转化为溶液B后溶液酸性增强,C错误;FeO与H+反
应生成Fe2+,故溶液C不能转化为溶液A,D错误。
10.答案 A
解析: A项,反应①生成的红棕色气体是溴蒸气,反应②白雾是氯化氢,说明浓硫酸能将溴离子
6
学科网(北京)股份有限公司氧化成溴单质,而不能将氯离子氧化成氯气说明还原性:Br->Cl-,正确;B项,反应③生成的是
二氧化硫气体,属于非氧化还原反应,而且亚硫酸钠与溴化钠不是同一类型,错误;C项,白雾说
明氯化氢易挥发,错误;D项,反应③生成的是二氧化硫气体,属于非氧化还原反应,错误。
11.答案:(1) 2HS+O===2S↓+2HO 弱
2 2 2
(2)bd
(3)2CO+SO =====S↓+2CO
2 2
解析:(1)X为HS,S最外层有6个电子,能与2个H原子形成共价键,其电子式为HSH;HS
2 2
水溶液在空气中变浑浊是因为HS被氧气氧化生成S,反应的化学方程式为2HS+O===2S↓+
2 2 2
2HO,所以S的非金属性比O的弱。
2
(2)Na SO 中S元素化合价为+2价,从氧化还原反应的角度分析,反应物中S元素化合价必须
2 2 3
分别大于+2价和小于+2价,a中S元素的化合价都小于+2价,c中S元素的化合价都大于+2价,
b、d符合题意。
12.答案 (1)褪色 还原 (2)褪色 漂白 (3)否 (4)BaSO
4
(5)BaSO SO +2OH-===SO+HO,Ba2++SO===BaSO ↓
3 2 2 3
13.答案: (1)F E (2)出现白色沉淀 品红未褪色 (3)吸收SO
2
(4)C+2H SO (浓) CO↑+2SO↑+2H O
2 4 2 2 2
(5)Ⅰ.D Ⅱ.B Ⅲ.A Ⅳ.C
【解析】(1)根据实验室浓HSO 氧化木炭的反应原理、条件,固液加热下反应,选择发生装置,酸性高
2 4
锰酸钾可氧化二氧化硫,用高锰酸钾酸性溶液除SO ,再通过品红溶液不褪色确认SO 已除干净,验证
2 2
木炭可被浓HSO 氧化成CO,可通过二氧化碳能使澄清的石灰水变浑浊确认;
2 4 2
(2)乙中为澄清的石灰水,澄清的石灰水和二氧化碳反应变浑浊,二氧化硫具有漂白性,二氧化硫能使品
红褪色,丁装置用酸性高锰酸钾溶液除SO ,再通过品红溶液不褪色;
2
(3)为了验证木炭可被浓HSO 氧化成CO,应先除去二氧化硫,用酸性高锰酸钾溶液除SO ;
2 4 2 2
(4)浓硫酸与木炭发生氧化还原反应,生成二氧化碳、二氧化硫和水,方程式为C+2H SO (浓)
2 4
CO↑+2SO↑+2H O;
2 2 2
(5)Ⅰ.浓硫酸可与水形成一系列稳定的水合物,故浓硫酸可吸收物质中游离态的水,具有强烈的吸水性,
浓硫酸常用作气体干燥剂,浓硫酸有酸性,可与碱性气体反应,所以只能干燥酸性或中性气体。
Ⅱ.Na CO 与HSO 反应,可生成NaSO 和CO,是两种化合物相互交换成分生成另外两种化合物的反
2 3 2 4 2 4 2
应,是复分解反应,生成盐和水,体现了硫酸的酸性;Ⅲ.向滤纸上滴加浓HSO ,滤纸变黑,体现脱水性;Ⅳ.
2 4
7
学科网(北京)股份有限公司浓硫酸能与铁片反应,使铁片表面形成一层致密的氧化物薄膜,阻止了浓硫酸与铁片进一步反应,即产
生钝化现象,在冷浓HSO 中放入铁片没明显现象,体现了浓硫酸的强氧化性。
2 4
14.答案 (1) BaSO
4
(2)4Na SO =====NaS+3NaSO
2 3 2 2 4
(3)2S2-+SO+6H+===3S↓+3HO
2
解析 亚硫酸钠隔绝空气加热分解质量并没有改变,说明并没有生成气体,应该是分解生成了几种
固体,加入盐酸后产生气体Y,根据密度算出气体Y的摩尔质量为34 g·mol-1,结合题目以及元素
守恒,推断气体Y为HS。那么NaSO 的分解生成物中一定有S2-(Na S),同时这是一个氧化还原
2 2 3 2
反应,+4价的S有降价必然还有升价,只能生成+6价,所以另一分解产物应该是含有硫酸根离
子的NaSO 。(3)X与亚硫酸钠混合,在酸性环境下产生了淡黄色沉淀,根据题目环境以及我们学
2 4
过的淡黄色沉淀推知生成S单质,显然这是一个S2-与SO的归中反应,反应物还有H+。
15.答案:(1)2CO+SO =====S↓+2CO
2 2
(2)①5 2 1 5 1 1 1 ②0.5
(3)A
(4)无明显现象
解析:(1)CO还原SO ,C元素被氧化,化合价由+2价→+4价,升高了2价,S元素被还原,化
2
合价由+4价→0价,降低了4价,最小公倍数为4,再依据原子守恒得:2CO+SO =====S↓+
2
2CO 。(2)①NaSO 中S元素化合价由+4价→+6价,升高了2价,KIO 中I元素化合价由+5价
2 2 3 3
→0 价,降低了 5 价,最小公倍数为 10,然后依据原子守恒得:5NaSO +2KIO +
2 3 3
HSO ===5Na SO +KSO +I +HO;②依据①生成1 mol I ,共转移电子10 mol,因此转移5 mol
2 4 2 4 2 4 2 2 2
电子,生成0.5 mol I 。(3)Fe3+具有氧化性,SO 具有还原性,两者发生氧化还原反应生成Fe2+、
2 2
SO,Ba2++SO===BaSO ↓,因此沉淀是硫酸钡,故选项A正确。(4)钝化:利用浓硫酸的强氧化性,
4
在铁表面产生一层致密的氧化物薄膜阻碍反应的进行。氧化膜是铁的氧化物,不与硫酸铜反应,因
此若铁棒表面无明显现象,则发生了钝化,如果没有发生钝化,会发生反应 Fe+Cu2+===Cu+Fe2
+,有红色物质附着在铁棒表面。
8
学科网(北京)股份有限公司9
学科网(北京)股份有限公司