文档内容
湖南省长沙市一中高一第一学期期末考试
化学试卷
时量:75分钟 满分:100分。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Al-27 C1-35.5 Fe-56
一、选择题(本题共10小题,每小题2分,共20分。每小题只有一个选有符合题目要求)
1. 下列关于实验事故或药品的处理方法中,正确的是
A. 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗
B. 大量氯气泄漏时,用肥皂水浸湿毛巾捂住嘴和鼻,顺风向地势低处逃离
C. 不慎酒出的酒精在桌上着火时,应立即用大量水扑灭
D. 可以将未用完的钠、钾、白磷放回原试剂瓶
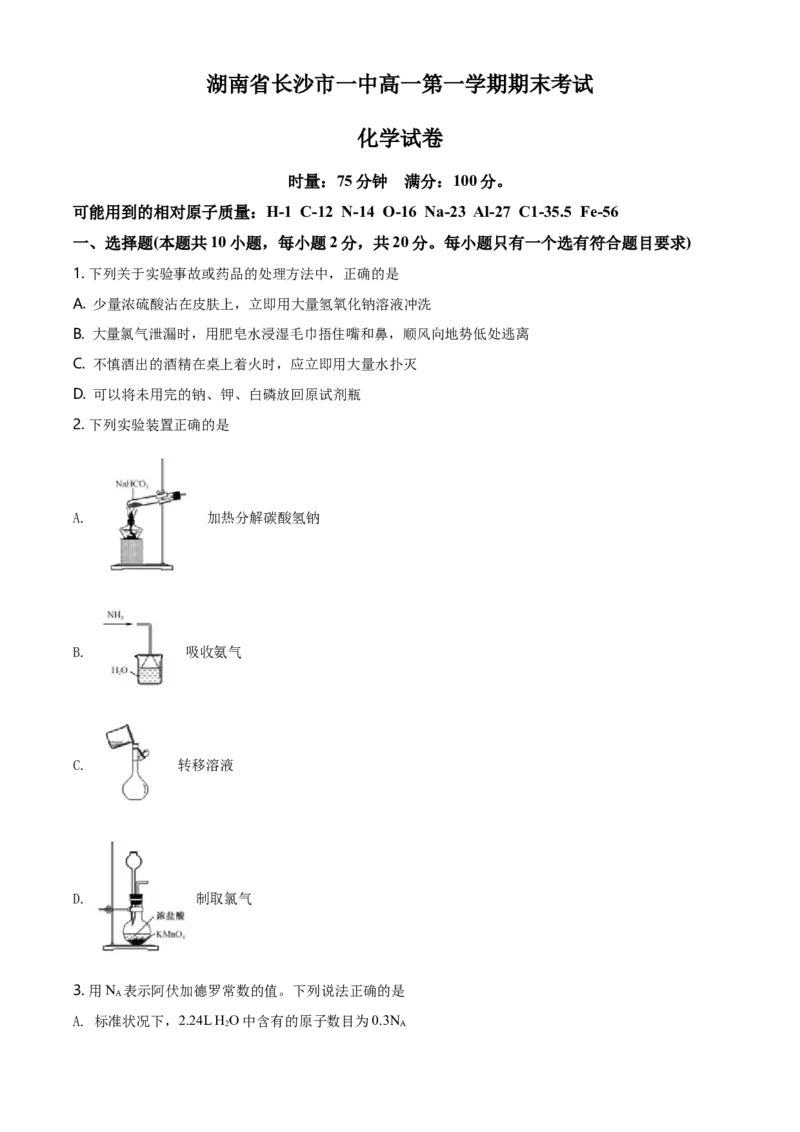
2. 下列实验装置正确的是
A. 加热分解碳酸氢钠
B. 吸收氨气
C. 转移溶液
D. 制取氯气
3. 用N 表示阿伏加德罗常数的值。下列说法正确的是
A
A. 标准状况下,2.24L H O中含有的原子数目为0.3N
2 AB. 常温常压下,4.6g NO 与NO 混合物中含有的氧原子数目为0.2N
2 2 4 A
C. 0.15mol·L-1 K CO 溶液中含有的钾离子数目为0.3N
2 3 A
D. 过氧化钠与水反应时,每生成1mol氧气转移电子数为N
A
4. 下列反应 的离子方程式书写正确的是
A. 氢氧化钡溶液与硫酸铜溶液反应:
B. 向氢氧化钠溶液中逐滴加入几滴FeCl 饱和溶液: (胶体)
3
C. 向氯化铝溶液中滴加足量氨水:
D. 氯化铁溶液与碘化钾溶液反应:
5. 下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是
.
A Na+、Ba2+、Cl-、 B. Ca2+、 、Cl-、K+
C. 、K+、Fe2+、H+ D. H+、Cl-、Na+、
6. 向下列溶液中通入足量CO 气体,最终不会产生沉淀的是( )
2
①饱和NaCO 溶液、②澄清石灰水、③BaCl 溶液、④氨水与NaCl构成的混合液(二者均饱和)
2 3 2
A. ①②③④ B. ②③ C. ①④ D. ③④
7. 为除去括号内的杂质,所选用的试剂不正确的是
A. Cl(HCl),通过饱和食盐水 B. SO (CO),通过酸性高锰酸钾溶液
2 2 2
C. NO(NO ),通入水中 D. NaOH溶液[Ca(OH) ],加入适量NaCO 溶液,过
2 2 2 3
滤
8. 下列叙述内容和结论均正确并且有因果关系的是
选项 内容 结论
A 向NaCO 溶液中滴加足量稀盐酸 有气泡产生,说明非金属性:Cl>C
2 3
B 浓硫酸具有强氧化性和吸水性 浓硫酸可干燥H 和HS,不可干燥SO 和NH
2 2 2 3
C SO 是酸性氧化物 SO 可使含有酚酞的NaOH溶液褪色
2 2
D 铵盐受热易分解 NH Cl和NH HCO 均可用作氮肥和制取氨气
4 4 3
A. A B. B C. C D. D
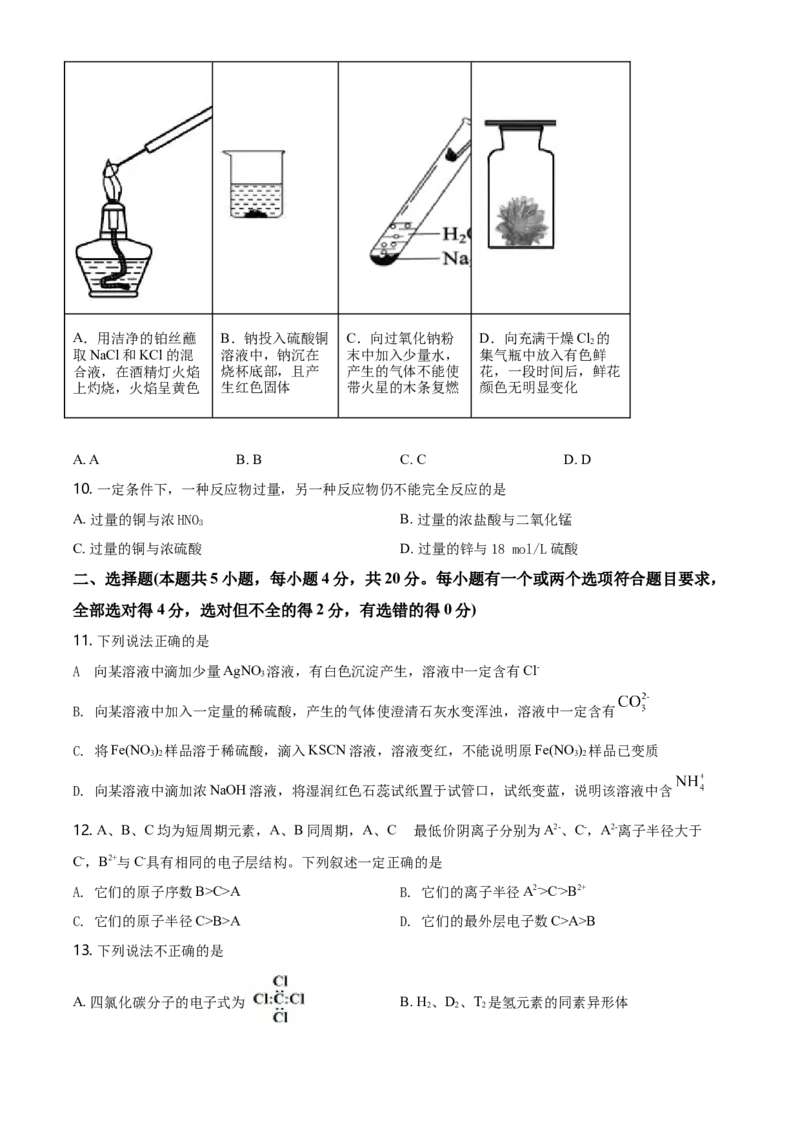
9. 下列实验操作对应的现象符合事实的是A.用洁净的铂丝蘸 B.钠投入硫酸铜 C.向过氧化钠粉 D.向充满干燥Cl 的
2
取NaCl和KCl的混 溶液中,钠沉在 末中加入少量水, 集气瓶中放入有色鲜
合液,在酒精灯火焰 烧杯底部,且产 产生的气体不能使 花,一段时间后,鲜花
上灼烧,火焰呈黄色 生红色固体 带火星的木条复燃 颜色无明显变化
A. A B. B C. C D. D
10. 一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是
A. 过量的铜与浓HNO B. 过量的浓盐酸与二氧化锰
3
C. 过量的铜与浓硫酸 D. 过量的锌与18 mol/L硫酸
二、选择题(本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分)
11. 下列说法正确的是
.
A 向某溶液中滴加少量AgNO 溶液,有白色沉淀产生,溶液中一定含有Cl-
3
B. 向某溶液中加入一定量的稀硫酸,产生的气体使澄清石灰水变浑浊,溶液中一定含有
C. 将Fe(NO ) 样品溶于稀硫酸,滴入KSCN溶液,溶液变红,不能说明原Fe(NO ) 样品已变质
3 2 3 2
D. 向某溶液中滴加浓NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸变蓝,说明该溶液中含
12. A、B、C均为短周期元素,A、B同周期,A、C 的最低价阴离子分别为A2-、C-,A2-离子半径大于
C-,B2+与C-具有相同的电子层结构。下列叙述一定正确的是
A. 它们的原子序数B>C>A B. 它们的离子半径A2->C->B2+
C. 它们的原子半径C>B>A D. 它们的最外层电子数C>A>B
13. 下列说法不正确的是
A. 四氯化碳分子的电子式为 B. H、D、T 是氢元素的同素异形体
2 2 2C. 次氯酸的结构式为H-O-Cl D. H O的沸点高于HS,是由于HO分子间存在氢键
2 2 2
14. 某核潜艇上的核反应堆使用了液态铝钠合金作载热介质,有关说法不恰当的是
A. 铝钠合金的熔点低于铝的熔点
B. 钠、铝在常温下都可以与空气中的氧气反应
C. 将mg不同组成的铝钠合金分别投入足量盐酸中,若放出H 越多,则合金中铝的质量分数越小
2
D. 将含0.1mol钠和0.2mol铝的合金投入到足量的水中,充分反应,产生氢气4.48L(标准状况)
15. 一种广泛用于锂离子电池的物质结构如图所示。X、Y、Z、W为原子序数依次递增的四种短周期主族
元素,Y、W同主族,原子半径r(X)>r(Y)>r(Z)。下列说法正确的是
A. 锂单质通常保存在煤油中
B. 离子化合物XZ 所有原子都满足8电子稳定结构
4
C. Z的单质能与水反应生成Y的单质
D. 简单离子的还原性W>Y
三、非选择题(本题共4小题,共60分)
16. 根据所学知识,回答下列问题:
(1)反应4HCl(浓) 中,氧化剂是_______,还原产物是_______;MnO 与被氧
2
化 的HCl的物质的量之比是_______。
(2)实验室用NaCO 固体配制500 mL 1 mol/L的NaCO 溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻
3 3 3 3
璃棒、_______、_______。定容时仰视刻度线会导致浓度_______(填“偏高”“偏低”或“无影响”,下同),定
容摇匀后发现液面低于刻度线再加水至刻度线,浓度会_______。
(3)在标准状况下,CO和CO 混合气体共33.6 L,质量为62 g,则两种气体的物质的量之和为
2
_______mol,Co与CO 物质的量之比为_______。
2
(4)联氨(又称联肼,NH,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,实验室可用NaClO溶
2 4
液与NH 反应制备联氨,反应的化学方程式为_______。已知 ,分析
3
联氨和NO 可作为火箭推进剂的主要原因为_______。
2 4
17. 铁、铜及其化合物在工业生产中有重要的用途。运用相关知识,回答下列问题:
(1)电子工业常用30%的FeCl 溶液腐蚀覆在绝缘板上的铜箔来制造印刷电路板。写出FeCl 溶液与铜发生反
3 3应的离子方程式_______。
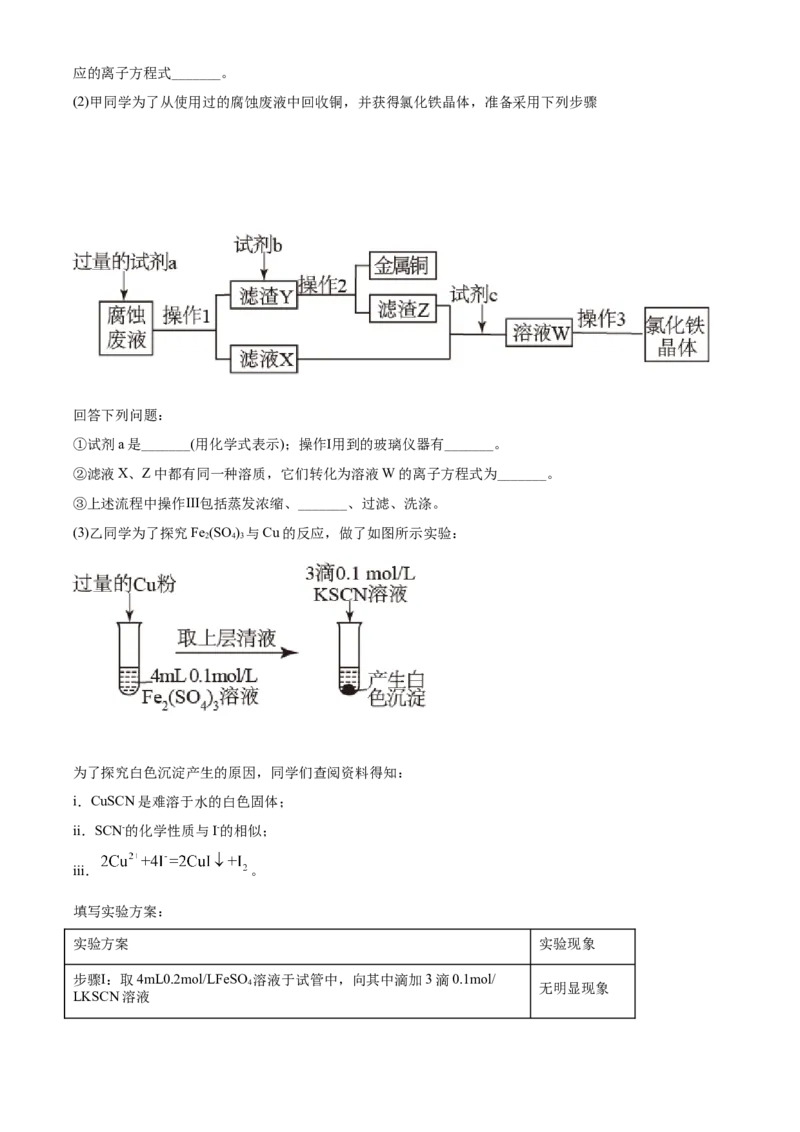
(2)甲同学为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤
回答下列问题:
①试剂a是_______(用化学式表示);操作Ⅰ用到的玻璃仪器有_______。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为_______。
③上述流程中操作Ⅲ包括蒸发浓缩、_______、过滤、洗涤。
(3)乙同学为了探究Fe (SO ) 与Cu的反应,做了如图所示实验:
2 4 3
为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN-的化学性质与I-的相似;
iii. 。
填写实验方案:
实验方案 实验现象
步骤Ⅰ:取4mL0.2mol/LFeSO 溶液于试管中,向其中滴加3滴0.1mol/
4 无明显现象
LKSCN溶液步骤2:取4mL_______mol/LCuSO 溶液于试管中,向其中滴加3滴
4 产生白色沉淀
0.1mol/LKSCN溶液
Cu2+与SCN-反应的离子方程式为_______。
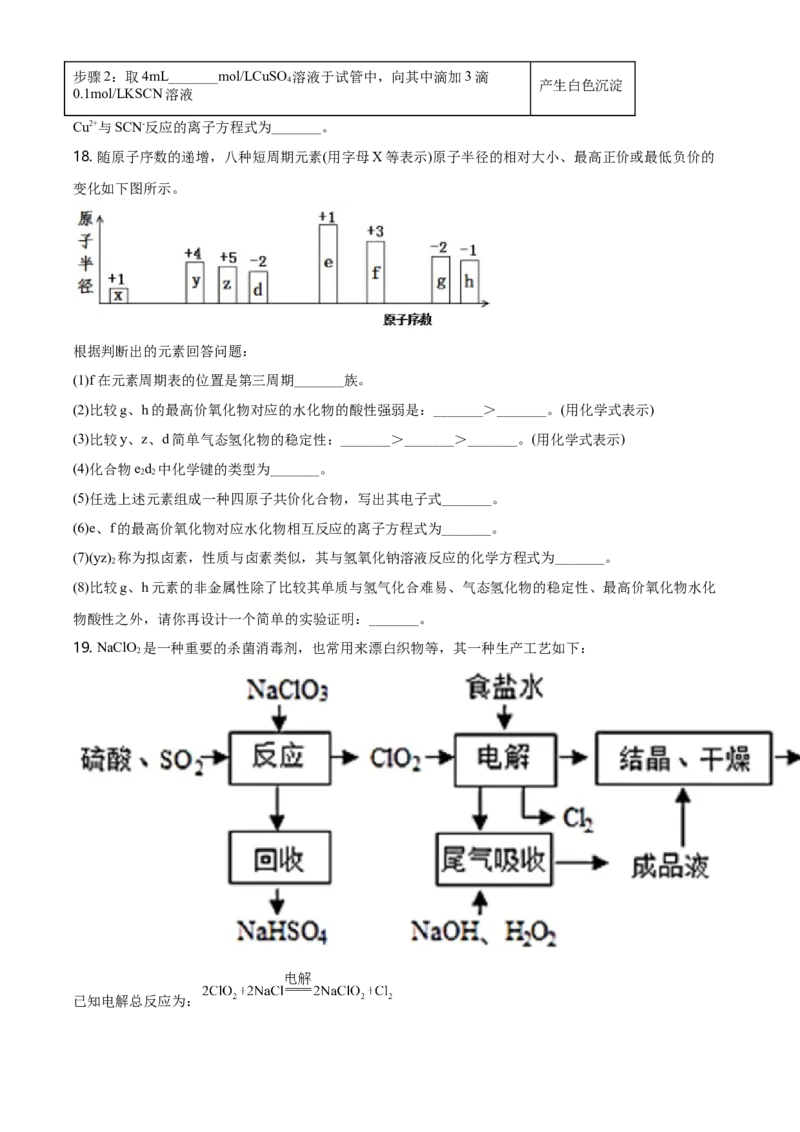
18. 随原子序数的递增,八种短周期元素(用字母X等表示)原子半径的相对大小、最高正价或最低负价的
变化如下图所示。
根据判断出的元素回答问题:
(1)f在元素周期表的位置是第三周期_______族。
(2)比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>_______。(用化学式表示)
(3)比较y、z、d简单气态氢化物的稳定性:_______>_______>_______。(用化学式表示)
(4)化合物ed 中化学键的类型为_______。
2 2
(5)任选上述元素组成一种四原子共价化合物,写出其电子式_______。
(6)e、f的最高价氧化物对应水化物相互反应的离子方程式为_______。
(7)(yz) 称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为_______。
2
(8)比较g、h元素的非金属性除了比较其单质与氢气化合难易、气态氢化物的稳定性、最高价氧化物水化
物酸性之外,请你再设计一个简单的实验证明:_______。
19. NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
2
已知电解总反应为:回答下列问题:
(1)NaClO 中Cl的化合价为_______。
2
(2)工业上常用黄铁矿(FeS )为原料制备硫酸,配平下面方程式:_____________。
2
_______FeS+_______O _______Fe O+_______。
2 2 2 3
(3)从物质分类角度来看,NaHSO 是_______(填字母代号)。
4
a.酸 b.酸式盐 c.电解质 d.非电解质 e.离子化合物 f.共价化合物
(4)写出“反应”步骤中生成ClO 的化学方程式_______。
2
(5)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为_______、
_______。
(6)“尾气吸收”是吸收“电解”过程排出的少量ClO 。此吸收反应中,氧化剂(ClO )与还原剂(H O)的物质的量
2 2 2 2
之比为_______。
(7)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
Cl 的氧化能力(NaClO、Cl 的还原产物都是Cl-)。NaClO 的有效氯含量为_______(计算结果保留两位小数)。
2 2 2 2