文档内容
下学期期末测试卷 01
高一化学
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
的
3.下列金属在冷、浓 硝酸或硫酸中,能形成致密氧化膜的是( )
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。 A.Mg B.Fe C.Cu D.Na
4.测试范围:新人教版(2019)必修2全册。 4.下列物质与水混合、振荡后静置,不出现分层现象的是
5.考试结束后,将本试卷和答题卡一并交回。
A.乙醇 B.苯 C.四氯化碳 D.乙酸乙酯
6.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
5.下列反应中,属于吸热反应的是
Ca 40 Fe 56
A.Al与稀硫酸的反应 B.Na与乙醇的反应
第Ⅰ卷
C.NaOH与硝酸的反应 D.Ba(OH) ·8H O与NH Cl的反应
2 2 4
6.下列化学用语不正确的是( )
一、选择题:本题共20小题,每小题2分,共40分。在每小题给出的四个选项中,只有一项符合题目要
求。
A.羟基的电子式: B.甲烷的空间充填模型:
1.垃圾分类并回收利用,可以节约自然资源,符合可持续发展的要求。与废弃矿泉水瓶对应的垃圾分类标
志是( )
C.丁烷的球棍模型: D.乙醇的分子式:C HO
2 6
7.下列关于氨气性质的描述中,不正确的是( )
A B C D A.无色、有刺激性气味气体
2.钧瓷是中国古代五大名瓷之一,以其独特的釉料及烧制方法而闻名于世。下列钧瓷的制作工艺中,主要 B.极易溶于水
发生了化学变化的是( ) C.相同条件下,密度比空气的大
A.掘泥 B.做坯 C.画坯 D.烧炉 D.能与水反应生成碱性物质
8.下列反应中,属于取代反应的是
A.乙烯在空气中燃烧 B.甲烷与氯气混合光照发生反应
C.乙醇使酸性高锰酸钾溶液褪色 D.乙烯与溴的四氯化碳溶液反应
9.硫代硫酸钠溶液与稀硫酸反应的化学方程式为: NaSO + H SO = NaSO + SO + S↓+ HO,下列各组实
2 2 3 2 4 2 4 2 2
验中最先出现浑浊的是A.利用蛋白质的颜色反应,检验某白色织物是否为蚕丝制品
NaSO 溶液 稀HSO HO
2 2 3 2 4 2
实验 反应温度/℃
B.利用油脂在碱性条件下的水解反应,可以制造甘油和肥皂
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
C.利用葡萄糖的银镜反应,可以检验淀粉是否完全发生了水解反应
A 25 5 0.1 10 0.1 5
D.利用乙烯的加成反应,可用溴水除去甲烷中混有的乙烯
B 25 5 0.2 5 0.2 10 15.下列实验装置或操作与实验目的不相符的是( )
C 35 5 0.1 10 0.1 5
D 35 5 0.2 5 0.2 10
10.下列各对物质中属于同分异构体的是( )
A.12C和14C
B.O 和O
2 3
A.分离乙醇和乙酸的 C.证明氨气易溶于水 D.配制100 mL0.500
B.证明铜与硝酸的反应
混合液 且水溶液呈碱性 mol•L-1HSO 溶液
2 4
C. 与 16.某温度时,在2 L容器中发生A、B两种物之间的转化反应,A、B 物质的量随时间变化的曲线如图所
示,下列说法正确的是( )
D. 与
11.化学与人类社会生产、生活有着密切联系。下列叙述中正确的是( )
A.煤的气化是将其通过物理变化转化为气态的过程
A.该反应的化学方程式是A 2B
B.高温或日常用的消毒剂可使新冠病毒蛋白质变性
B.2 min 时,正反应速率大于逆反应速率
C.重金属盐溶液能使蛋白质盐析,会使人中毒
C.4 min 时,A、B的物质的量相等且反应达到了平衡状态
D.燃煤中加入CaO主要是为了减少温室气体的排放
D.反应开始至 6 min,A的平均反应速率为0.l mol/(L•min)
12.下列金属中,通常采用热还原法冶炼的是
17.以下是镍催化乙烯与氢气的反应机理示意图,下列不正确的是( )
A.Na B.Al C.Fe D.Ag
13.除去下列物质中的杂质(括号内的物质),所使用的试剂和主要操作都正确的是( )
选项 物质 使用的试剂 主要操作
A 乙醇(水) 金属钠 蒸馏
B 乙酸乙酯(乙酸) 饱和碳酸钠溶液 分液
C FeCl (FeCl )溶液 过量铜粉 过滤
2 3 A.乙烯与氢气发生加成反应
D 乙烯(SO 2 ) 酸性高锰酸钾溶液 洗气 B.过程②吸收能量,过程③、④释放能量
14.下列各物质的检验方法中不正确的是( ) C.反应中有非极性键断裂、极性键形成D.催化剂可改变反应的能量变化
18.实验室制取少量乙酸乙酯的装置如下图所示,下列关于该实验的叙述中,不正确的是( )
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
B.试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
C.实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
D.采用长玻璃导管有导气兼冷凝的作用
A.海洋中不存在游离态的氮
19.一定温度下,探究铜与稀HNO 的反应,反应过程如下:
3
B.②中的含氮物质转化属于氮的固定
C.④中的含氮物质转化属于氮的还原
D.向海洋中排放含NO -的废水不会影响NH +的含量
3 4
第II卷(非选择题 60分)
21.(8分)某小组同学探究影响双氧水分解反应速率的因素。实验所用试剂:10%H O、蒸馏水、MnO
2 2 2
粉末。
实验序号 HO 浓度 V(H O 溶液) 温度 催化剂 实验现象
2 2 2 2
1 10% 20 mL 室温 无 无明显现象
2 10% 20 mL 50℃水浴 无 有较多气泡产生
MnO (0.2
下列说法错误的是( ) 3 10% 20 mL 室温 2 有较多气泡产生
g)
A.过程I中生成无色气体的离子方程式是3 Cu + 2 NO - + 8 H+ = 3 Cu2+ + 2 NO↑ + 4 HO
3 2
(1)实验1、2的目的是研究________对双氧水分解反应速率的影响。
B.过程Ⅱ中气体变成红棕色的反应为2 NO + O = 2 NO
2 2
(2)通过对比实验_______(填序号),可研究催化剂对双氧水分解反应速率的影响。
C.步骤III反应速率比I 快的原因一定是NO 溶于水,使c(HNO)增大
2 3
(3)为了准确地比较反应速率的快慢,观测的方法是:收集相同体积的气体,__________。
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
(4)利用上述实验试剂,并结合已有实验方案,进一步设计实验研究双氧水浓度对其分解反应速率的
20.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示,
影响。请将实验方案补全。
下列关于海洋氮循环的说法中,正确的是( )
实验序号 HO 浓度 实验现象
2 2
4 10% ①___ ②___ ③___ ④___ ⑤___
22.(11分)实验室里研究不同价态硫元素之间的转化可采用如下图所示装置进行:(3)某原电池的总反应是Zn + Cu2+ = Zn2+ + Cu,该原电池的正确组成是______。
A B C D
(4)从化学的角度分析,原电池装置产生电流的原因是:原电池装置可将____,并通过能导电的物质
形成闭合回路,产生电流
24.(14分)乙烯和丙烯是重要有机化工原料。
I.以乙烯 为原料可以制备乙二醇和高分子化合物B。
(1)A中发生反应的化学方程式为________________。
(2)B中的现象是__________________。
(3)C中出现淡黄色沉淀,反应中NaS做 ____________(填“氧化剂”或“还原剂”)。
2
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为________________价。
(5)某同学认为D中换成HO 溶液也可以实现上述硫元素的价态转化,并通过实验进一步证明了他
2 2
(1)①的化学方程式为______________。
的观点。实验方案和现象为:取D中反应后的溶液于试管中,_________。
(2)②为取代反应,通过A与NaOH溶液加热条件下完成转化。②的化学反应方程式为__________。
(6)E的作用是_____________,离子方程式为_________________________。
(3)③的反应类型为_______________,B的结构简式为________________。
(7)上述实验体现SO 的性质有__________________。
2
II.丙烯酸乙酯天然存在于菠萝等水果中,是一种天然香料,也可以由乙烯和丙烯为原料合成。
23.(16分)一种简单的原电池装置如下图所示。据图回答下列问题。
(4)有机物E中 的官能团是_________________。
(5)D与E反应生成丙烯酸乙酯的化学反应方程式为__________________。
(6)下列说法正确的是______________。
a.乙烯、丙烯是石油裂解的产物 b.乙二醇易溶于水
(1)锌是该电池的_______(填“正”或“负”)极。Zn片上发生的电极反应为_______。Cu片上发
c.E能使酸性高锰酸钾溶液褪色 d.D可以由葡萄糖分解得到
生的电极反应为__________。能证明化学能转化为电能的实验现象为______。
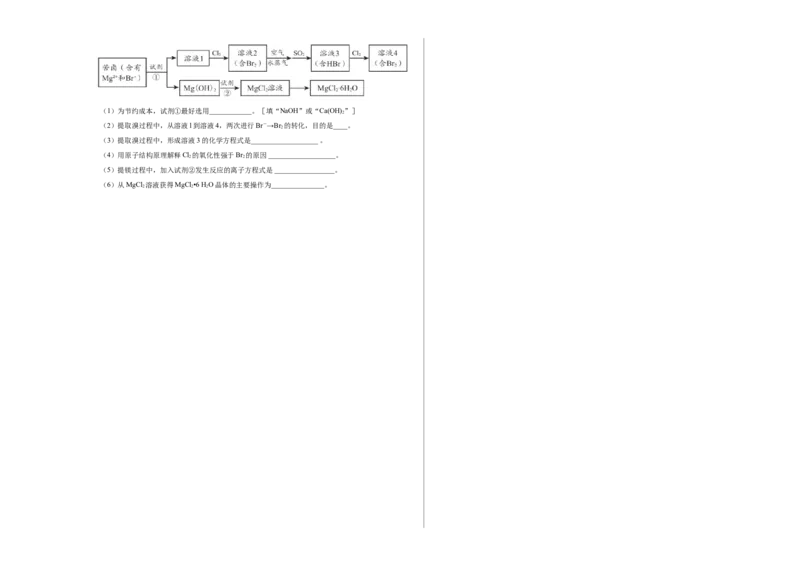
25.(11分)海水资源的利用具有广阔的前景。从海水中提取 Br 与 MgCl • 6 H O 的流程如下:
2 2 2
(2)装置中稀硫酸的作用是_______。
A.电极材料 B.电极反应物 C.电子导体 D.离子导体(1)为节约成本,试剂①最好选用____________。[填“NaOH”或“Ca(OH) ”]
2
(2)提取溴过程中,从溶液l到溶液4,两次进行Br-→Br 的转化,目的是____。
2
(3)提取溴过程中,形成溶液3的化学方程式是___________________ 。
(4)用原子结构原理解释Cl 的氧化性强于Br 的原因 ___________________。
2 2
(5)提镁过程中,加入试剂②发生反应的离子方程式是 _________________。
(6)从MgCl 溶液获得MgCl •6 HO晶体的主要操作为_______________。
2 2 2