文档内容
山东省高三年级适应性联考(一)
化学试题
本试卷共4页,20题。全卷满分100分。考试用时90分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在答题卡上,并将准考证号条形码粘贴在答题卡上
的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在
试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和答
题卡上的非答题区域均无效。
4.考试结束后请将本试题卷和答题卡一并上交。
可能用到的原子量:H 1 Li 7 C 12 O 16 Na 23 Mg 24 P 31 S 32 Cl 35.5 Fe 56
Ni 59
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与生产、生活和社会息息相关,下列有关说法错误的是( )
A.合成氨的反应塔与外加电源的正极相连,并维持一定的电压可以钝化防腐
B.药用泡腾片中含有碳酸氢钠,遇水产生大量气泡加速药物分散和溶解
C.运动员剧烈运动后,补充的运动饮料中含有糖类和一定浓度的 等
D.开发利用新能源,减少化石燃料的使用是实现“碳中和”目标的有效途径
2.下列关于元素与物质分类的说法正确的是( )
A. 中金属元素均为过渡金属元素
B. 可与氢氟酸反应,故 为碱性氧化物
C. 为正盐,故 为一元酸
D.直径介于 的氮化镓 为胶体
3.下列关于实验操作的说法正确的是( )
A.取用药品时,剩余药品均不得放回原试剂瓶
B.中和热测定时,只需记录溶液的初始温度和最高温度
C.稀硫酸、 溶液等沾到皮肤上应立即用大量清水冲洗
D.酸碱中和滴定时,不能加入蒸馏水,以免溶液稀释产生误差
4.设 为阿伏伽德罗常数的值,下列说法错误的是( )A. 石墨含 键数为
B.常温常压下, 中含质子数为
C. 和 的混合物中含 原子数为
D. 的 溶液中含 和 的总数为
5.下列有关说法正确的是( )
A. 和 均既有氧化性又有还原性
B.氢氧化铝胶体带正电荷,故明矾可以做净水剂
C.严禁使用有毒的 用于做食品漂白剂、防腐剂和抗氧化剂
D.电解质溶液导电是阴、阳离子在电场作用下的定向移动,为物理变化
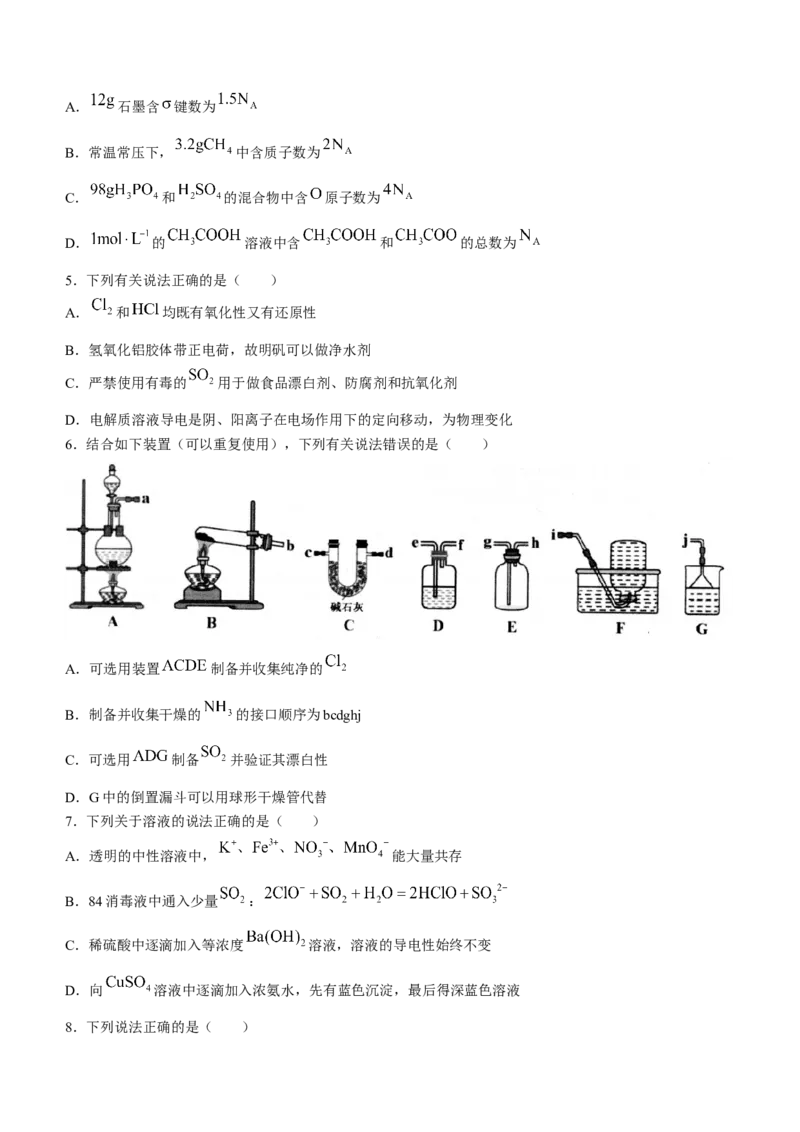
6.结合如下装置(可以重复使用),下列有关说法错误的是( )
A.可选用装置 制备并收集纯净的
B.制备并收集干燥的 的接口顺序为bcdghj
C.可选用 制备 并验证其漂白性
D.G中的倒置漏斗可以用球形干燥管代替
7.下列关于溶液的说法正确的是( )
A.透明的中性溶液中, 能大量共存
B.84消毒液中通入少量 :
C.稀硫酸中逐滴加入等浓度 溶液,溶液的导电性始终不变
D.向 溶液中逐滴加入浓氨水,先有蓝色沉淀,最后得深蓝色溶液
8.下列说法正确的是( )A. ,则
B. 的摩尔燃烧焓为 ,则
C. ,则完全破坏等质量的 和 中的化学键,需要的能量 大
D. ,则 与足量 反应放热
9.如图为铁镍电池又称爱迪生电池,具有优良的耐过充和过放性能。下列说法正确的是( )
A.放电时, 电极电势比 电势高
B.放电时, 极发生
C.充电时,阴极附近的 减小
D.充电时,每生成 ,有 被氧化
10.常温下部分难溶电解质的溶度积 如下表:
难溶电解
质
下列叙述中错误的是( )
A. 在等物质的量浓度的 和 溶液中的溶解度相同
B.向 悬浊液中加入 溶液,可完成沉淀的转化
C. 的平衡常数约为
D.含 和 固体的溶液中离子浓度关系为:
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
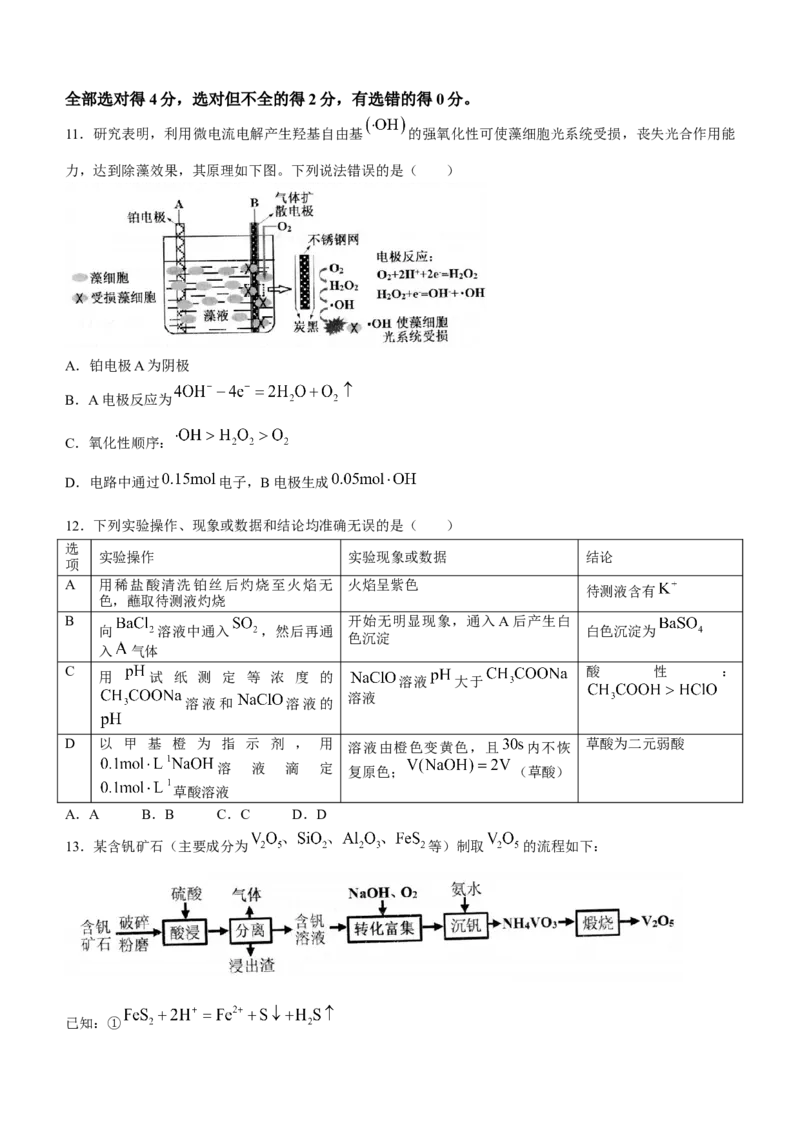
11.研究表明,利用微电流电解产生羟基自由基 的强氧化性可使藻细胞光系统受损,丧失光合作用能
力,达到除藻效果,其原理如下图。下列说法错误的是( )
A.铂电极A为阴极
B.A电极反应为
C.氧化性顺序:
D.电路中通过 电子,B电极生成
12.下列实验操作、现象或数据和结论均准确无误的是( )
选
实验操作 实验现象或数据 结论
项
A 用稀盐酸清洗铂丝后灼烧至火焰无 火焰呈紫色
待测液含有
色,蘸取待测液灼烧
B 开始无明显现象,通入A后产生白
向 溶液中通入 ,然后再通 白色沉淀为
色沉淀
入 气体
C 酸 性 :
用 试 纸 测 定 等 浓 度 的 溶液 大于
溶液
溶液和 溶液的
D 以 甲 基 橙 为 指 示 剂 , 用 溶液由橙色变黄色,且 内不恢 草酸为二元弱酸
溶 液 滴 定 复原色; (草酸)
草酸溶液
A.A B.B C.C D.D
13.某含钒矿石(主要成分为 等)制取 的流程如下:
已知:①②强酸性溶液中钒以 形式存在
③ 易溶于水、 难溶于水
下列说法错误的是( )
A.破碎粉磨含钒矿石的目的是加快酸浸速率和溶出率
B.浸出渣的主要成分为
C.转化富集的目的是除去含钒溶液中的
D.沉钒过程中发生反应的离子方程式为
14 . 实 验 室 使 用 标 准 溶 液 测 定 补 铁 剂 硫 酸 亚 铁 片 中 的 含 量 , 发 生 反 应 为
。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示
剂。下列说法错误的是( )
A.将硫酸亚铁片研碎,置于稀硫酸中溶解后过滤
B.标准重铬酸钾液应用酸式滴定管取用
C.由实验可知酸性溶液中还原性: 二苯胺磺酸钠
D.酸性 溶液与乙醇生成乙酸的离子方程式为:
15. 为二元弱酸,常温下向 溶液滴加 固体(忽略溶液体积变化),溶液中 、
的 百 分 含 量 与 的 关 系 如 图 所 示 , 已 知 ; 如 :
。下列说法正确的是( )A.曲线 是 的百分含量
B. 的 的数量级为
C.M点对应溶液中,
D. 溶液中
三、非选择题:本题共5小题,共60分。
16.(12分) 元素是自然界中以及生活中常见的元素,请回答下列有关问题。
(1)实验室制备氢氧化铁胶体,应向沸水中逐滴加入饱和_________溶液(填化学式),至溶液呈透明的
_________色。
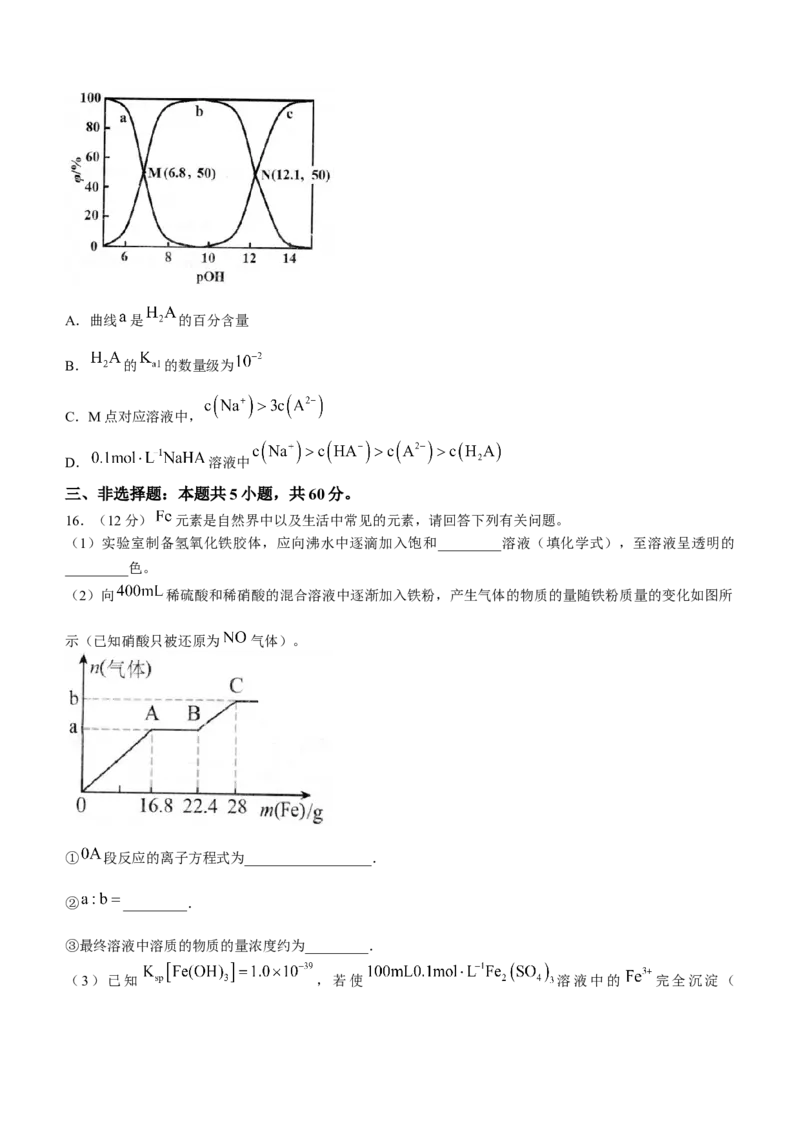
(2)向 稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体的物质的量随铁粉质量的变化如图所
示(已知硝酸只被还原为 气体)。
① 段反应的离子方程式为__________________.
② _________.
③最终溶液中溶质的物质的量浓度约为_________.
(3)已知 ,若使 溶液中的 完全沉淀(),应调节 最小为_________.
(4) 是一种新型高效水处理剂,可用 和 在碱性条件下制备,则该反应的化学方
程式为__________________.
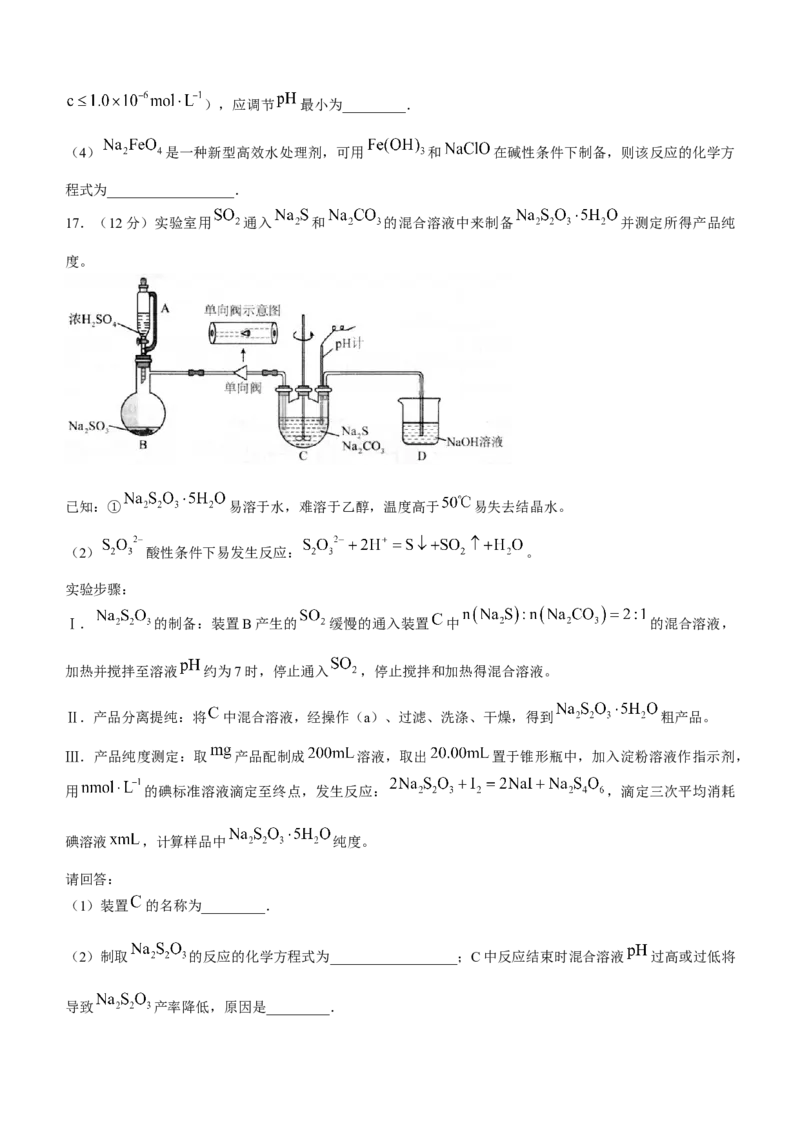
17.(12分)实验室用 通入 和 的混合溶液中来制备 并测定所得产品纯
度。
已知:① 易溶于水,难溶于乙醇,温度高于 易失去结晶水。
(2) 酸性条件下易发生反应: 。
实验步骤:
Ⅰ. 的制备:装置B产生的 缓慢的通入装置 中 的混合溶液,
加热并搅拌至溶液 约为7时,停止通入 ,停止搅拌和加热得混合溶液。
Ⅱ.产品分离提纯:将 中混合溶液,经操作(a)、过滤、洗涤、干燥,得到 粗产品。
Ⅲ.产品纯度测定:取 产品配制成 溶液,取出 置于锥形瓶中,加入淀粉溶液作指示剂,
用 的碘标准溶液滴定至终点,发生反应: ,滴定三次平均消耗
碘溶液 ,计算样品中 纯度。
请回答:
(1)装置 的名称为_________.
(2)制取 的反应的化学方程式为__________________;C中反应结束时混合溶液 过高或过低将
导致 产率降低,原因是_________.(3)Ⅱ为产品的分离提纯
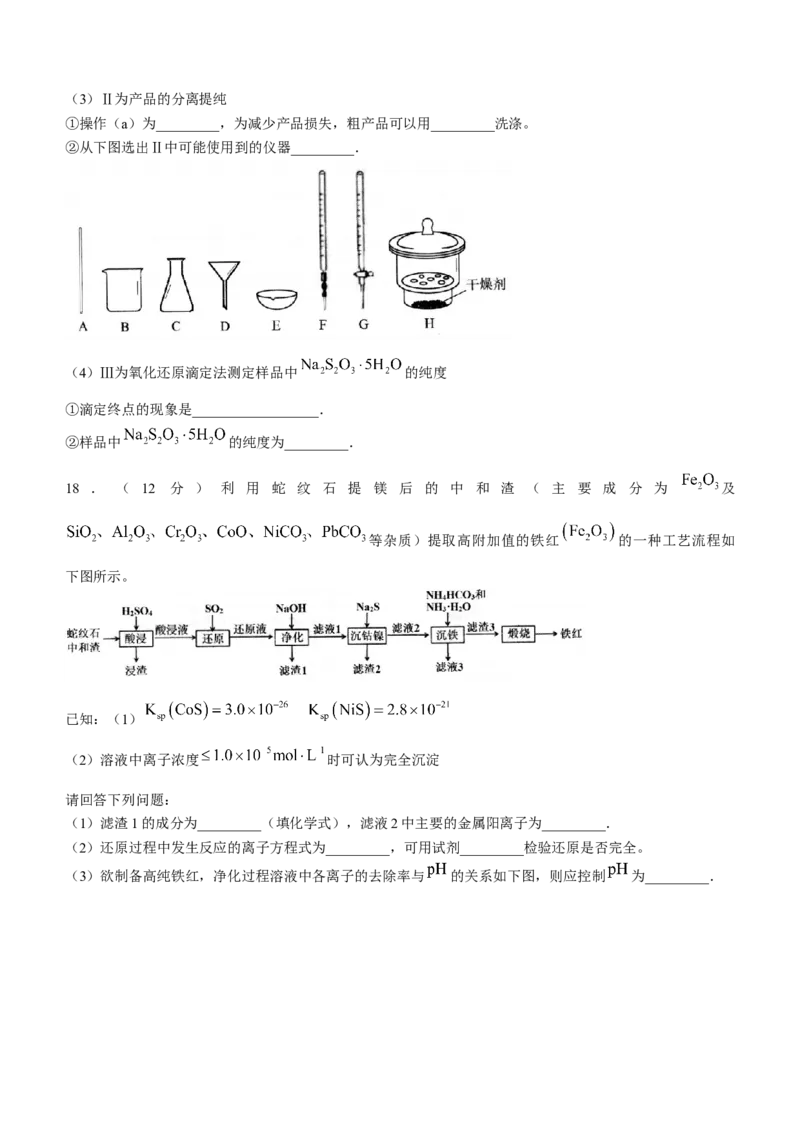
①操作(a)为_________,为减少产品损失,粗产品可以用_________洗涤。
②从下图选出Ⅱ中可能使用到的仪器_________.
(4)Ⅲ为氧化还原滴定法测定样品中 的纯度
①滴定终点的现象是__________________.
②样品中 的纯度为_________.
18 . ( 12 分 ) 利 用 蛇 纹 石 提 镁 后 的 中 和 渣 ( 主 要 成 分 为 及
等杂质)提取高附加值的铁红 的一种工艺流程如
下图所示。
已知:(1)
(2)溶液中离子浓度 时可认为完全沉淀
请回答下列问题:
(1)滤渣1的成分为_________(填化学式),滤液2中主要的金属阳离子为_________.
(2)还原过程中发生反应的离子方程式为_________,可用试剂_________检验还原是否完全。
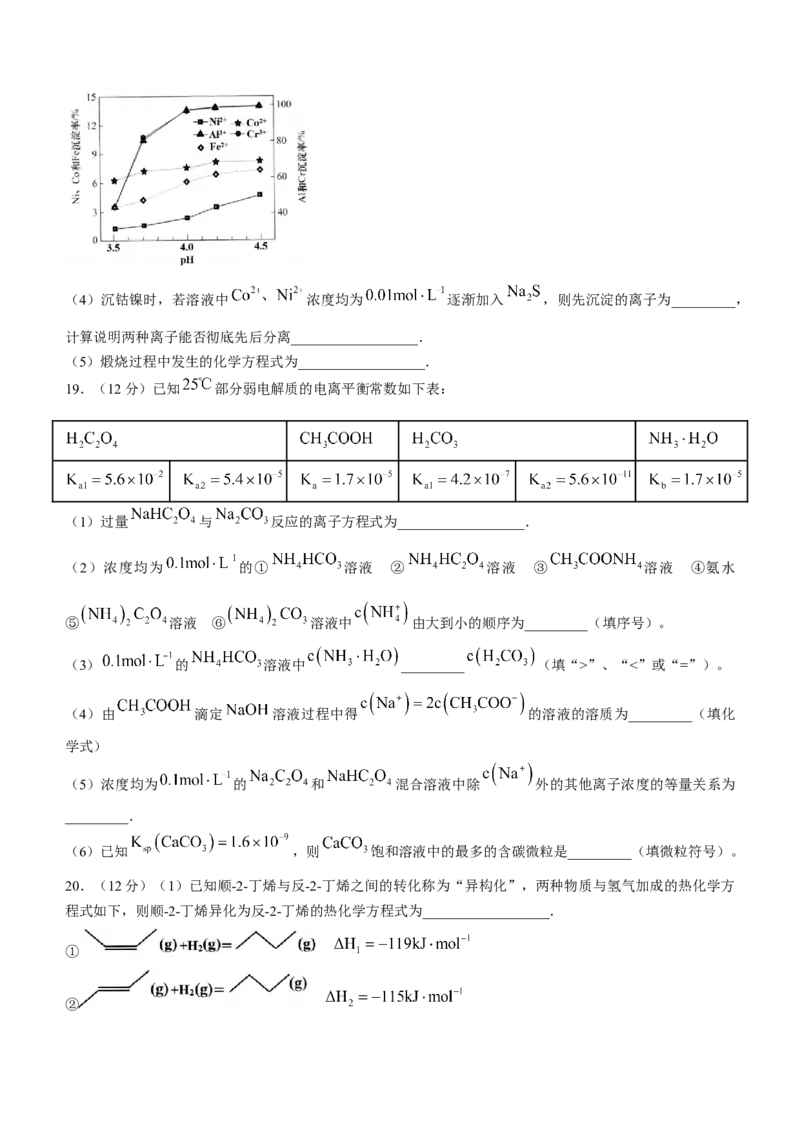
(3)欲制备高纯铁红,净化过程溶液中各离子的去除率与 的关系如下图,则应控制 为_________.(4)沉钴镍时,若溶液中 浓度均为 逐渐加入 ,则先沉淀的离子为_________,
计算说明两种离子能否彻底先后分离__________________.
(5)煅烧过程中发生的化学方程式为__________________.
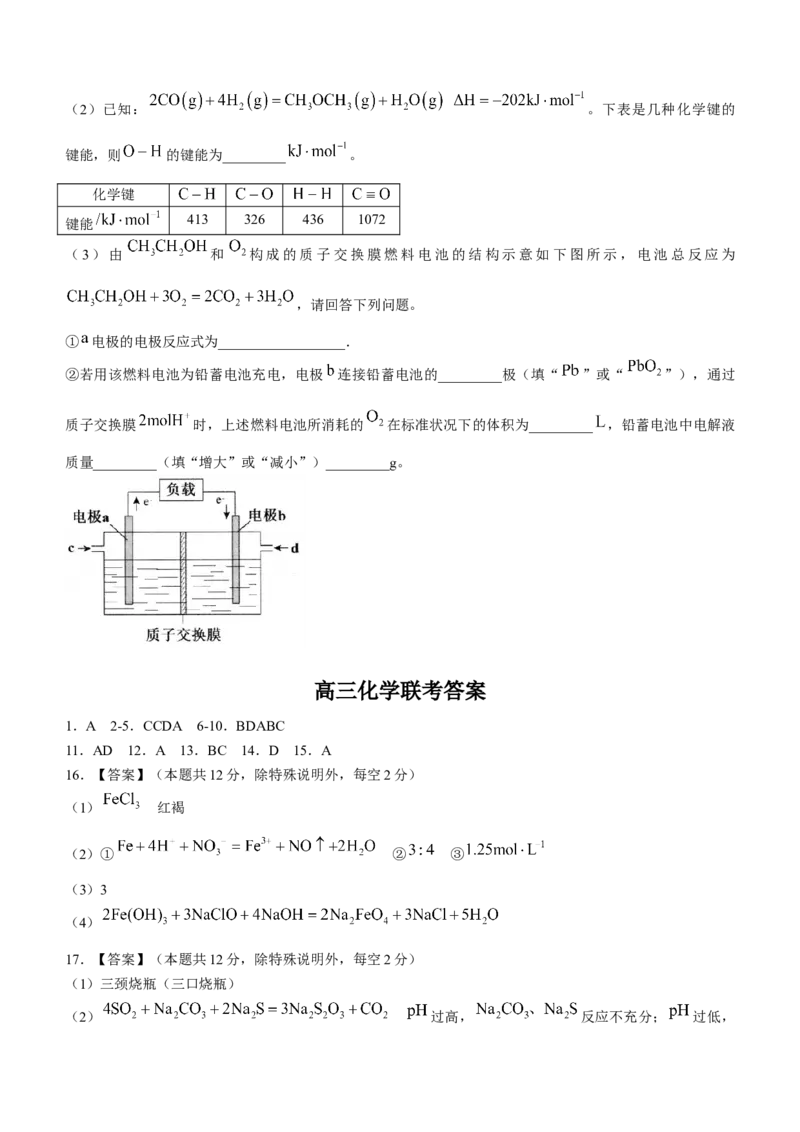
19.(12分)已知 部分弱电解质的电离平衡常数如下表:
(1)过量 与 反应的离子方程式为__________________.
(2)浓度均为 的① 溶液 ② 溶液 ③ 溶液 ④氨水
⑤ 溶液 ⑥ 溶液中 由大到小的顺序为_________(填序号)。
(3) 的 溶液中 _________ (填“>”、“<”或“=”)。
(4)由 滴定 溶液过程中得 的溶液的溶质为_________(填化
学式)
(5)浓度均为 的 和 混合溶液中除 外的其他离子浓度的等量关系为
_________.
(6)已知 ,则 饱和溶液中的最多的含碳微粒是_________(填微粒符号)。
20.(12分)(1)已知顺-2-丁烯与反-2-丁烯之间的转化称为“异构化”,两种物质与氢气加成的热化学方
程式如下,则顺-2-丁烯异化为反-2-丁烯的热化学方程式为__________________.
①
②(2)已知: 。下表是几种化学键的
键能,则 的键能为_________ 。
化学键
413 326 436 1072
键能
(3)由 和 构成的质子交换膜燃料电池的结构示意如下图所示,电池总反应为
,请回答下列问题。
① 电极的电极反应式为__________________.
②若用该燃料电池为铅蓄电池充电,电极 连接铅蓄电池的_________极(填“ ”或“ ”),通过
质子交换膜 时,上述燃料电池所消耗的 在标准状况下的体积为_________ ,铅蓄电池中电解液
质量_________(填“增大”或“减小”)_________g。
高三化学联考答案
1.A 2-5.CCDA 6-10.BDABC
11.AD 12.A 13.BC 14.D 15.A
16.【答案】(本题共12分,除特殊说明外,每空2分)
(1) 红褐
(2)① ② ③
(3)3
(4)
17.【答案】(本题共12分,除特殊说明外,每空2分)
(1)三颈烧瓶(三口烧瓶)
(2) 过高, 反应不充分; 过低,导致 转化为 和
(3)①蒸发浓缩、冷却结晶 乙醇 ②ABDEH
(4)①滴入最后半滴碘标准溶液后溶液由无色变蓝色,且半分钟内不恢复原色 ②
18.【答案】(本题共12分,除特殊说明外,每空2分)
(1) 和
(2) 溶液或苯酚
(3)4.5
(4) 当 恰好沉淀完全时, ,根据 ,此时
, ,不生成 沉淀,故可以
将 和 彻底先后分离。
(5)
19.【答案】(本题共12分,每空2分)
(1)
(2)⑤>⑥>②>③>①>④
(3)
(4) 和
(5)
(6)
20.【答案】(本题共12分,除特殊说明外,每空2分)
(1)
(2)480
(3)①
② 11.2 增大 160【解析】(1)由 得,过量 与 反应的离子方程式为
(2)可以将浓度相等的 6 种溶液分为 3 组,第 1 组电离生成 2 个铵根的盐溶液: 和
, 最大;第2组电离生成1个铵根的 和 次之,微
弱 电 离 的 弱 碱 最 小 。 分 组 讨 论 : 第 1 组 内 水 解 程 度 : 根 据
,得 促进 水解程度大, 较小,即⑤>⑥;第2组内水
解程度:根据 ,得 促进 水解程度最大,
最小, 促进 水解程度最小, 最大,②>③>①;综上得 由大到
小的顺序为⑤>⑥>②>③>①>④。
(3) ,根据“越弱越水解”得 溶液中
水解才度大于 ,溶液中 。
(4)由 滴定 溶液过程中得 的溶液中,应为 过量的溶
液,溶质为 和 。
19 . ( 5 ) 浓 度 均 为 的 和 混 合 溶 液 中 电 荷 守 恒 为 :
, 物 料 守 恒 为 :
, 所 以 质 子 守 恒 为 :
(6)过量 溶于水后,有沉淀溶解平衡 , 存在水解平衡:
、 (该步水解忽略),上层清液中物料
守 恒 为 ,, 则 。 则 上 层 清 液 中
(假设溶于水的 电离出的 第一步完全水
解) ,即 ,故上层清液中最多
的含碳微粒是 。