文档内容
2016年中考化学模拟试卷二
(满分:100分 时间:100分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 K-39 Cu-64 Zn-65
Ag-108
一、选择题(本大题25小题,1~12小题每题1分,13~25小题每题2分,共38分。在每小题给出的四
个选项中,只有一项是符合题目要求的)
1.下列过程中,只发生物理变化的是(B)
A.湿法炼钢 B.雕琢玉石 C.制造轮胎 D.葡萄酿酒
2.空气的成分中能供给人体呼吸的气体是(B)
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
3.下列物质中属于混合物的是(A)
A.碘酒 B.液氢 C.蒸馏水 D.高锰酸钾
4.下列做法不符合环保理念的是(B)
A.秸秆回收利用,不露天焚烧 B.预防传染病,不回收塑料制品
C.禁止在公共场所吸烟 D.提倡使用太阳能热水器
5.下列不属于化学研究范畴的是(D)
A.纳米铜的性质 B.C 的组成 C.单晶硅的结构 D.无人机的研发
60
6.“茉莉的香气清新淡雅,能够使人心情放松;檀木的香气持久醇厚,能缓解紧张焦虑的情绪……。”
从微观角度分析,语句中隐含的分子性质有(B)
①分子的质量很小 ②分子之间有间隔 ③分子是不断运动的 ④不同分子性质不同
A.①② B.③④ C.①③ D.②④
7.物质的性质决定其用途。下列物质的用途与性质对应关系错误的是(C)
A.氢氧化钙可用来改良酸性土壤——氢氧化钙溶液呈碱性
B.氮气常用作保护气——氮气化学性质稳定
C.固态二氧化碳可用于人工降雨——二氧化碳能与碱反应
D.氧化钙可作食品干燥剂——氧化钙能与水反应
8.如图是某元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是 (D)
A.该元素属于金属元素
B.该原子在化学变化中容易失去电子
C.该原子的大小主要决定于核外电子的运动空间
D.该原子的质量由构成其原子的质子和电子决定
9.下列属于不可再生能源的是(A)
A.煤 B.太阳能
C.风能 D.氢能
10.草木灰是一种农家肥料,其有效成分是KCO,它属于(C)
2 3A.氮肥 B.磷肥 C.钾肥 D.复合肥料
11.测定人体内或排出的液体pH,可以帮助人们了解身体的健康状况。人体内的一些液体的近似pH如下:
液体 胃液 胰液 胆汁 血浆
pH 0.9~1.5 7.5~8.0 7.1~7.3 7.35~7.45
下列液体中,碱性最强的是(B)
A.胃液 B.胰液 C.胆汁 D.血浆
12.地壳中含量最多的元素是(A)
A.氧 B.硅 C.铝 D.铁
13.下列常用仪器的操作方法正确的是(C)
A.用酒精灯火焰直接加热烧杯 B.打开试剂瓶取用试剂后没及时盖瓶塞
C.给试管内固体加热,试管口略向下倾斜 D.取用试剂后将滴管清洗再放回原滴瓶
14.下列化合物中氯元素的化合价为+5的是(B)
A.HClO B.KClO C.HClO D.KCl
4 3
15.下列认识或做法正确的是(D)
A.煤炉上放一壶水就能防止一氧化碳中毒 B.对于人体必需的元素摄入量越多越好
C.用铁制容器放波尔多液(含硫酸铜) D.用白醋除热水瓶胆内的水垢
16.下列物质的分类中不正确的是(B)
A.单质:硅、水银、金刚石 B.碱:氢氧化钡、氢氧化钠、乙醇
C.盐:硝酸银、氯化铁、高锰酸钾 D.氧化物:氧化镁、三氧化硫、五氧化二磷
17.2014年7月起,乒乓球国际比赛启用一种新型塑料球。生产这种乒乓球的塑料属于(B)
A.无机材料 B.合成材料 C.复合材料 D.天然材料
18.有X、Y、Z三种金属,只有Z在自然界中主要以单质形式存在,如果把Y加入X的硝酸盐溶液中,Y表
面有X析出。据此判断这三种金属的活动性由强到弱的顺序为(C)
A.X>Z>Y B.X>Y>Z C.Y>X>Z D.Z>Y>X
19.对下列有水生成的四个化学方程式的反应类型,判断不正确的是(D)
①2H+O=====2HO ②HCO===HO+CO↑ ③H+CuO=====Cu+HO
2 2 2 2 3 2 2 2 2
④SO+2NaOH===NaSO+HO
2 2 3 2
A.①是化合反应 B.②是分解反应 C.③是置换反应 D.④是复分解反应
20.婴儿“尿不湿”最关键的材料是聚丙烯酸钠,其吸水性是棉花、纸张的数十倍。它是由丙烯酸(CHO)
3 4 2
与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸的说法中,正确的是(C)
A.它是有机高分子化合物
B.其中氧元素与氢元素的质量比为9∶1
C.其中碳元素的质量分数为50%
D.一个丙烯酸分子由3个碳原子、4个氢原子和1个氧分子构成
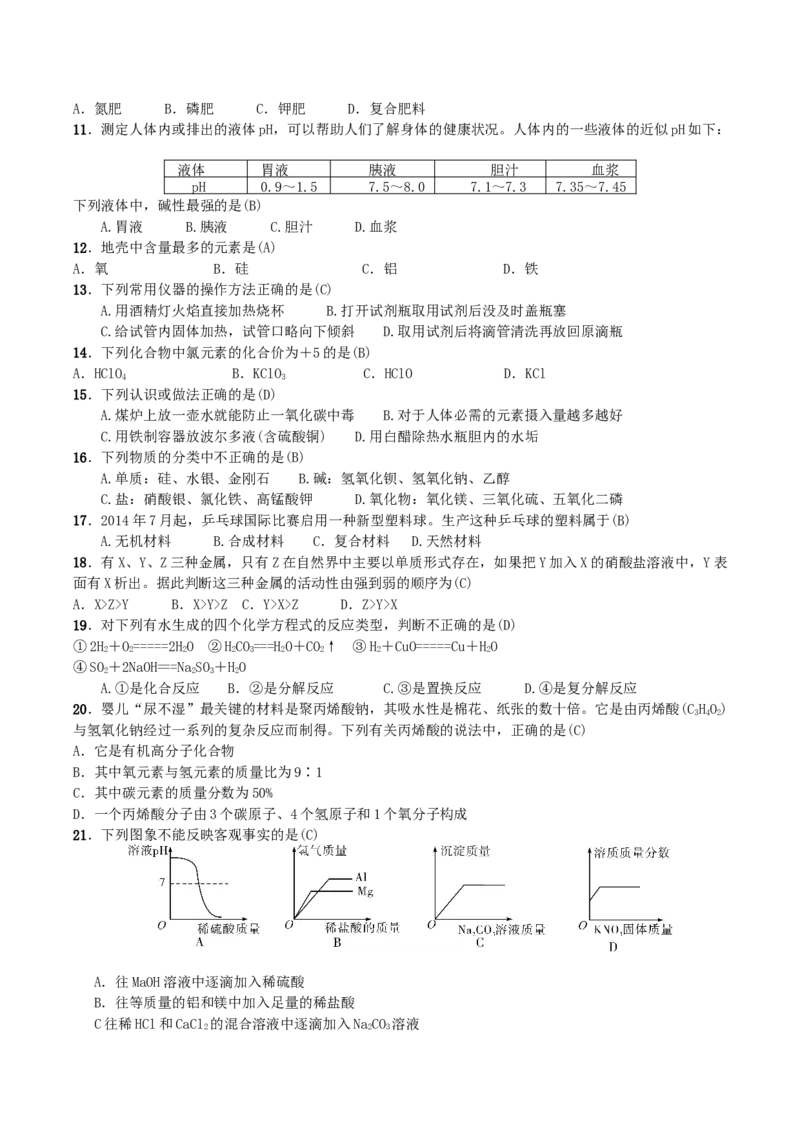
21.下列图象不能反映客观事实的是(C)
A.往MaOH溶液中逐滴加入稀硫酸
B.往等质量的铝和镁中加入足量的稀盐酸
C往稀HCl和CaCl 的混合溶液中逐滴加入NaCO 溶液
2 2 3D.等温条件下往接近饱和的硝酸钾溶液中不断加入硝酸钾固体
22.“类推”是化学学习过程中常用的思维方法。现有以下类推结果,其中正确的是(D)
A.因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液
B.金属铝与盐酸反应生产AlCl 和H,所以金属铁与盐酸反应生产FeCl 和H
3 2 3 2
C.因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件
D.因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素
23.下列各组物质的鉴别中,所选的鉴别试剂,不正确的是(C)
选项 待鉴别的物质 鉴别试剂
A 氧气、二氧化碳、空气 燃着的木条
B 氯化铵固体和氯化钠固体 氢氧化钠溶液
C 氢氧化钠溶液和碳酸钠溶液 酚酞试剂
D 稀盐酸和稀硫酸 BaCl 溶液
2
24.下列说法正确的是(C)
A.空气中一氧化碳、二氧化硫的增加能导致酸雨
B.生石灰在空气中变质需要消耗空气中的氧气和水
C.应适量的水能区分硝酸铵、氯化钠、硫酸铜三种白色固体
D.电解水时电源负极产生的是能使带火星木条复燃的气体
25.在一定条件下,物质A、B发生反应2A+2B===2C+D,探究学习小组在实验中得到下表数据:
物质 A B C D
反应前质量(g) 4.6 4.0 0 0
反应后质量(g) 0 0.4 8.0 a
下列说法正确的是(C)
A.反应后原子的数目减少 B.a=0.6
C.B、D的相对分子质量之比为9∶1 D.该反应一定是复分解反应
二、填空题(本大题4小题,共17分)
26.(4分)用正确的化学用语填空:
(1)硫的元素符号S;(2)2个锂原子2Li;
(3)4个铝离子 4A l 3 + ;(4)相对分子质量最小的氧化物HO。
2
27.(3分)陕西洛川被称为“苹果之乡”。苹果中富含多种对人体健康有益的物质,苹果酸和维生素 C就
是其中的两种。
(1)可用 p H 试纸 来测定某种苹果汁的酸碱度。
(2)人体若缺乏维生素C易患②(填序号)。
①甲状腺肿大 ②败血症 ③夜盲症
(3)为使苹果树茎叶茂盛,果实硕大,增强抗旱能力,可以施用的一种化肥是③(填序号)。
①NHNO ②KSO ③(NH)HPO
4 3 2 4 4 2 4
28.(5分)水是宝贵的自然资源。请回答下列问题:
(1)电解水的化学方程式是2H O ===== 2 H↑+_O↑,通过该实验得到的结论是水是由氢、氧两种元素
2 2 2
组成的。
(2)某自来水厂对汾河水进行净化,取水后,首先向其中加入明矾,再经过过滤、消毒灭菌后使之达到饮
用标准。明矾可用于净水,是因为明矾溶于水的生成物可以吸附悬浮于水中的杂质,加速沉降。要测定饮
用水是软水还是硬水,可用_肥皂水来检验。
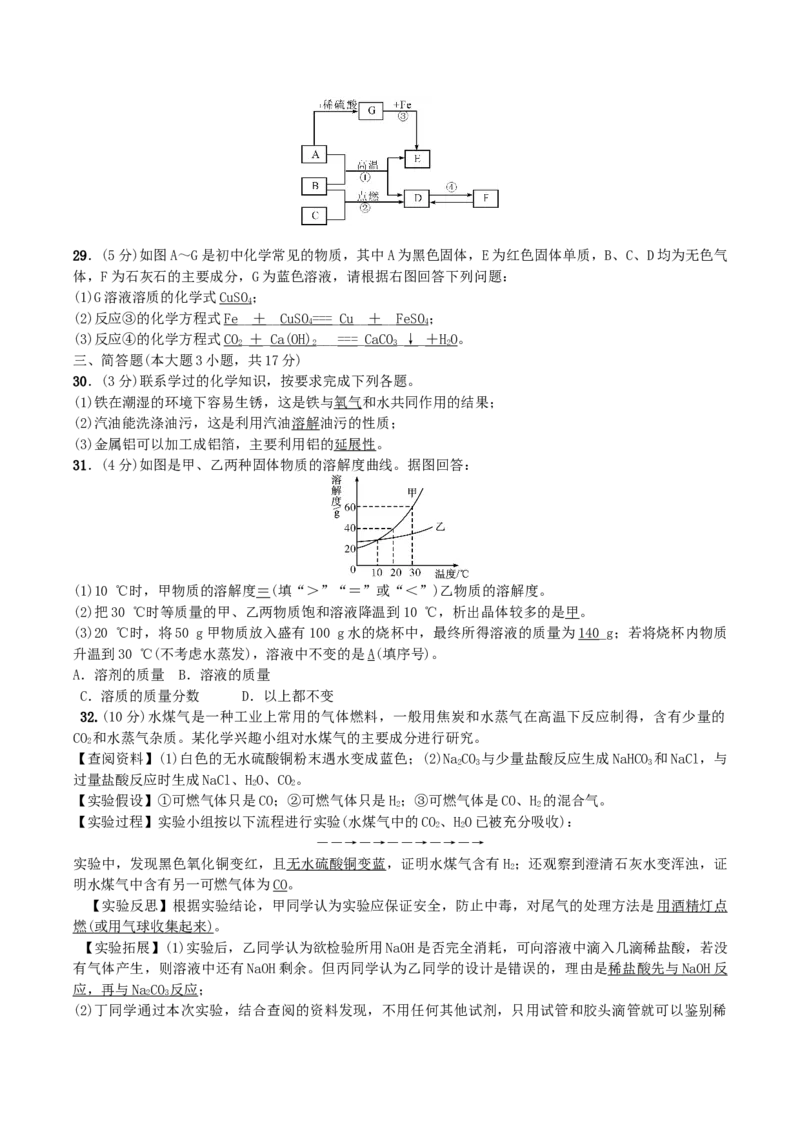
(3)水是一种重要的化学资源,写出实验室用水鉴别的一组物质:硝酸铵和氢氧化钠固体(合理即可)。29.(5分)如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气
体,F为石灰石的主要成分,G为蓝色溶液,请根据右图回答下列问题:
(1)G溶液溶质的化学式CuSO;
4
(2)反应③的化学方程式Fe__+__CuSO = = =_Cu__+__FeSO;
4 4
(3)反应④的化学方程式CO_+_Ca(OH)___ = = =_CaCO_↓_ + HO。
2 2 3 2
三、简答题(本大题3小题,共17分)
30.(3分)联系学过的化学知识,按要求完成下列各题。
(1)铁在潮湿的环境下容易生锈,这是铁与氧气和水共同作用的结果;
(2)汽油能洗涤油污,这是利用汽油溶解油污的性质;
(3)金属铝可以加工成铝箔,主要利用铝的延展性。
31.(4分)如图是甲、乙两种固体物质的溶解度曲线。据图回答:
(1)10 ℃时,甲物质的溶解度=(填“>”“=”或“<”)乙物质的溶解度。
(2)把30 ℃时等质量的甲、乙两物质饱和溶液降温到10 ℃,析出晶体较多的是甲。
(3)20 ℃时,将50 g甲物质放入盛有100 g水的烧杯中,最终所得溶液的质量为140_g;若将烧杯内物质
升温到30 ℃(不考虑水蒸发),溶液中不变的是A(填序号)。
A.溶剂的质量 B.溶液的质量
C.溶质的质量分数 D.以上都不变
32.(10分)水煤气是一种工业上常用的气体燃料,一般用焦炭和水蒸气在高温下反应制得,含有少量的
CO 和水蒸气杂质。某化学兴趣小组对水煤气的主要成分进行研究。
2
【查阅资料】(1)白色的无水硫酸铜粉末遇水变成蓝色;(2)NaCO 与少量盐酸反应生成NaHCO 和NaCl,与
2 3 3
过量盐酸反应时生成NaCl、HO、CO。
2 2
【实验假设】①可燃气体只是CO;②可燃气体只是H;③可燃气体是CO、H 的混合气。
2 2
【实验过程】实验小组按以下流程进行实验(水煤气中的CO、HO已被充分吸收):
2 2
――→―→――→―→―→
实验中,发现黑色氧化铜变红,且无水硫酸铜变蓝,证明水煤气含有H ;还观察到澄清石灰水变浑浊,证
2
明水煤气中含有另一可燃气体为CO。
【实验反思】根据实验结论,甲同学认为实验应保证安全,防止中毒,对尾气的处理方法是用酒精灯点
燃 ( 或用气球收集起来 )。
【实验拓展】(1)实验后,乙同学认为欲检验所用NaOH是否完全消耗,可向溶液中滴入几滴稀盐酸,若没
有气体产生,则溶液中还有NaOH剩余。但丙同学认为乙同学的设计是错误的,理由是 稀盐酸先与 NaOH 反
应,再与 N aCO 反应;
2 3
(2)丁同学通过本次实验,结合查阅的资料发现,不用任何其他试剂,只用试管和胶头滴管就可以鉴别稀盐酸和碳酸钠两种无色溶液。正确的鉴别方案及结论是用试管取少量其中一种无色溶液,胶头滴管吸取另
一种无色溶液,将胶头滴管中溶液滴几滴至试管中,若立即有气泡产生,则试管中液体为稀盐酸,胶头滴
管中液体为碳酸钠;若开始无气泡产生,则试管中液体为碳酸钠,胶头滴管中液体为稀盐酸。
四、实验题(本大题2小题,共18分)
33.(6分)某同学对含有泥沙的粗盐进行提纯,并用提纯后的氯化钠配制 100 g质量分数为5%的氯化钠溶
液。请回答有关问题:
(1)按下面步骤提纯粗盐:
①取一定质量的粗盐样品,加水溶解;②通过过滤操作将泥沙除去;③将滤液移入蒸发皿,蒸发结晶,得
到氯化钠晶体。
(2)在上述实验步骤中,都使用了同一仪器玻璃棒(填名称),它在步骤①和③的操作方法相同,但目的不
同,步骤①的目的是搅拌,加快食盐的溶解速率,步骤③的目的是搅拌,防止滤液飞溅。
(3)利用上述实验得到的氯化钠晶体,配制100 g质量分数为5%的氯化钠溶液:
①配制溶液的步骤:计算、称量、溶解、装瓶;
②量取所需的水应选用100mL的量筒。
34.(12分)通过化学学习,相信你已经初步掌握了实验室制取气体的有关知识。请结合图示回答问题:
(1)写出图中用数字标记的仪器名称:①酒精灯,②集气瓶
(2)实验室用KMnO 制取O ,应选用的发生装置为D(填字母,下同),收集装置可选用 F( 或 G) ,取用KMnO
4 2 4
药品时,应选用仪器A,写出该反应的化学方程式:2KMnO ==== = KMnO + Mn O + O↑。
4 2 4 2 2
(3)注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加水至淹没漏斗下端管口处。
②将注射器C连接到装置E的导管口处。
③缓慢拉动注射器C的活塞,观察到松开手后活塞位置复原,表示装置E的气密性良好。
(4)实验室用装置E制取CO 时,如用注射器C替换长颈漏斗,优点是节约药品。
2
五、计算题(本大题2小题,共10分)
35.(3分)据报道,“中东呼吸综合征”病毒与“非典”病毒类似,加强自身防护是抵御病毒的重要方法。
过氧乙酸(化学式为CHO)是常用的一种消毒剂。请计算:
2 4 3
(1)过氧乙酸(化学式为CHO)的相对分子质量76;
2 4 3
(2)过氧乙酸中氢、氧两种元素的质量比 1 ∶ 1 2。
36.(7分)某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成 100 g溶液,
将其全部加入到100 g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质
量是195.6 g,将溶液蒸干,得到15.6 g硫酸钠。
计算:(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
解:生成二氧化碳的质量:100 g+100 g-195.6 g=4.4 g
设样品中NaCO 的质量为x,反应的HSO 质量为y,生成NaSO 的质量为z。
2 3 2 4 2 4
NaCO+HSO===NaSO+HO+CO↑
2 3 2 4 2 4 2 2
106 98 142 44
x y z 4.4 g
===
x=10.6 g y=9.8 g z=14.2 g(1)硫酸溶液中溶质的质量分数:×100%=9.8%
(2)原样品的质量:10.6 g+(15.6 g-14.2 g)=12 g
原样品中碳酸钠的质量分数:×100%=88.3%
答:(1)加入的硫酸溶液的溶质质量分数为9.8%;(2)原样品中碳酸钠的质量分数为88.3%。