文档内容
铝的重要化合物
【学习目标】
1、掌握铝的重要化合物[AlO、Al(OH) 、Al3+、AlO、KAl(SO )·12H O]的主要性质及其应用
2 3 3 4 2 2
2、掌握“铝三角”及其转化,熟悉铝的化合物的互滴实验
【主干知识梳理】
一、氧化铝 (Al O)
2 3
1、物理性质:白色固体,难溶于水,熔点很高,是优良耐火材料
2、化学性质:Al O 是典性的两性氧化物,既能与酸,又能与碱反应
2 3
(1)能与酸反应:Al O+6HCl===2AlCl +3HO Al O+6H+===2Al3++3HO
2 3 3 2 2 3 2
(2)能与碱反应:Al O+2NaOH===2NaAlO +HO Al O+2OH—===2AlO —+HO
2 3 2 2 2 3 2 2
两性氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,称为两性氧化物
3、Al O 的制备
2 3
(1)实验室制法:2Al(OH) Al O+3HO
3 2 3 2
(2)工业制法:铝土矿→Al O
2 3
4、主要用途:制造耐火、耐高温器材、工业冶炼铝、可以制作各种宝石
【即学即练1】
1、下列叙述中不正确的是( )
A.氧化铝固体不溶于水,不导电,它是非电解质 B.氧化铝熔点很高,是一种较好的耐火材料
C.氧化铝是一种白色的固体,是冶炼铝的原料 D.铝表面形成的氧化铝薄膜可防止铝被腐蚀
2、下列关于氧化铝的叙述正确的是( )
A.氧化铝与酸、碱都能反应生成铝盐和水 B.氧化铝既是碱性氧化物又是酸性氧化物
C.氧化铝既不是碱性氧化物也不是酸性氧化物 D.氧化铝溶于水可得到氢氧化铝
3、下列说法正确的是( )
A.Al O 难溶于水,不跟水反应,所以它不是Al(OH) 对应的氧化物
2 3 3
B.因为Al O 是金属氧化物,所以它是碱性氧化物
2 3
C.Al O 能跟所有的酸、碱溶液反应
2 3
D.Al O 能跟强的酸、碱溶液反应
2 3
二、氢氧化铝 [Al(OH) ]
3
1、物理性质:白色胶状不溶于水的固体,有较强的吸附性
2、化学性质:Al(OH) 是典型的两性氢氧化物,既能与酸,又能与碱反应
3
(1)能与酸反应:Al(OH) +3HCl===AlCl +3HO Al(OH) +3H+ ===Al3++3HO
3 3 2 3 2
(2)能与碱反应:Al(OH) +NaOH===NaAlO +2HO Al(OH) +OH—===AlO —+2HO
3 2 2 3 2 2
两性氢氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物,称为两性氢氧化物
Al(OH) 的电离方式
3
Al(OH) 电离强度相当微弱,只有加入强酸(或强碱)时,大量H+(或OH-)才
3
能破坏Al(OH) 的电离平衡,使平衡向右(或左)移动,生成铝盐(或偏铝酸
3
与酸和碱反应过程 盐),所以 Al(OH) 既具有碱性,又具有酸性,当加入弱酸或弱碱时,因
3
H+或OH-浓度太小,不能使上述平衡移动,因此 Al(OH) 只溶于强酸或强
3
碱,而不溶于弱酸(H CO 等)、弱碱(NH ·H O)
2 3 3 2
强酸或强碱也是相对而言的,Al(OH) 不溶于HCO 、NH ·HO,但溶于
微点拨 3 2 3 3 2
CH COOH
3
(3)热稳定性差:2Al(OH) Al O+3HO
3 2 3 2
3、用途
(1)Al(OH) 有较强的吸附性,能凝聚水中悬浮物,又能吸附色素,可以用作净水剂
3
(2)Al(OH) 碱性不强,不至于对胃壁产生强烈的刺激作用或腐蚀作用,却可以与酸反应,起到中和胃酸的作用,
3可以用作胃酸中和剂
4、有关Al(OH) 的少量、过量问题
3
(1)NaOH和AlCl3
化学方程式 离子方程式
NaOH少量 AlCl +3NaOH(少量)===Al(OH) ↓+3NaCl Al3++3OH-===Al(OH) ↓
3 3 3
过渡反应 Al(OH) +NaOH===NaAlO +2HO Al(OH) +OH—===AlO —+2HO
3 2 2 3 2 2
NaOH过量 AlCl +4NaOH(过量)===NaAlO +3NaCl+2HO Al3++4OH—===AlO -+2HO
3 2 2 2 2
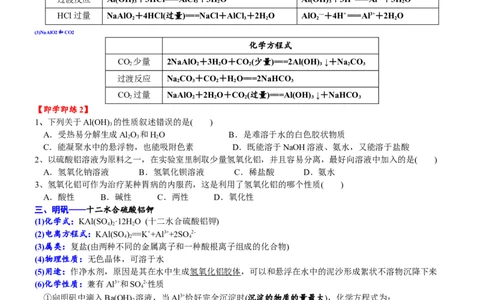
(2)NaAlO2和HCl
化学方程式 离子方程式
HCl少量 NaAlO +HCl(少量)+HO===Al(OH) ↓+NaCl AlO —+H+ +HO===Al(OH) ↓
2 2 3 2 2 3
过渡反应 Al(OH) +3HCl===AlCl +3HO Al(OH) +3H+ ===Al3++3HO
3 3 2 3 2
HCl过量 NaAlO +4HCl(过量)===NaCl+AlCl +2HO AlO —+4H+ ===Al3++2HO
2 3 2 2 2
(3)NaAlO2和CO2
化学方程式
CO 少量 2NaAlO +3HO+CO (少量)===2Al(OH) ↓+Na CO
2 2 2 2 3 2 3
过渡反应 Na CO +CO +HO===2NaHCO
2 3 2 2 3
CO 过量 NaAlO +2HO+CO (过量)===Al(OH) ↓+NaHCO
2 2 2 2 3 3
【即学即练2】
1、下列关于Al(OH) 的性质叙述错误的是( )
3
A.受热易分解生成Al O 和HO B.是难溶于水的白色胶状物质
2 3 2
C.能凝聚水中的悬浮物,也能吸附色素 D.既能溶于NaOH溶液、氨水,又能溶于盐酸
2、以硫酸铝溶液为原料之一,在实验室里制取少量氢氧化铝,并且容易分离,最好向溶液中加入的是( )
A.氢氧化钠溶液 B.氢氧化钡溶液 C.稀盐酸 D.氨水
3、氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的哪个性质( )
A.酸性 B.碱性 C.两性 D.氧化性
三、明矾——十二水合硫酸铝钾
(1)化学式:KAl(SO )·12H O (十二水合硫酸铝钾)
4 2 2
(2)电离方程式:KAl(SO )==K++Al3++2SO2-
4 2 4
(3)属类:复盐(由两种不同的金属离子和一种酸根离子组成的化合物)
(4)物理性质:无色晶体,可溶于水
(5)用途:作净水剂,原因是其在水中生成氢氧化铝胶体,可以和悬浮在水中的泥沙形成絮状不溶物沉降下来
(6)化学性质:兼有Al3+和SO 2-性质
4
①向明矾中滴入Ba(OH) 溶液,当Al3+恰好完全沉淀时(沉淀的物质的量最大),化学方程式为:
2
______________________________________________________________________________
②向明矾中滴入Ba(OH) 溶液,当SO 2-完全沉淀时(沉淀的质量最大),化学方程式为:
2 4
_________________________________________________________________________________
【即学即练3】
1、关于明矾的下列说法错误的是( )
A.明矾的化学式为KAl(SO ) B.明矾是纯净物
4 2
C.明矾中存在K+和Al3+两种阳离子 D.明矾是一种复盐
2、明矾是一种净水剂,明矾净水的原理是( )
A.Al3+有较强的吸附性 B.Al3+与悬浮物生成沉淀
C.Al3+与水反应生成的氢氧化铝胶体,具有吸附性 D.明矾难溶于水
四、互滴实验 (试剂的滴加顺序不同而产生的现象不同)
1、NaOH和AlCl
3(1)向AlCl 溶液中逐滴加入NaOH溶液 (开始时NaOH不足)
3
先:AlCl +3NaOH===Al(OH) ↓+3NaCl 产生白色沉淀
3 3
后:Al(OH) +NaOH===NaAlO +2HO 沉淀溶解
3 2 2
现象:先产生白色沉淀后沉淀消失
(2)向NaOH溶液中逐滴加入AlCl 溶液 (开始时NaOH过量)
3
先:AlCl +4NaOH===NaAlO +3NaCl+2HO 无白色沉淀产生
3 2 2
后:3NaAlO +AlCl +6HO===4Al(OH) ↓+3NaCl 产生白色沉淀
2 3 2 3
现象:开始无现象后出现白色沉淀
2、NaAlO 和盐酸
2
(1)向NaAlO 溶液中逐滴加入盐酸
2
先:NaAlO +HCl+HO===Al(OH) ↓+NaCl 产生白色沉淀
2 2 3
后:Al(OH) +3HCl===AlCl +3HO 沉淀溶解
3 3 2
现象:先产生白色沉淀后沉淀消失
(2)向盐酸中逐滴加入NaAlO 溶液
2
先:NaAlO +4HCl===NaCl+AlCl +2HO 无白色沉淀产生
2 3 2
后:3NaAlO +AlCl +6HO===4Al(OH) ↓+3NaCl 产生白色沉淀
2 3 2 3
现象:开始无现象后出现白色沉淀
3、Na CO 溶液与盐酸
2 3
(1)向Na CO 溶液中逐滴加入盐酸 (开始时酸不足)
2 3
先:NaCO+HCl===NaHCO+NaCl 无气体产生
2 3 3
后:NaHCO +HCl===NaCl+HO+CO↑ 有气体产生
3 2 2
现象:刚开始无气泡产生,盐酸滴加到一定量后,有气泡产生
(2)向盐酸中逐滴加入Na CO 溶液 (开始时酸过量)
2 3
2HCl+NaCO===2NaCl+CO↑+HO
2 3 2 2
现象:立即产生大量的气泡
【即学即练4】
1、(多选)下列各组物质的无色溶液,不用其他试剂即可鉴别的是( )
A.NaOH、AlCl B.NaHCO 、HSO C.NaAlO 、NaHSO
3 3 2 4 2 4
D.NaCO、HCl E.NaCO、NaHCO 、Ca(OH)
2 3 2 3 3 2
2、(多选)下列各组溶液中,只用试管和胶头滴管,不用其他任何试剂就可以鉴别的是( )
A.KOH和Al (SO ) B.稀盐酸和NaCO
2 4 3 2 3
C.CaCl 和NaCO D.Ba(OH) 和NaHSO
2 2 3 2 4
3、下列各组物质,前者逐滴滴加到后者中直至过量,先出现白色沉淀,后来沉淀又消失的是( )
A.HSO 滴入NaAlO 溶液中 B.Ba(OH) 溶液滴入Al (SO ) 溶液中
2 4 2 2 2 4 3
C.Al (SO ) 溶液滴入NaOH溶液中 D.氨水滴入Al (SO ) 溶液中
2 4 3 2 4 3
4、下列各项操作中符合“先出现沉淀后沉淀完全溶解”现象的有几组( )
①向饱和碳酸钠溶液中通入CO 至过量 ②向Fe(OH) 胶体中逐滴滴加稀HSO 至过量
2 3 2 4
③向BaCl 溶液中通入CO 至过量 ④向澄清石灰水中逐渐通入CO 至过量
2 2 2
⑤向Al (SO ) 溶液中逐滴滴加Ba(OH) 至过量 ⑥向NaAlO 溶液中逐滴滴加盐酸至过量
2 4 3 2 2
⑦向NaAlO 溶液中逐渐通入CO 至过量 ⑧向NaOH溶液中逐滴滴加AlCl 至过量
2 2 3
A.2 B.3 C.4 D.5
五、“铝三角”的转化关系及其应用
1、Al3+、Al(OH) 、AlO之间的转化关系
3
Al3+→Al(OH) ①Al3++3NH ·H O===Al(OH) ↓+3NH
3 3 2 3②Al3++3AlO+6HO===4Al(OH) ↓
2 3
③Al3++3OH-===Al(OH) ↓
3
Al(OH) →Al3+ Al(OH) +3H+===Al3++3HO
3 3 2
Al3+ →AlO Al3++4OH-===AlO+2HO
2
AlO→Al3+ AlO+4H+===Al3++2HO
2
①AlO+CO+2HO===Al(OH) ↓+HCO(CO 过量)
2 2 3 2
AlO→Al(OH)
3
②AlO+H++HO===Al(OH) ↓
2 3
Al(OH) →AlO Al(OH) +OH-===AlO+2HO
3 3 2
2、“铝三角”转化的应用
(1)选择制备Al(OH) 的最佳途径
3
①向铝盐中加入足量氨水,离子方程式为:Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②向偏铝酸盐中通入足量CO,离子方程式为:AlO+CO+2HO===Al(OH) ↓+HCO
2 2 2 3
③NaAlO 与AlCl 的溶液混合,离子方程式为:3AlO+Al3++6HO===4Al(OH) ↓
2 3 2 3
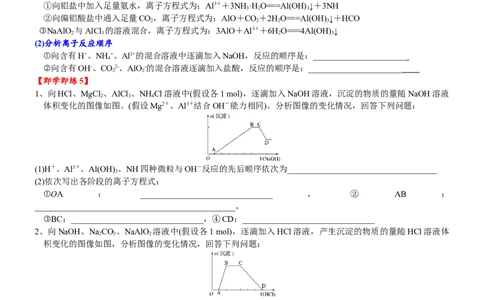
(2)分析离子反应顺序
①向含有H+、NH +、Al3+的混合溶液中逐滴加入NaOH,反应的顺序是:______________________
4
②向含有OH-、CO2-、AlO-的混合溶液逐滴加入盐酸,反应的顺序是:______________________
3 2
【即学即练5】
1、向HCl、MgCl 、AlCl 、NH Cl溶液中(假设各1 mol),逐滴加入NaOH溶液,沉淀的物质的量随NaOH溶液
2 3 4
体积变化的图像如图。(假设Mg2+、Al3+结合OH-能力相同)。分析图像的变化情况,回答下列问题:
(1)H+、Al3+、Al(OH) 、NH四种微粒与OH-反应的先后顺序依次为___________________________________
3
(2)依次写出各阶段的离子方程式:
①OA : _______________________________ , ② AB :
_______________________________________________,
③BC:_______________________________,④CD:_______________________________
2、向NaOH、NaCO 、NaAlO 溶液中(假设各1 mol),逐滴加入HCl溶液,产生沉淀的物质的量随HCl溶液体
2 3 2
积变化的图像如图,分析图像的变化情况,回答下列问题:
(1)OH-、CO、HCO、AlO、Al(OH) 这五种微粒与H+反应的先后顺序依次为_____________________
3
(2)依次写出各阶段的离子方程式:
①OA:_______________________________,②AB:_______________________________,
③BC:_____________________________________________,④CD:_______________________________
3、由Al3+―→Al(OH) ―→AlO―→―→Al3+系列变化中,中应填写的是( )
3
A.Al(OH) B.AlCl C.HCl D.NaOH
3 3
4、实验室制备Al(OH) 沉淀,最适宜的方法是( )
3
A.AlCl 溶液中加入NaOH溶液 B.AlCl 溶液中加入足量的氨水
3 3
C.NaAlO 溶液中加入浓盐酸 D.Al O 溶于足量的热水中
2 2 3
六、既能与强酸反应又能与强碱反应的物质
(1)某些单质:Al、Be、Zn、S、Si
(2)两性氧化物:Al O、BeO、ZnO
2 3(3)两性氢氧化物:Al(OH) 、Be(OH) 、Zn(OH)
3 2 2
(4)弱酸的铵盐:CH COONH
3 4
(5)多弱酸的酸式盐:NaHCO 、KHS、KHSO 、NaH PO
3 3 2 4
(6)某些酸:HS、浓HSO
2 2 4
(7)蛋白质、氨基酸
【即学即练6】
1、按要求填空。①NaHSO ②Al O ③Al(OH) ④(NH )CO ⑤CHCOONH ⑥NaHCO ⑦Al
3 2 3 3 4 2 3 3 4 3
(1)在以上物质中,既能与强酸反应,又能与强碱反应的是________
(2)属于两性化合物的是________
2、下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO ②(NH )SO ③Al O ④Al(OH) ⑤Al ⑥NaHSO ⑦AlCl ⑧NaSiO
3 4 2 3 2 3 3 4 3 2 3
A.全部 B.①②③④⑤ C.③④⑤⑥⑦ D.②③④⑤⑧
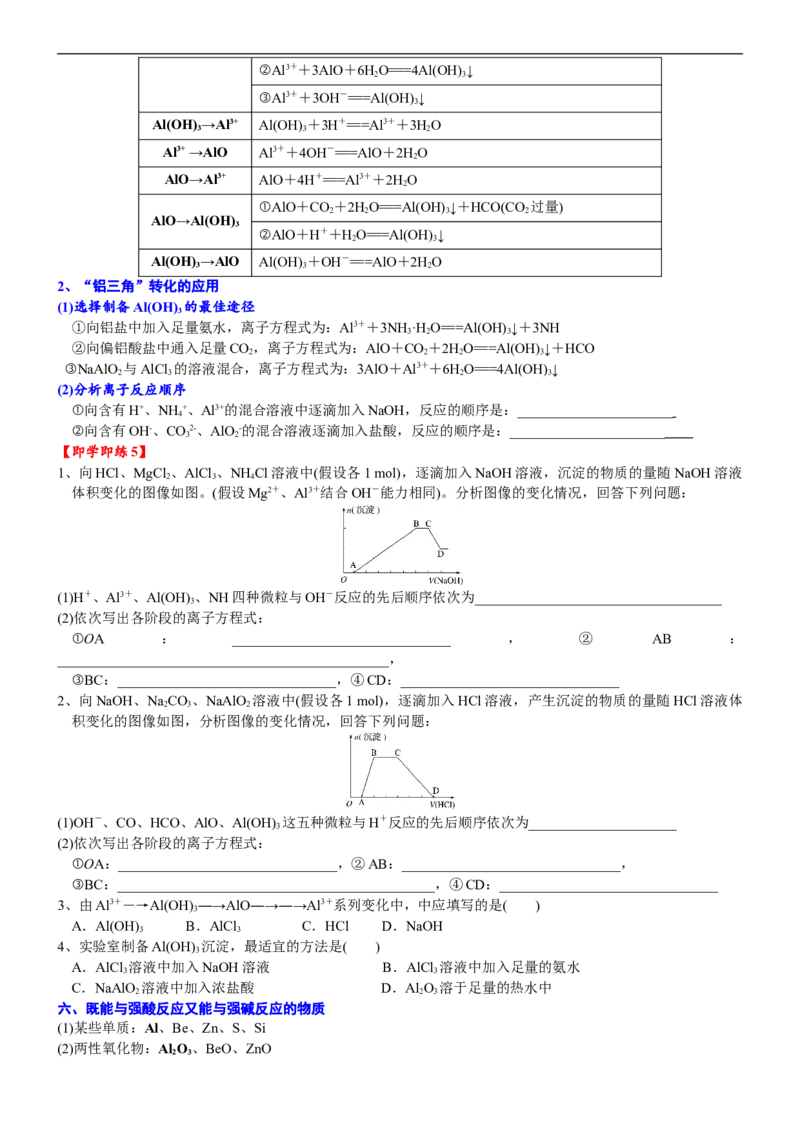
七、工业炼铝的流程
铝是地壳中含量最多的金属元素,在自然界主要以化合态形式存在于氧化铝中。铝土矿的主要成分是
Al O ,此外还含有少量SiO 、Fe O 、MgO等杂质,冶炼金属铝很重要的一个过程是Al O 的提纯。由于Al O
2 3 2 2 3 2 3 2 3
是两性氧化物,而杂质SiO 是酸性氧化物,Fe O、MgO是碱性氧化物,因而可设计出两种提纯氧化铝的方案
2 2 3
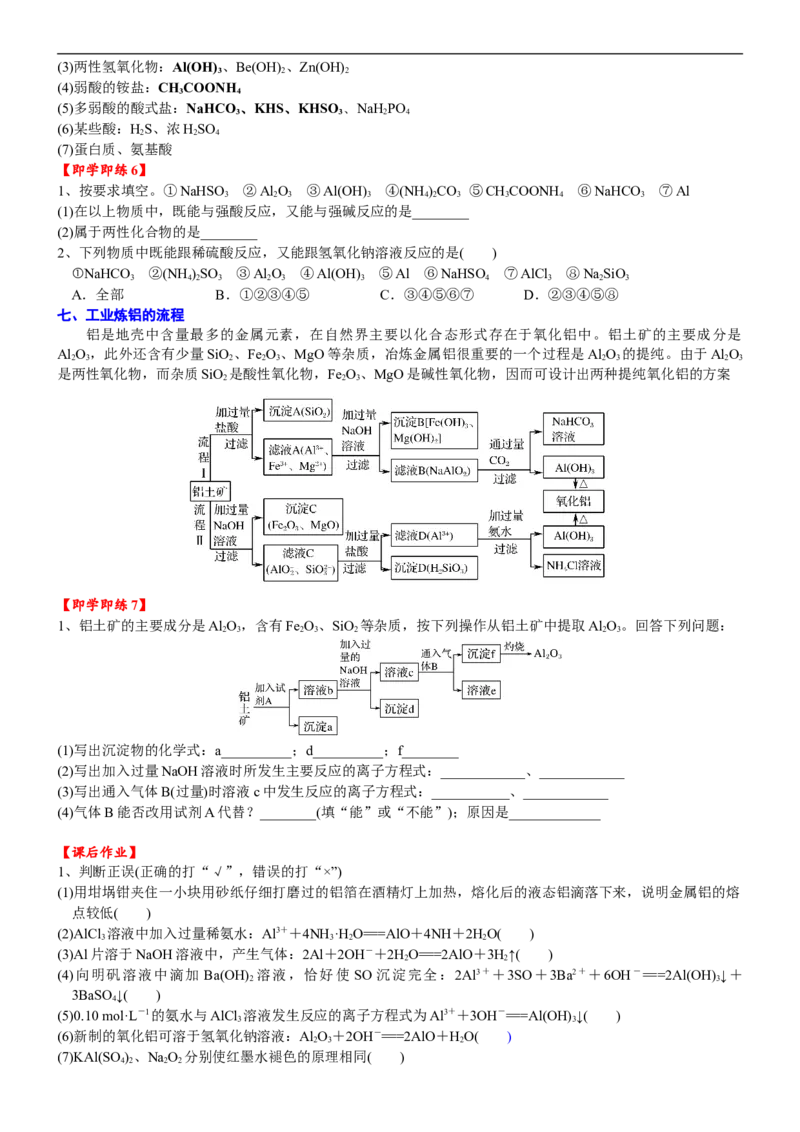
【即学即练7】
1、铝土矿的主要成分是Al O,含有Fe O、SiO 等杂质,按下列操作从铝土矿中提取Al O。回答下列问题:
2 3 2 3 2 2 3
(1)写出沉淀物的化学式:a__________;d__________;f________
(2)写出加入过量NaOH溶液时所发生主要反应的离子方程式:____________、____________
(3)写出通入气体B(过量)时溶液c中发生反应的离子方程式:___________、____________
(4)气体B能否改用试剂A代替?________(填“能”或“不能”);原因是_____________
【课后作业】
1、判断正误(正确的打“√”,错误的打“×”)
(1)用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,说明金属铝的熔
点较低( )
(2)AlCl 溶液中加入过量稀氨水:Al3++4NH ·H O===AlO+4NH+2HO( )
3 3 2 2
(3)Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2HO===2AlO+3H↑( )
2 2
(4)向明矾溶液中滴加 Ba(OH) 溶液,恰好使 SO 沉淀完全:2Al3++3SO+3Ba2++6OH-===2Al(OH) ↓+
2 3
3BaSO↓( )
4
(5)0.10 mol·L-1的氨水与AlCl 溶液发生反应的离子方程式为Al3++3OH-===Al(OH) ↓( )
3 3
(6)新制的氧化铝可溶于氢氧化钠溶液:Al O+2OH-===2AlO+HO( )
2 3 2
(7)KAl(SO)、NaO 分别使红墨水褪色的原理相同( )
4 2 2 22、列说法中正确的是( )
A.Al O 和MgO均可与NaOH溶液反应
2 3
B.向Al (SO ) 溶液中加入过量NH ·H O:Al3++4NH ·H O===AlO+2HO+4NH
2 4 3 3 2 3 2 2
C.制备Al(OH) 悬浊液:向1 mol·L-1AlCl 溶液中加过量的6 mol·L-1 NaOH溶液
3 3
D.用CO 鉴别NaAlO 溶液和CHCOONa溶液
2 2 3
3、某氧化物X难溶于水,能与烧碱反应,生成易溶于水的化合物Y,将少量Y溶液滴入盐酸中无沉淀生成,
则X是( )
A.SiO B.Al O C.MgO D.CuO
2 2 3
4、氧化铝用来制造耐火坩埚、耐火管和耐高温的实验仪器,是利用了氧化铝( )
A.不溶于水 B.熔点很高 C.是金属氧化物 D.高温下很难反应
5、氧化铝是铝土矿的主要成分,氧化铝属于( )
A.碱性氧化物 B.酸性氧化物 C.两性氧化物 D.混合物
6、氢氧化铝受热易分解,产生水并吸收热量,可用作阻燃剂;氢氧化铝能与盐酸、氢氧化钠溶液反应,是药物
“胃舒平”的主要成分之一。下列判断不正确的是( )
A.氢氧化铝具有很好的热稳定性 B.复方胃舒平可用于治疗胃酸过多
C.氢氧化铝灭火的原因之一是降低了可燃物的温度 D.氢氧化铝是一种两性氢氧化物
7、下列变化不可能通过一步实验直接完成的是( )
A.Al(OH) ―→Al O B.Al O―→Al(OH)
3 2 3 2 3 3
C.Al―→AlO D.Al3+―→Al(OH)
3
8、下列关于明矾的说法不正确的是( )
A.化学式为KAl(SO )·12H O B.属于混合物 C.是一种硫酸盐 D.水溶液能导电
4 2 2
9、下列有关物质的性质与其应用不对应的是( )
A.MgO、Al O 的熔点很高,可制作耐高温材料
2 3
B.NaHCO 能与碱反应,食品工业上用作焙制糕点的膨松剂
3
C.Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
D.利用钠蒸气放电发光的性质制造的高压钠灯,可发出射程远、透雾能力强的黄光,航空、航海常用高压
钠
灯作指示灯
10、下列有关说法中不正确的是( )
A.Al(OH) 在用于治疗胃酸过多类疾病时表现出弱碱性
3
B.明矾溶于水后可得到少量的有强吸附性的Al(OH) ,故明矾可作净水剂
3
C.Al(OH) 可用于中和馒头制作过程(如发酵阶段)中产生的酸
3
D.Al O 可用于制作耐火材料而Al(OH) 不能
2 3 3
11、(多选)下列各项操作中,能出现“先产生沉淀,然后沉淀又溶解”现象的是( )
A.向饱和碳酸钠溶液中通入过量的CO B.向NaAlO 溶液中逐滴加入过量的稀盐酸
2 2
C.向AlCl 溶液中逐滴加入过量稀氢氧化钠溶液 D.向硅酸钠溶液中逐滴加入过量的盐酸
3
12、下列除杂质的方法不正确的是( )
A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.FeCl 溶液中混有少量AlCl :加入过量的氨水,过滤洗涤沉淀,将沉淀再用适量盐酸溶解
3 3
C.Fe O 中混有少量Al O:加入过量NaOH溶液充分反应,过滤、洗涤、干燥
2 3 2 3
D.Al(OH) 中混有少量Mg(OH) :加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO 后过滤
3 2 2
13、下列除去杂质的方法不正确的是( )
A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.用过量氨水除去Fe3+溶液中的少量Al3+
C.Al(OH) 中混有少量Mg(OH) :加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO 后过滤
3 2 2
D.MgO中混有少量Al O:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO
2 3
14、探究氢氧化铝的两性,最适宜的试剂是( )
A.Al、NaOH溶液、稀盐酸 B.Al O、氨水、稀盐酸
2 3C.Al (SO ) 溶液、NaOH溶液、稀盐酸 D.AlCl 溶液、氨水、稀盐酸
2 4 3 3
15、列叙述中正确的是( )
A.依据铝热反应原理,能发生反应2Al+3MgO=====3Mg+Al O
2 3
B.在加入铝粉能放出氢气的溶液中,K+、NH、CO、Cl-一定能够大量共存
C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液
D.氯化铝溶液中加入过量氨水反应实质是:Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
16、向1.0 mol·L-1的甲溶液中逐滴加入1.0 mol·L-1的乙溶液至过量,产生氢氧化铝沉淀的质量与加入的乙溶液
的体积关系如图所示。符合图中关系的是下列各组溶液中的( )
A.甲为氯化铝,乙为氢氧化钠 B.甲为氢氧化钠,乙为氯化铝
C.甲为偏铝酸钠,乙为盐酸 D.甲为氯化铝,乙为氨水
17、现有Al、Cl 、Al O 、HCl(aq)、Al(OH) 、NaOH(aq)6种物质,它们之间有如图所示转化关系,图中每条线
2 2 3 3
两端的物质之间都可以发生反应,下列推断不合理的是( )
A.N一定是HCl(aq) B.X可能为Al或Cl
2
C.Y一定为NaOH(aq) D.Q、Z中的一种必定为Al O
2 3
18、工业上用某种氧化铝矿石(含Fe O 杂质)为原料冶炼铝的工艺流程如下,对上述流程中的判断正确的是(
2 3
)
A.试剂X可以为氨水,沉淀中含有铁的化合物
B.CO 可以用HSO 溶液或稀盐酸代替
2 2 4
C.反应Ⅱ中的离子方程式为CO+Al(OH) ]-===Al(OH) ↓+HCO
2 4 3
D.工业上还可采用Fe还原Al O 的方法制Al,成本更低
2 3
19、用含少量镁粉的铝粉制取纯净的氢氧化铝,下列操作步骤中最恰当的组合是( )
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量CO 生成Al(OH) 沉淀
2 3
⑤加入盐酸生成Al(OH) 沉淀 ⑥加入过量烧碱溶液
3
A.①⑥⑤③ B.②③④③ C.②③⑤③ D.①③⑤③
20、相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )
A.Al B.Al(OH) C.AlCl D.Al O
3 3 2 3
21、A、B、C、D、E五种化合物均含有某种短周期(前18号元素)常见元素,它们的转化关系如图所示,其中A
的溶液为澄清溶液,C为难溶的白色固体,E则易溶于水,取A的溶液灼烧,焰色反应为浅紫色(透过蓝色钴
玻璃)(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B:______________________________________________;
A→D:______________________________________________
22、已知A为金属单质,如图所示流程中的各步反应的最后生成物E是白色沉淀。
(1)请写出其化学式:A________、C________
(2)写出下列各步反应的离子方程式。
②_______________________________________________;
④_______________________________________________;
⑤_______________________________________________
23、从铝土矿(主要成分为Al O,还有少量杂质)中提取铝的工艺流程及步骤如下:
2 3
试回答下列问题:
(1)试剂X为________
(2)操作Ⅰ、操作Ⅱ均为________(填操作名称),在实验室进行该操作时需要的玻璃仪器有___________________
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应,该反应的化学方程式为____________________________,
请举一例该反应的用途________________
(4)反应Ⅱ的离子方程式为___________________________________________________________
(5)电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是________ g
【铝的重要化合物】答案
【即学即练1】
1、A。解析:氧化铝熔点很高,常用来制造耐火坩埚、耐火管和耐高温的实验仪器;工业上常用电解熔融氧化
铝来制取金属铝。
2、C。解析:氧化铝既不是碱性氧化物也不是酸性氧化物,而是一种两性氧化物;能与酸反应生成铝盐和水,
能与碱溶液反应生成偏铝酸盐和水;氧化铝难溶于水,不能与水反应生成氢氧化铝。
3、D。解析:Al O 虽然难溶于水,但是2Al(OH) Al O +3HO,Al O 和Al(OH) 中Al的化合价相同,所
2 3 3 2 3 2 2 3 3
以Al O 是Al(OH) 对应的氧化物;金属氧化物与碱性氧化物是两个不同的概念,二者没有必然的联系;Al O
2 3 3 2 3
是两性氧化物;Al O 与酸、强碱溶液反应,与弱碱溶液不反应。
2 3
【即学即练2】
1、D。解析:Al(OH) 是两性氢氧化物,能溶于酸,也能溶于NaOH、KOH等强碱,但Al(OH) 不能溶于氨水
3 3等弱碱。
2、D。解析:氢氧化铝能溶于强碱溶液,但不能溶于氨水,因此在实验室里制取少量氢氧化铝,最好向硫酸铝
溶液中加入氨水。
3、B。解析:氢氧化铝可与胃酸反应,表现出了碱性。
【即学即练3】
1、A。解析:明矾的化学式为KAl(SO )·12H O,是纯净物,明矾在水溶液中电离出K+、Al3+两种阳离子和SO
4 2 2
一种阴离子,明矾属于复盐。
3、C
【即学即练4】
1、ACD。解析:都使用互滴法,两次操作应产生不同的现象。A向含Al3+的溶液中滴加NaOH溶液:先生成
白色沉淀,后沉淀又逐渐溶解;向NaOH溶液中滴加含Al3+的溶液:开始无沉淀产生,后产生白色沉淀,且沉
淀不溶解。两次现象不同,可以鉴别。B不论是NaHCO 滴入HSO 中还是HSO 滴入NaHCO 中都会立即产生
3 2 4 2 4 3
气泡,现象相同,无法鉴别。CNaHSO===Na++H++SO,溶液显强酸性。向NaAlO 溶液中滴加NaHSO :开
4 2 4
始出现白色沉淀后沉淀逐渐溶解;向NaHSO 溶液中滴加NaAlO 溶液:开始无现象,后出现白色沉淀。现象不
4 2
同,可以鉴别。D向NaCO 溶液中滴加盐酸:开始无现象,后产生气泡;向盐酸中滴加NaCO 溶液:立即产
2 3 2 3
生气泡。现象不同,可以鉴别。E无论是NaHCO 还是NaCO 加到Ca(OH) 中都会产生白色沉淀,无法鉴别。
3 2 3 2
2、AB
3、A
4、B。解析:①相同条件下,碳酸氢钠的溶解度比碳酸钠的小,则向饱和碳酸钠溶液中通入CO 至过量,有晶
2
体析出,不符合;③盐酸的酸性比碳酸的酸性强,则向BaCl 溶液中通入CO 至过量,不发生反应,不符合;
2 2
⑤向Al (SO ) 溶液中逐滴滴加Ba(OH) 至过量,开始反应生成硫酸钡、氢氧化铝沉淀,后碱过量时氢氧化铝溶
2 4 3 2
解,最后还存在硫酸钡沉淀,不符合;⑦向NaAlO 溶液中逐渐通入CO 至过量生成氢氧化铝沉淀,沉淀不会溶
2 2
解,不符合;⑧向NaOH溶液中逐滴滴加AlCl 至过量,开始阶段氢氧化钠过量,不会产生沉淀,后出现氢氧化
3
铝沉淀,不符合;答案选B。
【即学即练5】
1、(1)H+、Al3+、NH、Al(OH)
3
(2)①H++OH-===H O
2
②Al3++3OH-===Al(OH) ↓,Mg2++2OH-===Mg(OH) ↓
3 2
③NH+OH-===NH·HO
3 2
④Al(OH) +OH-===AlO+2HO
3 2
2、(1)OH-、AlO、CO、HCO、Al(OH)
3
(2)①OH-+H+===H O
2
②AlO+H++HO===Al(OH) ↓
2 3
③CO+H+===HCO,HCO+H+===CO↑+HO
2 2
④Al(OH) +3H+===Al3++3HO
3 2
3、A。解析:由Al3+转化为AlO需要通过Al(OH) ,同样由AlO转化为Al3+,也需要通过Al(OH) ,在AlO中
3 3
加入强酸,先生成Al(OH) ,再加强酸,Al(OH) 转化为Al3+。
3 3
4、B。解析:A项,氢氧化钠过量时会生成偏铝酸钠,错误;B项,氨水过量,生成的氢氧化铝不会溶解,正
确;C项,盐酸过量时生成的氢氧化铝会溶解,错误;D项,氧化铝不与水反应,错误。
【即学即练6】
1、(1)①②③④⑤⑥⑦ (2)②③
2、B
【即学即练7】
1、(1)SiO Fe(OH) Al(OH)
2 3 3
(2)Al3++4OH-===[Al(OH) ]- Fe3++3OH-===Fe(OH) ↓
4 3
(3)CO+Al(OH) ]-===Al(OH) ↓+HCO CO +OH-===HCO
2 4 3 2
(4)不能 生成的氢氧化铝能够溶于强酸
解析 (1)根据流程图可知沉淀a为SiO,沉淀b为Fe(OH) ,沉淀f为Al(OH) 。
2 3 3
(2)溶液b中含有铁离子和铝离子,加入过量氢氧化钠溶液后反应的离子方程式为Al3++4OH-===Al(OH) ]-,Fe3
4++3OH-===Fe(OH) ↓。
3
(3)根据流程图可知,溶液c中含有氢氧化钠和偏铝酸根,Na[Al(OH) ]]溶液与过量的CO 反应生成Al(OH) 沉
4 2 3
淀,反应的离子方程式为CO+[Al(OH) ]-===Al(OH) ↓+HCO,过量的CO 与OH-反应生成HCO,反应的离
2 4 3 2
子方程式为CO+OH-===HCO。
2
(4)气体B为二氧化碳,试剂A为强酸,氢氧化铝能与过量的强酸反应而溶解,无法控制加入酸的量。
【课后作业】
1、(1)× (2)× (3)√ (4)× (5)× (6)√ (7)×
2、D。解析:A项中MgO与NaOH溶液不反应,A不正确。Al(OH) 不溶于氨水,B项离子方程式书写错误,
3
应为Al3++3NH ·H O===Al(OH) ↓+3NH。Al(OH) 溶于过量的NaOH溶液,C项不正确。D项中CO 通入到
3 2 3 3 2
NaAlO 溶液中可产生白色沉淀,通入到CHCOONa溶液中没有明显现象,故可鉴别二者,D项正确。
2 3
3、B
4、B。解析:氧化铝熔点很高,是一种较好的耐火材料,常用来制造耐火坩埚、耐火管和耐高温的实验仪器。
5、C。解析:氧化铝既能与酸反应又能与碱反应均生成盐和水,属于两性氧化物。
6、A。解析:氢氧化铝很不稳定,受热易分解,产生水并吸收热量,能降低可燃物的温度,可用于灭火;氢氧
化铝具有两性,能与盐酸、氢氧化钠溶液反应;“胃舒平”中含有氢氧化铝,可用于治疗胃酸过多。
7、B。解析:Al(OH) 加热分解可直接得Al O ,Al与强碱溶液反应可得AlO,Al3+遇弱碱可直接得Al(OH) ,
3 2 3 3
Al O 难溶于水,不能通过一步反应得Al(OH) ,应将Al O 与酸或碱反应得Al3+或AlO,再与碱或酸反应,才能
2 3 3 2 3
得Al(OH) 。
3
8、B。解析:明矾为纯净物,属于复盐或硫酸盐,在水溶液中电离出 K+、Al3+两种阳离子和SO一种阴离子,
其水溶液能导电。
9、B。解析:MgO、Al O 的熔点很高,故可制作耐高温材料,A项正确;在食品工业上用作焙制糕点的膨松剂
2 3
是因为NaHCO 不稳定,受热容易分解:2NaHCO NaCO+CO↑+HO,产生的CO 气体使糕点松软、
3 3 2 3 2 2 2
多孔,B项错误;金属Al具有良好的延展性,由于在空气中能与氧气发生反应生成一层致密的氧化物薄膜,对
内层的金属起到了保护作用,因此有良好的抗腐蚀性,所以可制成铝箔包装物品,C项正确;钠蒸气放电可以
发出透雾能力强的黄光,由于黄色的光波长,射程远,故高压钠灯可以作航空、航海的指示灯,D项正确。
10、C。解析:治疗胃酸过多时要消耗胃中的酸,因此Al(OH) 表现出弱碱性,A项正确;Al(OH) 有强吸附性,
3 3
能吸附水中悬浮的杂质并最终转化为沉淀而使水变澄清,B项正确;馒头制作过程中加小苏打是用于发泡和中
和酸的,不用Al(OH) ,因其不能与弱酸反应,C项错误;耐火材料本身具有热稳定性且熔点很高,而 Al(OH)
3 3
受热易分解,D项正确。
11、BC。解析:A中NaCO 与CO、HO反应生成NaHCO ,由于NaCO 的溶解度比NaHCO 的大,因而只会
2 3 2 2 3 2 3 3
产生沉淀;BNaAlO 中加入稀盐酸,开始时产生白色沉淀Al(OH) ,当盐酸过量时,Al(OH) 又溶于盐酸;C向
2 3 3
AlCl 溶液中加入NaOH溶液,开始时产生白色沉淀Al(OH) ,当NaOH过量时,Al(OH) 又溶于NaOH;D只会
3 3 3
生成HSiO 沉淀。
2 3
12、B [B项,加入过量氨水,Fe3+、Al3+均沉淀且均不溶于氨水,无法除去杂质。
13、B。解析:Al(OH) 不溶于氨水,故向含少量Al3+的Fe3+溶液中加入过量氨水时,Fe3+、Al3+均转化为氢氧
3
化物沉淀,达不到除杂的目的。
14、C。解析:可溶性的铝盐Al (SO ) 溶液与少量NaOH溶液反应生成氢氧化铝沉淀,继续加过量的氢氧化钠,
2 4 3
氢氧化铝沉淀会溶解,氢氧化铝沉淀中加盐酸也会溶解。
15、D。解析:铝热反应的原理:Al与活动性比其差的金属氧化物发生置换反应,Mg的活动性强于铝,故Al
与MgO不能反应,故A错误;加入铝粉产生H 的溶液中,可能存在H+或OH-,NH与OH-不能大量共存,
2
CO与H+不能大量共存,故B错误;镁铝合金可溶于过量盐酸,但 Mg不与NaOH反应,故不能完全溶于
NaOH溶液,故C错误;Al(OH) 不溶于氨水,只溶于强碱,故D正确。
3
16、D。解析:向AlCl 溶液中逐滴加入NaOH溶液,先产生沉淀,后沉淀溶解,A项不符合图中关系;向
3
NaOH溶液中逐滴加入AlCl 溶液,开始无沉淀,B项不符合图中关系;向NaAlO 溶液中逐滴加入盐酸,先产
3 2
生沉淀,后沉淀溶解,C项不符合图中关系;向AlCl 溶液中逐滴加入氨水,产生沉淀,继续加入氨水沉淀不溶
3
解,D项符合图中关系。
17、B。解析:由题图可知Y为NaOH(aq),N一定是HCl(aq),M为Al。
18、C。解析:A项,试剂X应为强碱溶液,使Al O 溶解;B项,若用强酸代替CO ,强酸过量时,Al(OH)
2 3 2 3
会溶解,不能生成Al(OH) 沉淀;D项,因Al比Fe活泼,不能用Fe置换Al。
319、B。解析:若先加盐酸,Mg、Al均溶解,制取Al(OH) 的步骤较多;从NaAlO 制备Al(OH) ,加盐酸不容
3 2 3
易控制量的多少,故B项操作步骤为最佳顺序。
20、A。解析:根据题设要求所发生的反应及Na原子守恒,有:n(NaOH)=n(Na+),Al→NaAlO →NaOH,
2
Al(OH) →NaAlO →NaOH,AlCl →(NaAlO +3NaCl)→4NaOH,Al O→2NaAlO →2NaOH。设4种固体的质量
3 2 3 2 2 3 2
均为m,则消耗碱的物质的量分别为m/27 mol,m/78 mol,m/33.375 mol,m/51 mol,可知选项A正确。
21、(1)KAlO Al(OH) Al O AlCl NaAlO
2 3 2 3 3 2
(2)AlO+2HO+CO ===Al(OH) ↓+HCO AlO+4H+===Al3++2HO
2 2 3 2
解析:在短周期元素形成的化合物中,既能与盐酸反应,又能与 NaOH溶液反应的物质必为两性物质,又因为
B受热时转化为C,故可知C为Al O ,B为Al(OH) ,由此推出D是AlCl ,A与过量CO 反应生成Al(OH) ,
2 3 3 3 2 3
且A的溶液的焰色反应为浅紫色,则A为KAlO ,E为NaAlO 。
2 2
22、(1)Al NaAlO
2
(2)②2Al+2OH-+2HO===2AlO+3H↑
2 2
④Al3++3NH ·HO===Al(OH) ↓+3NH
3 2 3
⑤AlO+CO +2HO===Al(OH) ↓+HCO
2 2 3
解析:根据题中各物质转化关系,A为金属单质,能与氢氧化钠反应生成C,C又与过量的二氧化碳反应生成
E,可以确定 A为Al,结合图中各物质反应条件可推知 D为Al (SO ) ,C为NaAlO ,E为Al(OH) ,B为
2 4 3 2 3
AlCl ;铝和氯气反应生成氯化铝,铝和氢氧化钠反应生成偏铝酸钠和氢气,铝和稀硫酸发生置换反应,反应④
3
氯化铝与氨水反应生成氢氧化铝,偏铝酸钠与过量二氧化碳反应生成氢氧化铝和碳酸氢钠,硫酸铝与氨水反应
生成氢氧化铝沉淀。
23、(1)NaOH溶液
(2)过滤 烧杯、漏斗、玻璃棒
(3)2Al+FeO=====2Fe+Al O 焊接铁轨
2 3 2 3
(4)AlO+CO +2HO===Al(OH) ↓+HCO
2 2 3
(5)5.4
解析:氧化铝属于两性氧化物,能溶于强酸和强碱,所以氧化铝和氢氧化钠反应,离子方程式为:Al O +2OH
2 3
-===2AlO+HO,生成可溶性的偏铝酸钠和水,为溶液甲,同时得到沉淀 1,二氧化碳和偏铝酸钠反应生成氢
2
氧化铝和碳酸氢钠,离子方程式为:AlO+CO +2HO===Al(OH) ↓+HCO,沉淀2为Al(OH) ,溶液乙为
2 2 3 3
NaHCO 溶液。
3
(5)电解氧化铝的方程式为:2Al O=====4Al+3O↑,设得到铝的质量为x,
2 3 2
2Al O =====4Al+3O↑ 转移电子
2 3 2
108 g 12 mol
x 0.6 mol
108 g∶12 mol=x∶0.6 mol,
解得x==5.4 g。