文档内容
镁及其重要化合物
【学习目标】
1、掌握镁和镁的重要化合物的主要性质及其应用
2、了解镁及其重要化合物的制备方法
【主干知识梳理】
一、镁的性质
1、物理性质:具有银白色金属光泽的固体,密度、硬度均较小,熔点较低,有良好的导电、传热和延展性
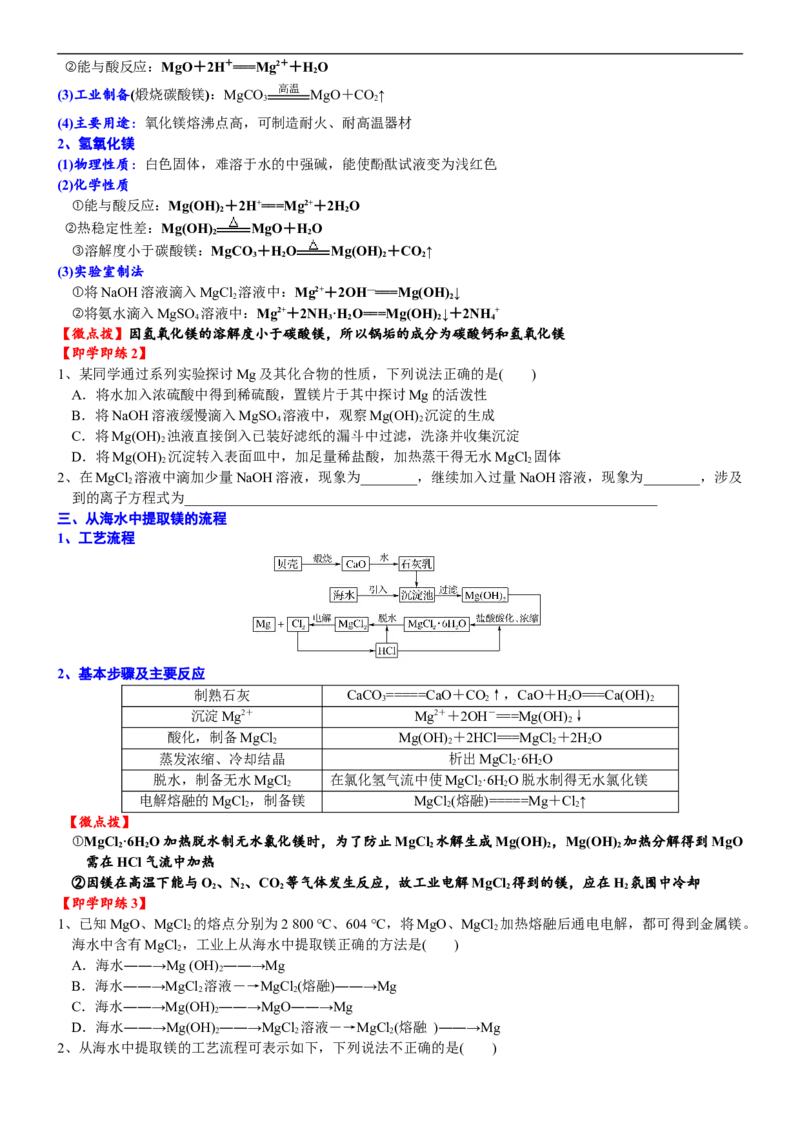
2、镁的结构和存在:镁的原子结构示意图为 ,从原子结构来看,镁原子最外层有2 个电子,在化学反
应中钠原子很容易失去 2个电子而形成最外层为8 个电子稳定结构,因此金属镁的化学性质 非常 活泼 ,表现
出很强的还原性它们都是活泼的金属,在自然界中全部以化合态的形式存在 (地壳和海水中)
3、化学性质
(1)与非金属反应 (O 、Cl、N 等)
2 2 2
①与O 反应:2Mg+O=====2MgO (发出耀眼的白光)
2 2
②与Cl 反应:Mg+Cl =====MgCl
2 2 2
③与N 反应:3Mg+N=====MgN
2 2 3 2
④与S反应:Mg+S MgS
(2)与HO反应:Mg+2HO Mg(OH) +H↑ (冷水慢,沸水快)
2 2 2 2
(3)与非氧化性酸(如:稀盐酸、稀硫酸)的反应:Mg+2HCl===MgCl +H↑ Mg+2H+===Mg2++H↑
2 2 2
(4)与CO 反应:2Mg+CO =====2MgO+C (剧烈燃烧,生成白色粉末和黑色固体)
2 2
(5)与盐溶液反应:Mg+CuSO ===MgSO +Cu Mg+Cu2+ Mg2++Cu
4 4
4、镁的用途
镁合金 用于制造火箭、导弹和飞机的部件
镁 制造信号弹和焰火;冶金工业上用作还原剂和脱氧剂
【微点拨】
①Mg在CO 中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火
2
②镁也可在氮气中燃烧,生成氮化镁(Mg N),氮化镁能与水剧烈反应生成Mg(OH) 沉淀并放出氨气
3 2 2
【即学即练1】
1、正确的打“√”,错误的打“×”
(1)镁表面能形成氧化膜对内部金属起保护作用,因此实验室对镁条不需要特殊保护( )
(2)镁失火可用CO 灭火器灭火( )
2
(3)2.4 g Mg在足量O 中燃烧,转移的电子数为0.1N ( )
2 A
(4)相同质量的镁条分别在足量的CO 和O 中完全燃烧,所得固体的质量相同( )
2 2
(5)工业上制造镁粉时,可将镁蒸气在N 中冷却( )
2
2、镁是一种活泼的金属单质,下列关于金属镁的说法中正确的是( )
A.镁能与NaOH溶液反应生成Mg(OH) 沉淀 B.大量镁条燃烧引起的火灾不能用干冰灭火器灭火
2
C.镁在任何条件下都不能与水反应 D.镁能在N 中燃烧,且生成MgN
2
二、镁的重要化合物
1、氧化镁
(1)物理性质:白色固体,难溶于水,熔点较高,是优良的耐火材料
(2)化学性质:属于碱性氧化物,具有碱性氧化物的通性
①与水能缓慢反应:MgO+HO===Mg(OH)
2 2②能与酸反应:MgO+2H+===Mg2++HO
2
(3)工业制备(煅烧碳酸镁):MgCO
高温
M gO+CO↑
3 2
(4)主要用途:氧化镁熔沸点高,可制造耐火、耐高温器材
2、氢氧化镁
(1)物理性质:白色固体,难溶于水的中强碱,能使酚酞试液变为浅红色
(2)化学性质
①能与酸反应:Mg(OH) +2H+===Mg2++2HO
2 2
②热稳定性差:Mg(OH) MgO+HO
2 2
③溶解度小于碳酸镁:MgCO +HO Mg(OH) +CO ↑
3 2 2 2
(3)实验室制法
①将NaOH溶液滴入MgCl 溶液中:Mg2++2OH—===Mg(OH) ↓
2 2
②将氨水滴入MgSO 溶液中:Mg2++2NH ·HO===Mg(OH) ↓+2NH +
4 3 2 2 4
【微点拨】因氢氧化镁的溶解度小于碳酸镁,所以锅垢的成分为碳酸钙和氢氧化镁
【即学即练2】
1、某同学通过系列实验探讨Mg及其化合物的性质,下列说法正确的是( )
A.将水加入浓硫酸中得到稀硫酸,置镁片于其中探讨Mg的活泼性
B.将NaOH溶液缓慢滴入MgSO 溶液中,观察Mg(OH) 沉淀的生成
4 2
C.将Mg(OH) 浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
2
D.将Mg(OH) 沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl 固体
2 2
2、在MgCl 溶液中滴加少量NaOH溶液,现象为________,继续加入过量NaOH溶液,现象为________,涉及
2
到的离子方程式为___________________________________________________________________
三、从海水中提取镁的流程
1、工艺流程
2、基本步骤及主要反应
制熟石灰 CaCO =====CaO+CO↑,CaO+HO===Ca(OH)
3 2 2 2
沉淀Mg2+ Mg2++2OH-===Mg(OH) ↓
2
酸化,制备MgCl Mg(OH) +2HCl===MgCl +2HO
2 2 2 2
蒸发浓缩、冷却结晶 析出MgCl ·6H O
2 2
脱水,制备无水MgCl 在氯化氢气流中使MgCl ·6H O脱水制得无水氯化镁
2 2 2
电解熔融的MgCl ,制备镁 MgCl (熔融)=====Mg+Cl↑
2 2 2
【微点拨】
①MgCl ·6HO加热脱水制无水氯化镁时,为了防止MgCl 水解生成Mg(OH) ,Mg(OH) 加热分解得到MgO
2 2 2 2 2
需在HCl气流中加热
②因镁在高温下能与O、N、CO 等气体发生反应,故工业电解MgCl 得到的镁,应在H 氛围中冷却
2 2 2 2 2
【即学即练3】
1、已知MgO、MgCl 的熔点分别为2 800 ℃、604 ℃,将MgO、MgCl 加热熔融后通电电解,都可得到金属镁。
2 2
海水中含有MgCl ,工业上从海水中提取镁正确的方法是( )
2
A.海水――→Mg (OH) ――→Mg
2
B.海水――→MgCl 溶液―→MgCl (熔融)――→Mg
2 2
C.海水――→Mg(OH) ――→MgO――→Mg
2
D.海水――→Mg(OH) ――→MgCl 溶液―→MgCl (熔融 )――→Mg
2 2 2
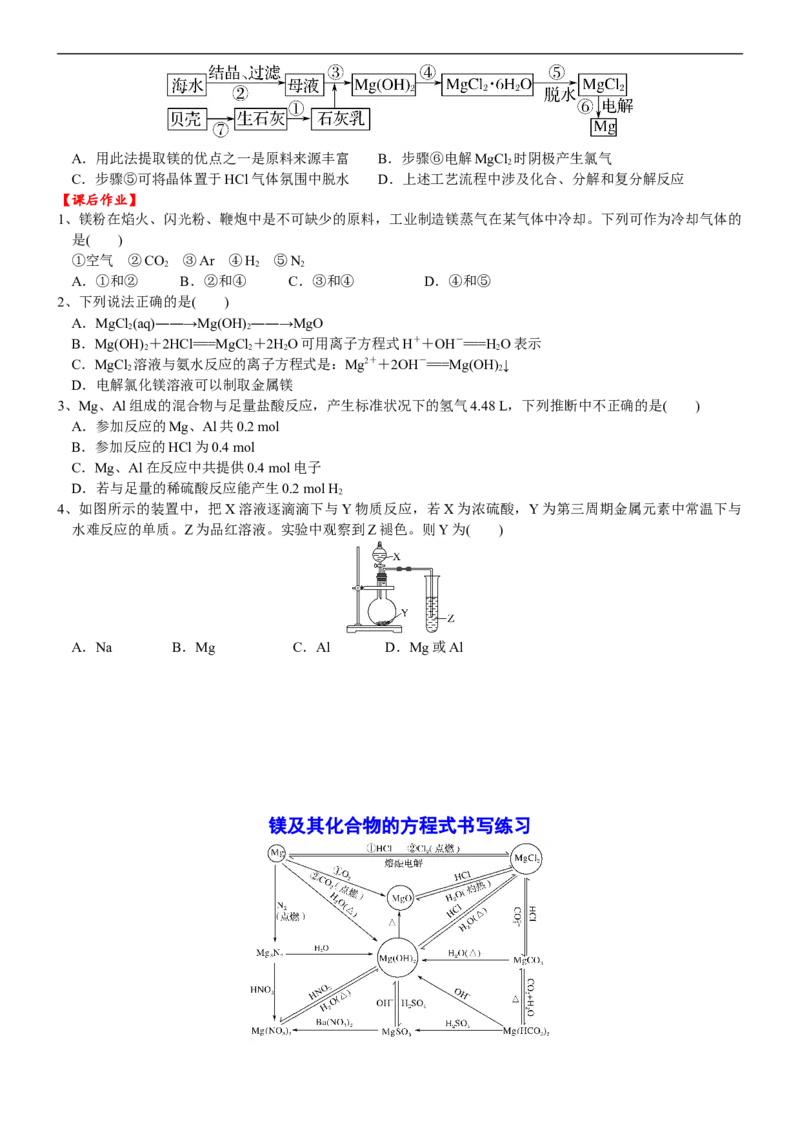
2、从海水中提取镁的工艺流程可表示如下,下列说法不正确的是( )A.用此法提取镁的优点之一是原料来源丰富 B.步骤⑥电解MgCl 时阴极产生氯气
2
C.步骤⑤可将晶体置于HCl气体氛围中脱水 D.上述工艺流程中涉及化合、分解和复分解反应
【课后作业】
1、镁粉在焰火、闪光粉、鞭炮中是不可缺少的原料,工业制造镁蒸气在某气体中冷却。下列可作为冷却气体的
是( )
①空气 ②CO ③Ar ④H ⑤N
2 2 2
A.①和② B.②和④ C.③和④ D.④和⑤
2、下列说法正确的是( )
A.MgCl (aq)――→Mg(OH) ――→MgO
2 2
B.Mg(OH) +2HCl===MgCl +2HO可用离子方程式H++OH-===H O表示
2 2 2 2
C.MgCl 溶液与氨水反应的离子方程式是:Mg2++2OH-===Mg(OH) ↓
2 2
D.电解氯化镁溶液可以制取金属镁
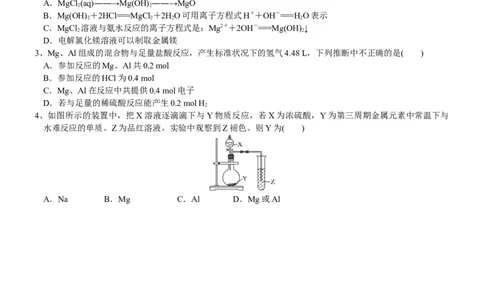
3、Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.48 L,下列推断中不正确的是( )
A.参加反应的Mg、Al共0.2 mol
B.参加反应的HCl为0.4 mol
C.Mg、Al在反应中共提供0.4 mol电子
D.若与足量的稀硫酸反应能产生0.2 mol H
2
4、如图所示的装置中,把X溶液逐滴滴下与Y物质反应,若X为浓硫酸,Y为第三周期金属元素中常温下与
水难反应的单质。Z为品红溶液。实验中观察到Z褪色。则Y为( )
A.Na B.Mg C.Al D.Mg或Al
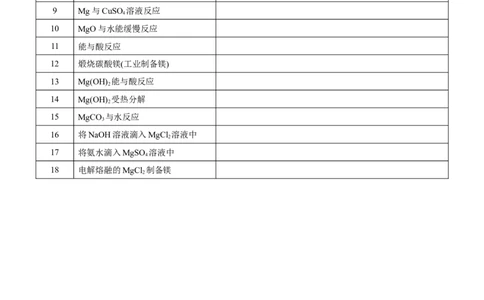
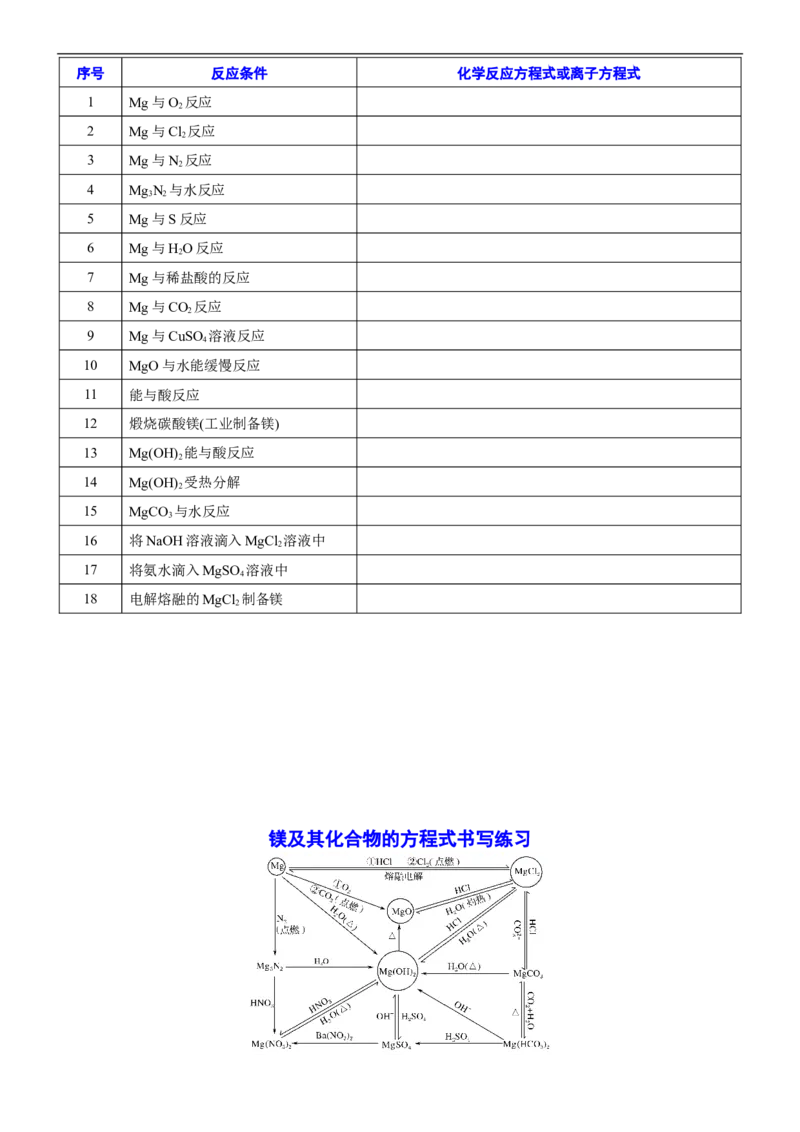
镁及其化合物的方程式书写练习序号 反应条件 化学反应方程式或离子方程式
1 Mg与O 反应
2
2 Mg与Cl 反应
2
3 Mg与N 反应
2
4 MgN 与水反应
3 2
5 Mg与S反应
6 Mg与HO反应
2
7 Mg与稀盐酸的反应
8 Mg与CO 反应
2
9 Mg与CuSO 溶液反应
4
10 MgO与水能缓慢反应
11 能与酸反应
12 煅烧碳酸镁(工业制备镁)
13 Mg(OH) 能与酸反应
2
14 Mg(OH) 受热分解
2
15 MgCO 与水反应
3
16 将NaOH溶液滴入MgCl 溶液中
2
17 将氨水滴入MgSO 溶液中
4
18 电解熔融的MgCl 制备镁
2
镁及其化合物的方程式书写练习序号 反应条件 化学反应方程式或离子方程式
1 Mg与O 反应 2Mg+O=====2MgO
2 2
2 Mg与Cl 反应 Mg+Cl =====MgCl
2 2 2
3 Mg与N 反应 3Mg+N=====MgN
2 2 3 2
4 MgN 与水反应 MgN+6HO 3Mg(OH) +2NH↑
3 2 3 2 2 2 3
5 Mg与S反应 Mg+S MgS
6 Mg与HO反应 Mg+2HO Mg(OH) +H↑
2 2 2 2
7 Mg与稀盐酸的反应 Mg+2HCl===MgCl +H↑ Mg+2H+===Mg2++H↑
2 2 2
8 Mg与CO 反应 2Mg+CO =====2MgO+C
2 2
9 Mg与CuSO 溶液反应 Mg+CuSO ===MgSO +Cu Mg+Cu2+ Mg2++Cu
4 4 4
10 MgO与水能缓慢反应 MgO+HO===Mg(OH)
2 2
11 能与酸反应 MgO+2H+===Mg2++HO
2
12 煅烧碳酸镁(工业制备镁) MgCO
3
高温
M gO+CO
2
↑
13 Mg(OH) 能与酸反应 Mg(OH) +2H+===Mg2++2HO
2 2 2
14 Mg(OH) 受热分解 Mg(OH) MgO+HO
2 2 2
15 MgCO 与水反应 MgCO +HO Mg(OH) +CO ↑
3 3 2 2 2
16 将NaOH溶液滴入MgCl 溶液中 Mg2++2OH—===Mg(OH) ↓
2 2
17 将氨水滴入MgSO 溶液中 Mg2++2NH ·HO===Mg(OH) ↓+2NH +
4 3 2 2 4
18 电解熔融的MgCl 制备镁 MgCl (熔融)=====Mg+Cl ↑
2 2 2
【镁及其重要化合物】答案
【即学即练1】
1、(1)√ (2)× (3)× (4)× (5)×
2、B。解析:镁不是两性金属,不能与NaOH溶液反应,故A错误;镁能在CO 中燃烧,故B正确;镁在加热
2
条件下能与水反应生成氢氧化镁和氢气,故C错误;镁能在N 中燃烧,且生成MgN,故D错误。
2 3 2
【即学即练2】
1、B。解析:浓HSO 稀释时应将浓HSO 加到水中,A错误;过滤时用玻璃棒引流,C错误;由于MgCl 水
2 4 2 4 2
解,故加热蒸干MgCl 溶液时,得不到MgCl 固体。
2 2
2、有白色沉淀生成 沉淀不溶解 Mg2++2OH-===Mg(OH) ↓
2
【即学即练3】
1、D。解析:工业上提取镁除从理论上可行外还要考虑设备、原料、成本等问题。A项中使用NaOH成本高,
且Mg(OH) 是一种不溶性碱,加热熔融时会发生分解,因此不可行;B项中海水加HCl得不到MgCl ;C项中
2 2
电解MgO时,由于MgO的熔点很高,耗能大,经济效益差。
2、B。解析:电解MgCl 时阳极产生氯气,阴极产生Mg。
2
【课后作业】
1、C2、A
3、A。解析:反应的实质为Mg+2H+===Mg2++H↑,2Al+6H+===2Al3++3H↑,n(H )==0.2 mol,则参加
2 2 2
反应的 n(HCl)=n(H+)=0.4 mol。因为盐酸过量,故产生 H 的量取决于金属的量,所以若换成过量的稀
2
HSO ,同样产生0.2 mol H 。依据得失电子守恒,由2H+→H 得电子总数为0.4 mol。0.2 mol Mg在反应中提供
2 4 2 2
0.4 mol电子,0.2 mol Al在反应中提供0.6 mol电子,0.2 mol Mg、Al混合物提供的电子应大于0.4 mol而小于
0.6 mol,A项不正确。
4、B。解析:实验中品红溶液褪色,说明反应中有SO 产生,因为铝在常温下遇浓硫酸钝化,而钠是活泼的金
2
属,极易与水反应,因此该金属是镁,B项正确。