文档内容
综合计算题题型训练 ( 六 )
1.在“2A+3B===2C+4D”的反应中,已知8 g物质A完全反应生成11 g物质C和9 g物质
D。若A的相对分子质量为32,则物质B的相对分子质量( )
A.16 B.32 C.48 D.64
2.2016·泸州向5.6 g铁中加入200 g硫酸溶液,铁与硫酸恰好完全反应,下列有关说法正
确的是( )
A.反应后溶液中的溶质是Fe (SO )
2 4 3
B.反应后溶液中SO 2-的质量是9.8 g
4
C.原硫酸溶液的溶质质量分数是4.9%
D.反应后溶液的质量是205.5 g
3.我国科学家屠呦呦因为发现青蒿素(化学式为C H O)——一种用于治疗疟疾的药物,
15 22 5
挽救了全球特别是发展中国家的数百万人的生命而获得2015年诺贝尔生理学或医学奖。磺胺
(化学式为C HNOS)是青蒿素之前最热门的抗疟药物之一。回答下列问题。
6 8 2 2
(1)一个青蒿素分子中含有________个原子。
(2)青蒿素中氢元素与氧元素的质量比是________。[来源:学&科&网Z&X&X&K]
(3)14.1 g青蒿素中含有碳元素的质量和多少克磺胺中含有碳元素的质量相等?[来源:学.
科.网]
4.取硫酸钠和氯化钠的混合物15 g,加入180 g水使其完全溶解,再加入100 g氯化钡溶
液恰好完全反应,过滤,得271.7 g滤液(不考虑实验过程中质量的损失)。计算:
(1)该混合物中硫酸钠的质量分数。(计算结果精确到0.1%)
(2)反应后所得滤液中溶质的质量分数。(计算结果精确到0.1%)5.某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,
他取出50 g该溶液,向其中逐滴加入溶质质量分数为20%的氢氧化钠溶液,反应过程中生成
沉淀的质量与所用氢氧化钠溶液的质量关系如图KZ6-1所示。请你仔细分析此关系图,并进
行计算。
(1)当滴入氢氧化钠溶液________g时,硫酸铜与氢氧化钠恰好完全反应,此时溶液中的
溶质为__________(填化学式)。
(2)计算此硫酸铜溶液中溶质的质量分数。(写出解题过程)
图KZ6-1
[来源:学_科_网]
[来源:学科网ZXXK]
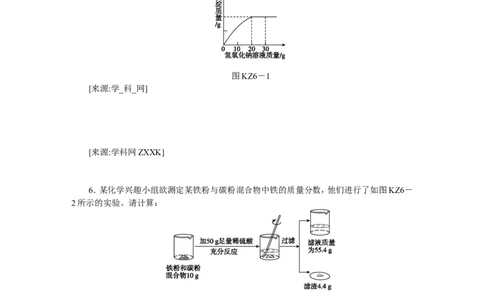
6.某化学兴趣小组欲测定某铁粉与碳粉混合物中铁的质量分数,他们进行了如图KZ6-
2所示的实验。请计算:
图KZ6-2[来源:Zxxk.Com]
(1)混合物中铁的质量。
(2)反应后烧杯中稀硫酸无剩余,请计算所用稀硫酸中溶质的质量分数。
(3)欲用98%的浓硫酸配制该浓度的稀硫酸200 g,需要水多少克?[来源:学科网ZXXK]
7.为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取40 g石
灰石样品等分为4份(分别编号为①②③④),每份样品分别与一定量的稀盐酸反应,所得数据
如下表所示。
样品编号 ① ② ③ ④
稀盐酸的质量/g 25 50 m(80<m<150) 150
剩余固体的质量/g 7.5 5 2 2
然后,为了探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将编号③所得溶液过滤,
取滤液质量的于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,
有关的变化如图KZ6-3所示。
分析题中有关信息和图表,回答下列问题。
(1)该石灰石样品的纯度为________。
(2)编号③所用稀盐酸的质量m为________g。
(3)A点处对应的溶液中溶质的质量分数是多少?(写出计算过程)
图KZ6-3[来源:Zxxk.Com]
8.请根据如图KZ6-4所示的实验过程和提供的数据计算。
图KZ6-4
(1)a、b的数值分别为________、________。
(2)合金中锌的质量分数为________。
(3)第二次加入a g 14.6%的稀盐酸充分反应后所得溶液中溶质的质量分数。(写出计算过
程,计算结果精确至0.1%)
参考答案
1.B [解析] 依据质量守恒定律可知反应的B的质量是11 g+9 g-8 g=12 g。设B的相对分子质量是x。
2A+3B===2C+4D
64 3x
8 g 12 g
= x=32
2.C
3.(1)42
(2)11∶40
(3)解:设磺胺的质量为x。
14.1 g××100%=x××100%
x=21.5 g
答:和21.5 g磺胺中含有碳元素的质量相等。
4.解:(1)生成硫酸钡的质量为15 g+180 g+100 g-271.7 g=23.3 g。
设混合物中硫酸钠的质量为x,生成的氯化钠质量为y。
NaSO +BaCl ===BaSO ↓+2NaCl
2 4 2 4
142 233 117
x 23.3 g y
= x=14.2 g
= y=11.7 g
该混合物中硫酸钠的质量分数为×100%≈94.7%。
(2)反应后所得滤液中氯化钠的质量为11.7 g+(15 g-14.2 g)=12.5 g。
反应后所得滤液中溶质的质量分数为×100%≈4.6%。
答:(1)该混合物中硫酸钠的质量分数为94.7%;(2)反应后所得滤液中溶质的质量分数为
4.6%。
5.(1)20 NaSO
2 4
(2)设参与反应的CuSO 质量为x。
4
2NaOH + CuSO ===Na SO +Cu(OH) ↓
4 2 4 2
80 160
20 g×20% x
= x=8 g
硫酸铜溶液中溶质的质量分数为×100%=16%。
答:此硫酸铜溶液中溶质的质量分数为16%。
6.解:(1)4.4 g滤渣为碳,则铁的质量为10 g-4.4 g=5.6 g。
(2)设所用稀硫酸中溶质的质量为x。
Fe + HSO ===FeSO+H↑
2 4 4 2
56 98
5.6 g x
= x=9.8 g[来源:Z&xx&k.Com]
所用稀硫酸中溶质的质量分数为×100%=19.6%。
(3)设需要浓硫酸的质量为y。
98%×y=200 g×19.6% y=40 g
需要水的质量为200 g-40 g=160 g。
答:(1)混合物中铁的质量为5.6 g;(2)所用稀硫酸中溶质的质量分数为19.6%;(3)需要水
160 g。7.(1)80% (2)100
(3)解:设氯化钙与碳酸钠生成氯化钠的质量为e,生成碳酸钙沉淀的质量为f。
CaCl +NaCO === CaCO ↓+2NaCl
2 2 3 3
106 100 117
20 g×10.6% f e
= f=2 g
= e=2.34 g[来源:学_科_网]
由表中①数据可求得盐酸的质量分数为7.3%;与5 g碳酸钠反应的盐酸的质量为5 g,生
成NaCl质量为0.585 g,生成CO 质量为0.22 g;表中③生成CO 质量为3.52 g,所以A点处对
2 2
应的溶液中溶质的质量分数是
×100%≈6.0%。
答:A点处对应的溶液中溶质质量分数是6.0%。
[解析] (1)该石灰石样品的纯度为×100%=80%。
(2)依据①中的数据进行计算。
设盐酸的质量分数为x。[来源:学*科*网]
CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
100 73
2.5 g x×25 g
= x=7.3%
设编号③所用稀盐酸的质量为y,生成二氧化碳质量为z,生成氯化钙质量为a。
CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
100 73 111 44
8 g y×7.3% a z
= y=80 g
= a=8.88 g
= z=3.52 g
设与碳酸钠反应的过量的盐酸质量为b,生成氯化钠质量为c,生成二氧化碳质量为d。
NaCO + 2HCl===2NaCl+HO+CO↑
2 3 2 2
106 73 117 44
5 g×10.6% b×7.3% c d
= b=5 g
= c=0.585 g
= d=0.22 g
所以编号③所用稀盐酸的质量m为80 g+4×5 g=100 g。
8.(1)50 8.5 (2)90%
(3)解:设第二次加入a g 14.6%的稀盐酸充分反应后所得溶液中溶质的质量为x,生成氢
气的质量为y。
两次消耗锌的质量为15 g-2 g=13 g。
Zn+2HCl===ZnCl +H↑
2 2
65 136 2
13 g x y
= x=27.2 g
= y=0.4 g
第二次加入稀盐酸充分反应后所得溶液中溶质的质量分数为×100%≈24.2%。答:第二次加入稀盐酸充分反应后所得溶液中溶质的质量分数为24.2%。