文档内容
高州市 2010 年初三“缅茄杯”学科竞赛化学试卷
题号 一 5 6 7 8 9 总分
得分
评卷人
可能用到的相对原子质量:H:1; C:12; N:14; O:16; S:32; Cl:35.5
Na:23; Mg:24; Al:27; K:39; Ca:40;
Mn:55; Fe:56; Cu:64;Ag:108
一、选择题(每题有1-2个答案,每题2分,共8分。有两个答案的每选对1个得1
分,选有1个错的得0分,将答案代号填入各题的括号中)。
1、合作学习小组讨论辨析了以下各组说法,其中正确的是( )
A、“酸可以除锈”、“塑料会老化”都是发生了化学变化;冰和干冰既是纯
净物又是化合物
B、沼气和水蒸气都是可再生能源;非金属元素不能形成盐类物质
C、不锈钢和目前流通的硬币都是合金;只由一种原子形成的物质不一定是
纯净物
D、硝酸铵溶于水降温是吸热反应;饱和溶液升温溶质质量分数增大
2、常温下,饱和石灰水的pH约为11.3,现往一定量饱和石灰水中加入下列固体
物质,恢复到常温时,溶液的pH一定不会发生改变的是( )。
A、NaOH B、Ca(OH) C、CaO D、
2
Na CO
2 3
3、甲、乙为两种单质,其组成元素的相对原子质量均小于50,丙、丁为两种化合
物,它们存在如右图的转化关系,下列各组物质表示甲、乙,其中符合的是(
)
A、镁和氢 B、铜和银 C、碳和铜 D、铝和钙
4、下表是几种原子或分子的示意图,根据图示的反应历程判断,下列说法
正确的是( )二、非选择题(5小题,共32分)
5、(6分)化学反应可表示为A+B—C+H O(其中A、B、C可以是化合物或单质)。
2
请你在下列表格里写出两个不同反应类型的具体化学方程式,并说明该反应的一
种用途。
6、(5分)生活中的一些现象可用我们所学的化学知识加以解释。试解释下列现象,
有化学反应的要写出化学方程式。
现象 解释 化学方程式
① 一壶水烧开后,壶盖被顶开
② 农民利用温室生产蔬菜时,在温室
里燃烧木炭
③ 炒菜时油锅中的油不慎着火,盖上
锅盖可灭火
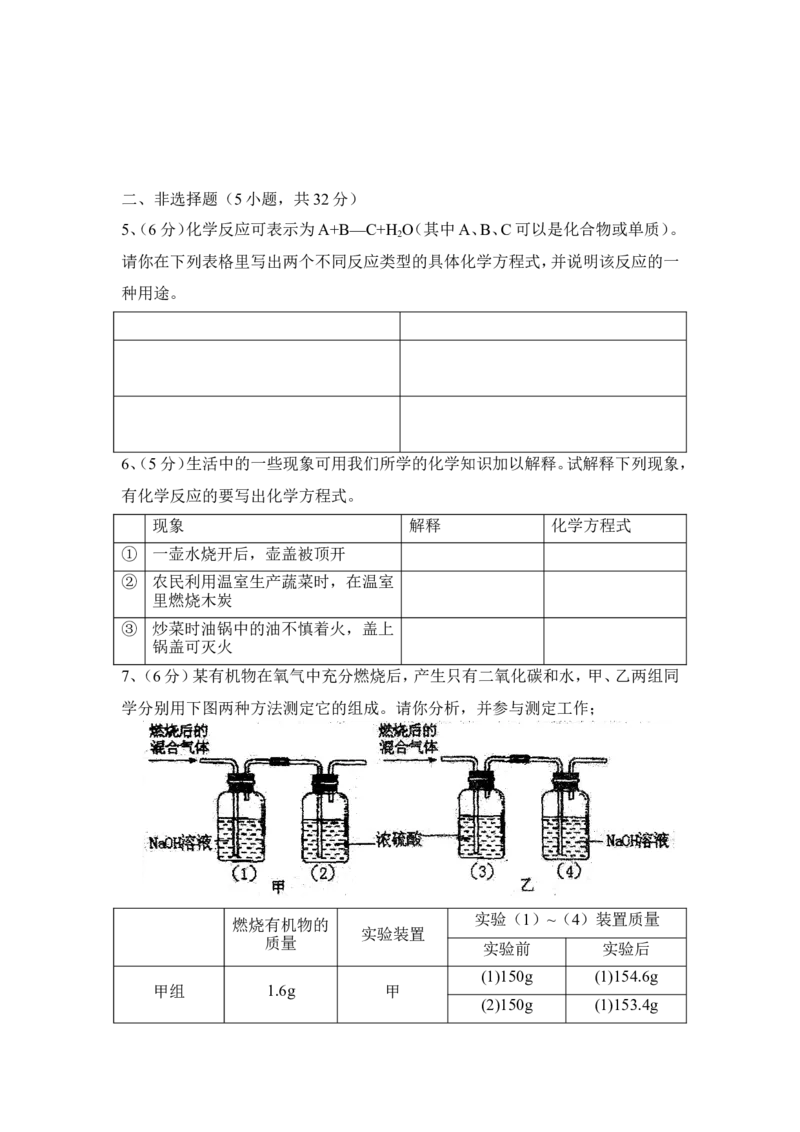
7、(6分)某有机物在氧气中充分燃烧后,产生只有二氧化碳和水,甲、乙两组同
学分别用下图两种方法测定它的组成。请你分析,并参与测定工作;
实验(1)~(4)装置质量
燃烧有机物的
实验装置
质量
实验前 实验后
(1)150g (1)154.6g
甲组 1.6g 甲
(2)150g (1)153.4g(3)150g (1)153.6g
乙组 1.6g 乙
(4)150g (1)154.5g
(1)你选用的实验装置是__________(“甲”或“乙”),你不选另一个装置
的原因是
_____________________________________________________________________
_____________________________________________________________________
_____________________
(2)根据表中数据,推测出该有机物是由_______________________元素组
成的,各元素的质量比为__________________________________(假设实验过程
中气体均全部被吸收)。
8.(7分)某白色粉末可能含有(NH ) SO 、CaCO 、MgCl 。请设计简便、合理的实
4 2 4 3 2
验方案,探究该白色粉末的组成。
限选实验仪器与试剂:烧杯、试管、玻璃棒、玻璃片、胶头滴管、药匙、酒精灯、
火柴、 试管跟镊子;稀硫酸、稀盐酸、NaOH溶液、熟石灰、澄清石灰水、蒸馏水。
完成以下实验探究过程:
(1)提出假设:
根据题意,该自色粉末的组成有____________种可能的情况。
(2)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(在头脑中设计,
不用在试卷上写出来)。
(3)根据(2)的实验方案,叙述实验操作、预期现象和结论,填入下表。
实验操作 预期现象和结论
步骤1:
步骤2:
步骤3:
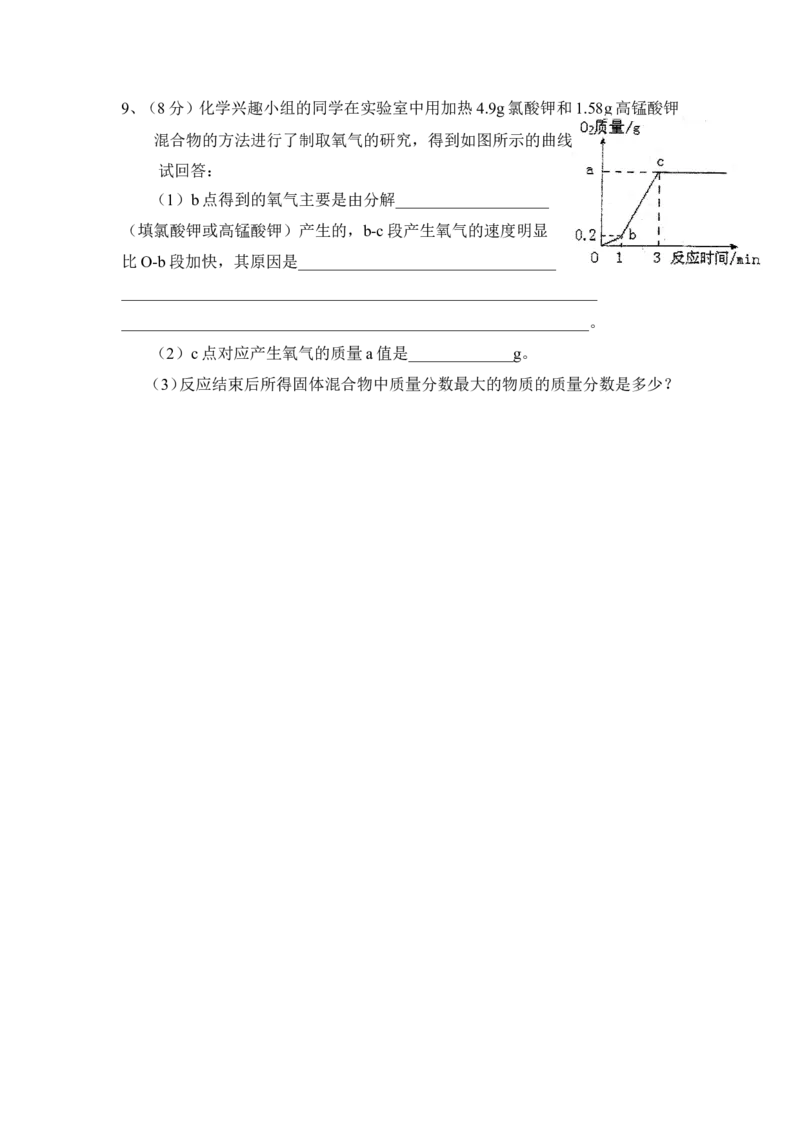
……9、(8分)化学兴趣小组的同学在实验室中用加热4.9g氯酸钾和1.58g高锰酸钾
混合物的方法进行了制取氧气的研究,得到如图所示的曲线图。
试回答:
(1)b点得到的氧气主要是由分解___________________
(填氯酸钾或高锰酸钾)产生的,b-c段产生氧气的速度明显
比O-b段加快,其原因是________________________________
___________________________________________________________
__________________________________________________________。
(2)c点对应产生氧气的质量a值是_____________g。
(3)反应结束后所得固体混合物中质量分数最大的物质的质量分数是多少?2010 年初三“缅茄杯”学科竞赛化学试卷
参考答案与评分标准
说明:化学方程式中化学式错0分,不配平扣一半分,欠箭头、条件扣0.5分。
一、选择题(每题有1—2个答案,每题2分,共8分。有两个答案的每选对1个得1分,
选有1个错的得0分)。
1.AC 2.BC 3.A 4. BC
二、非选择题(5小题,共32分)
5.(6分)开放性答案。两个化学方程式为同一类型的只计一道方程式的分(氧化化物与酸或
碱反应作复分解反应处理),用途与化学方程式要对应,不对应则扣用途的分。
化学方程式 用途
Al(OH) +3HCl=AlCl +3H O 中和胃酸
3 3 2
CuO+H △ Cu+H O 二业制备铜
2 2
6、(5分)
现象 解释 化学方程式
① 液态水变为气态水,水分子问的间隔增大了
CO 是气体肥料,燃烧木炭可增加温室中CO
② 2 2 C+O 点燃 CO(2分)
的含量 2 2
③ 盖上锅盖能使油与空气隔绝而灭火
7、(6分() 1)(1分),因为甲将混合气体先通过NaOH溶液再通过浓硫酸,会影响对原混合气
体中水分质量的测量(1分) (2)碳、氢(2分); 3:1(2分)
8.(7分)(1)7 (1分) 其余各l分每个空格
实验操作 预期现象和结论
步骤1:分别用药匙取少量粉末和适熟石灰 闻到一股刺激性气味,说明原粉末中含有
放在玻璃片上,用玻璃棒将两种固体混合研 (NH )SO
4 2 4
磨
步骤2:用药匙取少量原粉末于试管A中,加 粉末部分溶解,上层为无色溶液,试管底有白
入适量蒸馏水,振荡、静置。 色沉淀,说明原粉末中含有CaCO
3
步骤3:将试管A中上层清液倾倒入试管B 清溶液产生白色沉淀,说明原粉末中含有
中用胶头滴管往试管B中滴入过量的NaOH MgCl
2
溶液、振荡。
……
9、(8分)(1)高锰酸钾(1分),高锰酸钾分解产生的二氧化锰作为催化剂,加速了氯酸钾的
分解。(1分)
(2)2.08g(2分)(3)(4分)解:设氯酸钾分解得到氯化钾的质量为x。
2KClO 2KCl + 3O↑
3 2
245 149
4.9g x
解之得:x=2.98g (1分)
1.58gKMnO 分解,剩余固体质量肯定小于KCl的2.98g,故剩余固体混合物中质量分数最
4
大的只能是KCl。
剩余固体混合物的质量为4.9g+1.58g-2.08g=4.4g (1分)
KCl的质量分数为 (1分)
答:固体混合物中KCl的质量分数最大,其数值为67.73%