文档内容
2025届普通高中毕业班摸底测试
化学试卷参考答案
1.D 【解析】本题主要考查化学与文物的关系,侧重考查学生对基础知识的认知能力。漆绘铜
盆、垂珠金耳坠的主要材料为金属,A、C项不符合题意;钧窑天青釉三足炉的主要材料为硅
酸盐,B项不符合题意。
2.A 【解析】本题主要考查传统文化与化学,侧重考查学生对基础知识的认知能力。水滴石穿
包含碳酸钙与二氧化碳水溶液的反应,未发生化合价变化,不涉及氧化还原反应,A项符合
题意。
3.D 【解析】本题主要考查物质的结构与性质,侧重考查学生对基础知识的认知能力。CO 的
2
键角大于H O,A项错误;NH 为分子晶体,NHCl为离子晶体,B项错误;热稳定性:NaCl
2 3 4
>NaHCO ,C项错误。
3
4.C 【解析】本题主要考查物质的性质与用途,侧重考查学生对基础知识的认知能力。FeO
3 4
用于制造电讯器材,是因为它具有磁性,C项符合题意。
5.B 【解析】本题主要考查仪器的使用方法和装置的作用,侧重考查学生对实验仪器的使用能
力。乙醇和水互溶,不能用分液漏斗分离,A项不符合题意;吸收 HCl气体应加防倒吸装置,
C项不符合题意;应将长颈漏斗插入液面以下或使用分液漏斗,D项不符合题意。
6.B 【解析】本题主要考查有机化合物,侧重考查学生对有机化合物的结构和性质的理解和应
用能力。马兜铃酸A不含酚羟基,遇氯化铁溶液不能发生显色反应,B项错误。
7.A 【解析】本题主要考查离子方程式书写的正误判断,侧重考查学生对基础知识的理解和应
用能力。FeO会被硝酸氧化为Fe3+,B项错误;铁与硫酸铜溶液反应生成铜和硫酸亚铁,C
项错误;氨水不能溶解氢氧化铝,D项错误。
8.D 【解析】本题主要考查元素推断和元素周期律,侧重考查学生的分析推理能力。短周期
中,只有S、O同主族且原子序数成2倍关系,故X为N,Y为O,Z为S,W 为Cl。SO 的漂
2
白作用是由于它能与某些有色物质生成不稳定的无色物质,ClO 的漂白原理基于其强氧化
2
性,D项错误。
9.D 【解析】本题主要考查晶体结构与性质,侧重考查学生对晶体结构的理解能力和计算能
1 1
力。根据均摊法可知每个晶胞中含Au原子个数为8× +6× =4,A项错误;Au原子的
8 2
配位数为12,B项错误;立方晶胞中,位于面对角线上的3个Au原子相切,2个Au原子的最
槡2
近距离为 犪nm,C项错误。
2
10.A 【解析】本题主要考查实验方案的设计与评价,侧重考查学生的实验探究能力。炔烃也
能使溴的四氯化碳溶液褪色,B项不符合题意;AgNO 溶液过量,无法比较犓 (AgCl)和
3 sp
犓 (AgI)的大小,C项不符合题意;比较元素的非金属性强弱,应比较其最高价含氧酸的酸
sp
【高三化学·参考答案 第 1页(共4页)】
书书书性强弱,此实验方法无法比较氮、硅、硫的非金属性强弱,D项不符合题意。
11.D 【解析】本题主要考查电化学知识,侧重考查学生对电化学知识的理解和应用能力。Br-
转化为Br,Br 在水中氧化碳碳双键形成环氧结构,A项错误;铂电极上的电极反应式为
2 2
2H O+2e-H ↑+2OH-,铂电极附近溶液的pH升高,B项错误;没有标明标准状况,
2 2
不能根据体积计算气体物质的量,C项错误。
12.C 【解析】本题主要考查以铅丹为原料制备铬黄的工艺流程,侧重考查学生对元素化合物知识
的理解和应用能力。分离出铬黄后的滤液中含NO-、Cl-、OH-、CrO2-,C项错误。
3 4
13.C 【解析】本题主要考查醇转化为醛或酮的反应历程,侧重考查学生从反应历程图中获取
有用信息的能力。H O是极性分子,醇是弱极性分子,故分子的极性:RCH OH<H O,C
2 2 2
项错误。
14.C 【解析】本题主要考查电解质溶液的相关知识,侧重考查学生获取信息,并对信息进行分
析、处理、加工的能力。犕点对应的溶液中犮(HA)=犮(A-),代入电离常数表达式可得犓
a
犮(H+)·犮(A-) 犮(A-)
=10-3.83。根据犓 = 可推出pH=3.83+lg ,犮(HA)越大,pH 越
a 犮(HA) 犮(HA)
小,A项正确;犮(HA)=犮(A-)时,溶液的缓冲能力最强,B项正确;常温下,A-的水解常数
犓
犓 = w =10-10.17<犓 ,即犮(A-)>犮(HA),pH>3.83,C项错误;pH=3、pH=5的 HA
h 犓 a
a
犮(OH-) 10-11 1
溶液中水的电离程度比值为 1 = = ,D项正确。
犮(OH-) 10-9 100
2
15.(1)增大接触面积,使反应快速而充分(2分);SiO 、CaSO (每个1分,共2分)
2 4
(2)ClO-+6Fe2++6H+Cl-+6Fe3++3H O(2分)
3 2
(3)4.7(1分);8.9(1分)
(4)趁热过滤(2分)
(5)C(1分)
150~200℃
(6)MgSO ·H OMgSO +H O(2分);B(2分)
4 2 4 2
【解析】本题主要考查以菱镁矿渣为原料制备泻盐的工艺流程,考查学生对基础知识的理解
和综合应用能力。
(6)初始取硫酸镁晶体0.1mol,晶体受热失重时,先部分脱水,后全部脱水,然后硫酸镁部
分分解,最终硫酸镁全部分解,生成稳定的氧化镁。根据每个点数据,依据相对分子质量判
断。在失重过程中镁元素始终存在于固体中且质量不变。各点对应物质的组成如下:
代号 犪 犫 犮 犱 犲
相对分子质量 246 138 120 93.3 40
组成 MgSO 4 ·7H 2 O MgSO 4 ·H 2 O MgSO 4 MgO 1 (SO 4 ) 2 MgO
3 3
根据平均值原理,犱点物质组成介于犮和犲点之间,MgO (SO ) 可以看成由 MgSO 和
1 4 2 4
3 3
MgO组成的 MgO(SO ),也可以看成 MgO·2MgSO 。
3 4 2 4
【高三化学·参考答案 第 2页(共4页)】
25-66犆16.(1)防止空气中的水进入C装置(2分)
(2)排尽装置内空气(2分)
△
(3)(NH )CrO CrO +N ↑+4H O(2分)
4 2 2 7 2 3 2 2
(4)①b(1分)
②CrO +2MnO- 2MnO +CrO2-(2分);>(2分)
2 3 4 2 2 7
(5)①c(1分)
②6(2分)
【解析】本题主要考查氮化锂的制备实验,考查学生化学实验设计、实验现象分析和计算等
能力。
(4)①根据实验可知,三氧化二铬类似氧化铝,是两性氧化物。
②三氧化二铬与酸性高锰酸钾溶液反应生成二氧化锰、重铬酸钾。由此可知,氧化剂高锰酸
钾的氧化性强于氧化产物重铬酸钾。
(5)①棕色滴定管有避光作用,硝酸银类似浓硝酸,见光易分解。
②根据AgNO 计算,狀(Cl-)=0.1mol·L-1×20×10-3L=2×10-3mol,根据固体组成,
3
25.00mL
狀(CoCl·狓H O)=1.0×10-3 mol,固体质量 犿=2.38g× =0.238g,
2 2 250mL
238-130
犕(CoCl·狓H O)=238g·mol-1,狓= =6。
2 2 18
17.(1)含有过氧键(1分)
(2)HSO +H OHSO +H O (2分)
2 5 2 2 4 2 2
(3)5SO2-+2Mn2++8H O2MnO-+10SO2-+16H+(2分);D(1分)
2 8 2 4 4
(4)①c(2分)
②C(1分)
(5)①I-(1分)
3
②4×10-3(2分);25(2分)
【解析】本题主要考查化学反应原理,考查学生对基础知识的理解和应用能力。
(3)溶液变紫红色表明生成了高锰酸根离子。
(5)①两种极稀溶液混合体积近似加合。根据初始投入物质的量及化学计量数可知,曲线犪
代表I-浓度与时间关系,曲线犫代表SO2- 浓度与时间关系,曲线犮代表SO2- 浓度与时
2 8 4
间关系,曲线犱代表I- 浓度与时间关系。
3
0.05-0.03
②狏(SO2-)= mol·L-1·min-1=4×10-3mol·L-1·min-1。观察图示,根
2 8 5
0.03×0.062
据平衡时各离子浓度计算平衡常数,犓= L·mol-1=25L·mol-1。
0.02×0.063
18.(1)环氧乙烷(2分)
(2)羟基(1分);取代反应(1分)
【高三化学·参考答案 第 3页(共4页)】師師 師師
(3)帨帨師師 Br+NaCN→帨帨師師 CN +NaBr(2分)
(4)ac(2分)
CH CH CHCl
3 3 2
Cl Cl
師師 師師 師師
(5)10(2分); 帨帨師師 或 帨帨師師 或師師帪帪 (2分)
Cl Cl
Cl
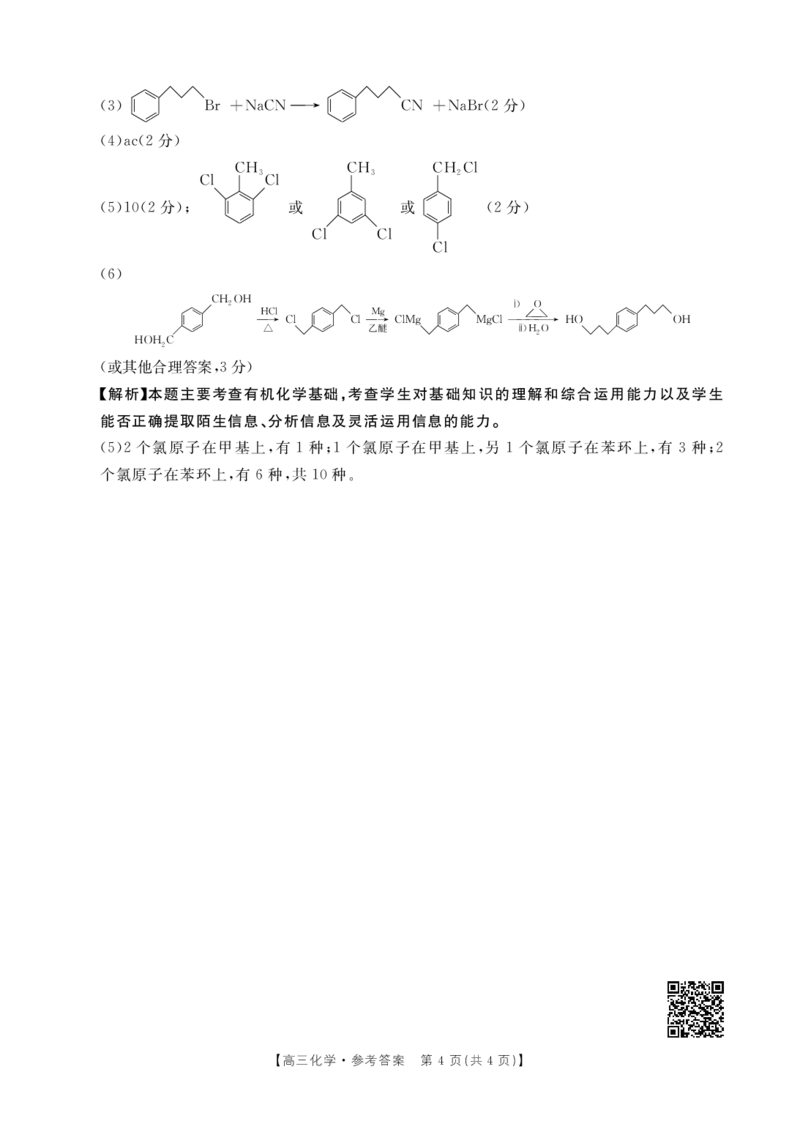
(6)
師師 CH 2 OH HCl 師師 Mg 師師 ⅰ) O 師師
帨帨師師 → Cl 帨帨師師 Cl→ ClMg 帨帨師師 MgCl→ HO 帨帨師師 OH
△ 乙醚 ⅱ)H 2 O
HOHC
2
(或其他合理答案,3分)
【解析】本题主要考查有机化学基础,考查学生对基础知识的理解和综合运用能力以及学生
能否正确提取陌生信息、分析信息及灵活运用信息的能力。
(5)2个氯原子在甲基上,有1种;1个氯原子在甲基上,另1个氯原子在苯环上,有3种;2
个氯原子在苯环上,有6种,共10种。
【高三化学·参考答案 第 4页(共4页)】