文档内容
扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}扫描全能王 创建
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}2024 年十堰市六县市区一中教联体 11 月联考
高二化学试卷答案详解
1. 【答案】B【解析】乙烯具有催熟的作用,即文中的“气”是指乙烯,B错误。
2. 【答案】A【解析】将煤炭通过煤液化技术转化为甲醇燃料,甲醇燃料在燃烧时,不会减少二氧化碳的
排放量,不会实现“碳中和”,A错误。制取等量的硝酸铜,消耗浓硝酸的量较大,且放出的有毒气体的
量相对较多,即使用稀硝酸比使用浓硝酸排放的污染物更少,B正确。工业制硫酸尾气中的SO 回收常
2
采用氨水吸收法,即先用氨水吸收二氧化硫,当吸收液中NH HSO 达到一定浓度后,再与硫酸反应放出
4 3
SO ,可以循环利用,C正确。乙烷和氯气光照发生取代反应有副产物氯化氢气体生成;而乙烯与氯化
2
氢发生加成反应只生成氯乙烷,反应物全部转化为生成物,没有副产物,原子利用率达到100%,D正确。
3. 【答案】C【解析】泡沫灭火器的反应原理为铝离子和碳酸氢根离子通过盐的水解相互促进反应,生
成二氧化碳和水:Al3++3HC -===Al(OH) ↓+3CO ↑,A错误;氨水吸收足量SO 生成亚硫酸氢铵,反应
3 2 2
的离子方程式为NH ·H O+SO ===HSO +NH ,B错误;向Ca(ClO) 溶液中通入少量SO , 反应
3 2 O3 2 2 2
生成硫酸钙、盐酸和次氯酸,反应的离子方程式为Ca2++2ClO-+SO +H O===CaSO ↓+Cl-+H+
2 2 4
+HClO,D错误。
4. 【答案】B【解析】气态水转化为液态水放出热量,H 的燃烧热ΔH应小于-241.8kJ·mol-1,故A错误;
2
2mol碳单质完全燃烧时放出热量更多,ΔH更小,ΔH <ΔH ,故B正确;浓硫酸溶于水的过程放热,
1 2
则用浓硫酸与NaOH溶液反应生成1mol水,放出的热量大于57.3kJ,故C错误;石墨转化为金刚石
吸热,说明石墨的能量低于金刚石,而物质能量越低越稳定,故石墨比金刚石更稳定,故D错误。
5. 【答案】C【解析】A项, CO g H g CH g CO g 是放热反应,反应物总能量高于生
成物总能量,加催化剂会导致活化能降低,但不影响反应热,与图像含义符合,故A不选;B项,
2 +2 2 = 4 + 2
放热反应,反应物的键能和小于生成物的键能和,故B不选;C项,酸碱中和反应为放热反应,物
质的量浓度相等、体积分别为V 、V 的HCl、NaOH溶液混合,V +V =60mL,则V =30mL,V =30mL
1 2 1 2 1 2
时HCl、NaOH溶液恰好完全反应,放出的热量最多,即横坐标为30时的温度应该最高,图象与实
际反应相符,故C符合题意;D项,已知稳定性顺序为B<A<C,物质的总能量越低越稳定,则物
质具有的能量B>A>C,图示中表示的能量变化曲线符合实际,故D不选。
6. 【答案】B【解析】由图可知,CH 在催化剂表面发生化学吸附生成H*和CH*,表示为CH (g)H*+
4 3 4
CH*,A项正确;由图可知,反应中只有C—C和O—H的生成,B项错误;②过程H*和CH COO*
3 3
在催化剂的作用下生成CH COOH,则②过程表示CH COOH分子的脱附过程,C项正确;反应物
3 3
的总能量大于生成物的总能量,该合成反应是放热反应,D项正确。
7. 【答案】C【解析】有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加单位体积
内活化分子的数目,从而使反应速率加快,但活化分子的百分数不变,A不正确;催化剂之所以能
改变化学反应速率,是因为它能改变反应历程,从而改变反应的活化能,但不能改变反应的焓变,B
不正确;活化能是活化分子具有的平均能量与反应物分子具有的平均能量之差值,活化能越小,反
应越容易发生,C正确;升高温度能增加活化分子百分数,增加反应物浓度,活化分子的百分数不
变,但它们都能增大单位体积内的活化分子数,从而使单位时间内的有效碰撞次数增加,从而增加
化学反应速率,D不正确;故选C。
8. 【答案】B【解析】滴加10滴6mol·L-1NaOH溶液,氢离子浓度降低,平衡正向移动,实验现象应
是黄色加深,故A错误;根据溶液褪色时间长短可知不同催化剂的催化效果,故B正确;FeCl 过
3
1
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}量,不能用检验Fe3+的存在来证明该反应是可逆反应,故C错误;恒容容器中充入氦气增大总压强,
但反应物浓度不变,故平衡不移动,故D错误。
9. 【答案】A【解析】由①②数据得b=1, 由①④数据得a=1,由②③数据得c=2,则反应体系的三
种物质中,H+(aq)的浓度对反应速率影响最大,A正确;结合A分析,将①中数据代入 RO
R H 中,则 , =3.75,B错误;由A分析a 可知−,
v=k⋅c ( 3)⋅
abbc分−别为c 1、+1、2,C错误;实−8验⑤中, 2 ,D错
c ( )⋅c ( ) 2.4×10 =k⋅0.001⋅0.10⋅ 0.008 k
误;故选A。 2 −8
v1 =3.75×0.001×0.40× 0.008 =9.6×10
10. 【答案】A【解析】其他条件不变,将密闭容器的容积扩大1倍,若平衡不移动,则B气体的浓度为0.3
mol·L-1,实际上B的浓度变为0.4mol·L-1,说明平衡向逆反应方向移动,故a+b>c+d,ΔS<0,ΔH>0,任
意温度均不自发,A错误;密闭容器的容积加倍,平衡逆向移动,但各物质的浓度都要减小,即A气体
的浓度也减小,B正确;由A选项的分析知将密闭容器的容积扩大1倍平衡向逆反应方向移动,故D
气体的体积分数减小,C正确;恒温下扩大容器体积,减压,正逆反应速率均减小,D正确。
11. 【答案】B【解析】t 时刻充入了一定量的C,v 瞬间不变,A错误;依据图像分析,温度升高平均
0 正
相对分子质量减小,平均相对分子质量减小,总质量不变,说明气体物质的量变大,所以平衡逆向进行,
逆反应是吸热反应,正反应是放热反应,ΔH<0,C错误;容器体积越大,压强越小,而该反应为气体分子数
增大的反应,加压,平衡逆向移动,N 的百分含量减小,则E、F点为平衡点,G点因压强过小,速率过慢,
2
未达到平衡,D错误。
12. 【答案】D【解析】A.若N不是气体,则该反应前后气体物质的量不变,改变压强平衡不移动,M的体
积分数不变,与图像不符合,故在该反应条件下N为气体,故A正确;B.温度为300 ℃、压强为p 条件
1
下,M的体积分数为50%,设X的转化量为xmol,则平衡时各物质的量为n(X)=n(Y)=(1-x)mol,n(M)=2x
mol,n(N)=xmol,则可得 ×100%=50%,解得x= ,故X的平衡转化率为 ×100%≈66.7%,故B正确;
2
( - )
2x 2 3
C.温度为300 ℃、压强 2 为 1xp+12 条 x+ 件 x 下,C点未达到平衡状 3 态,该条件下平衡时刻 1 M的体积分数应对应B
点,C点M的体积分数比B点M的体积分数小,故反应正在向正反应方向进行,故v(正)>v(逆),故C正
确;D.由图像可知,升高温度,M的体积分数减小,说明升温平衡逆向移动,平衡常数减小,且平衡常数只
与温度有关,温度相同,平衡常数相同,故A、B、D三点平衡常数,K(A)>K(B)>K(D),故D错误。
13. 【答案】B【解析】由两种溶液的浓度与pH可知,HA是强酸,BOH是弱碱,弱碱的电离是可逆过程,A
项错误;因等物质的量浓度、等体积的两溶液混合时,二者恰好完全反应得到BA溶液,该溶液呈酸性,
而混合后的溶液呈中性,说明碱过量,B项正确;BA为强酸弱碱盐,其水溶液显酸性,则c(H+)>c(OH-),C
项错误;将pH=11的强碱溶液稀释100倍后,所得溶液的pH=9,而BOH是弱碱,稀释过程中会继续电
离出OH-,故将0.1mol·L-1BOH溶液稀释至0.001mol·L-1,溶液的pH范围为93c(S -),故C错误;根据图中信息得到, 2 NaHSO 溶液pH大约为4,说明溶液2显酸性,是亚硫酸
O3 3O3 O3 O3
氢根电离占主2要,抑制水的电离,因此溶液中水电离出的c(H+)<1×10-7mol·L-1,故D正确。
O3
15. 【答案】D【解析】由题意可知,c(M2+)越小,pM越大,常温下K (ZnS)>K (PbS),则c(S2-)相同且分别
sp sp
2
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}达到沉淀溶解平衡时c(Zn2+)>c(Pb2+),可得出曲线①代表PbS的沉淀溶解关系,曲线②代表ZnS的沉淀
溶解关系。常温下,B点对应溶液中Pb2+的浓度大于曲线①上相同c(S2-)时对应的Pb2+的浓度,所以B
点Q>K (PbS),为过饱和溶液,A错误;若x=1.6×10-10,则y=-lg =-lg =18-lg2≈17.7,B错误;
sp
−28
Ksp(PbS) 3.2×10
若对A点浊液进行加热,PbS溶解度增大,Pb2+、S2-浓度均增大,pcM(S 2−将 ) 会减 1 小 .6×,1 温 0 −度10升高,K sp 增大,A点不
沿曲线①移动,C错误;在ZnS和PbS同时沉淀的浊液中 = = =5×103,D正确。
2+ −24
c(Zn ) Ksp(ZnS) 1.6×10
16. (14分)【答案】(1)C
2
H
8
N
2
(l)+2N
2
O
4
(g)===3N
2
(g)+2COc(P2 (bg 2+ )+) K4sHp(P2bOS)(g)3.2×Δ10H −2=8 (y-2x)kJ·mol-1(2分)
(2)C H (g)+5O (g)===3CO (g)+4H O(l) ΔH=-2220kJ·mol-1(2分)
3 8 2 2 2
CH −8e−+10OH−===C -+7H O(2分)
4 2
(3) 946(2分) 小于(1分� ) (4)(E -E )+ΔH+(E -E )(2分)
�� 1 2 3 4
(5)玻璃搅拌器(1分) 偏小(2分)
【解析】(1)根据盖斯定律,由反应2-2×反应1可得目标反应的热化学方程式;(4)由图中能量变化情
况分析可知,过程中的焓变=(E -E )+ΔH+(E -E );(6)会造成热量损失,所测得温差的数值变小。
1 2 3 4
17. (13分)【答案】(1) 浓度 或 Na S O 溶液的浓度 或 反应物的浓度(1分)
2 2 3
(2)8(2分) 控制硫酸的起始浓度相同(1分) (3)Ⅲ(1分)
(4)酚酞(2分) (5)26.60(2分) (6)0.1100mol L (2分) (7)CD(2分)
【解析】(1)对比实验Ⅰ、Ⅱ,所加Na S O 溶液的体−积� 不同,即Na S O 的物质的量不同,所加H SO
2 2 3 ⋅ 2 2 3 2 4
溶液的体积、浓度均相同,实验温度相同,则实验Ⅰ、Ⅱ为探究Na S O 溶液的浓度对该反应速率的影
2 2 3
响。(2)实验Ⅰ、Ⅱ所加H SO 溶液的体积、浓度均相同,为保证溶液混合后H SO 的浓度相同,则要
2 4 2 4
加入蒸馏水,由实验可知,溶液混合后总体积为10mL,则V=8。(3)实验Ⅲ中温度最高,Na S O 溶液的浓
2 2 3
度较大,故推测反应速率最快的是Ⅲ。
(4)氢氧化钠与醋酸恰好反应溶液呈碱性,应用碱性范围内变色的指示剂:酚酞;
(5)结束时,碱式滴定管中的液面如图所示,则此时读数为26.60;
(6)根据表格可知三次实验耗氢氧化钠标准溶液体积分别为:22.01,19.10,21.99,由于第二次数据
差距较大,舍去;剩余两次实验耗体积平均为22.00,
根据 c CH COOH = c NaOH V NaOH 0.1000mol/L 22.00 10-3L =0.1100mol/L
3 V CH3COOH 20.00
×
10-3L
×
(7)根据 c CH COOH = c NaOH V NaO = H 所有误差×分析都归到耗标准溶液体积,A.滴定前平视读数,滴
3
V CH3COOH
定终点时俯视读数,耗标准溶液体积偏小,结果偏低,A不符合要求;B.锥形瓶用蒸馏水洗过后未
晾干直接盛装待测液,无影响,B不符合要求;C.碱式滴定管滴定前有气泡,滴定后无气泡,耗标
准溶液体积偏大,结果偏高,C符合要求;D.配制标准溶液所用 NaOH固体中含有少量 Na CO 杂
3
质,耗标准溶液体积偏大,结果偏高,D符合要求;故CD符合要求
2
18. (14分)【答案】(1) (1分) D(2分)
(2)大于(1分) −�� Na H OH (2分) AB(2分)
��
− + + −
(3) (2分) �(4�)��Na�� OH�� �� H (2分) (5)0.05(2分)
【解 � � 析 − � � + 】 .� � � (1)加酸抑制水 � 的电 + 离, � 若 � A点 − 的 �p�H= ��3� − ,该 � 点 � 溶 + 液中由水电离出的c(H+)=10-11mol/L。
(2)B点加入NaOH体积为10mL,溶质为等浓度的HNO 和NaNO ,溶液显酸性,故HNO 的电离程
度大于N 的水解程度,该点溶液中离子浓度由大到小的顺序是c(N )>c(Na+)>c(H+)>c(OH-)。
2 2 2
等浓度的H − NO 和NaNO ,电荷守恒:c(Na+)+c(H+)=c(OH-)+c(N ),−元素守恒:c(N )+c(HNO )
O2 O2
− −
2 2 3 O2 O2 2
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}=2c(Na+)= ×0.1mol·L-1),由上述两式可得c(HNO )+2c(H+)=c(N )+2c(OH−),综上A、B均正确。
(3)C点溶液呈 2 3 中性,则c(H+)=c(OH-)=10-7mol/L,2 由元素守恒可 O 知 2 − c(N )+c(HNO )=
−
= mol/L ,由电荷守恒可知c(Na+)+c(H+)=c(OH-)+Oc(2N ),则 c2(N )=c(Na
−3
0.1mol/L×20×10 L 2 − −
−3
+)=(20+x)×10 L 2=0+x mol/L,c(HNO )= mol/L- mol/L= Om2ol/L。 O2
−3
0.1mol/L×x×10 L 0.1x 2 0.1x 2−0.1x
(4)E点加 (20 入 +x)N×1a0O−3HL 体积 2 为 0+x40mL,溶质为等2 浓度 20 的 +x NaOH和 20N+axNO ,溶液 20 显 +x 碱性
(5)D点NaNO 溶液0.05mol·L−1,等体积混合浓度均减半,K ≤ 2 解得 ≥0.05mol·L−1
sp
+
0.05 c(Ag ) +
19. (14分)【答案2 】(1)BD(2分) (2)1.1(2分) 逆向移动 (2
2
分
×
)
2 c(Ag )
(3)>(1分) a(2分) K(a)=K(b)=K(c)(2分)
(4)>(1分) >(1分) 高温 (1分)
【解析】(1)由质量守恒定律可知,反应前后气体的质量相等,该反应是气体体积减小的反应,反应
中容器内气体的平均摩尔质量增大,则容器内气体的平均摩尔质量保持不变说明正逆反应速率相等,
反应已达到平衡,故A正确;正反应方向始终v(NH ) =2v(N ) ,无法判断反应是否达到平衡,故B
3 正 2 正
不正确;该反应是气体体积减小的反应,反应中容器内压强减小,则容器内压强保持不变说明正逆
N g + 3H g 2NH
2 2 3
始 1 0
反应速率相等,反应已达到平衡,故C正确; ⇌ N 始终占
转 a 3a 2a 2
(mol) 1
末 -a 1-3a 2a
(mol)
50%,无法判断反应是否达到平衡,故D错误;故选BD;
(mol) 1
(2)设平衡时消耗氮气的物质的量为amol,由题意可建立如下三段式:
N g + 3H g 2NH
2 2 3
始 0.80 1.60 0
⇌
转 a 3a 2a
(mol)
平 0.80-a 1.60-3a 2a
(mol)
0.4
由氨气的体积分数为20%可得:(mol2)a ×100%=20%,解得a=0.2,则反应的平衡常数为 ( 2 ) ≈1.1;
2.40-2a 0.6 ( 12 )
2 2
( 0.8 ) × 3
若达平衡后再向该容器中充入0.40mol氮气和0.40mol氨气,反应的浓度熵Q= 2 =2.56>1.1,则
1 12
( )
2 2
平衡向逆反应方向移动,故答案为:逆向移动; × 3
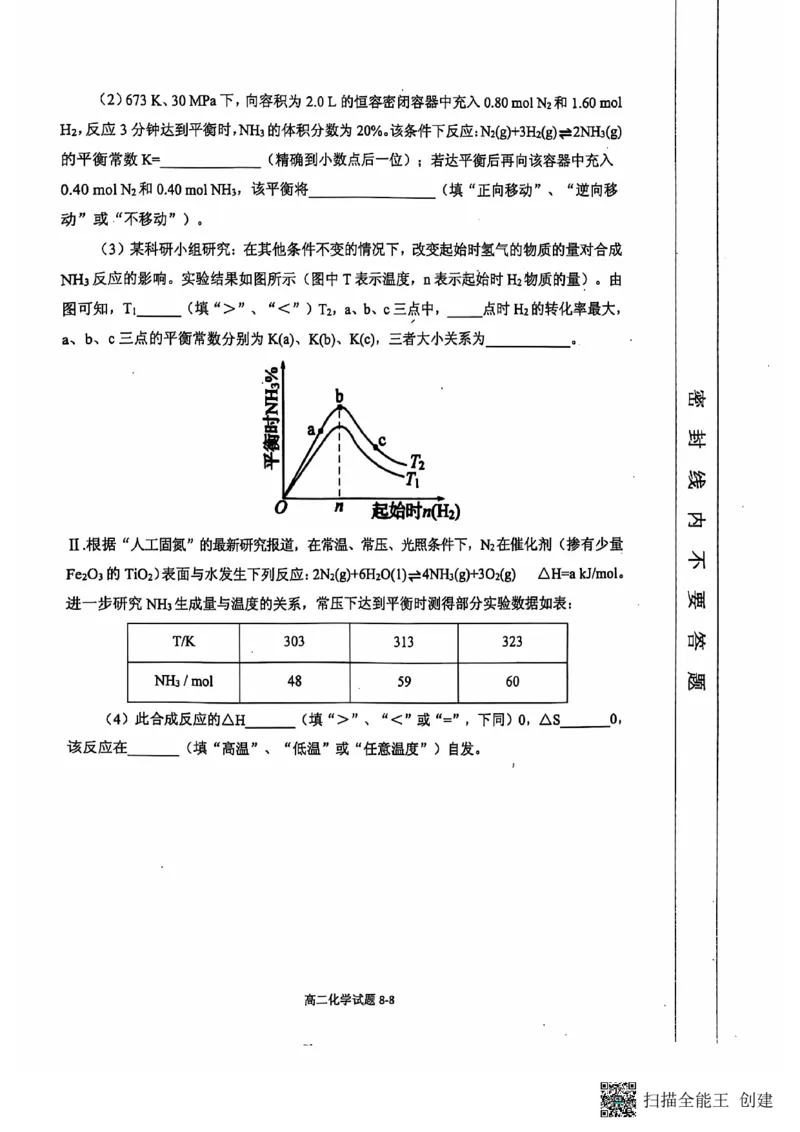
(3)由图可知,n(H )相同时,温度 T 对应氨气含量高,反应为放热反应,降低温度有利于生成氨气,则
2 2
T >T ;a、b、c三点,n(H )越大,平衡正向移动的程度越大,N 的转化率越大,H 的转化率却越小,a点时
1 2 2 2 2
氢气的物质的量最小,a点H 的转化率最高;温度不变化学平衡常数不变,故a、b、c三点的平衡常数
2
K值相等。
(4)由表格数据可知,升高温度,反应的平衡常数增大,说明向正反应方向移动,该反应为熵增的吸
热反应,反应的△H>0、△S>0,高温下△G<0。
4
{#{QQABDYCAgggAAgBAAAgCEQWCCkEQkgAAAagGRFAAsAAByAFABAA=}#}