文档内容
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}2024 年高二 9 月起点考试
高二化学参考答案
一、选择题:本题共15小题,每小题3分,共45分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A C D D A C C D D A C D B C A
1. 【答案】A
【解析】
A.啤酒中存在CO
2
(g)+H
2
O(l)H
2
CO
3
(aq),开启啤酒瓶后,减小压强,平衡逆向移动,
故瓶中立刻泛起大量泡沫,能用勒夏特列原理解释,A符合题意;
B.钢铁生锈的过程中不存在化学平衡,属于吸氧腐蚀,故不能用勒夏特列原理解释,B不
合题意;
C.合成氨的正反应是一个放热反应,故在合成氨的反应中,升温不利于氨的合成,之所以
提高温度来合成氨是为了加快反应速率提高生产效率,C不合题意;
D.H 、I 、HI三者的平衡混合气,由于反应H (g)+I (g)2HI(g)前后气体的体积不变,
2 2 2 2
加压(缩小容器体积)后平衡不移动,颜色变深是由于I 蒸汽的浓度增大造成的,故不能
2
用勒夏特列原理解释,D不合题意;
故答案为:A。
2. 【答案】C
【解析】
A.吸热反应和放热反应的判断跟条件无关,有些吸热反应需要加热,有些不需要加热,放
热反应也是如此,故A错误;
B.若反应物的总能量低于生成物的总能量,则该反应是吸热反应,故B错误;
C.化学反应发生时有化学键的断裂和形成,就伴随着能量的变化,故C正确;
D.浓硫酸使蔗糖变黑体现脱水性,故D错误;
故本题选C。
3. 【答案】D
【解析】常温下浓硫酸与铁发生钝化阻碍了反应进行,故改用98%的浓硫酸后不能增大生成
氢气的速率,A错误;加入氯化钠溶液后,氯化钠不参与反应,但溶液体积增大,相当于稀释,
湖北省新高考联考协作体*化学参考答案(共8页)第 1 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}导致稀盐酸浓度减小,反应速率减小,B错误;升高温度,反应速率增大,C错误;压强越小反
应速率越慢,所以减小压强反应速率减慢,D正确。
4. 【答案】D
【解析】
A.合成氨反应为可逆反应,标准状况下,11.2L的N 和过量H 反应,生成氨气的分子数小
2 2
于N ,故A错误;
A
B.1个甲基中含有9个电子,15g甲基所含电子数为9N ,故B错误;
A
C.铜与稀硫酸不反应,100mL18mol/L的浓硫酸与足量Cu粉加热反应,参加反应的硫酸小
于1.8mol,产生SO 分子数小于0.9N ,故C错误;
2 A
D.乙烯和丙烯的最简式均为CH ,常温常压下,28g乙烯和丙烯的混合气体中含有的碳原
2
子数为2N ,故D正确;
A
故本题选D。
5. 【答案】A
【解析】
A.容器绝热,当温度不变时反应达到平衡,A符合题意;
B.无论是否平衡,同一方向F (g)与ClF (g)速率之比恒等于计量数之比,B不符合题意;
2 3
C.根据元素守恒可知,无论是否平衡,混合物中Cl元素质量分数都不变,C不符合题意;
D.断裂1molF—F键,同时生成3molF—Cl键,表示的都是正反应,无论是否平衡都满足
此关系,D不符合题意;
综上所述答案为A。
6. 【答案】C
【分析】该电池中以液态肼(N H )为燃料,氧气为氧化剂,所以通入N H 电极即电极甲
2 4 2 4
为负极,通入氧气电极即电极乙为正极。
【解析】
A.甲为负极,乙为正极,正极电势高于负极,故电极乙的电势比电极甲高,A项正确;
B.放电时原电池中阴离子向负极移动,O2-由电极乙移向电极甲,B项正确;
C.反应生成物均为无毒无害的物质,所以N H 被氧气氧化生成N 和H O,电解质为固体
2 4 2 2
氧化物,O2-在该固体氧化物电解质中自由移动,故负极反应为N H -4e-+2O2-=N +2H O,
2 4 2 2
C项错误;
湖北省新高考联考协作体*化学参考答案(共8页)第 2 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}D.电路中转移1mol电子,乙电极上有0.25molO 参与反应,质量为8g,D项正确;
2
答案选C。
7. 【答案】C
【解析】酸性KMnO 溶液和H C O 溶液反应生成Mn2+和二氧化碳,随着反应进行高锰酸
4 2 2 4
钾溶液褪色,可以通过记录溶液褪色时间来测定反应速率,A不选;单位时间内产生的沉淀的质
量越多,则反应速率越快,反之反应速率越慢,测量依据可行,B不选;该反应前后气体分子数
不变,故温度、体积一定时,反应前后气体总压不变,则测量依据不可行,C选;单位时间内,
I-浓度减小得越多,反应速率越快,反之,反应速率越慢,测量依据可行,D不选。
8. 【答案】D
【解析】
A . 已 知 Fe3+ 能 够 氧 化 I- , 故 氢 氧 化 铁 溶 于 氢 碘 酸 的 离 子 方 程 式 为 :
2FeOH 6H+2I-=2Fe2I 6H O,A错误;
3 2 2
B.NaHSO 电离出Na+、H+和硫酸根离子,故氧化铜溶于硫酸氢钠溶液的离子方程式为:
4
,B错误;
CuO2H Cu2+H O
2
C.硫氢化钠溶液与稀硫酸溶液混合不发生氧化还原反应,故离子方程式为:HS-+H+=HS,
2
C错误;
D.已知HClO是具有强氧化性的弱酸,故次氯酸钙溶液中通入少量二氧化硫的离子方程式
为:Ca2 3ClOSO H OCaSO Cl2HClO ,D正确;
2 2 4
故答案为:D。
9. 【答案】D
【解析】升高温度,更多分子成为活化分子,活化分子百分数增大,则化学反应速率增大,
A正确;增大压强,单位体积内活化分子数目增多,活化分子百分数不变,则化学反应速率增大,
故B正确;加入催化剂,降低了反应所需的活化能,更多普通分子成为活化分子,活化分子百分
数增大,化学反应速率增大,C正确。加入反应物,反应物的浓度增大,单位体积活化分子的数
目增大,活化分子的百分数不变,D错误;
故答案为D。
10. 【答案】A
【解析】比较反应Ag4Bg CgDs 四种不同的情况下的反应速率快慢,都转化
为用 B 表示的速率进行比较且单位要保持一致,速率之比等于计量系数之比,A 项
湖北省新高考联考协作体*化学参考答案(共8页)第 3 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}vB0.06mol Ls0.0660mol Lmin3.6mol Lmin,
B
项4vAvB0.6mol Lmin,C 项4vCvB1.6mol Lmin,生成物D是固态,
浓度是定值,不能用D表示速率;故选A。
11. 【答案】C
【解析】
A.K只与温度有关,温度不变,则K值不变,A错误;
B.容器a、b的体积分别为2L和1L,容器b的体积小,则浓度大,反应速率快,达到平衡
所用时间短,则达到平衡所用时间:容器a>容器b,B错误;
0.6mol
C.0~1min内,容器b中
v(CO) 1L 0.6molL1min1
,化学反应速率之比等于化学计
1min
量数之比,则v(H )1.2molL1min1,C正确;
2
D.5min时,容器a中已达到平衡,反应速率:v v ,D错误;
正 逆
故选C。
12. 【答案】D
【解析】由第二组和第四组数据,A浓度相同,B浓度不同,速率相等,可知n=0,再由第
0.50
3.2×10-3
一组和第二组数据代入v=k×cm(A)×cn(B)可得( )m= ,可知m=1;将第一组数据代入
0.25 1.6×10-3
计算,可得k=6.4×10-3,则v=k×c(A)×c0(B)=6.4×c(A)×10-3。当速率为4.8×10-3mol·L-1·min-1
时,由上述可知c =0.75mol/L,c(A)=1mol/L时速率为6.4×10-3mol·L-1·min-1,A正确;速率
1
常数k=6.4×10-3,B正确;存在过量的B时,反应掉93.75%的A可以看作经历4个半衰期,即
4×0.8
50%+25%+12.5%+6.25%,因此所需的时间为 =500min,C正确;速率常数与浓
6.4×10-3min-1
度无关,缩小容积(加压)不会使k增大,D错误。
13. 【答案】B
【解析】催化剂能改变反应的途径,降低反应活化能,加快反应速率,A正确; 反应的活化
能越大,反应速率越慢,化学反应的速率取决于最慢的一步,由图可知,C H 转化为C H* 时
4 10 4 10
的活化能最大,则该历程中决速步骤为C H ===C H* ,B错误;由图可知,该反应的化学方程
4 10 4 10
式为C H →C H +H ,反应中有氢氢非极性键形成,C正确;由图可知,反应的热化学方程式
4 10 4 8 2
为C H (g)===C H (g)+H (g) ΔH=+0.06N eV,D正确。
4 10 4 8 2 A
湖北省新高考联考协作体*化学参考答案(共8页)第 4 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}14. 【答案】C
【解析】
A.化学反应速率之比等于化学计量数之比,根据图可知,v(A)=3v(D),故A错误;
B.根据图像可知,反应达平衡状态,A物质增加1.2mol、D物质增加0.4mol、B物质减少
0.6mol、C物质减少0.8mol,根据反应系数之比等于其物质的量变化之比,且反应物未消耗
完全,则该反应的化学方程式为3B4C6A2D ,故B错误;
0.6mol
C.6s内,B物质消耗0.6mol,则B的平均反应速率:v= =0.05 mol/(L·s),故C正确;
2L6s
D.反应进行到6s时,反应达平衡状态,各物质速率之比等于化学计量数之比,化学计量数
不同,则各物质的反应速率不相等,故D错误;
故答案为:C。
15. 【答案】A
【分析】溶液a中通入SO ,转化为溶液b,化学方程式为Fe (SO ) +SO +2H O=2FeSO
2 2 4 3 2 2 4
+2H SO ;溶液b中通入空气,转化为溶液c,化学方程式为4FeSO +O +2H SO =2Fe (SO )
2 4 4 2 2 4 2 4 3
+2H O。
2
【解析】
A.由分析可知,操作I中Fe3+ 氧化SO ,发生反应的离子方程式为2Fe3++SO +2H O=
2 2 2
2Fe2++SO 2-+4H+;A正确;
4
B.溶液b中,阳离子有Fe2+、H+,可能含有Fe3+,B错误;
C.溶液a转化为溶液b的过程中,SO 转化为H SO ,SO 失电子被氧化,C错误;
2 2 4 2
D.由分析可以看出,溶液c中含有Fe (SO ) 、H SO ,加入FeO后,FeO和H SO 反应会
2 4 3 2 4 2 4
生成FeSO ,D错误;
4
故答案为:A。
二、非选择题(本大题共 4 小题,共 55 分)
16. (15分,除标注外,每空2分)
(1)ad(2分)
(2)负(1分) 2NH -6e-+6OH-=N +6H O(2分)
3 2 2
(3)<(1分) N 和H 反应是可逆反应,转化率要低于100%,因此放出的热量要小于92kJ(1分)
2 2
(4)①0.004mol·L-1·s-1(2分) 87.5%(2分) 1400(2分) ②随着反应进行,反应物浓度
逐渐减小(2分)
湖北省新高考联考协作体*化学参考答案(共8页)第 5 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}【解析】
(1)a.该反应前后化学计量数不相等,容器内压强不再随时间而发生变化,反应达到平衡,a
正确;b.反应速率vNH =vN ,不能判断正逆反应进行方向,无法判断反应是否达到平衡,
3 2
b错误;c.容器内各物质的物质的量之比等于化学计量数之比,不能判断反应达到平衡,c错误;
d. 容器内N 的物质的量分数不再随时间而发生变化,说明其浓度不变,反应达到平衡,d正确;
2
e.有12molN-H键断裂的同时生成5molN≡N键,均表示正反应速率,不能判断反应达到平衡,e
错误;f.混合气体的密度为定值,密度不随时间的变化而变化,不能判断反应达到平衡,f错误;
故选ad。
(2)M电极氨气转化为氮气,氮元素化合价升高,失去电子,为负极,N电极NO转化为氮气,
化合价降低,得到电子,为正极,N电极上发生的电极反应为2NO+4e-+2H O=N +4OH-,M电极
2 2
上发生的电极反应为2NH -6e-+6OH-=N +6H O。
3 2 2
(3)氮气和氢气反应生成氨气的反应为可逆反应,取1molN 和3molH 放在一密闭容器中,在
2 2
催化剂存在时进行反应,测得反应放出的热量总小于92kJ(理论消耗1molN 放出92kJ的热量),
2
其原因是N 和H 反应是可逆反应,转化率要低于100%,因此放出的热量要小于92kJ。
2 2
(4)① 用 N O 表 示 0~2s 内 该 反 应 的 平 均 速 率 v(N O )=
2 4 2 4
1 1 0.040mol-0.008mol
v(NO ) 0.004mol/(Lgs) , 在 第 5s 时 , NO 的 转 化 率 为
2 2 2 2L2s 2
0.0400.005
100%87.5%;用平衡时浓度,根据公式计算K=1400。
0.040
②浓度减小,速率减慢,根据上表可以看出,随着反应的进行,反应速率逐渐减小,其原因
是随着反应进行,反应物浓度逐渐减小。
17. (10分,每空2分)
(1)b
催化剂
(2)4NH +5O 4NO+6H O
3 2 2
Δ
(3)分离液态空气得到的氮气用于合成氨,得到的氧气用于氨的催化氧化
(4)①
催化剂
②4NH 6NO 5N 6H O
3 2 2
湖北省新高考联考协作体*化学参考答案(共8页)第 6 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}18. (15分,除标注外,每空2分)
(1)玻璃搅拌器 (1分)
(2)偏大 不盖杯盖会有一部分热量散失,但中和热焓变是负值,反应热(ΔH)将偏大
(3)相等
(4)偏小
(5)-55.2kJ/mol 偏大
(6)a
【详解】
(1)根据量热计的构造可知,该装置缺少的仪器是玻璃搅拌器,其作用是搅拌,使强酸和强碱
充分反应,故答案为:玻璃搅拌器;
(2)简易量热计如果不盖杯盖,热量损耗大,测得数值将偏小,中和热ΔH为负值,即反应热
(ΔH)将偏大,故答案为:偏大;不盖杯盖会有一部分热量散失,但中和热焓变是负值,反应
热(ΔH)将偏大;
(3)反应放出的热量和所用酸以及碱的用量成正比,改用 80mL0.50mol•L-1 的盐酸和
80mL0.55mol•L-1的NaOH溶液进行反应,与上述实验相比,生成水的量减少,所放出的热量减
少,即不相等,但二者所求中和热数据相等,故答案为:相等;
(4)氨水是弱电解质,电离吸热,用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测
得中和反应的中和热的数值与57.3kJ•mol-1相比较会偏小;
(5)若0.50mol/L盐酸和0.55mol/LNaOH溶液的密度都是1g/cm3,反应后生成的溶液比热容
c=4.18J/(g·℃),用80mL0.50mol·L-1盐酸和80mL0.55mol·L-1NaOH溶液进行4次实验测得反应前
后的温度差值为 3.4℃、3.3℃、4.7℃、3.2℃,第三组实验数据明显误差舍去,平均温差为:
3.4℃+3.3℃+3.2℃
=3.3℃,生成 H O 的物质的量为:0.08L×0.50mol/L=0.04mol,则得中和热
2
3
1604.183.3103
ΔH=- =-55.176kJ/mol,与默认中和热ΔH=-57.3kJ/mol 比较偏大,故答案为:
0.04
-55.2kJ/mol;偏大;
(6)a.若用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平,否则俯视或仰视都会造
成测量结果出现误差,a正确;
b.量筒中残留液体为标定以外的体积,则将用量筒量取好的稀盐酸加入内筒后,快速用水
冲洗量筒内壁剩余的稀盐酸至内筒中会使HCl的物质的量偏大,导致测量结果偏高,b错误;
c.缓慢而匀速地加入会造成热量散失,导致测定结果误差较大,c错误;
湖北省新高考联考协作体*化学参考答案(共8页)第 7 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}d.内筒洗净后,未及时烘干,直接用该内筒进行实验会导致混合溶液总质量偏大,最高温
度值偏低,所测放热量少,中和热ΔH偏大,d错误;
故答案为:a。
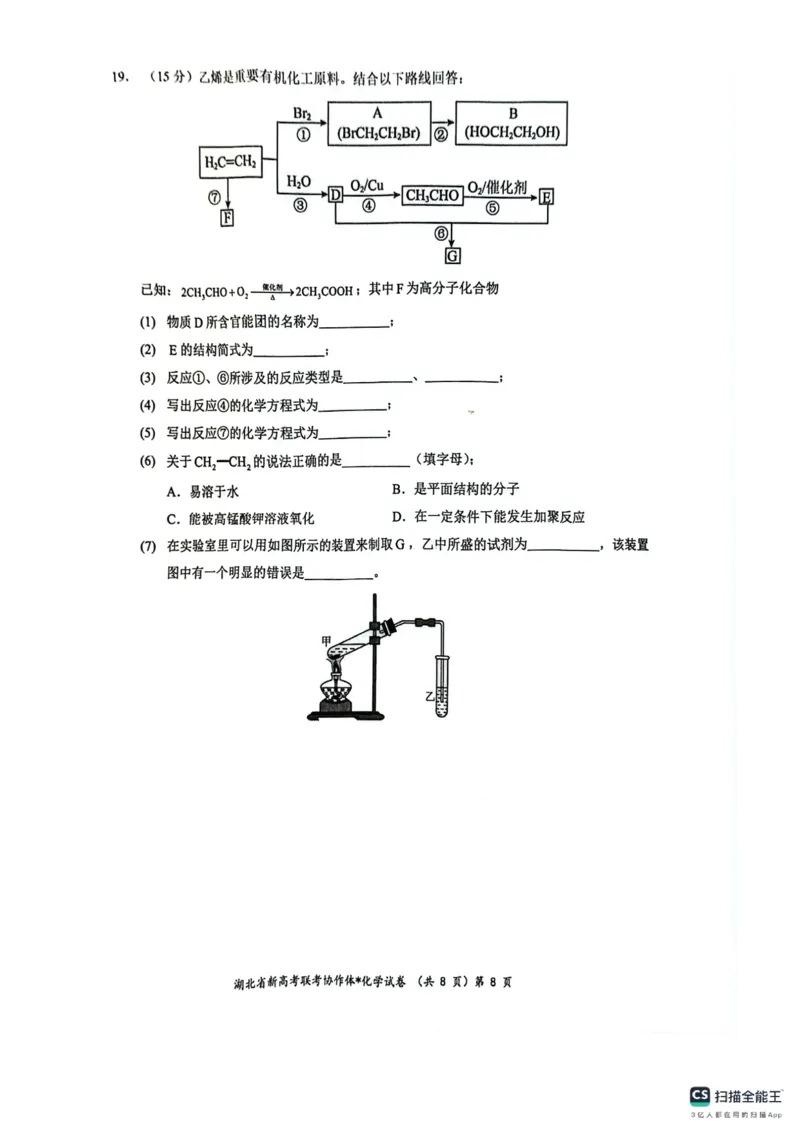
19. (15分,除标注外,每空2分)
(1)羟基(1分)
(2)CH COOH(2分)
3
(3)加成反应 (1分) 酯化反应或(取代反应)(1分)
(4)2CH CH OH+O Cu2CH CHO+2H O(2分)
3 2 2 Δ 3 2
(5)nCH =CH 一定条件 (2分)
2 2
(6)BCD(2分)
(7)饱和碳酸钠溶液(2分) 导气管的出口伸入到了液面以下(2分)
【分析】乙烯和水发生加成反应生成乙醇,D是CH CH OH;乙醇发生催化氧化生成乙醛,
3 2
乙醛氧化为乙酸,E是CH COOH,乙醇和乙酸发生酯化反应生成乙酸乙酯,G是CH COOCH CH ;
3 3 2 3
乙烯发生加聚反应生成高分子化合物聚乙烯,F是聚乙烯 。
【解析】
(1)根据物质D的结构简式,可知所含官能团的名称为羟基;
(2)乙烯和水发生加成反应生成乙醇,D是CH CH OH,E为CH COOH
3 2 3
(3)反应①是乙烯和溴发生加成反应生成1,2-二溴乙烷,反应类型是加成反应;⑥是乙醇和乙
酸发生酯化反应生成乙酸乙酯和水,反应类型是取代反应(酯化反应);
(4) 反 应 ④ 是 乙 醇 发 生 催 化 氧 化 生 成 乙 醛 和 水 , 反 应 的 化 学 方 程 式 为
2CH CH OH+O Cu2CH CHO+2H O;
3 2 2 Δ 3 2
(5)反应⑦是乙烯发生加聚反应生成高分子化合物聚乙烯,反应的化学方程式为
nCH =CH 一定条件 ;
2 2
(6)A. 乙烯难溶于水,故A错误;B.CH =CH 是平面结构的分子,6个原子共平面,故B正
2 2
确;C.CH =CH 含有碳碳双键,能被高锰酸钾溶液氧化,故C正确;D.CH =CH 含有碳碳双键,
2 2 2 2
在一定条件下能发生加聚反应生成聚乙烯,故D正确;选BCD。
(7)饱和碳酸钠溶液能降低乙酸乙酯的溶解度,溶解乙醇,中和乙酸,乙试管中收集乙酸乙酯,
湖北省新高考联考协作体*化学参考答案(共8页)第 8 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}所盛的试剂为饱和碳酸钠溶液,为防止倒吸,导气管的出口应在液面以上,该装置图中有一个明
显的错误是导气管的出口伸入到了液面以下。
湖北省新高考联考协作体*化学参考答案(共8页)第 9 页
{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}{#{QQABaYKQogioAJBAABgCAwXKCEOQkAEACQgOQAAIsAAAgRFABAA=}#}