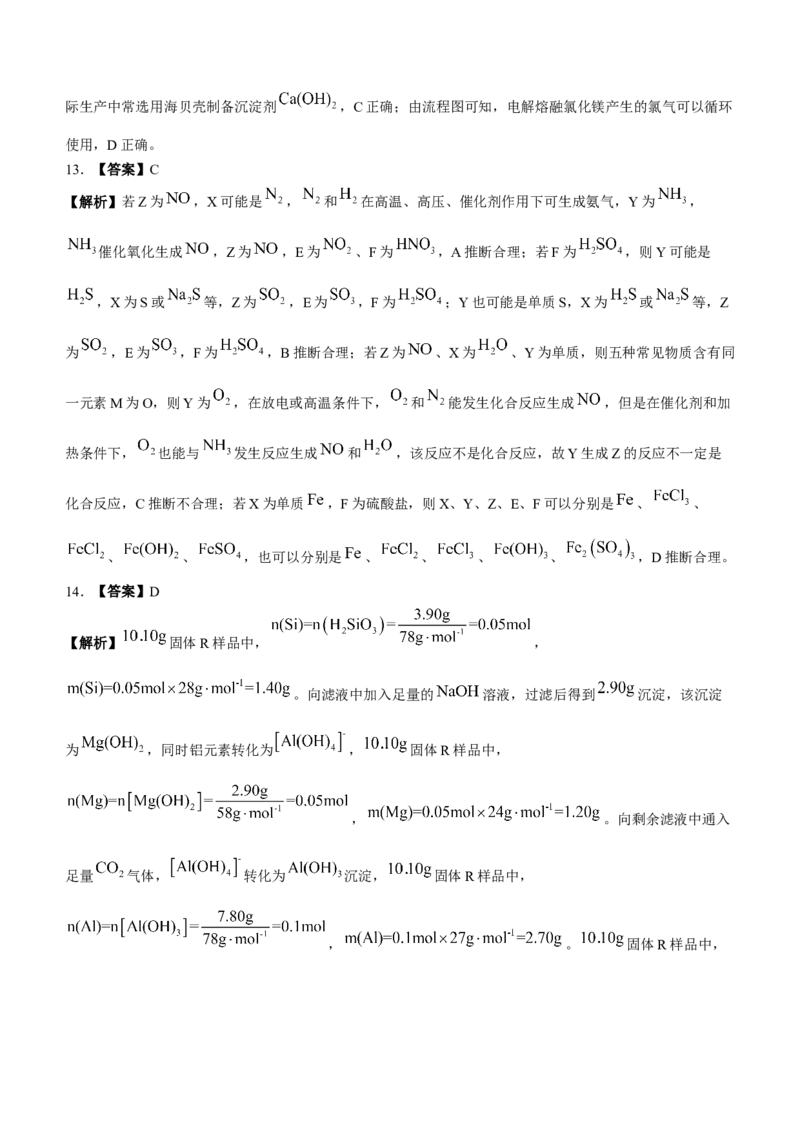文档内容
2025 年普通高等学校全国统一模拟招生考试
金科·新未来 10 月联考
化学
全卷满分100分,考试时间75分钟。
注意事项:
1,答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上的
指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题
区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
符合题目要求。
1.为我国化工事业的发展作出了卓越贡献,是我国近代化学工业的奠基人之一的化工专家是( )
A.侯德榜 B.袁隆平 C.屠呦呦 D.徐光宪
2.关于实验室安全,下列表述错误的是( )
A.具有 标识的化学品为爆炸类物质,实验时不准敲击、摩擦和挤压
B.在做钠在空气中燃烧的实验过程中,移动坩埚时应使用坩埚钳夹取
C.不慎将苯酚沾到皮肤上,应立即用 溶液冲洗,再用水冲洗
D.氯气有毒,有关氯气性质的实验要在通风橱中进行
3.化学材料的使用对人类生活质量的提高和科技的发展有重要作用。下列说法错误的是( )
A.彩色玻璃是制玻璃过程中加入一些金属氧化物或盐制得的,可用于建筑和装饰
B.新型陶瓷碳化硅能承受比较高的温度,可用作耐高温结构材料、耐高温半导体材料
C.橡胶消声瓦可有效降低潜艇航行时的噪声,天然橡胶的主要成分是异戊二烯
D.有机玻璃为聚甲基丙烯酸甲酯,其透光性好,易加工,可制成飞机和车辆的风挡
4.氮化硅 可由石英与焦炭在高温的氮气流中通过以下反应制取:
。 为阿伏加德罗常数的值,下列说法错误的是( )
学科网(北京)股份有限公司A. 中所含电子的数目为
B. 参与该反应,理论上转移电子的数目为
C.常温常压下, 和 的混合气体中所含的原子数为
D. 中含 键的数目为
5.邻二苯酚(化合物M)制备2,4-己二烯二酸单甲酯(化合物L)的合成路线如下。下列说法正确的是(
)
A.物质的量相等的M和L分别与足量的氢气发生加成反应,消耗氢气的量相等
B.M中有2种官能团,L中有3种官能团
C.M的含有苯环的同分异构体还有2种,L能发生加聚反应
D.鉴别1,6-己二醇 和L可以用酸性高锰酸钾溶液
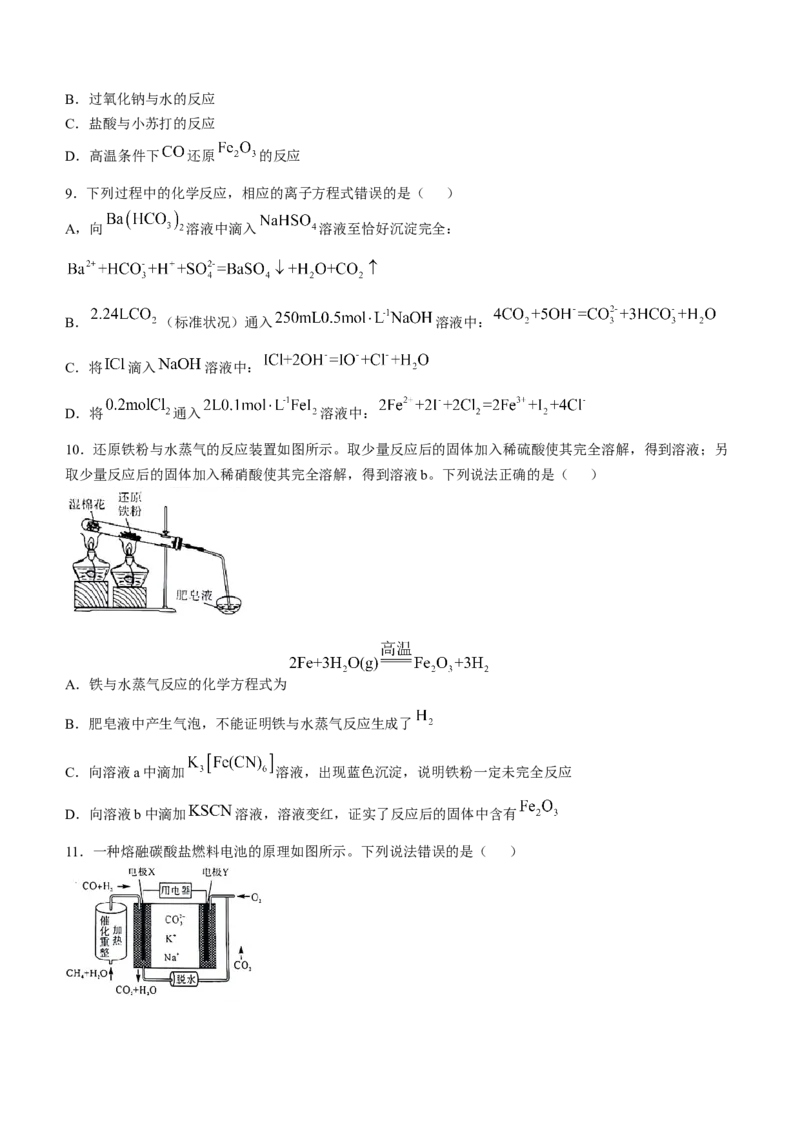
6.下列有关实验原理、装置、操作或结论的描述中,正确的是( )
D.用硫酸吸收氨气
A.实验室制备 B.分离 与 溶液反 C.验证 和的热
应生成的碘 稳定性
A.A B.B C.C D.D
7.X、Y、Z、W为原子序数依次增大的短周期主族元素,单质 可用作粮仓中的粮食保护气,Y、Z原子
的最外层电子数之和等于W原子的最外层电子数,Z原子的核外电子总数是W原子的最外层电子数的2倍,
Y、Z、W处于同一周期,Z的氧化物可用来生产光导纤维。下列说法错误的是( )
A.原子半径: B.简单氢化物的稳定性: 、
C.最高正化合价: D.最高价氧化物对应的水化物的酸性:
8.下列反应为放热反应的是( )
A.将 晶体与 晶体放入烧杯中,用玻璃棒搅拌
学科网(北京)股份有限公司B.过氧化钠与水的反应
C.盐酸与小苏打的反应
D.高温条件下 还原 的反应
9.下列过程中的化学反应,相应的离子方程式错误的是( )
A,向 溶液中滴入 溶液至恰好沉淀完全:
B. (标准状况)通入 溶液中:
C.将 滴入 溶液中:
D.将 通入 溶液中:
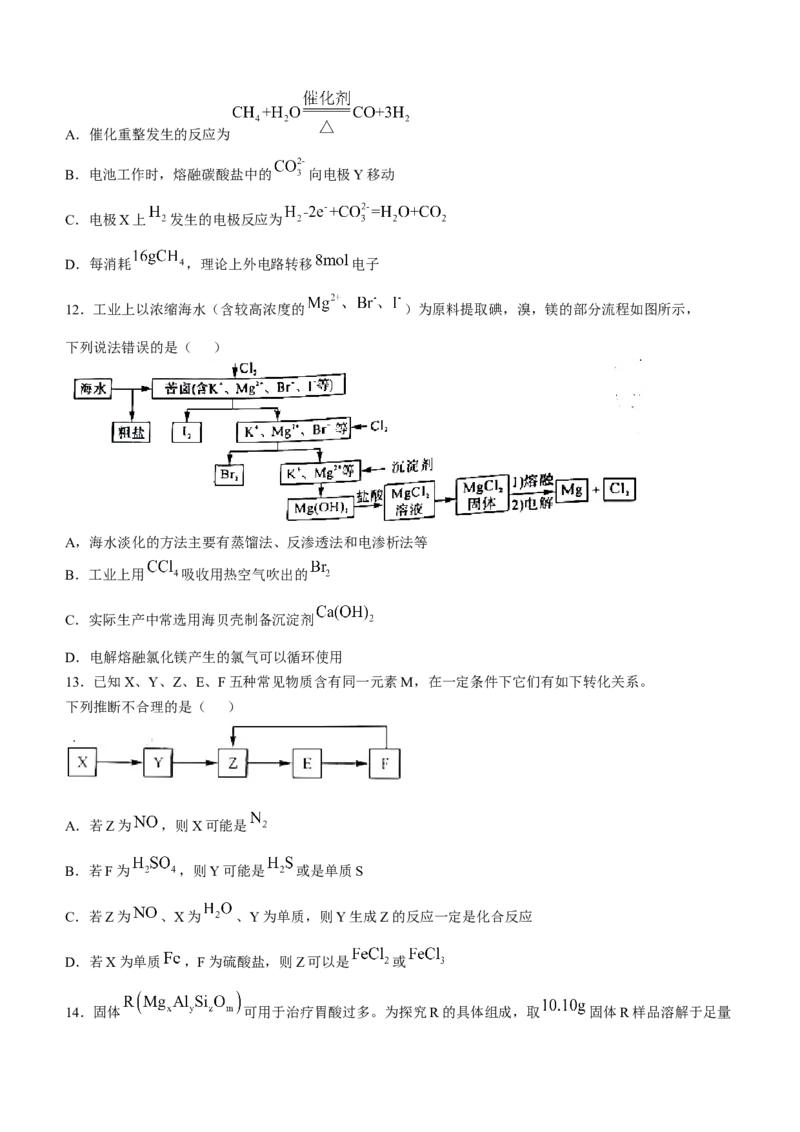
10.还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解,得到溶液;另
取少量反应后的固体加入稀硝酸使其完全溶解,得到溶液b。下列说法正确的是( )
A.铁与水蒸气反应的化学方程式为
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成了
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉一定未完全反应
D.向溶液b中滴加 溶液,溶液变红,证实了反应后的固体中含有
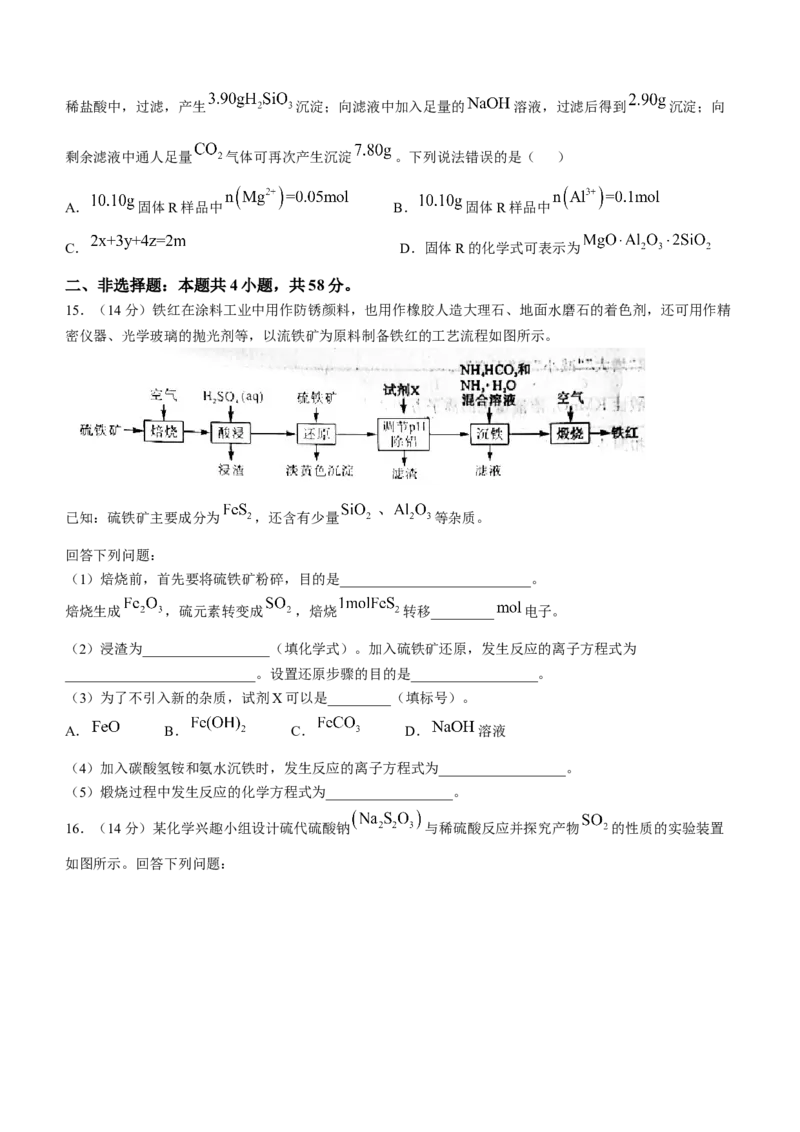
11.一种熔融碳酸盐燃料电池的原理如图所示。下列说法错误的是( )
学科网(北京)股份有限公司A.催化重整发生的反应为
B.电池工作时,熔融碳酸盐中的 向电极Y移动
C.电极X上 发生的电极反应为
D.每消耗 ,理论上外电路转移 电子
12.工业上以浓缩海水(含较高浓度的 )为原料提取碘,溴,镁的部分流程如图所示,
下列说法错误的是( )
A,海水淡化的方法主要有蒸馏法、反渗透法和电渗析法等
B.工业上用 吸收用热空气吹出的
C.实际生产中常选用海贝壳制备沉淀剂
D.电解熔融氯化镁产生的氯气可以循环使用
13.已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系。
下列推断不合理的是( )
A.若Z为 ,则X可能是
B.若F为 ,则Y可能是 或是单质S
C.若Z为 、X为 、Y为单质,则Y生成Z的反应一定是化合反应
D.若X为单质 ,F为硫酸盐,则Z可以是 或
14.固体 可用于治疗胃酸过多。为探究R的具体组成,取 固体R样品溶解于足量
学科网(北京)股份有限公司稀盐酸中,过滤,产生 沉淀;向滤液中加入足量的 溶液,过滤后得到 沉淀;向
剩余滤液中通人足量 气体可再次产生沉淀 。下列说法错误的是( )
A. 固体R样品中 B. 固体R样品中
C. D.固体R的化学式可表示为
二、非选择题:本题共4小题,共58分。
15.(14分)铁红在涂料工业中用作防锈颜料,也用作橡胶人造大理石、地面水磨石的着色剂,还可用作精
密仪器、光学玻璃的抛光剂等,以流铁矿为原料制备铁红的工艺流程如图所示。
已知:硫铁矿主要成分为 ,还含有少量 等杂质。
回答下列问题:
(1)焙烧前,首先要将硫铁矿粉碎,目的是___________________________。
焙烧生成 ,硫元素转变成 ,焙烧 转移_________ 电子。
(2)浸渣为__________________(填化学式)。加入硫铁矿还原,发生反应的离子方程式为
___________________________。设置还原步骤的目的是__________________。
(3)为了不引入新的杂质,试剂X可以是_________(填标号)。
A. B. C. D. 溶液
(4)加入碳酸氢铵和氨水沉铁时,发生反应的离子方程式为__________________。
(5)煅烧过程中发生反应的化学方程式为__________________。
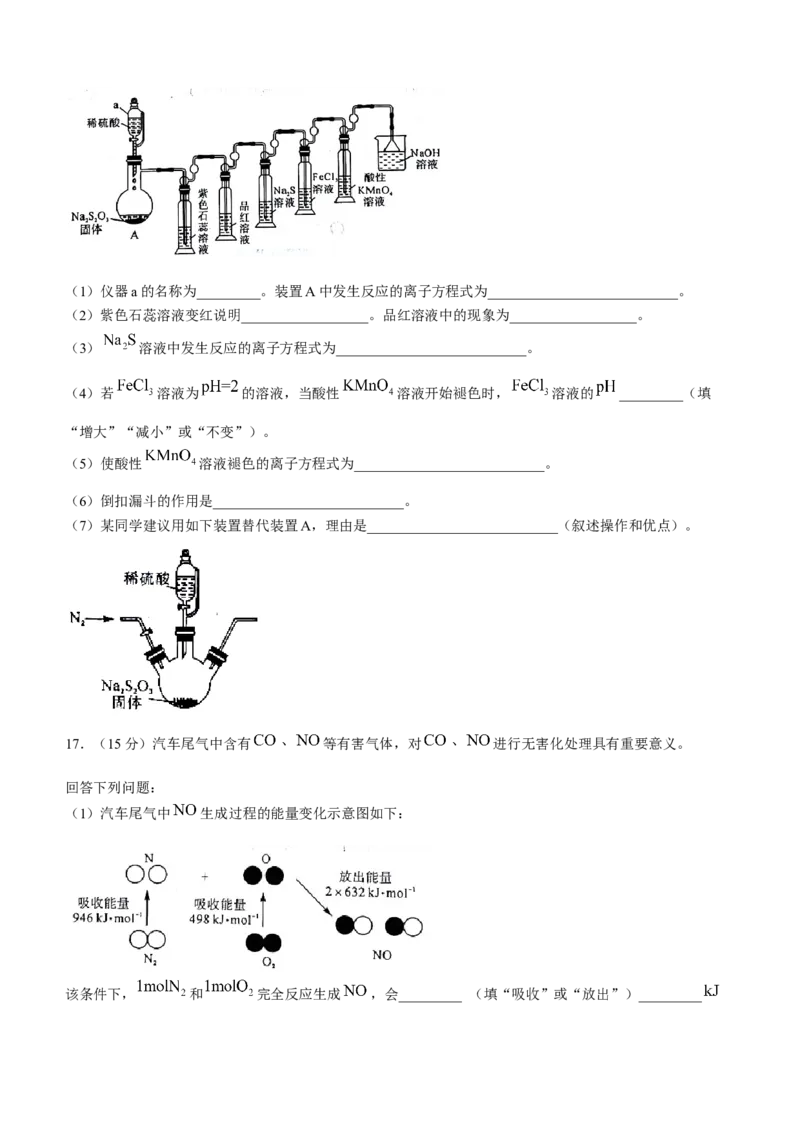
16.(14分)某化学兴趣小组设计硫代硫酸钠 与稀硫酸反应并探究产物 的性质的实验装置
如图所示。回答下列问题:
学科网(北京)股份有限公司(1)仪器a的名称为_________。装置A中发生反应的离子方程式为___________________________。
(2)紫色石蕊溶液变红说明__________________。品红溶液中的现象为__________________。
(3) 溶液中发生反应的离子方程式为___________________________。
(4)若 溶液为 的溶液,当酸性 溶液开始褪色时, 溶液的 _________(填
“增大”“减小”或“不变”)。
(5)使酸性 溶液褪色的离子方程式为___________________________。
(6)倒扣漏斗的作用是___________________________。
(7)某同学建议用如下装置替代装置A,理由是___________________________(叙述操作和优点)。
17.(15分)汽车尾气中含有 等有害气体,对 进行无害化处理具有重要意义。
回答下列问题:
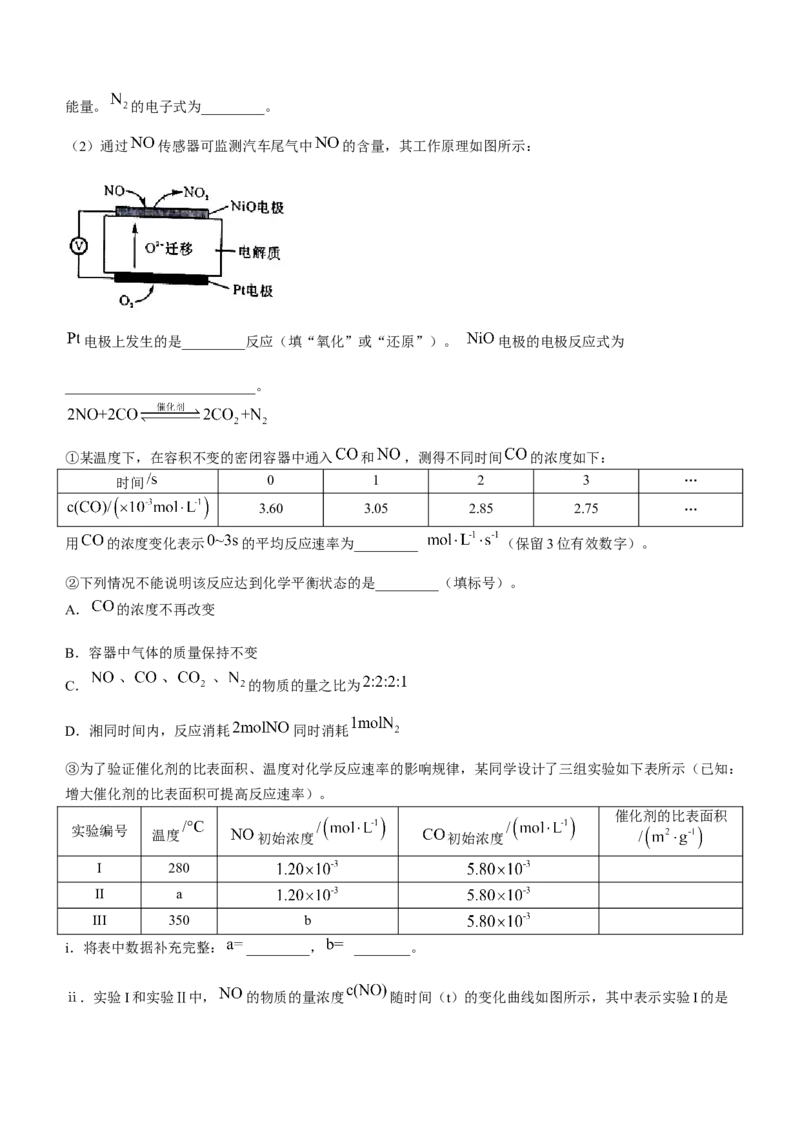
(1)汽车尾气中 生成过程的能量变化示意图如下:
该条件下, 和 完全反应生成 ,会_________ (填“吸收”或“放出”)_________
学科网(北京)股份有限公司能量。 的电子式为_________。
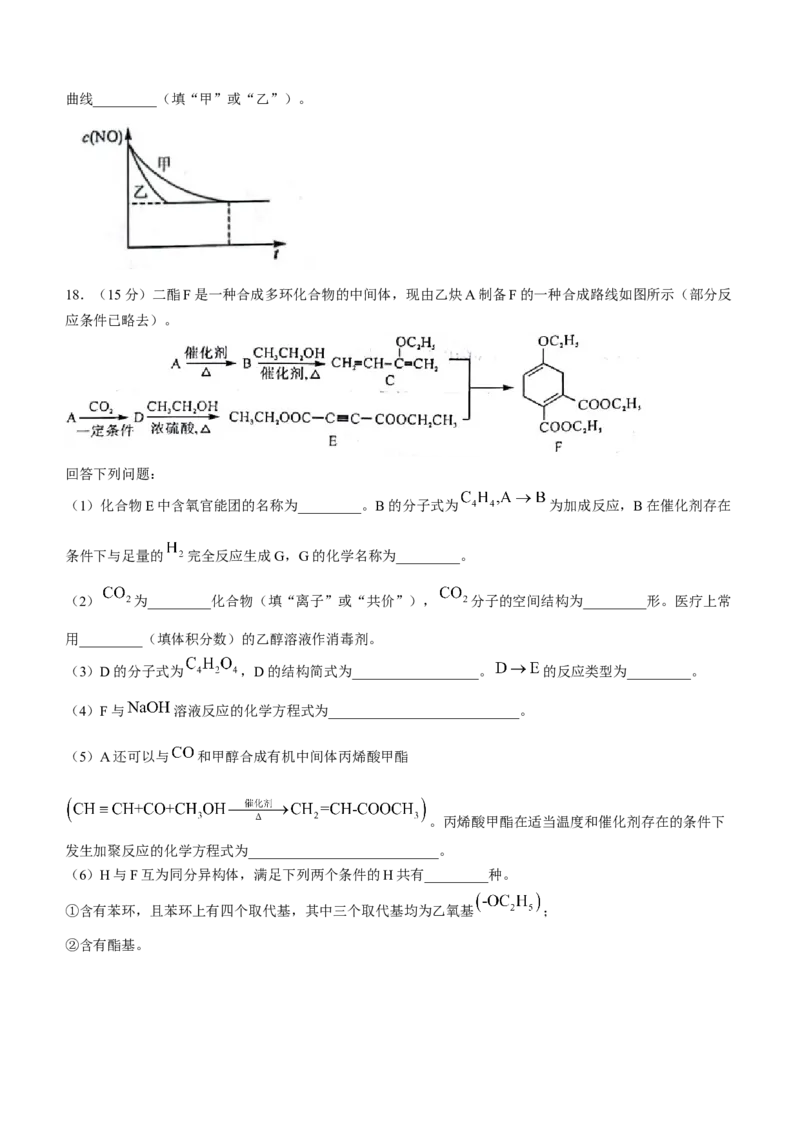
(2)通过 传感器可监测汽车尾气中 的含量,其工作原理如图所示:
电极上发生的是_________反应(填“氧化”或“还原”)。 电极的电极反应式为
___________________________。
①某温度下,在容积不变的密闭容器中通入 和 ,测得不同时间 的浓度如下:
时间 0 1 2 3 …
3.60 3.05 2.85 2.75 …
用 的浓度变化表示 的平均反应速率为_________ (保留3位有效数字)。
②下列情况不能说明该反应达到化学平衡状态的是_________(填标号)。
A. 的浓度不再改变
B.容器中气体的质量保持不变
C. 的物质的量之比为
D.湘同时间内,反应消耗 同时消耗
③为了验证催化剂的比表面积、温度对化学反应速率的影响规律,某同学设计了三组实验如下表所示(已知:
增大催化剂的比表面积可提高反应速率)。
催化剂的比表面积
实验编号
温度 初始浓度 初始浓度
I 280
II a
III 350 b
i.将表中数据补充完整: _________, ________。
ⅱ.实验I和实验Ⅱ中, 的物质的量浓度 随时间(t)的变化曲线如图所示,其中表示实验I的是
学科网(北京)股份有限公司曲线_________(填“甲”或“乙”)。
18.(15分)二酯F是一种合成多环化合物的中间体,现由乙炔A制备F的一种合成路线如图所示(部分反
应条件已略去)。
回答下列问题:
(1)化合物E中含氧官能团的名称为_________。B的分子式为 为加成反应,B在催化剂存在
条件下与足量的 完全反应生成G,G的化学名称为_________。
(2) 为_________化合物(填“离子”或“共价”), 分子的空间结构为_________形。医疗上常
用_________(填体积分数)的乙醇溶液作消毒剂。
(3)D的分子式为 ,D的结构简式为__________________。 的反应类型为_________。
(4)F与 溶液反应的化学方程式为___________________________。
(5)A还可以与 和甲醇合成有机中间体丙烯酸甲酯
。丙烯酸甲酯在适当温度和催化剂存在的条件下
发生加聚反应的化学方程式为___________________________。
(6)H与F互为同分异构体,满足下列两个条件的H共有_________种。
①含有苯环,且苯环上有四个取代基,其中三个取代基均为乙氧基 ;
②含有酯基。
学科网(北京)股份有限公司金科大联考·2025 届高三 10 月质量检测·化学
参考答案、提示及评分细则
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 A C C B C D D B D B B B C D
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
符合题目要求。
1.【答案】A
【解析】化工专家侯德榜发明了联合制碱法,对世界制碱工业作出了巨大贡献,是我国近代化学工业的奠基
人之一,A符合题意;袁隆平是杂交水稻之父,2001年,获得首届国家最高科学技术奖,B不符合题意;女
科学家屠呦呦发现了一种可用于治疗疟疾的药物——青蒿素(分子式为 ),2015年10月屠呦呦获
得诺贝尔生理医学奖,C不符合题意;“稀土之父”徐光宪化学家提出了稀土串级萃取理论,其基本操作是
利用有机络合剂把稀土离子从水相富集到有机相再进行分离,荣获了2008年度国家最高科学技术奖,D不符
合题意。
2.【答案】C
【解析】爆炸类物质实验时,不准敲击、摩擦和挤压,A正确;在做钠在空气中燃烧的实验过程中,移动坩
埚时应使用坩埚钳夹取,以防烫伤,B正确;苯酚有毒,对皮肤有腐蚀性, 溶液对皮肤也有腐蚀性,
不慎将苯酚沾到皮肤上,应立即用乙醇冲洗,再用水冲洗,C错误;氯气有毒,有关氯气性质的实验要在通
风橱中进行,防止发生中毒,D正确。
3.【答案】C
【解析】金属氧化物或盐可以使玻璃呈现不同的颜色,故制玻璃过程中加入一些金属氧化物或盐可制得彩色
玻璃,彩色玻璃可用于建筑和装饰,A正确;新型陶瓷 具有优异的高温抗氧化性能,使用温度可达
,可用作耐高温结构材料、耐高温半导体材料,B正确;天然橡胶的主要成分是聚异戊二烯,C错
误;有机玻璃透光性好,易加工,可制成飞机和车辆的风挡,D正确。
4.【答案】B
【解析】1个 中含有 个电子, 中所含电子的数日为 ,A正确;没
有指出是标准状况,故不能用标准状况下的气体摩尔体积进行相关计算,B错误; 和 的摩尔质量均为
,且两者都是双原子分子, 和 的混合气体的物质的量为 ,所含的原子数为 ,
C正确;在 中, 和O构成了硅氧四面体,每个 结合4个O, 在中心,O在四面体的4个顶角,
学科网(北京)股份有限公司许多这样的四面体通过顶角的O相互连接,每个O为两个四面体所共有,与2个 相结合,故 中
含 键的数目为 ,D正确。
5.【答案】C
【解析】 与足量的氢气发生加成反应消耗 , 与足量的氢气发生加成反应消耗
,故物质的量相等的M和L分别与足量的氢气发生加成反应,消耗氢气的量不相等,A错误;M
中只有1种官能团,B错误;M的含有苯环的同分异构体还有两个羟基相间和两个羟基相对2种,L中含有
碳碳双键,L能发生加聚反应,C正确;1,6-己二醇中的羟基、L中的碳碳双键均能被酸性高锰酸钾溶液氧
化,而使酸性高锰酸钾溶液褪色,故酸性高锰酸钾溶液不能鉴别1,6-己二醇和L,D错误。
6.【答案】D
【解析】制备 ,不能用硫酸,否则生成的微溶物 会覆盖在 上,阻止反应进一步发生,不
能达到实验目的,A错误;应采用萃取、分液、蒸馏的方法得到 ,B错误; 受热易分解,
受热不分解,大试管的温度高,故小试管中应盛装 ,大试管中应盛装 ,C错误;
硫酸能吸收氨气,氨气不溶于 ,能防止倒吸,D正确。
7.【答案】D
【解析】根据题意可知,元素X、Y、Z、W分别为 。原子半径: ,A正确;
简单氢化物的稳定性: ,B正确;最高正化合价: ,C正确;最高价氧化物对应的
水化物的酸性: ,D错误。
8.【答案】B
【解析】 晶体与 晶体的反应是吸热反应,A不符合题意;过氧化钠与水的反应是放
热反应,B符合题意;盐酸与小苏打的反应是吸热反应,C不符合题意;高温条件下 还原 的反应
是吸热反应,D不符合题意。
9.【答案】D
【解析】沉淀完全时, 与 的物质的量之比为 ,即 与 的物质的量比为 ,
离子方程式为 ,A正确;标准状况下, 的物
学科网(北京)股份有限公司质的量为 , 溶液中溶质 的物质的量为 ,
,反应的离子方程式为 ,B正确; 与
的反应为非氧化还原反应,离子方程式为 ,C正确;还原性: ,
氯气先氧化碘离子,后氧化亚铁离子, 和 反应时,氯气与碘离子恰好完全反应,离
子方程式为 ,D错误。
10.【答案】B
【解析】 与水蒸气反应生成四氧化三铁和氢气,化学方程式为 ,A错误;
肥皂液中产生气泡,只能说明有气体从导管中冒出,不能说明反应生成了氢气,B正确;向溶液中滴加
溶液,出现蓝色沉淀,说明溶液a中含有 ,但不能确定 是来自剩余的铁粉还是反应
后生成的 ,C错误;向溶液b中滴加 溶液,溶液变红,说明溶液b中含有 ,由于溶液b是
反应后的固体加入稀硝酸溶解得到的,稀硝酸有强氧化性,即使反应后的固体中不含有三价铁而含有二价铁,
稀硝酸也能将二价铁氧化成三价铁,D错误。
11.【答案】B
【解析】根据装置图可知,催化重整发生的反应为 ,A正确;电极X通入的
气体是 和 ,电极X为负极,电池工作时,熔融碳酸盐中的 向电极X移动,B错误;电极X上
发生的电极反应为 ,C正确;催化重整时,每消耗 (即 ) ,同
时生成 和 , 和 在电极X上放电生成 和 ,故理论上外电路转移 电
子,D正确。
12.【答案】B
【解析】海水淡化的方法主要有蒸馏法、反渗透法和电渗析法等,A正确;工业上用二氧化硫水溶液吸收用
热空气吹出的 ,使 转化为氢溴酸,达到与空气分离的目的,再用氯气将氢溴酸氧化为溴后蒸馏分离,
B错误;海贝壳的主要成分为 ,高温下分解生成 , 与水反应生成沉淀剂 ,故实
学科网(北京)股份有限公司际生产中常选用海贝壳制备沉淀剂 ,C正确;由流程图可知,电解熔融氯化镁产生的氯气可以循环
使用,D正确。
13.【答案】C
【解析】若Z为 ,X可能是 , 和 在高温、高压、催化剂作用下可生成氨气,Y为 ,
催化氧化生成 ,Z为 ,E为 、F为 ,A推断合理;若F为 ,则Y可能是
,X为S或 等,Z为 ,E为 ,F为 ;Y也可能是单质S,X为 或 等,Z
为 ,E为 ,F为 ,B推断合理;若Z为 、X为 、Y为单质,则五种常见物质含有同
一元素M为O,则Y为 ,在放电或高温条件下, 和 能发生化合反应生成 ,但是在催化剂和加
热条件下, 也能与 发生反应生成 和 ,该反应不是化合反应,故Y生成Z的反应不一定是
化合反应,C推断不合理;若X为单质 ,F为硫酸盐,则X、Y、Z、E、F可以分别是 、 、
、 、 ,也可以分别是 、 、 、 、 ,D推断合理。
14.【答案】D
【解析】 固体R样品中, ,
。向滤液中加入足量的 溶液,过滤后得到 沉淀,该沉淀
为 ,同时铝元素转化为 , 固体R样品中,
, 。向剩余滤液中通入
足量 气体, 转化为 沉淀, 固体R样品中,
, 。 固体R样品中,
学科网(北京)股份有限公司, 。
,即R为 。根据分析可知, 固体R样品中
,A正确; 固体R样品中 ,B正确;正负化合价的代数和等于
0,即 ,C正确;固体R的化学式 可表示为 ,D错误。
二、非选择题:本题共4小题,共58分。
15.【答案及评分细则】(14分)
(1)增大固体与空气接触的表面积,使硫铁矿焙烧充分(1分)11(2分)
(2) (1分) (2分)
将 还原为 ,有利于后续 的去除(2分)
(3)ABC(2分。少选且正确的,给1分;选错或四个选项全选的,不给分)
(4) (2分。将 写成 ,扣1分)
(5) (2分)
【解析】(1)焙烧时, 与 发生反应的化学方程式为 ,根据关系
式 ~转移 可知,焙烧 转移 电子。
16.【答案及评分细则】(14分)
(1)恒压滴液漏斗(1分) (2分)
(2) 的水溶液显酸性(1分) 品红褪色(1分)
(3) (2分。写成 ,同样给分)
(4)减小(2分)
(5) (2分)
(6)防止倒吸(1分)
(7)实验完毕后,打开通氮气的旋塞,向其中通入 一段时间,可防止拆卸装置时有毒气体污染空气(2
分。
学科网(北京)股份有限公司只答出“防止有毒气体污染空气”,给1分)
【解析】(4) 和 溶液反应的离子方程式为 ,反应后溶液
中 增大,故溶液的 减小。
17.【答案及评分细则】(15分)
(1)吸收(1分) 180(2分) (1分)
(2)还原(1分) (2分)
(3)① (2分)
②BC(2分。少选且正确的,给1分;选错或多选的,不给分)
③280(1分) (1分)甲(2分)
【解析】(1)该条件下, 和 完全反应断键需要吸收的能量是 ,生
成 时形成化学键释放的能量是 ,所以会吸收1
能量。
(3)① 内 浓度减少了 ,用 的浓度变化
表示 的平均反应速率为 。
② 的浓度不再改变,说明正、逆反应速率相等,该反应达到化学平衡状态,A不符合题意;容器中气体
的质量始终保持不变,不能据此说明该反应达到化学平衡状态,B符合题意; 的物质
的量之比为 ,并不能说明正、逆反应速率相等,不能据此说明该反应达到化学平衡状态,C符合题
意;相同时间内,反应消耗 同时消耗 ,说明正、逆反应速率相等,该反应达到化学平衡
状态, D不符合题意。选BC。
③ⅰ.实验I、Ⅱ中催化剂的比表面积不同,则其他条件应相同,故 ;实验I、Ⅲ中温度不同,侧其他
条件应相同,故 。
ⅱ.实验Ⅱ中催化剂的比表面积大,反应速率快,达到平衡的时间短,则其中表示实验Ⅱ的是曲线乙,表示
实验I的是曲线甲。
学科网(北京)股份有限公司18.【答案及评分细则】(15分)
(1)酯基(1分) 正丁烷(或丁烷)(2分)
(2)共价(1分) 直线(1分) (1分)
(3) (2分) 取代反应(或酯化反应)(1分)
(4) (2分)
(5) (2分。反应条件“催化剂”未写,扣1分)
(6)18(2分)
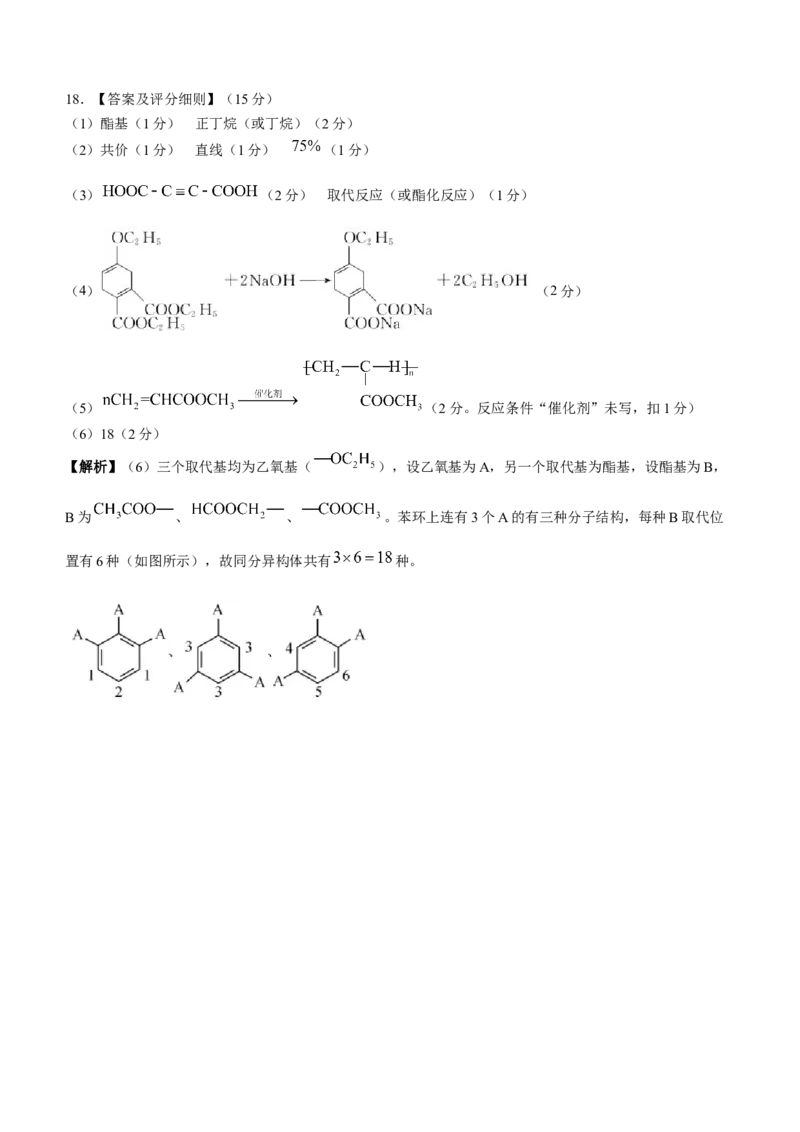
【解析】(6)三个取代基均为乙氧基( ),设乙氧基为A,另一个取代基为酯基,设酯基为B,
B为 、 、 。苯环上连有3个A的有三种分子结构,每种B取代位
置有6种(如图所示),故同分异构体共有 种。
学科网(北京)股份有限公司