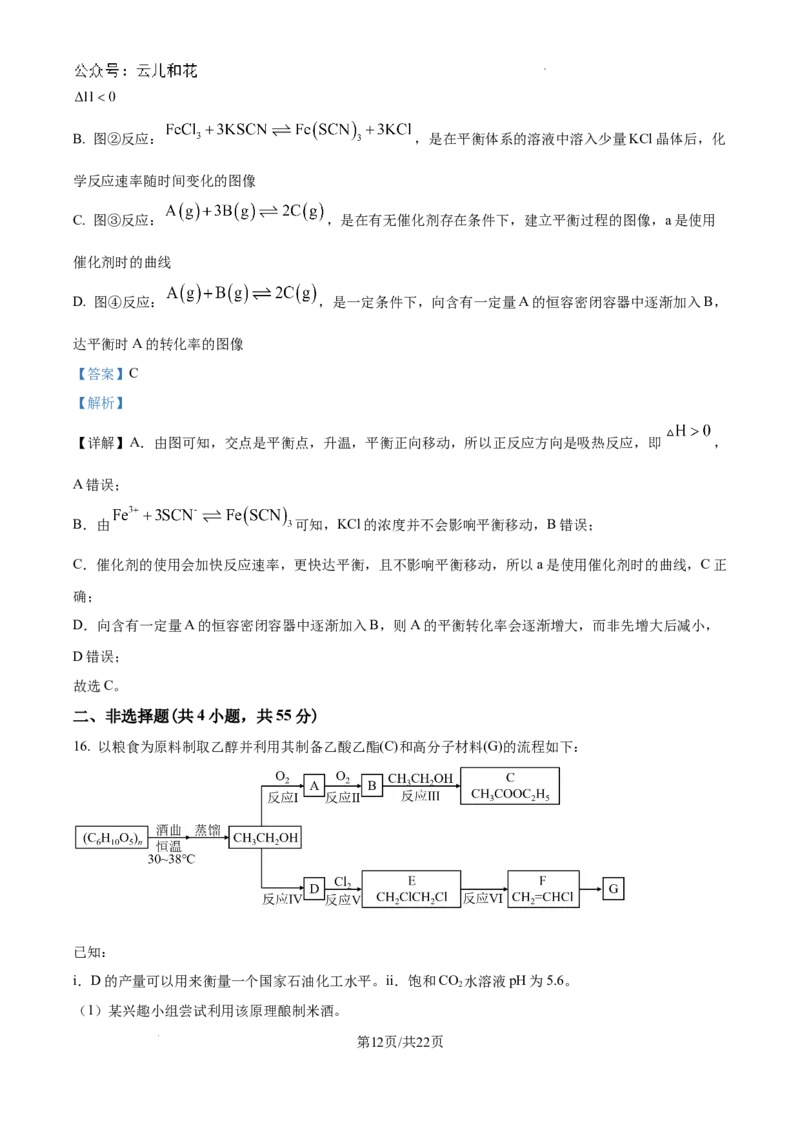
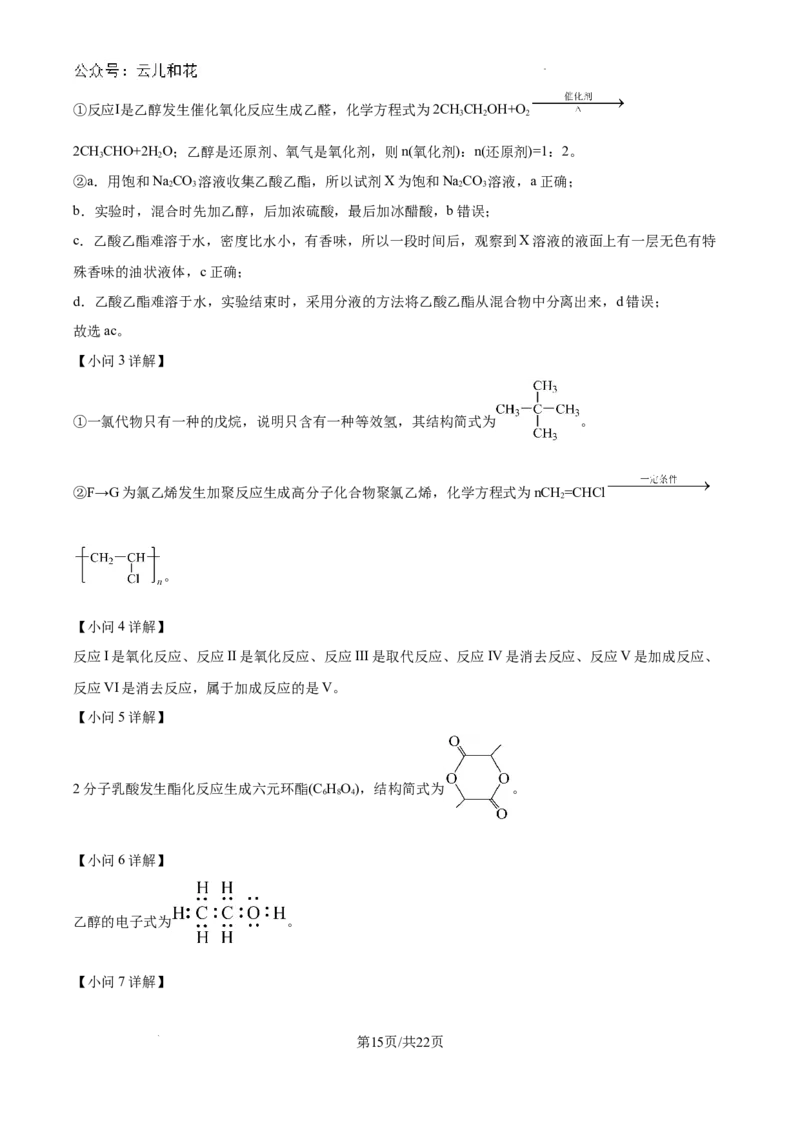
文档内容
2024-2025 学年高二上学期开学检测
化学
注意事项:
1.答卷前,考生务必将自己的姓名和座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡的相应位置上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一、选择题(共15小题,每题3分,共45分)
1. 下列化学用语正确的是
A. HCl的电子式: B. 乙烯的球棍模型
C. 的结构示意图 D. 丙烯的结构简式:
【答案】B
【解析】
【详解】A.HCl 是共价化合物,H原子和Cl原子之间共用1对电子,Cl原子外围达到8电子结构,其电
子式为 ,故A错误;
B.乙烯含有碳碳双键,分子中含有2个C、4个H,碳原子的原子半径大于氢原子,球棍模型为
,故B正确;
C.Cl-的质子数为17,核外电子数为18,最外层电子数为8,其结构示意图为 ,故C错误;
D.丙烯分子中含有碳碳双键,其正确的结构简式为:CHCH=CH,故D错误;
3 2
故选:B。
第1页/共22页
学科网(北京)股份有限公司2. 一定条件,水煤气发生变换反应: ,下列说法错误的是
A. 增大 浓度,使单位体积内活化分子数增多,可加快反应速率
B. 升高温度,活化分子百分数增大,加快反应速率
C. 适当压缩容积,单位体积内活化分子数增大,加快反应速率
D. 使用催化剂,降低反应活化能,活化分子百分数增大,反应速率及平衡转化率都增大
【答案】D
【解析】
【详解】A.增大反应物CO的浓度,可以增大单位体积的活化分子数目,从而加快反应速率,A正确;
B.升高温度,可以增加反应物分子的能量,增大活化分子的百分数,加快反应速率,B正确;
C.将容器的容积压缩,相当于增大压强,可增大单位体积内活化分子数,从而加快反应速率,C正确;
D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,但不影响反应物的平衡转化率,D错
误;
故选D。
3. 藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法错误的是
A. 可以发生水解反应 B. 所有碳原子处于同一平面
C. 含有2种含氧官能团 D. 能与溴水发生加成反应
【答案】B
【解析】
【详解】A.藿香蓟 的分子结构中含有酯基,因此其可以发生水解反应,A说法正确;
B.藿香蓟的分子结构中的右侧有一个饱和碳原子连接着两个甲基,类比甲烷分子的空间构型可知,藿香
蓟分子中所有碳原子不可能处于同一平面,B说法错误;
C.藿香蓟的分子结构中含有酯基和醚键,因此其含有2种含氧官能团,C说法正确;
D.藿香蓟的分子结构中含有碳碳双键,因此,其能与溴水发生加成反应,D说法正确;
综上所述,本题选B。
第2页/共22页
学科网(北京)股份有限公司4. 能证明蚁酸(HCOOH)是弱酸的实验事实是
A. HCOOH溶液与Zn反应放出H
2
B. 0.1 mol·L-1 HCOOH溶液可使紫色石蕊溶液变红
C. HCOOH溶液与NaCO 反应生成CO
2 3 2
D. 常温时0.1 mol·L-1 HCOOH溶液的pH=2.3
【答案】D
【解析】
【详解】A.HCOOH溶液与Zn反应生成氢气,说明HCOOH具有酸性,不能说明HCOOH部分电离,则
不能证明甲酸为弱酸,故A错误;
B.0.1mol/L的HCOOH溶液可以使紫色石蕊试液变红色,说明甲酸为酸,不能说明甲酸部分电离,则不
能证明甲酸为弱酸,故B错误;
C.HCOOH溶液和碳酸钠溶液反应生成二氧化碳,说明甲酸酸性大于碳酸,不能说明甲酸部分电离,则
不能证明甲酸为弱酸,故C错误;
D.常温下0.1mol•L-1HCOOH溶液的pH=2.3,说明HCOOH部分电离,则HCOOH为弱酸,故D正确;
故选:D。
5. 用N 表示阿伏加德罗常数的值,下列说法正确的是
A
A. 1mol甲基(电子式为 )中所含电子的数目为7N
A
B. 已知NO 和NO 可以相互转化: ,46g NO 气体的分子数为N
2 2 4 2 A
C. 标准状况下,11.2L甲烷和乙烯混合物中含有的氢原子数目为2N
A
D. 1mol CH 与1mol Cl 在光照下反应,生成的CHCl分子数为N
4 2 3 A
【答案】C
【解析】
【详解】A.1mol甲基(电子式为 )中所含电子的数目为9N ,故A错误;
A
B.已知NO 和NO 可以相互转化: ,46g NO 气体的分子数为小于N ,故B错
2 2 4 2 A
误;
C.标准状况下,11.2L甲烷和乙烯混合气体的物质的量为0.5mol,甲烷和乙烯分子中都含4个H原子,含
有的氢原子数目为2N ,故C正确;
A
第3页/共22页
学科网(北京)股份有限公司D.CH 与1mol Cl 在光照下发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳,1mol CH 与
4 2 4
1mol Cl 在光照下反应,生成的CHCl分子数为小于N ,故D错误;
2 3 A
选C。
6. 用可再生能源给锌铁液流电池充电,该电池工作原理如下图所示。下列说法正确的是
A. 放电时,M为正极
B. 放电时,M极发生的电极反应为:
C. 充电时, 穿过交换膜进入N极室
D. 充电时,总反应为:
【答案】D
【解析】
【详解】A.锌易失电子,放电时,Zn失电子生成 ,所以M为负极,故A错误;
B.锌易失电子,放电时,Zn失电子生成 ,M极发生的电极反应为:
,故B错误;
C.充电时,阳离子向阴极移动,M是阴极、N是阳极, 穿过交换膜进入M极室,故C错误;
D.充电时,阴极 发生还原反应生成Zn,阳极 发生氧化反应生成 ,总反应
为 ,故D正确;
第4页/共22页
学科网(北京)股份有限公司选D。
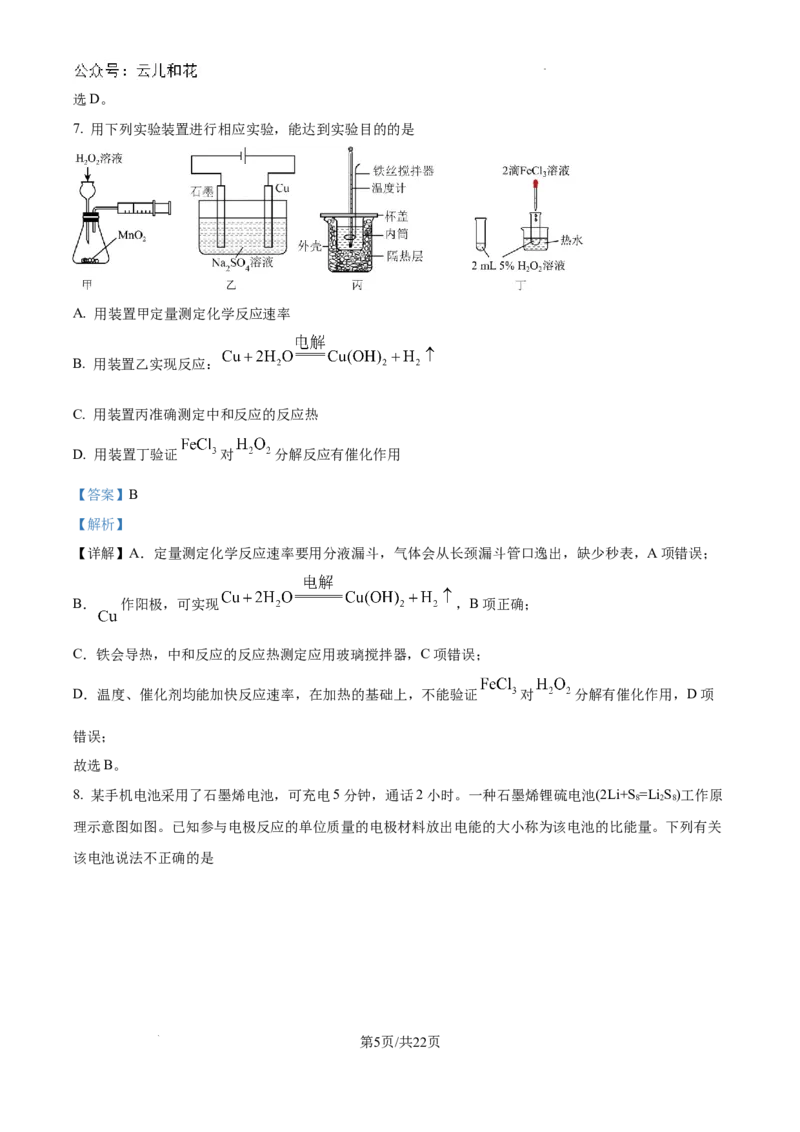
7. 用下列实验装置进行相应实验,能达到实验目的的是
A. 用装置甲定量测定化学反应速率
B. 用装置乙实现反应:
C. 用装置丙准确测定中和反应的反应热
D. 用装置丁验证 对 分解反应有催化作用
【答案】B
【解析】
【详解】A.定量测定化学反应速率要用分液漏斗,气体会从长颈漏斗管口逸出,缺少秒表,A项错误;
B. 作阳极,可实现 ,B项正确;
C.铁会导热,中和反应的反应热测定应用玻璃搅拌器,C项错误;
D.温度、催化剂均能加快反应速率,在加热的基础上,不能验证 对 分解有催化作用,D项
错误;
故选B。
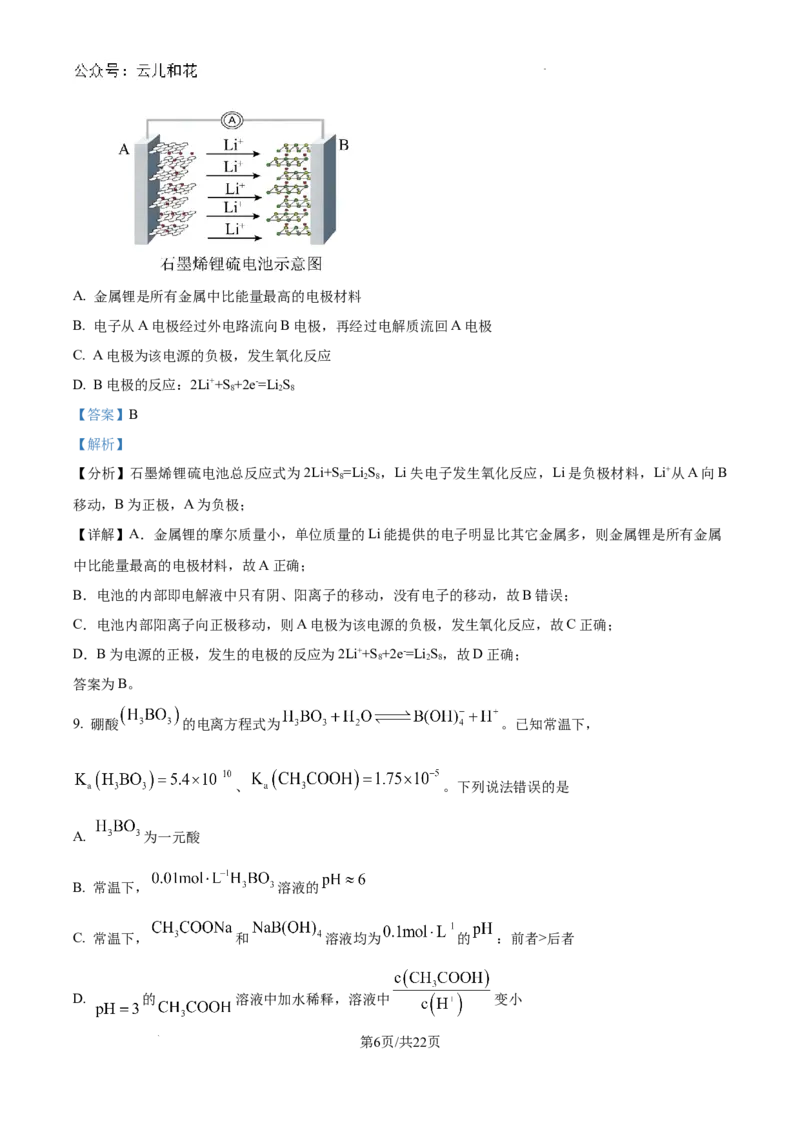
8. 某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。一种石墨烯锂硫电池(2Li+S =Li S)工作原
8 2 8
理示意图如图。已知参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量。下列有关
该电池说法不正确的是
第5页/共22页
学科网(北京)股份有限公司A. 金属锂是所有金属中比能量最高的电极材料
B. 电子从A电极经过外电路流向B电极,再经过电解质流回A电极
C. A电极为该电源的负极,发生氧化反应
D. B电极的反应:2Li++S +2e-=Li S
8 2 8
【答案】B
【解析】
【分析】石墨烯锂硫电池总反应式为2Li+S=Li S ,Li失电子发生氧化反应,Li是负极材料,Li+从A向B
8 2 8
移动,B为正极,A为负极;
【详解】A.金属锂的摩尔质量小,单位质量的Li能提供的电子明显比其它金属多,则金属锂是所有金属
中比能量最高的电极材料,故A正确;
B.电池的内部即电解液中只有阴、阳离子的移动,没有电子的移动,故B错误;
C.电池内部阳离子向正极移动,则A电极为该电源的负极,发生氧化反应,故C正确;
D.B为电源的正极,发生的电极的反应为2Li++S +2e-=Li S,故D正确;
8 2 8
答案为B。
9. 硼酸 的电离方程式为 。已知常温下,
、 。下列说法错误的是
A. 为一元酸
B. 常温下, 溶液的
C. 常温下, 和 溶液均为 的 :前者>后者
D. 的 溶液中加水稀释,溶液中 变小
第6页/共22页
学科网(北京)股份有限公司【答案】C
【解析】
【详解】A.根据题意可知HBO 只存在一步电离,产生一个氢离子,所以为一元酸,A不符合题意;
3 3
B.设0.01mol•L-1H BO 溶液中c(H+)=x,则c[ ]也可近似认为等于x,则有Ka(H BO)=5.4×10-10,
3 3 3 3
解得x≈2.3×10-6mol/L,所以pH≈6,B不符合题意;
C.Ka(H BO)< Ka(CH COOH),所以NaB(OH) 的水解程度更大,浓度相同时硼酸钠碱性更强,则等浓度
3 3 3 4
溶液的pH:CHCOONa<NaB(OH) ,C错误;
3 4
D.常温下,pH=3的CHCOOH溶液加水稀释后,CHCOOH、CHCOO-和H+浓度都减小,OH-浓度增大,
3 3 3
Ka只与温度有关,溶液中 减小,D不符合题意;
故选C。
10. 常温下,在 的氨水中存在电离平衡: ,下列叙述正确的是
A. 加入水时,平衡正向移动, 电离常数增大
B. 向该溶液中加少量 固体,平衡正向移动
C. 向该溶液中滴加几滴 ,平衡逆向移动, 减小
D. 通入少量 气体,平衡正向移动, 减少
【答案】D
【解析】
【详解】A.加水时,促进NH ⋅HO电离,平衡正向移动,但温度不变,则NH ⋅HO电离常数不变,故
3 2 3 2
A项错误;
B.向该溶液中加少量NH Cl固体,铵根离子浓度增大,抑制NH ⋅HO电离,平衡逆向移动,故B项错误;
4 3 2
C.向该溶液中滴加几滴0.1mol⋅L−1NaOH,c(OH−)增大,抑制NH ⋅HO电离,平衡逆向移动,故C项错
3 2
误;
D.通入少量HCl气体,c(OH−)浓度减小,促进NH ⋅HO电离,平衡正向移动,故D项正确;
3 2
故本题选D。
第7页/共22页
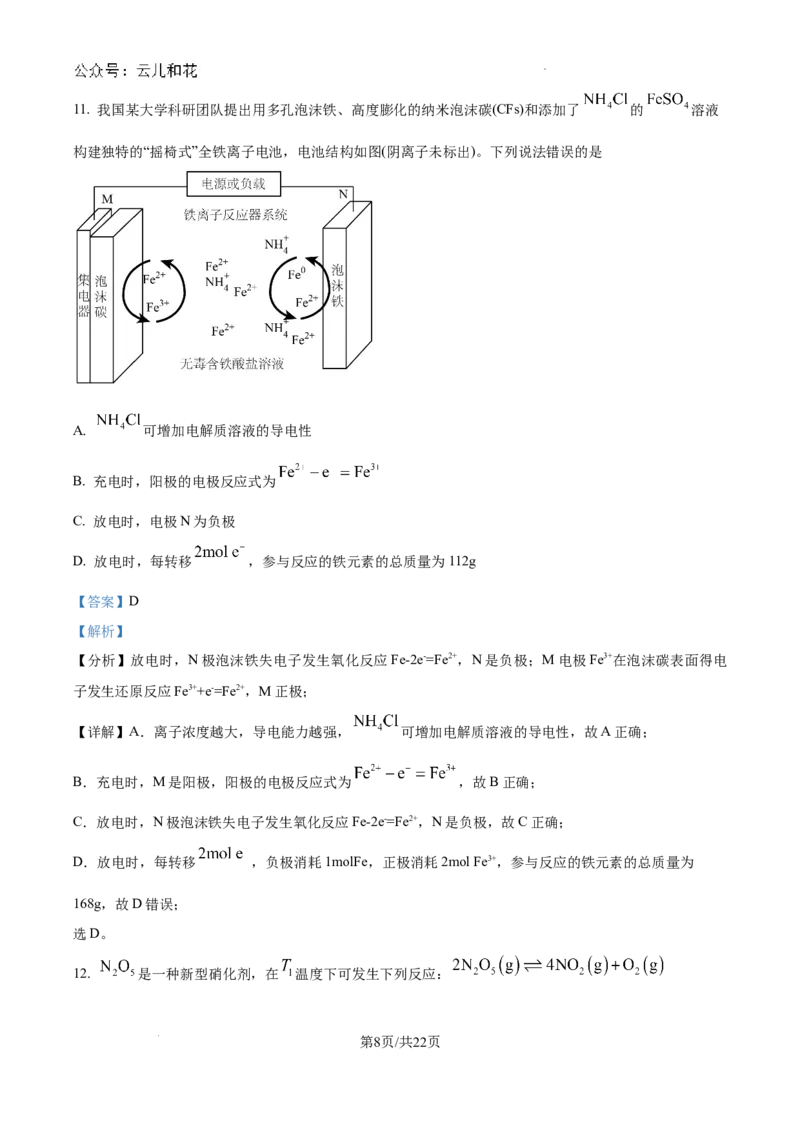
学科网(北京)股份有限公司11. 我国某大学科研团队提出用多孔泡沫铁、高度膨化的纳米泡沫碳(CFs)和添加了 的 溶液
构建独特的“摇椅式”全铁离子电池,电池结构如图(阴离子未标出)。下列说法错误的是
A. 可增加电解质溶液的导电性
B. 充电时,阳极的电极反应式为
C. 放电时,电极N为负极
D. 放电时,每转移 ,参与反应的铁元素的总质量为112g
【答案】D
【解析】
【分析】放电时,N极泡沫铁失电子发生氧化反应Fe-2e-=Fe2+,N是负极;M电极Fe3+在泡沫碳表面得电
子发生还原反应Fe3++e-=Fe2+,M正极;
【详解】A.离子浓度越大,导电能力越强, 可增加电解质溶液的导电性,故A正确;
B.充电时,M是阳极,阳极的电极反应式为 ,故B正确;
C.放电时,N极泡沫铁失电子发生氧化反应Fe-2e-=Fe2+,N是负极,故C正确;
D.放电时,每转移 ,负极消耗1molFe,正极消耗2mol Fe3+,参与反应的铁元素的总质量为
168g,故D错误;
选D。
12. 是一种新型硝化剂,在 温度下可发生下列反应:
第8页/共22页
学科网(北京)股份有限公司的
。 温度下 平衡常数为 。下列说法错误的是
A. 反应的
B. 该反应在高温下可自发进行
C. 温度下的平衡常数为 , 温度下的平衡常数为 ,若 ,则
D. 温度下,在体积为1 L的恒温密闭容器中充入2 mol ,4 mol ,1 mol ,此时反应将向
正反应方向进行
【答案】C
【解析】
【详解】A.由热化学方程式可知,该反应为气体分子数增加的反应即熵增,则ΔS>0,故A项正确;
B.ΔH>0,ΔS>0,该反应若可以自发进行,需ΔG=ΔH-TΔS<0,则该反应在高温下可自发进行,故B项正
确;
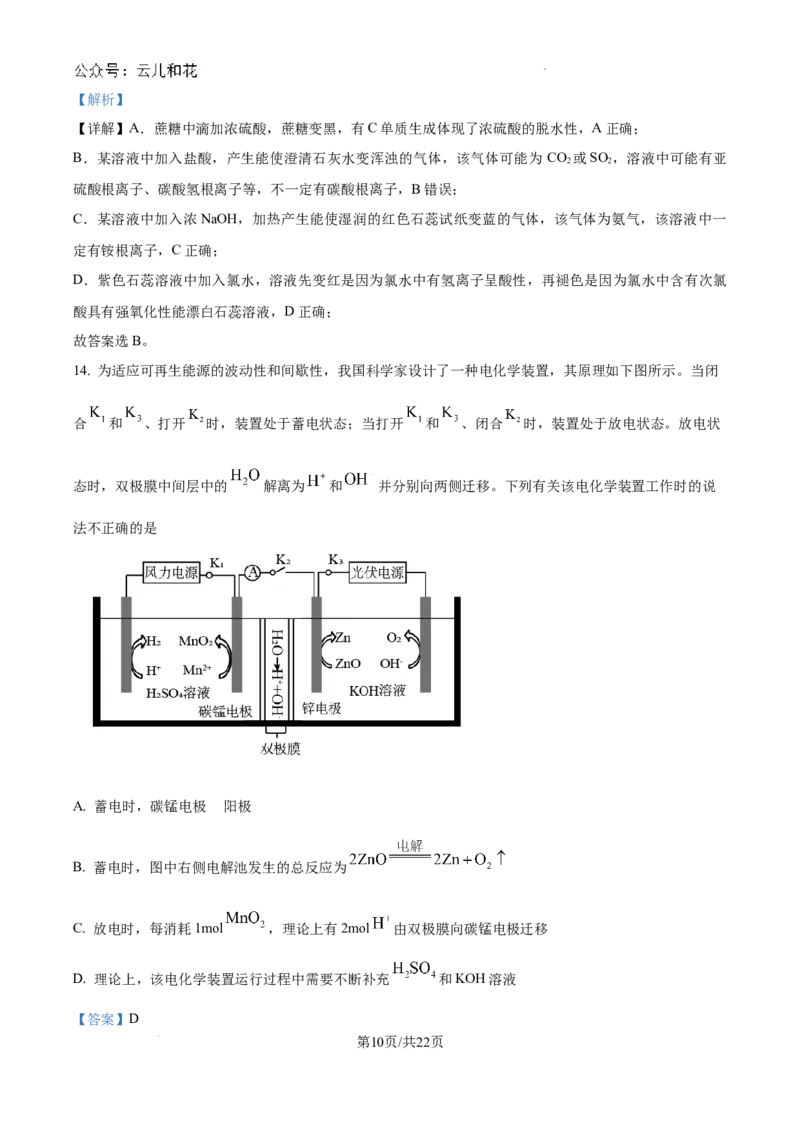
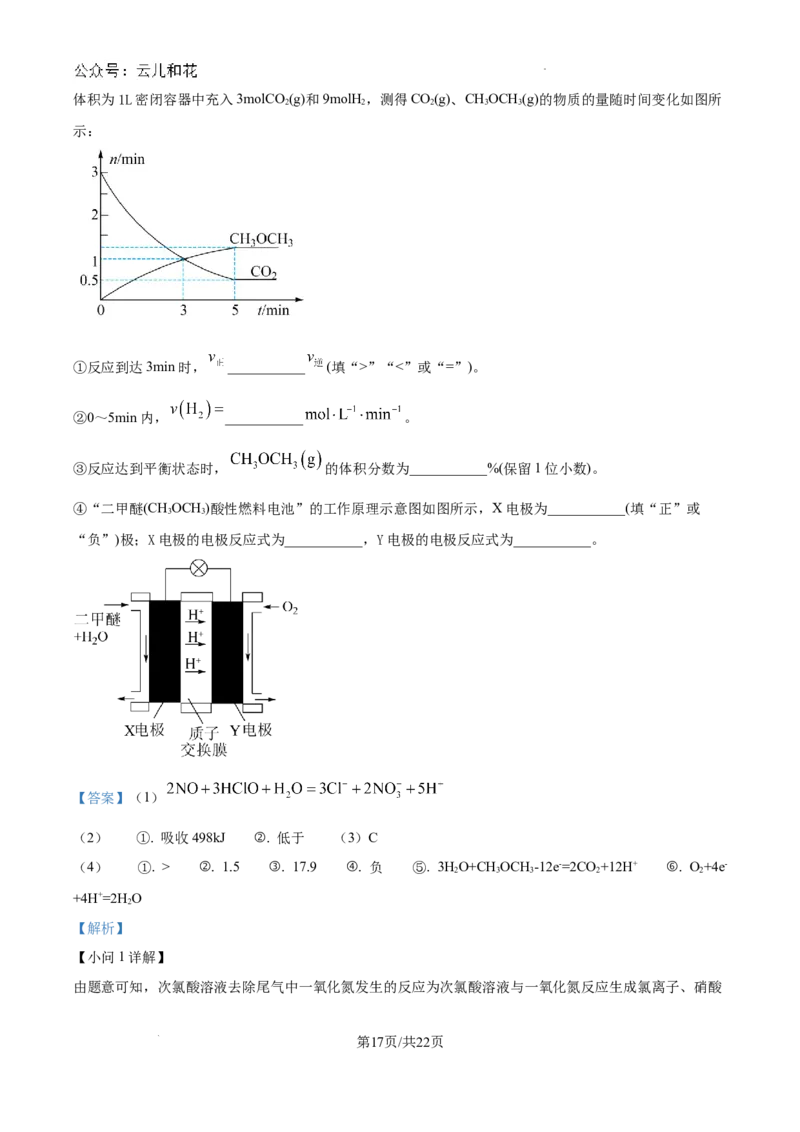
C.该反应为吸热反应,温度越高平衡常数越大,若K ”“<”或“=”)。
②0~5min内, ___________ 。
③反应达到平衡状态时, 的体积分数为___________%(保留1位小数)。
④“二甲醚(CHOCH )酸性燃料电池”的工作原理示意图如图所示,X电极为___________(填“正”或
3 3
“负”)极;X电极的电极反应式为___________,Y电极的电极反应式为___________。
【答案】(1)
(2) ①. 吸收498kJ ②. 低于 (3)C
(4) ①. > ②. 1.5 ③. 17.9 ④. 负 ⑤. 3HO+CHOCH -12e-=2CO +12H+ ⑥. O+4e-
2 3 3 2 2
+4H+=2H O
2
【解析】
【小问1详解】
由题意可知,次氯酸溶液去除尾气中一氧化氮发生的反应为次氯酸溶液与一氧化氮反应生成氯离子、硝酸
第17页/共22页
学科网(北京)股份有限公司根离子和氢离子,反应的离子方程式为 ,故答案为:
;
【小问2详解】
由图可知,断裂1mol氧气分子中的共价键需要吸收的热量为498kJ/mol×1mol=498kJ,断裂1mol氮气中的
共价键需要吸收的热量为946kJ/mol×1mol=946kJ,则氮气与氧气反应生成一氧化氮时,断裂生成物共价
键需要吸收的热量为498kJ+946kJ=1444kJ,生成2mol一氧化氮放出的热量为632kJ/mol×2mol=1264kJ,所
以该反应是反应物总能量大于生成物总能量的吸热反应,故答案为:498kJ;高于;
【小问3详解】
A.反应物甲烷和生成物氮气的浓度相等不能说明正逆反应速率相等,无法判断反应是否达到平衡,故错
误;
B.由质量守恒定律可知,反应前后气体的质量相等,在恒容密闭容器中混合气体的密度始终不变,则混
合气体的密度保持不变不能说明正逆反应速率相等,无法判断反应是否达到平衡,故错误;
C.容器内二氧化氮的物质的量浓度不再变化说明正逆反应速率相等,反应已达到平衡,故正确;
D.单位时间内,消耗2mol甲烷同时生成2mol二氧化碳都代表正反应速率,不能说明正逆反应速率相等,
无法判断反应是否达到平衡,故错误;
故选C;
【小问4详解】
①由图可知,反应到达3min时,二甲醚的物质的量未达到最大,说明反应未达到平衡,是平衡的形成过
程,所以正反应速率大于逆反应速率,故答案为:>;
②由图可知,5min 时,二甲醚的物质的量为1.25mol,则由方程式可知,0~5min内,氢气的反应速率为
=1.5 mol/(L·min),故答案为:1.5;
③由图可知,反应达到平衡状态时,二甲醚的物质的量为1.25mol,由方程式可知,平衡时气体总体积为
12mol—1.25mol×4=7mol,则二甲醚的体积分数为 ×100%≈17.9%,故答案为:17.9;
④由氢离子的移动方向可知,X电极为燃料电池的负极,水分子作用下二甲醚在负极失去电子发生氧化反
第18页/共22页
学科网(北京)股份有限公司应生成二氧化碳和氢离子,电极反应式为3HO+CHOCH -12e-=2CO +12H+,Y电极为正极,酸性条件下氧
2 3 3 2
气在正极得到电子发生还原反应生成水,电极反应式为O+4e-+4H+=2H O,故答案为:负;
2 2
3HO+CHOCH -12e-=2CO +12H+;O+4e-+4H+=2H O。
2 3 3 2 2 2
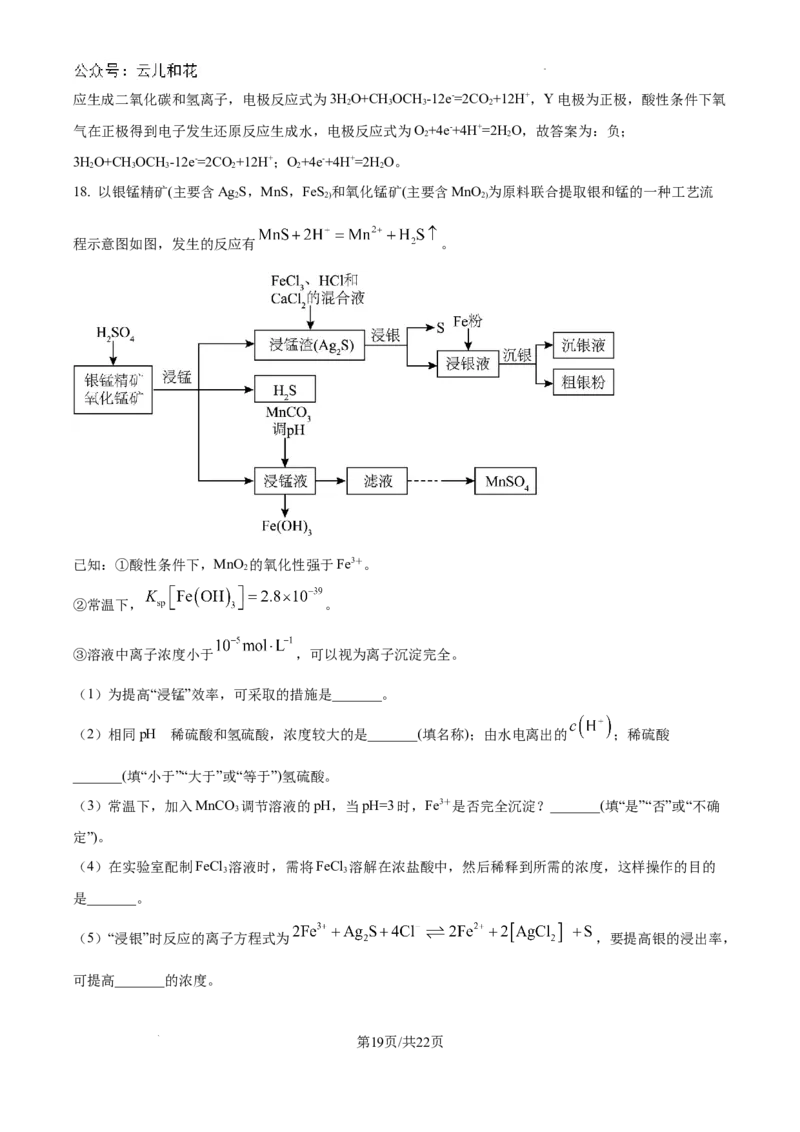
18. 以银锰精矿(主要含Ag S,MnS,FeS 和氧化锰矿(主要含MnO 为原料联合提取银和锰的一种工艺流
2 2) 2)
程示意图如图,发生的反应有 。
已知:①酸性条件下,MnO 的氧化性强于Fe3+。
2
②常温下, 。
③溶液中离子浓度小于 ,可以视为离子沉淀完全。
(1)为提高“浸锰”效率,可采取的措施是_______。
(2)相同pH 的稀硫酸和氢硫酸,浓度较大的是_______(填名称);由水电离出的 ;稀硫酸
_______(填“小于”“大于”或“等于”)氢硫酸。
(3)常温下,加入MnCO 调节溶液的pH,当pH=3时,Fe3+是否完全沉淀?_______(填“是”“否”或“不确
3
定”)。
(4)在实验室配制FeCl 溶液时,需将FeCl 溶解在浓盐酸中,然后稀释到所需的浓度,这样操作的目的
3 3
是_______。
(5)“浸银”时反应的离子方程式为 ,要提高银的浸出率,
可提高_______的浓度。
第19页/共22页
学科网(北京)股份有限公司(6)银锰精矿中的FeS 若S元素转化成 )和氧化锰矿中的MnO 发生反应的离子方程式为_______。
2( 2
【答案】(1)搅拌、适当增加硫酸浓度、加热等
(2) ①. 氢硫酸 ②. 等于
(3)是 (4)抑制FeCl 的水解
3
(5)HCl、CaCl 、FeCl
2 3
(6)
【解析】
【分析】银锰精矿和氧化锰矿混合加硫酸溶液,二氧化锰具有氧化性使得二价铁氧化为三价铁同时二氧化
锰能被还原生成锰离子,使矿石中的锰元素浸出,同时去除 FeS ,浸锰液中主要的金属阳离子有 Fe3+、
2
Mn2+,矿石中的银以Ag S的形式残留于浸锰渣中,浸锰渣中Ag S与过量氯化铁、盐酸、氯化钙的混合液
2 2
反应,将Ag S中的银以[AgCl ] 形式浸出,用铁粉把[AgCl ] 还原为金属银,据此分析。
2 2 2
【小问1详解】
为提高“浸锰”效率,可采取的措施有搅拌、适当增加硫酸浓度、加热等;
【小问2详解】
硫化氢是弱酸,相同pH的稀硫酸和氢硫酸,浓度较大的是氢硫酸;相同pH则对水的电离抑制程度相同,
由水电离出的 相同;
【小问3详解】
当pH=3时, ,
,可知Fe3+完全沉淀;
【小问4详解】
的
配制FeCl 溶液时,需将FeCl 溶解在浓盐酸中,然后稀释到所需 浓度,这样操作的目的是提供酸性环境,
3 3
抑制FeCl 的水解;
3
【小问5详解】
根据平衡 ,要提高银的浸出率,可提高 HCl、CaCl 、
2
FeCl 的浓度,增加氯离子浓度,平衡正向移动;
3
第20页/共22页
学科网(北京)股份有限公司【小问6详解】
FeS 和氧化锰矿中的MnO 发生反应,S元素转化成 ,二氧化锰被还原生成锰离子,离子方程式为
2 2
。
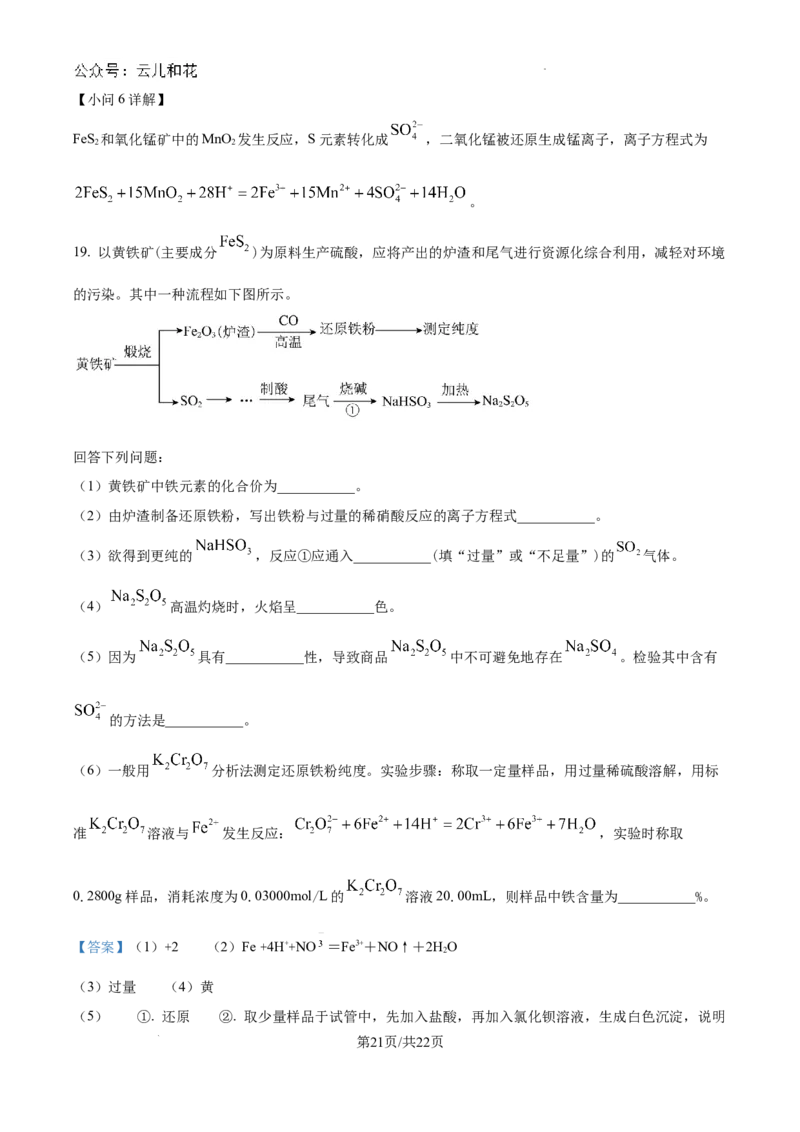
19. 以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境
的污染。其中一种流程如下图所示。
回答下列问题:
(1)黄铁矿中铁元素的化合价为___________。
(2)由炉渣制备还原铁粉,写出铁粉与过量的稀硝酸反应的离子方程式___________。
(3)欲得到更纯的 ,反应①应通入___________(填“过量”或“不足量”)的 气体。
(4) 高温灼烧时,火焰呈___________色。
(5)因为 具有___________性,导致商品 中不可避免地存在 。检验其中含有
的方法是___________。
(6)一般用 分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标
准 溶液与 发生反应: ,实验时称取
0.2800g样品,消耗浓度为0.03000mol/L的 溶液20.00mL,则样品中铁含量为___________%。
【答案】(1)+2 (2)Fe +4H++NO =Fe3++NO↑+2HO
2
(3)过量 (4)黄
(5) ①. 还原 ②. 取少量样品于试管中,先加入盐酸,再加入氯化钡溶液,生成白色沉淀,说明
第21页/共22页
学科网(北京)股份有限公司含有
(6)72
【解析】
【分析】黄铁矿(主要成分FeS)煅烧生成氧化铁和二氧化硫,氧化铁用CO还原得到还原铁粉,用 KCr O
2 2 2 7
滴定分析法测定还原铁粉纯度;二氧化硫经过一系列步骤生成硫酸,尾气中含有二氧化硫,用氢氧化钠溶
液吸收生成NaHSO,加热后生成NaSO,据此分析解答。
3 2 2 5
【小问1详解】
黄铁矿中硫元素是-1价,则铁元素的化合价为+2价。
【小问2详解】
铁粉与过量的稀硝酸反应的离子方程式为Fe +4H++NO =Fe3++NO↑+2HO;
2
【小问3详解】
二氧化硫不足时容易生成亚硫酸钠,所以欲得到更纯的 ,反应①应通入过量的 气体。
【小问4详解】
钠的焰色试验显黄色,所以 高温灼烧时,火焰呈黄色。
【小问5详解】
NaSO 转化为NaSO 过程中S元素的化合价升高,被氧化,体现了NaSO 的还原性;检验其中含有
2 2 5 2 4 2 2 5
的方法是首先用盐酸酸化,除去 ,再加入氯化钡溶液,看有无白色沉淀生成,若生成白色沉淀,
证明含有 ,否则没有 ;
【小问6详解】
称取一定量样品,用过量稀硫酸溶解,用标准KCr O 溶液滴定其中的Fe2+,存在关系式:6Fe~6Fe2+~
2 2 7
,滴定过程中消耗的KCr O 物质的量为0.03 mol·L-1×0.02 L=0.0006mol,则锥形瓶中含有的Fe2+的
2 2 7
物质的量为0.0006mol×6=0.0036mol,质量是0.0036mol×56g/mol=0.2016g,则样品中铁含量为
。
第22页/共22页
学科网(北京)股份有限公司