文档内容
2025年9月高二上学期化学月考试题
一、单选题(每题3分,共48分)
1.下列变化过程中需要吸收能量的是
A.氢气球发生燃烧爆炸 B.向污染的河水中投入生石灰
C. D.灼热的炭与二氧化碳反应
2.中华文化源远流长,很多古诗词和文献中都涉及丰富的化学知识。下列解释正确的是
A.“榆荚只能随柳絮,等闲缭乱走空园”中的柳絮的主要成分是蛋白质
B.“春蚕到死丝方尽,蜡炬成灰泪始干”,古代的蜡是高级脂肪酸酯,属于高分子化
合物
C.“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”文中的“气”指
乙烯,将“气”通入水中很快可生成乙醇
D.“凡研硝( )不以铁碾入石臼,相激火生,祸不可测。”文中的 性质不稳
定,撞击易爆炸
3.硫酸是一种重要的化工原料,生产过程中涉及反应 。
下列实际工业生产中的措施不能用勒夏特列原理来解释的是
A.适当提高氧气的投料比例用于提高SO 转化率
2
B.使用合适的催化剂提高合成SO 的效率
3
C.及时分离出SO 用于提高原料转化率
3
D.适当增大压强可以提高SO 的产率
3
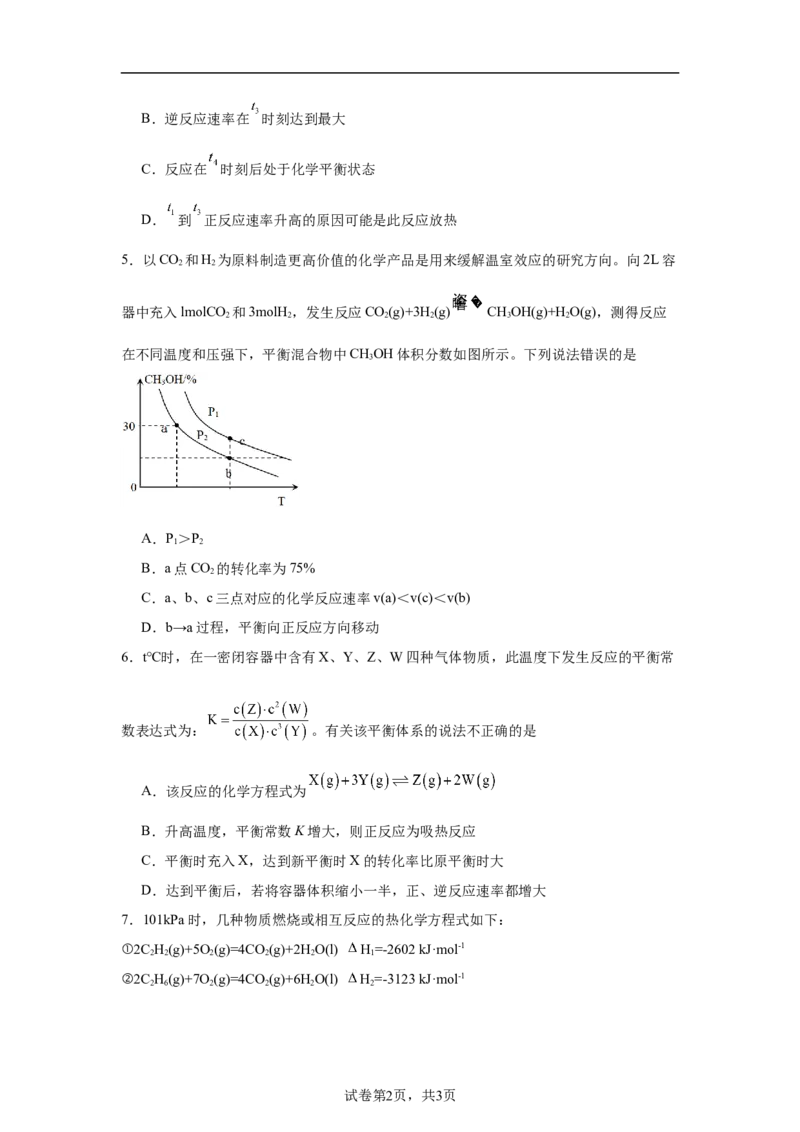
4.向某恒容密闭容器中充入一定量的气体A和气体B,发生反应:
,正反应速率随时间变化的曲线如图所示。下列说法错误的是
A. 时刻反应物的浓度大于 时刻反应物的浓度B.逆反应速率在 时刻达到最大
C.反应在 时刻后处于化学平衡状态
D. 到 正反应速率升高的原因可能是此反应放热
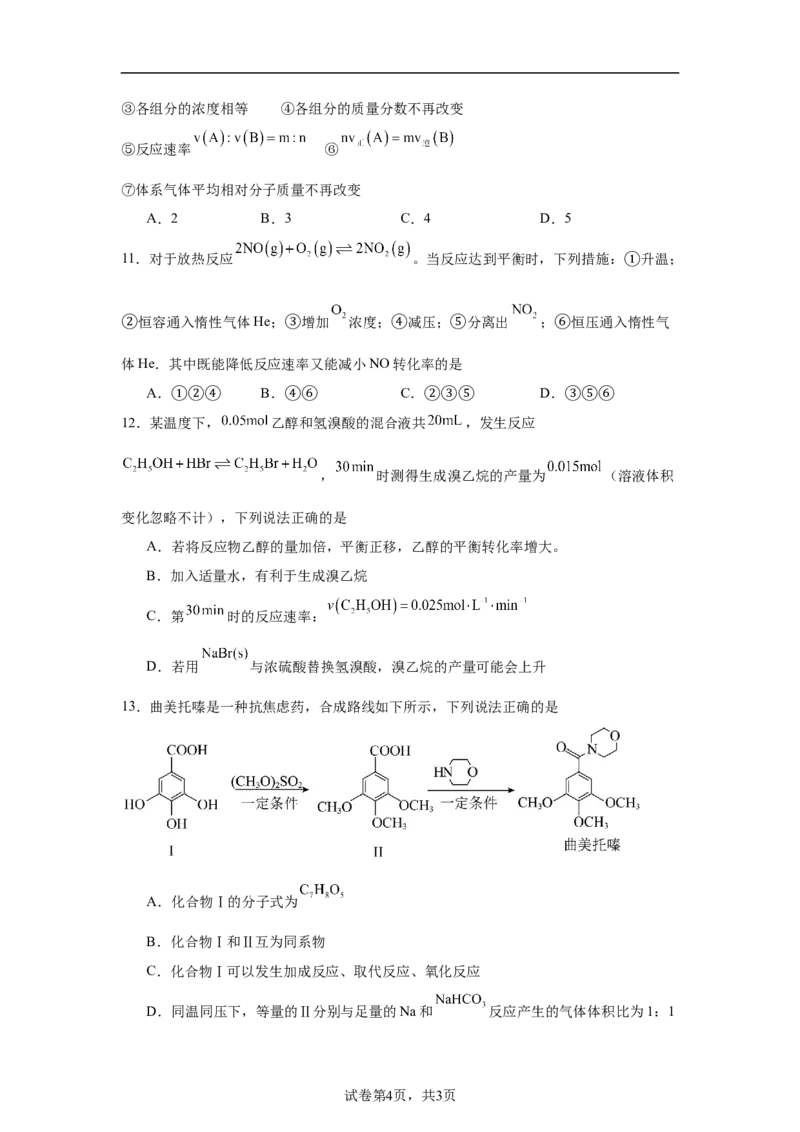
5.以CO 和H 为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。向2L容
2 2
器中充入lmolCO 和3molH ,发生反应CO(g)+3H(g) CHOH(g)+H O(g),测得反应
2 2 2 2 3 2
在不同温度和压强下,平衡混合物中CHOH体积分数如图所示。下列说法错误的是
3
A.P>P
1 2
B.a点CO 的转化率为75%
2
C.a、b、c三点对应的化学反应速率v(a)<v(c)<v(b)
D.b→a过程,平衡向正反应方向移动
6.t℃时,在一密闭容器中含有X、Y、Z、W四种气体物质,此温度下发生反应的平衡常
数表达式为: 。有关该平衡体系的说法不正确的是
A.该反应的化学方程式为
B.升高温度,平衡常数K增大,则正反应为吸热反应
C.平衡时充入X,达到新平衡时X的转化率比原平衡时大
D.达到平衡后,若将容器体积缩小一半,正、逆反应速率都增大
7.101kPa时,几种物质燃烧或相互反应的热化学方程式如下:
①2C H(g)+5O(g)=4CO (g)+2HO(l) H=-2602 kJ·mol-1
2 2 2 2 2 1
②2C H(g)+7O(g)=4CO (g)+6HO(l) H=-3123 kJ·mol-1
2 6 2 2 2 2
试卷第2页,共3页③ H=-286kJ·mol-1
3
④C H(g)+2H(g)=C H(g) H
2 2 2 2 6 4
下列叙述错误的是
A.乙炔的燃烧热 H=-2602 kJ·mol-1
B.等物质的量完全燃烧放出的热量:C H>C H
2 6 2 2
C.C H(g)+2H(g)=C H(g) H<0
2 2 2 2 6 4
D.2H(g)+O(g)=2HO(g) H>-572 kJ·mol-1
2 2 2
8.下列有关原子结构和元素周期律的表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④ⅠA族的元素都是金属元素
⑤原子序数为12的元素位于元素周期表的第三周期ⅡA族
⑥最外层有2个电子的元素一定在ⅡA族
A.①② B.①③ C.②⑤ D.④⑥
9.甲、乙、丙三个容器中起始物质及其物质的量如图所示,三个容器最初的容积、温度相
同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法
正确的是
A.平衡时各容器内c(NO )的大小顺序为乙>甲>丙
2
B.平衡时NO 的百分含量:乙>甲=丙
2 4
C.平衡时甲中NO 与丙中NO 的转化率一定相同
2 2 4
D.其它条件不变,向平衡后的丙容器中再加入少量NO,新平衡后 的值变大
2 4
10.在一个不传热的固定容积的密闭容器中,可逆反应 ,
当m、n、p、q为任意整数时,下列说法一定能说明反应已达到平衡有几个
①体系的密度不再改变 ②体系的温度不再改变③各组分的浓度相等 ④各组分的质量分数不再改变
⑤反应速率 ⑥
⑦体系气体平均相对分子质量不再改变
A.2 B.3 C.4 D.5
11.对于放热反应 。当反应达到平衡时,下列措施: 升温;
①
恒容通入惰性气体He; 增加 浓度; 减压; 分离出 ; 恒压通入惰性气
② ③ ④ ⑤ ⑥
体He.其中既能降低反应速率又能减小NO转化率的是
A. B. C. D.
12.某温①度②下④, 乙④醇和⑥氢溴酸的混合液共②③⑤,发生反应 ③⑤⑥
, 时测得生成溴乙烷的产量为 (溶液体积
变化忽略不计),下列说法正确的是
A.若将反应物乙醇的量加倍,平衡正移,乙醇的平衡转化率增大。
B.加入适量水,有利于生成溴乙烷
C.第 时的反应速率:
D.若用 与浓硫酸替换氢溴酸,溴乙烷的产量可能会上升
13.曲美托嗪是一种抗焦虑药,合成路线如下所示,下列说法正确的是
A.化合物Ⅰ的分子式为
B.化合物Ⅰ和Ⅱ互为同系物
C.化合物Ⅰ可以发生加成反应、取代反应、氧化反应
D.同温同压下,等量的Ⅱ分别与足量的Na和 反应产生的气体体积比为1:1
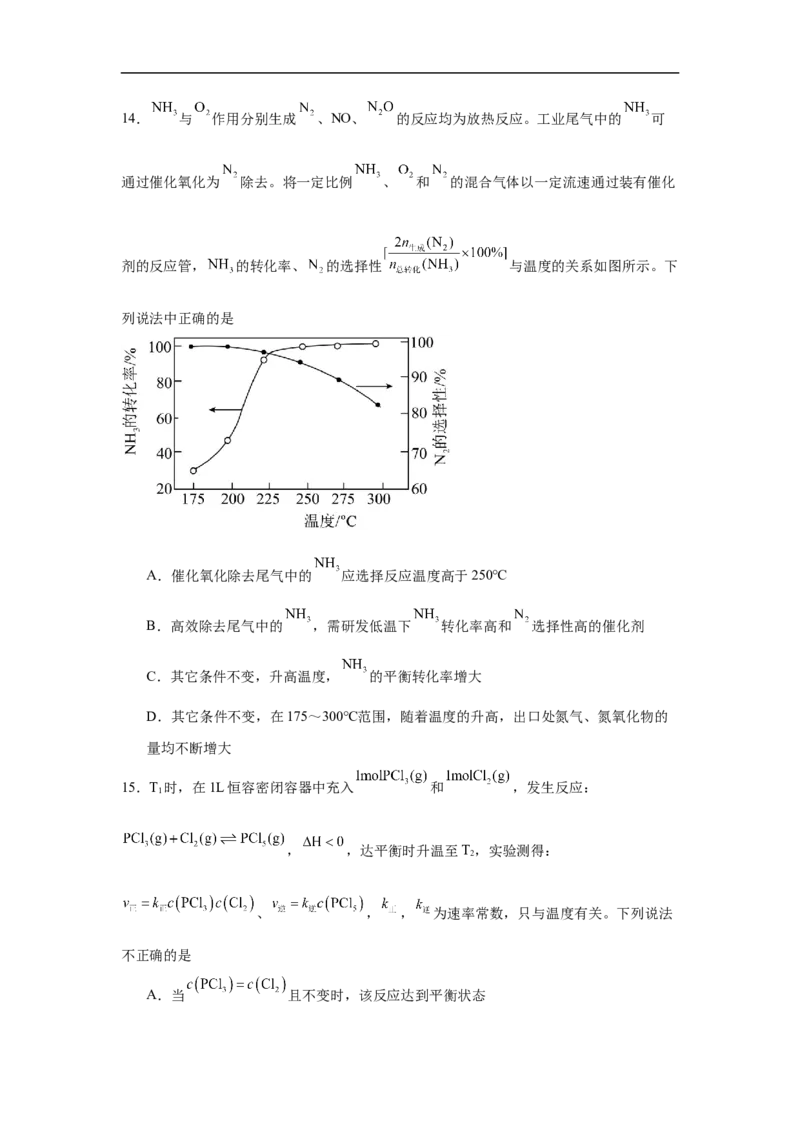
试卷第4页,共3页14. 与 作用分别生成 、NO、 的反应均为放热反应。工业尾气中的 可
通过催化氧化为 除去。将一定比例 、 和 的混合气体以一定流速通过装有催化
剂的反应管, 的转化率、 的选择性 与温度的关系如图所示。下
列说法中正确的是
A.催化氧化除去尾气中的 应选择反应温度高于250℃
B.高效除去尾气中的 ,需研发低温下 转化率高和 选择性高的催化剂
C.其它条件不变,升高温度, 的平衡转化率增大
D.其它条件不变,在175~300℃范围,随着温度的升高,出口处氮气、氮氧化物的
量均不断增大
15.T 时,在1L恒容密闭容器中充入 和 ,发生反应:
1
, ,达平衡时升温至T,实验测得:
2
、 , , 为速率常数,只与温度有关。下列说法
不正确的是
A.当 且不变时,该反应达到平衡状态B.该反应的平衡常数可表示为 ,
C.向T 温度下的平衡体系再充入 ,平衡正向移动,产物 的体积分
1
数变大
D.T 时,在一恒压密闭容器中充入 和 ,发生上述反应,
1
的转化率变大
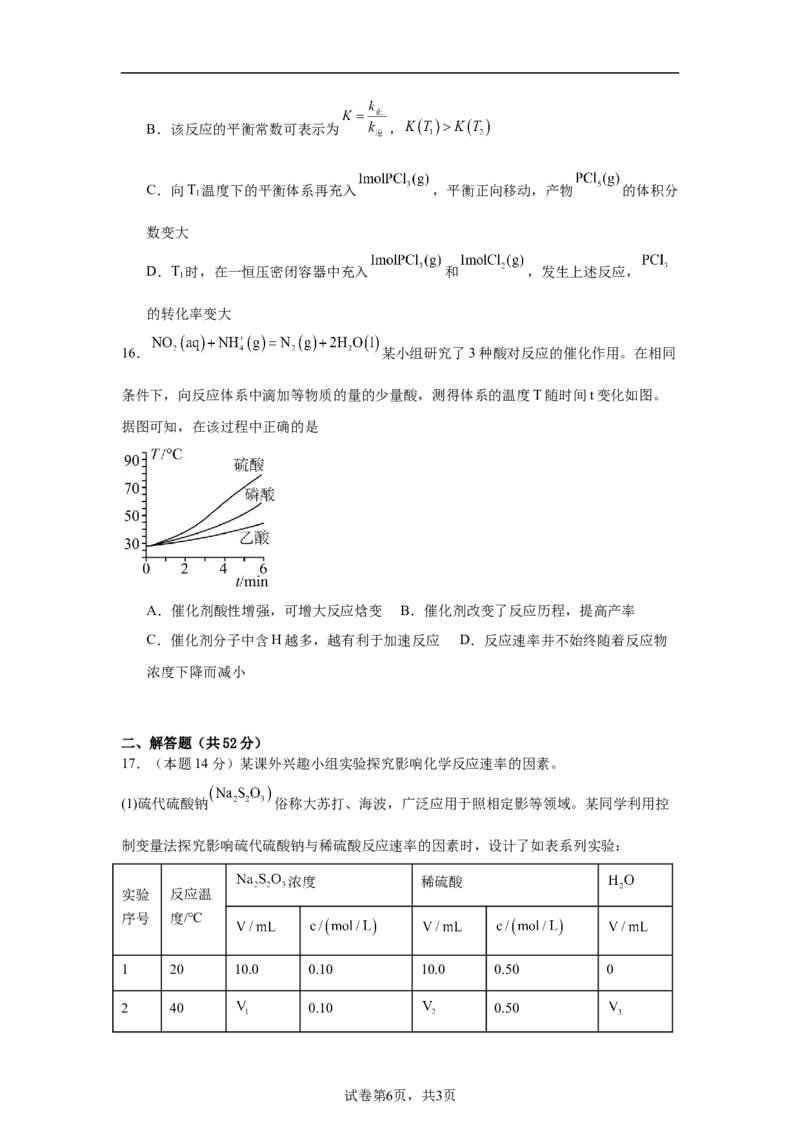
16. 某小组研究了3种酸对反应的催化作用。在相同
条件下,向反应体系中滴加等物质的量的少量酸,测得体系的温度T随时间t变化如图。
据图可知,在该过程中正确的是
A.催化剂酸性增强,可增大反应焓变 B.催化剂改变了反应历程,提高产率
C.催化剂分子中含H越多,越有利于加速反应 D.反应速率并不始终随着反应物
浓度下降而减小
二、解答题(共52分)
17.(本题14分)某课外兴趣小组实验探究影响化学反应速率的因素。
(1)硫代硫酸钠 俗称大苏打、海波,广泛应用于照相定影等领域。某同学利用控
制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如表系列实验:
浓度 稀硫酸
实验 反应温
序号 度/℃
1 20 10.0 0.10 10.0 0.50 0
2 40 0.10 0.50
试卷第6页,共3页3 20 0.10 4.0 0.50
①硫代硫酸钠与稀硫酸反应的化学方程式: 。
②该实验1和3可探究 对反应速率的影响,因此 mL。实验1和2可探
究温度对反应速率的影响,因此 mL。
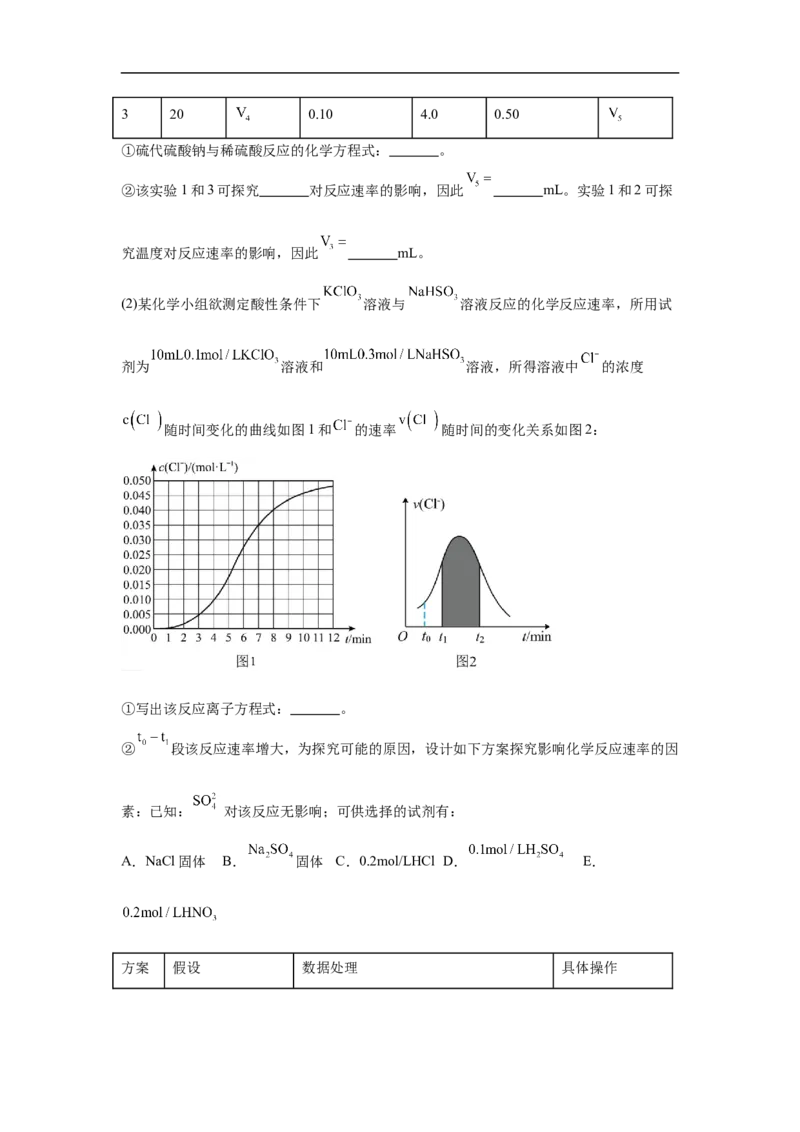
(2)某化学小组欲测定酸性条件下 溶液与 溶液反应的化学反应速率,所用试
剂为 溶液和 溶液,所得溶液中 的浓度
随时间变化的曲线如图1和 的速率 随时间的变化关系如图2:
①写出该反应离子方程式: 。
② 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因
素:已知: 对该反应无影响;可供选择的试剂有:
A.NaCl固体 B. 固体 C.0.2mol/LHCl D. E.
方案 假设 数据处理 具体操作取 溶液于烧杯
反应产物 对反
Ⅰ 应有催化作用,加 中,先加入_______(填字母),再加入
快了化学反应速率 溶液。
通过绘制
分别向两个烧杯中加
随时间变化的曲
反应中溶液酸性增 溶液。烧杯①: 线与图1对比
Ⅱ 强,加快了化学反 加入lmL水,烧杯②:加入
应速率 lmL_______(填字母)。再分别向两个烧
杯中加入 溶液。
a.方案Ⅰ中所选试剂 ,方案Ⅱ中所选试剂 。
b.除方案Ⅰ和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设 。
18.(本题12分)以软锰矿(主要成分为 、 等)为原料制备高纯 的流程如
下:
(1)滤渣中含大量硫单质,酸浸时主要反应的化学方程式: 。
(2)酸性条件下,用合适的氧化剂可以将 转化为高纯 。
①用 作氧化剂时会同时产生 ,该反应的离子方程式: 。
②反应中 的用量不宜过多的原因是 。
③用适量的 作氧化剂,反应后溶液中无锰元素剩余。理论上消耗 与生成
的 。
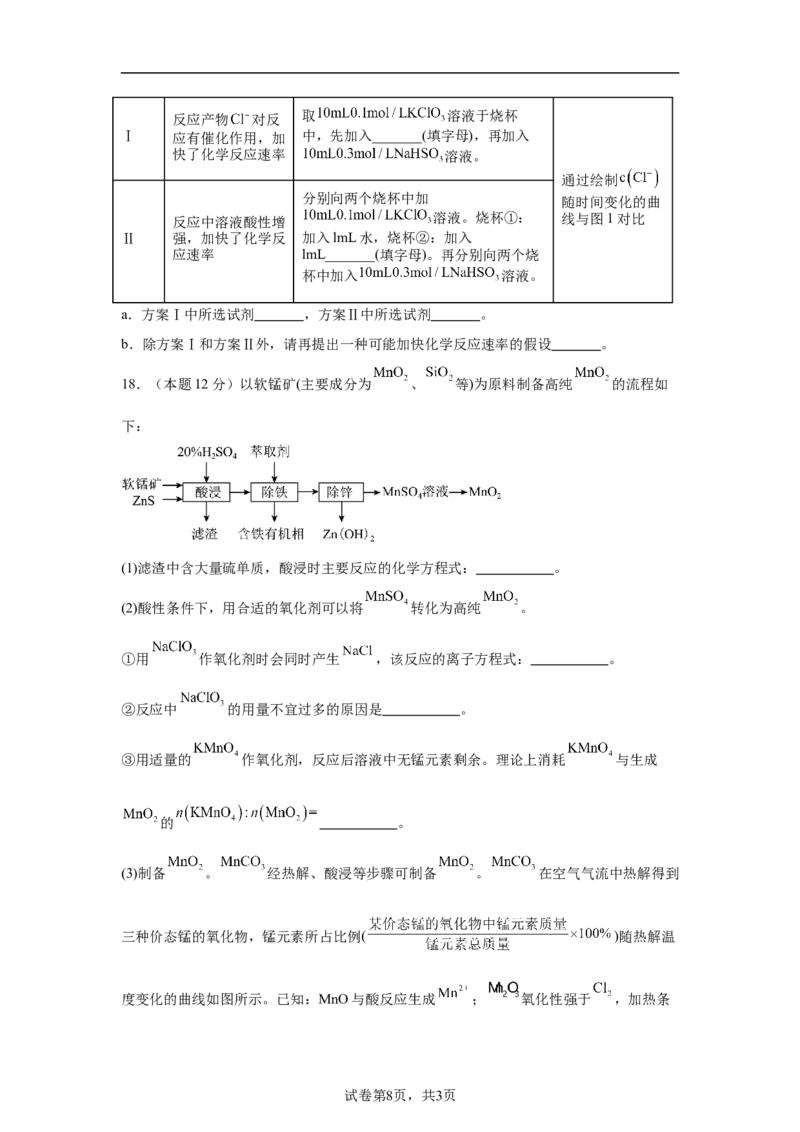
(3)制备 。 经热解、酸浸等步骤可制备 。 在空气气流中热解得到
三种价态锰的氧化物,锰元素所占比例( )随热解温
度变化的曲线如图所示。已知:MnO与酸反应生成 ; 氧化性强于 ,加热条
试卷第8页,共3页件下 在酸性溶液中转化为 和 。
为获得较高产率的 ,请补充实验方案:取一定量 置于热解装置中,通空气气
流,加热至 分解一段时间,将冷却后的固体边搅拌边分批加入 中,
加热,充分反应后过滤,洗涤,直到 ,说明洗涤干净,干燥,即得 。
(可选用的试剂: 溶液、 HCl溶液、 溶液、 溶液)。
19.(本题12分)某化学研究性学习小组用CO和H 模拟工业合成甲醇。
2
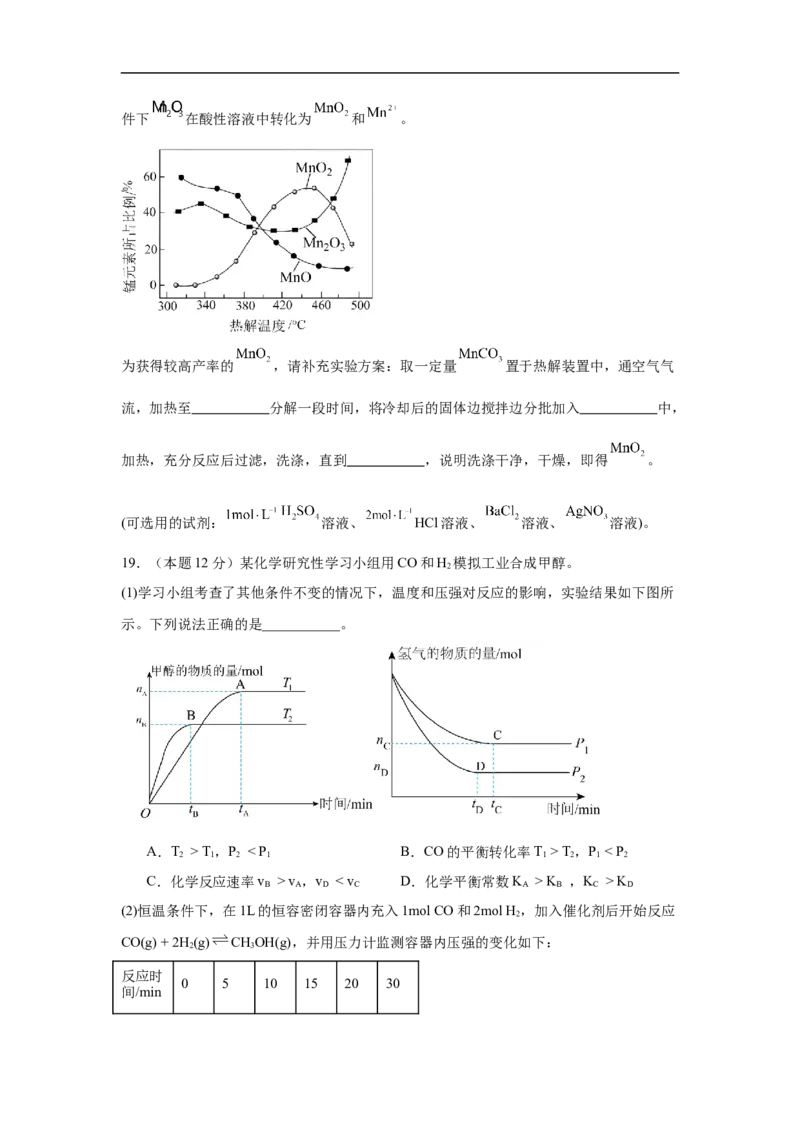
(1)学习小组考查了其他条件不变的情况下,温度和压强对反应的影响,实验结果如下图所
示。下列说法正确的是___________。
A.T > T,P < P B.CO的平衡转化率T > T,P < P
2 1 2 1 1 2 1 2
C.化学反应速率v > v ,v < v D.化学平衡常数K > K ,K > K
B A D C A B C D
(2)恒温条件下,在1L的恒容密闭容器内充入1mol CO和2mol H,加入催化剂后开始反应
2
CO(g) + 2H(g) CHOH(g),并用压力计监测容器内压强的变化如下:
2 3
反应时
0 5 10 15 20 30
间/min压
强/ 25.2 21.6 19.0 17.4 16.8 16.8
MPa
①下列说法正确的是 。
A.当n(CO):n(H ):n(CHOH) = 1:2:1时,反应达到平衡
2 3
B.容器内气体的平均相对分子质量不变,则反应达到平衡
C.在恒温恒容的平衡体系中充入Ar气,甲醇的产率升高
D.改变催化剂,反应物的平衡转化率不变
②从反应开始到20min时,CO的平均反应速率为 。
③其它条件不变,向容器中充入2mol CO和4mol H,则CO的平衡转化率 (填
2
“变大”“变小”或“不变”)。
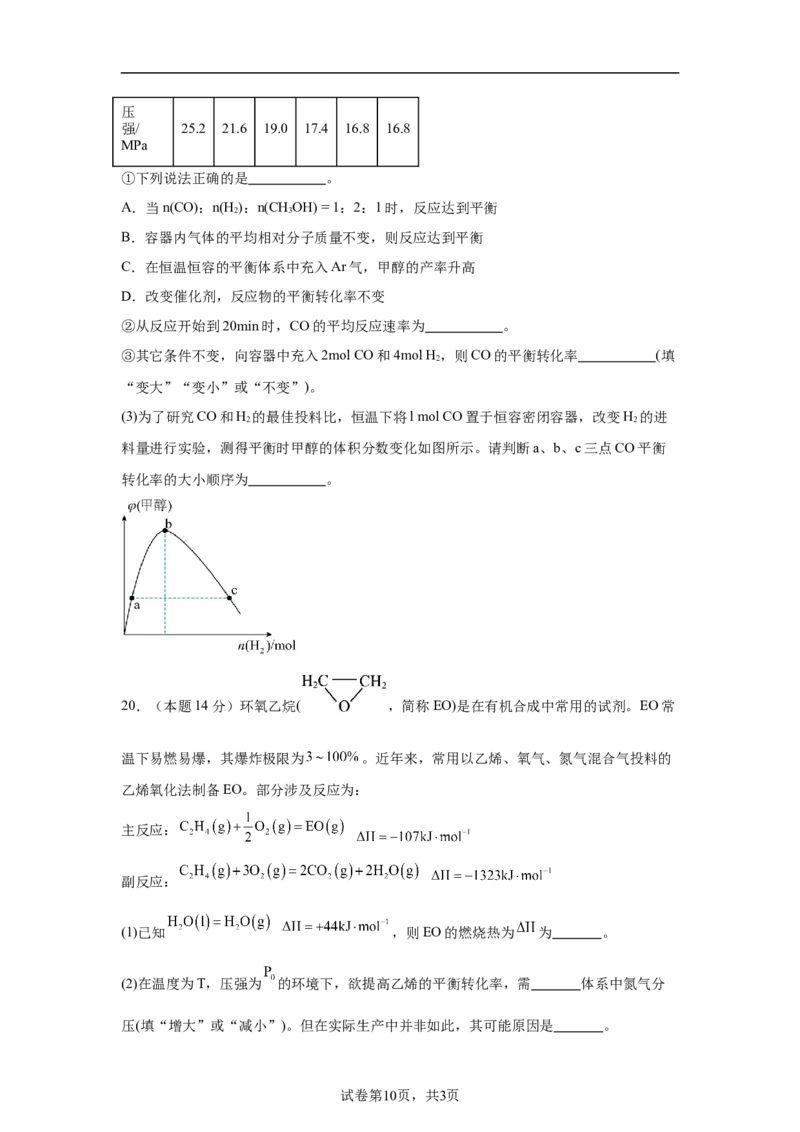
(3)为了研究CO和H 的最佳投料比,恒温下将l mol CO置于恒容密闭容器,改变H 的进
2 2
料量进行实验,测得平衡时甲醇的体积分数变化如图所示。请判断a、b、c三点CO平衡
转化率的大小顺序为 。
20.(本题14分)环氧乙烷( ,简称EO)是在有机合成中常用的试剂。EO常
温下易燃易爆,其爆炸极限为 。近年来,常用以乙烯、氧气、氮气混合气投料的
乙烯氧化法制备EO。部分涉及反应为:
主反应:
副反应:
(1)已知 ,则EO的燃烧热为 为 。
(2)在温度为T,压强为 的环境下,欲提高乙烯的平衡转化率,需 体系中氮气分
压(填“增大”或“减小”)。但在实际生产中并非如此,其可能原因是 。
试卷第10页,共3页(3)向温度为T,刚性容器中加入投料比为 的乙烯、氧气、氮气。已知平衡后:
, (其中二碳化合物为分子中含两个碳原子的化合物)。忽略
其他反应,乙烯的平衡转化率为 ,副反应的平衡常数 为 (列出计算式即
可)。
(4)以 为催化剂的反应机理如下:
反应Ⅰ: 慢
反应Ⅱ: 快
反应Ⅲ: 快
下列操作一定能够提高主反应反应速率的措施有_______(填标号)。
A.降低温度 B.通入氮气 C.增大 浓度 D.增大 浓度题号 1 2 3 4 5 6 7 8 9 10
答案 D D B B C C A C B B
题号 11 12 13 14 15 16
答案 B D C B C D
17.(1) 硫酸浓度对反应速率的影响
6.0 0.0
(2) +3 =Cl-+3 +3H+ A D 温度升高,加快了化学反应速率
18.(1)
(2) 过量的NaClO 在酸性条件下与Cl-
3
反应会生成有毒的Cl 2:5
2
(3) 450℃ 溶液 加热,充分反应后过滤,洗涤,取最后一次
洗涤滤液加盐酸酸化的 溶液不变浑浊
19.(1)B
(2) BD 0.025mol·L-1·min-1 变大
(3)c>b>a
20.(1)
(2) 减小 EO在常温下易燃易爆,其爆炸极限为3%~100%,需加入氮气稀释气体,
防止环氧乙烷浓度高而爆炸
(3) 50% 或
(4)D