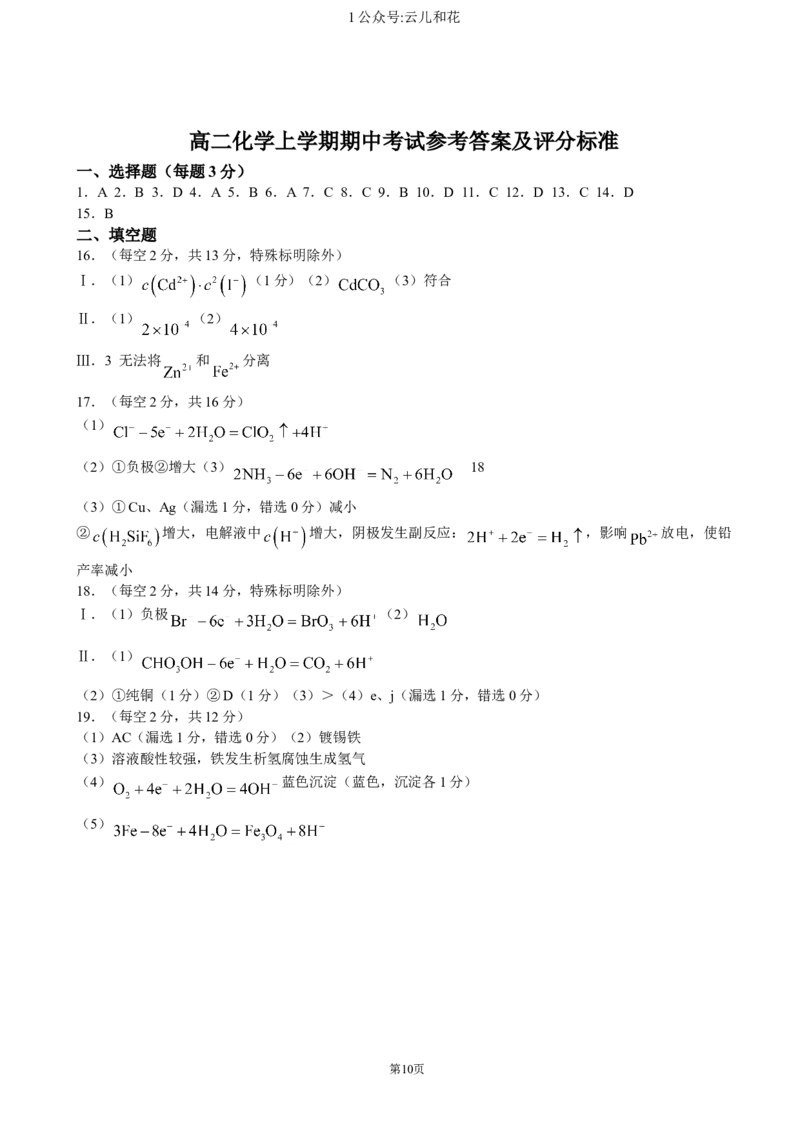文档内容
1公众号:云儿和花
辽宁省重点高中沈阳市郊联体
2024—2025 学年度上学期期中考试高二年级试题
化学
考试时间:75分钟试卷总分:100分
注意事项:
本试卷由第Ⅰ卷和第Ⅱ卷组成。第Ⅰ卷为选择题部分,一律答在答题卡上;第Ⅱ卷为非选择题部分,按要
求答在答题卡相应位置上。
可能用到的相对原子质量:H1C 12N14O16F19P31K39Fe56Cu64Zn65Cd112
Pb207
第Ⅰ卷选择题(共45分)
一、选择题(本题共15个小题,每小题3分,共45分。每小题只有1个选项符合题意)
1.化学与社会、生活密切相关。下列说法正确的是()
A.人体血液中存在缓冲体系,可以维持较小的pH变化范围
B.含较多 的盐碱地可通过施加适量熟石灰进行改良
C.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理
D.制造焊锡时,把铅加入锡,形成原电池,从而增加锡的抗腐蚀能力
2.能正确表示下列变化的离子方程式是()
A.泡沫灭火器原理:
B.用银作电极电解稀盐酸:
C.在水溶液中 的水解方程式:
D.方铅矿(PbS)遇 溶液生成铜蓝(CuS);
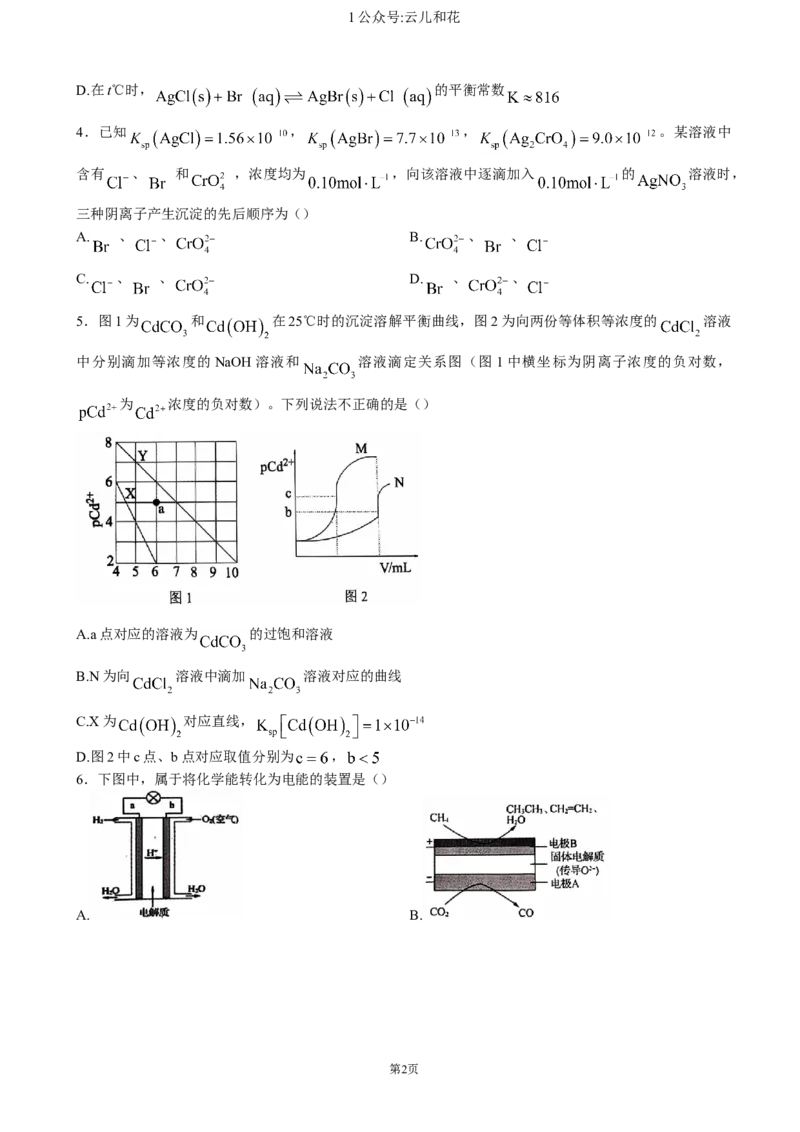
3.在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t℃时AgCl的 ,下列说法正
确的是()
A.常温下,AgBr的
B.在t℃时,图中a点对应的是AgBr的饱和溶液
C.只改变温度,可使溶液由c点到b点
第1页
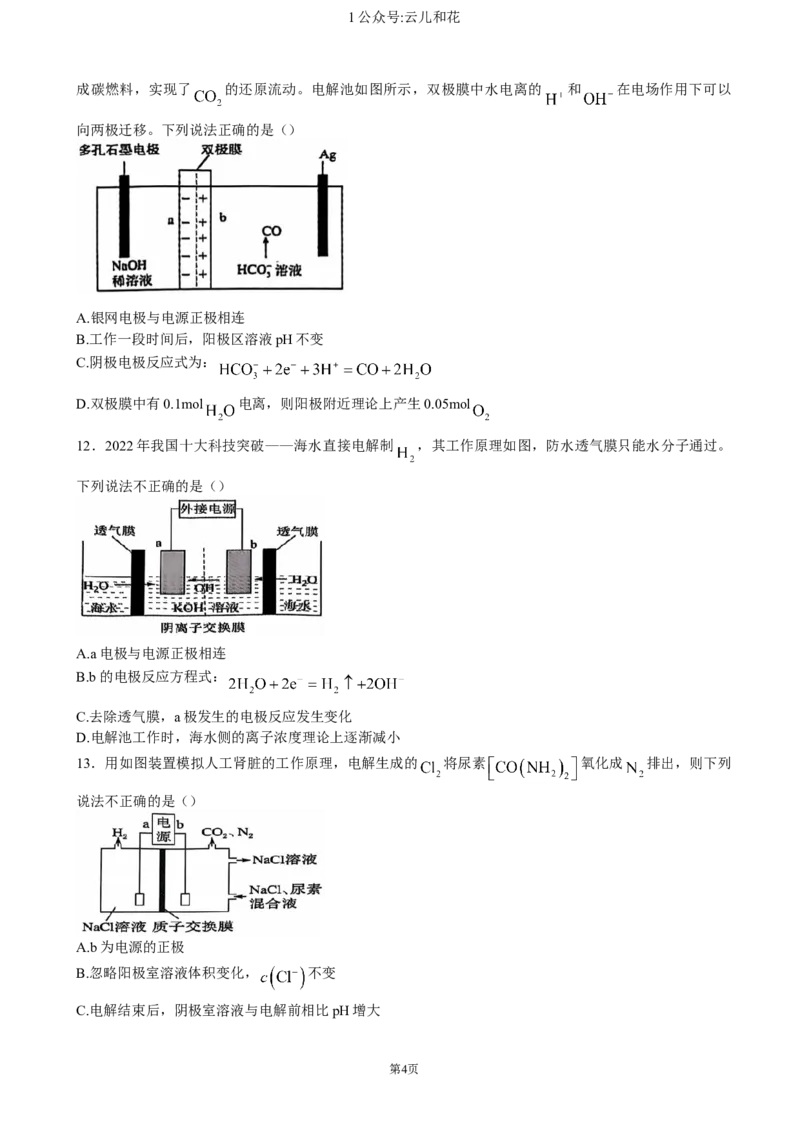
Br1公众号:云儿和花
D.在t℃时, 的平衡常数
4.已知 , , 。某溶液中
含有 、 和 ,浓度均为 ,向该溶液中逐滴加入 的 溶液时,
三种阴离子产生沉淀的先后顺序为()
A. 、 、 B. 、 、
C. 、 、 D. 、 、
5.图1为 和 在25℃时的沉淀溶解平衡曲线,图2为向两份等体积等浓度的 溶液
中分别滴加等浓度的NaOH溶液和 溶液滴定关系图(图1中横坐标为阴离子浓度的负对数,
为 浓度的负对数)。下列说法不正确的是()
A.a点对应的溶液为 的过饱和溶液
B.N为向 溶液中滴加 溶液对应的曲线
C.X为 对应直线,
D.图2中c点、b点对应取值分别为 ,
6.下图中,属于将化学能转化为电能的装置是()
A. B.
第2页1公众号:云儿和花
C. D.
7.应用电解法制备的物质主要有三种:一是铝的工业制备;二是电解饱和NaCl溶液制备烧碱;三是金属
钠的制备。下列关于这三个工业生产的描述中不正确的是()
A.电解法制铝时一般是用熔融态的氧化铝进行电解,但不可用熔融态的
B.电解法生产铝时,每转移3mol电子的时候,理论上就能生产出1mol的铝单质
C.电解饱和NaCl溶液和金属钠的冶炼都用到了NaCl,电解时它们的阳极都是 得电子
D.在电解饱和NaCl溶液中,电解池中的阴极区产生的是 和NaOH
8.串联电路中的四个电解池分别装有 的下列溶液,连接直流电源,用铂电极电解一段时间后,
溶液的pH明显变小的是()
A.盐酸 B.NaCl C. D.
9.在世界海运史上曾发生过这样一个悲剧:一艘名叫“阿那吉纳”的货轮满载着精铜砂,在向日本海岸
行驶时突然发生大面积漏水,最终沉没。坚硬的钢制船体为什么会突然漏水呢?事后的事故调查结果表明
导致沉船的原因与船上的精铜砂密切相关。下列对此调查结论的理解正确的是()
A.精铜砂装载过多导致沉船
B.在潮湿的环境中,船体与铜构成了原电池,加速了作为负极的船体的腐蚀
C.在潮湿的环境中,船体与铜构成了电解池,钢制船体作阳极而被氧化腐蚀
D.运输途中铜与空气中的氧气发生氧化反应导致质量增大超过船的承载能力
10.将电化学法和生物还原法有机结合,利用微生物电化学方法可生产甲烷,装置如图所示。下列说法正
确的是()
A.通电时,电子由b→电解池阴极→电解液→电解池阳极→a
B.X为阴离子交换膜
C.生成0.1mol甲烷时阳极室理论上生成4.48L二氧化碳
D.阳极反应式为:
11.为实现“碳中和”目标,实现 循环利用,现利用双极膜电解含有 的溶液,使 转化
第3页1公众号:云儿和花
成碳燃料,实现了 的还原流动。电解池如图所示,双极膜中水电离的 和 在电场作用下可以
向两极迁移。下列说法正确的是()
A.银网电极与电源正极相连
B.工作一段时间后,阳极区溶液pH不变
C.阴极电极反应式为:
D.双极膜中有0.1mol 电离,则阳极附近理论上产生0.05mol
12.2022年我国十大科技突破——海水直接电解制 ,其工作原理如图,防水透气膜只能水分子通过。
下列说法不正确的是()
A.a电极与电源正极相连
B.b的电极反应方程式:
C.去除透气膜,a极发生的电极反应发生变化
D.电解池工作时,海水侧的离子浓度理论上逐渐减小
13.用如图装置模拟人工肾脏的工作原理,电解生成的 将尿素 氧化成 排出,则下列
说法不正确的是()
A.b为电源的正极
B.忽略阳极室溶液体积变化, 不变
C.电解结束后,阴极室溶液与电解前相比pH增大
第4页1公众号:云儿和花
D.阳极收集到 4.48L(标准状况)时,被氧化的尿素为4.0g
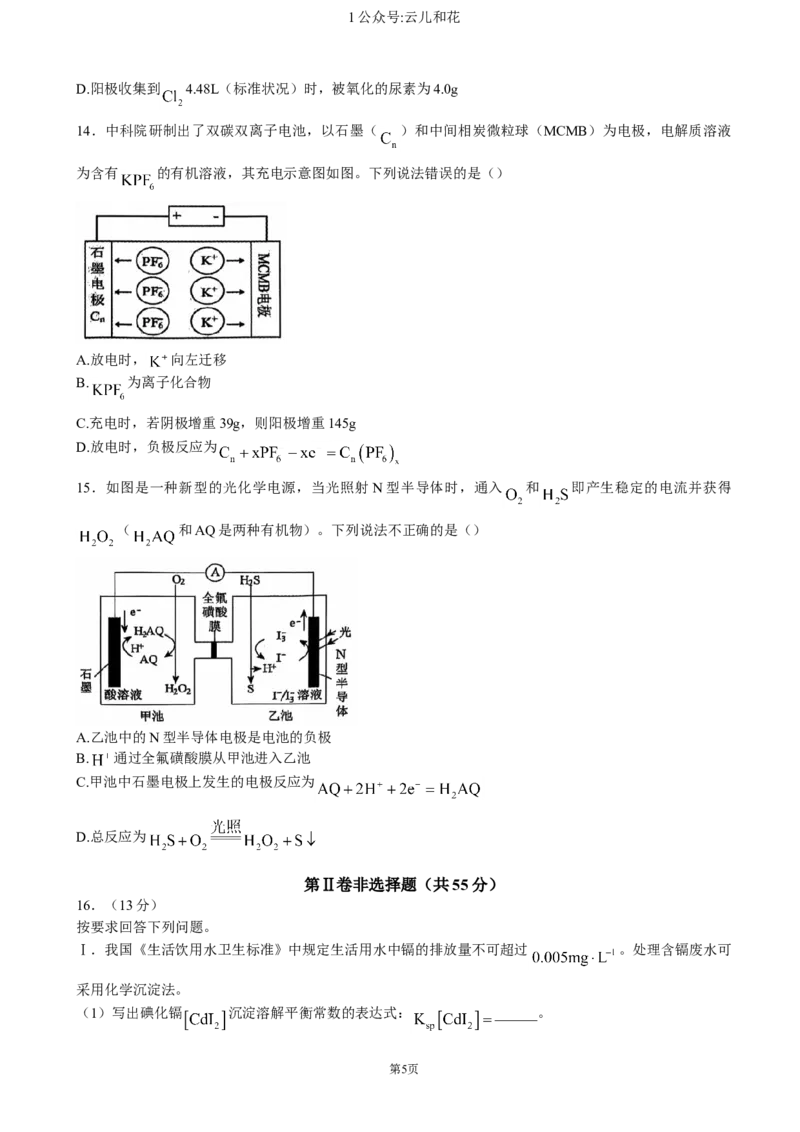
14.中科院研制出了双碳双离子电池,以石墨( )和中间相炭微粒球(MCMB)为电极,电解质溶液
为含有 的有机溶液,其充电示意图如图。下列说法错误的是()
A.放电时, 向左迁移
B. 为离子化合物
C.充电时,若阴极增重39g,则阳极增重145g
D.放电时,负极反应为
15.如图是一种新型的光化学电源,当光照射N型半导体时,通入 和 即产生稳定的电流并获得
( 和AQ是两种有机物)。下列说法不正确的是()
A.乙池中的N型半导体电极是电池的负极
B. 通过全氟磺酸膜从甲池进入乙池
C.甲池中石墨电极上发生的电极反应为
D.总反应为
第Ⅱ卷非选择题(共55分)
16.(13分)
按要求回答下列问题。
Ⅰ.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不可超过 。处理含镉废水可
采用化学沉淀法。
(1)写出碘化镉 沉淀溶解平衡常数的表达式: ______。
第5页1公众号:云儿和花
(2)一定温度下, 的 , 的 ,该温度下______[填“
”或“ ”]的饱和溶液中 浓度较小。
(3)向某含镉废水中加入 ,当 浓度达到 时,此时废水中 ______(填
“符合”或“不符合”)《生活饮用水卫生标准》。[已知 ]
Ⅱ.(1) 溶液与 溶液混合会生成难溶的 ( ),现将等体积的
溶液与 溶液混合,若混合前 溶液的浓度为 ,则生成沉淀所需
溶液的最小浓度为______ 。
(2)在某温度下, ,FeS 饱和溶液中 与 之间存在关系:
,为了使溶液里 达到 ,现将适量FeS投入其饱和溶液
中,应调节溶液中的 约为______ 。
Ⅲ.已知:部分难溶化合物的相关数据如下表所示:
化合物
近似值
用废电池的锌皮制备 的过程中,需除去锌皮中的少量杂质铁,其方法是加足量的稀
和 溶解,并在常温下加碱调节至 ______时,铁元素刚好沉淀完全(离子浓度小于
时,即可认为该离子沉淀完全)。若上述过程未加入 ,会导致的后果是______。
17.(16分)
(1)目前已开发出电解法制取 的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取 ,
写出阳极产生 的电极反应式:______。
(2)相同金属与其不同浓度盐溶液可形成浓差电池。以浓差电池为电源,利用 制备高纯 和 的
装置如图所示(M、N均为石墨电极)。
①甲池中Cu电极为______(填“正极”或“负极”)
②电解一段时间后,丁室中KOH的浓度______(填“增大”“减小”或“不变”)。
③M极发生的电极反应式为______;电路中每通过1moL电子,丁池溶液质量减少______g。
第6页1公众号:云儿和花
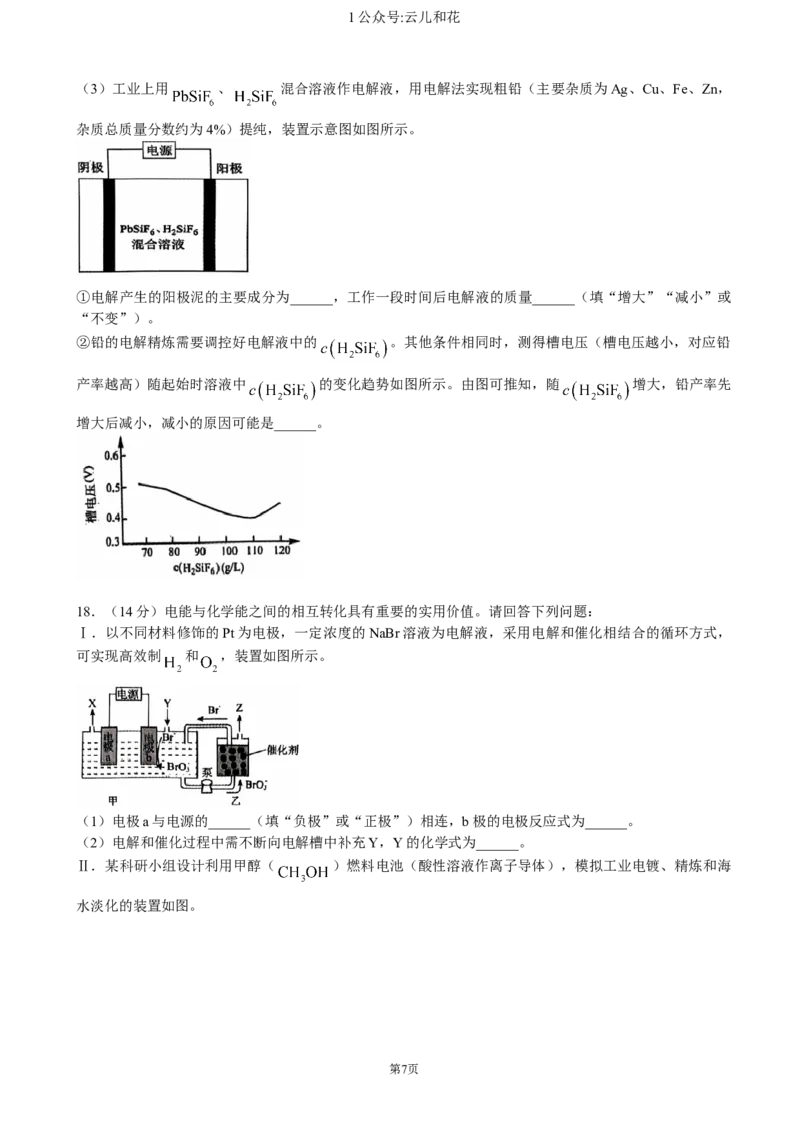
(3)工业上用 、 混合溶液作电解液,用电解法实现粗铅(主要杂质为Ag、Cu、Fe、Zn,
杂质总质量分数约为4%)提纯,装置示意图如图所示。
①电解产生的阳极泥的主要成分为______,工作一段时间后电解液的质量______(填“增大”“减小”或
“不变”)。
②铅的电解精炼需要调控好电解液中的 。其他条件相同时,测得槽电压(槽电压越小,对应铅
产率越高)随起始时溶液中 的变化趋势如图所示。由图可推知,随 增大,铅产率先
增大后减小,减小的原因可能是______。
18.(14分)电能与化学能之间的相互转化具有重要的实用价值。请回答下列问题:
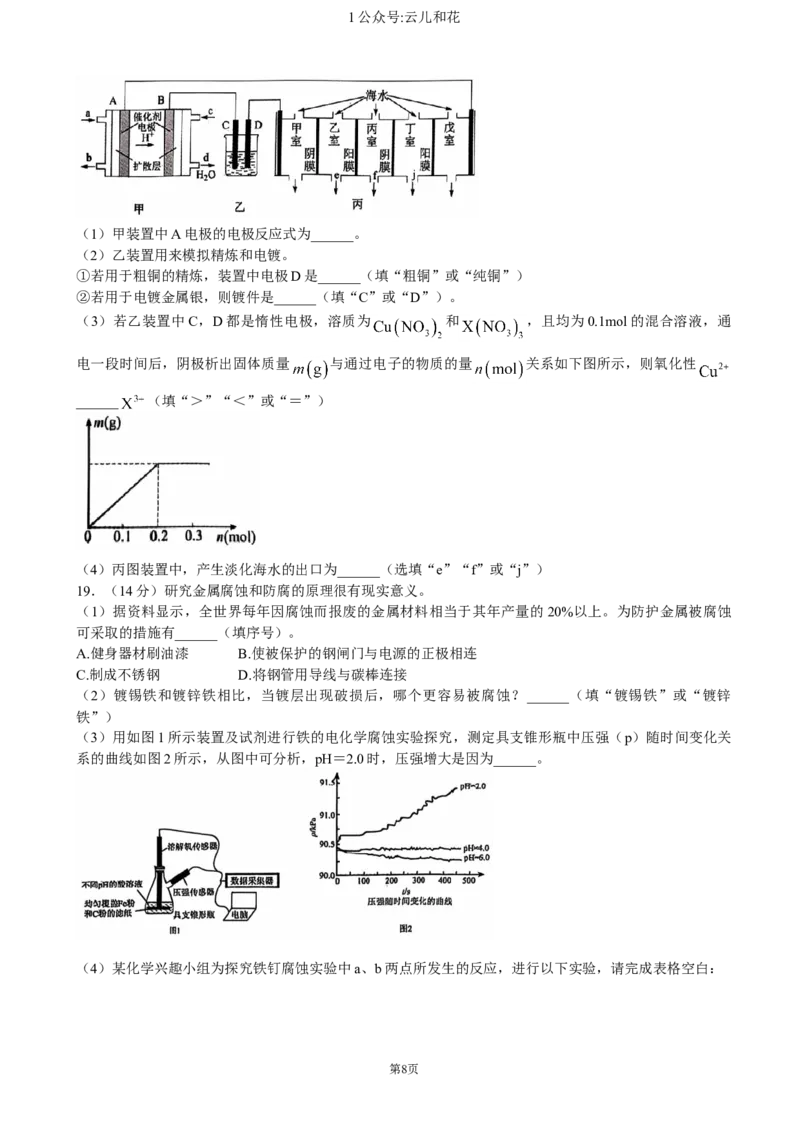
Ⅰ.以不同材料修饰的Pt为电极,一定浓度的NaBr溶液为电解液,采用电解和催化相结合的循环方式,
可实现高效制 和 ,装置如图所示。
(1)电极a与电源的______(填“负极”或“正极”)相连,b极的电极反应式为______。
(2)电解和催化过程中需不断向电解槽中补充Y,Y的化学式为______。
Ⅱ.某科研小组设计利用甲醇( )燃料电池(酸性溶液作离子导体),模拟工业电镀、精炼和海
水淡化的装置如图。
第7页1公众号:云儿和花
(1)甲装置中A电极的电极反应式为______。
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极D是______(填“粗铜”或“纯铜”)
②若用于电镀金属银,则镀件是______(填“C”或“D”)。
(3)若乙装置中C,D都是惰性电极,溶质为 和 ,且均为0.1mol的混合溶液,通
电一段时间后,阴极析出固体质量 与通过电子的物质的量 关系如下图所示,则氧化性
______ (填“>”“<”或“=”)
(4)丙图装置中,产生淡化海水的出口为______(选填“e”“f”或“j”)
19.(14分)研究金属腐蚀和防腐的原理很有现实意义。
(1)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上。为防护金属被腐蚀
可采取的措施有______(填序号)。
A.健身器材刷油漆 B.使被保护的钢闸门与电源的正极相连
C.制成不锈钢 D.将钢管用导线与碳棒连接
(2)镀锡铁和镀锌铁相比,当镀层出现破损后,哪个更容易被腐蚀?______(填“镀锡铁”或“镀锌
铁”)
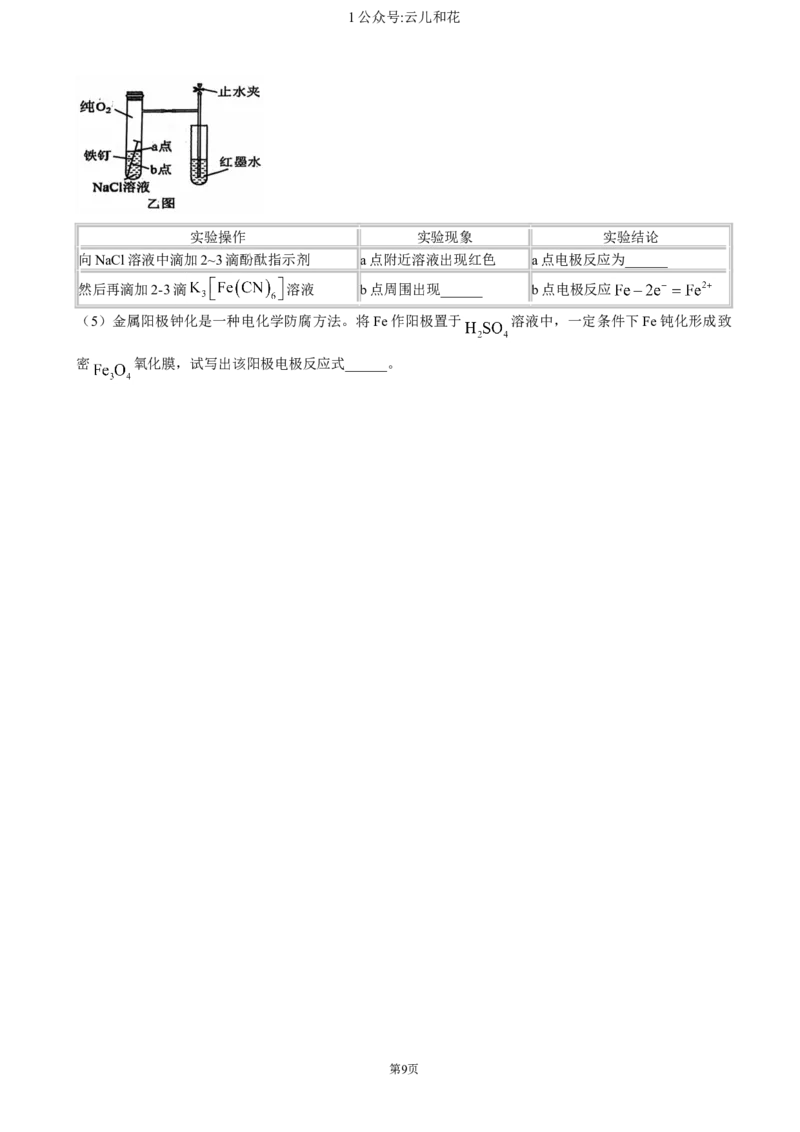
(3)用如图1所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强(p)随时间变化关
系的曲线如图2所示,从图中可分析,pH=2.0时,压强增大是因为______。
(4)某化学兴趣小组为探究铁钉腐蚀实验中a、b两点所发生的反应,进行以下实验,请完成表格空白:
第8页1公众号:云儿和花
实验操作 实验现象 实验结论
向NaCl溶液中滴加2~3滴酚酞指示剂 a点附近溶液出现红色 a点电极反应为______
然后再滴加2-3滴 溶液 b点周围出现______ b点电极反应
(5)金属阳极钟化是一种电化学防腐方法。将Fe作阳极置于 溶液中,一定条件下Fe钝化形成致
密 氧化膜,试写出该阳极电极反应式______。
第9页1公众号:云儿和花
高二化学上学期期中考试参考答案及评分标准
一、选择题(每题3分)
1.A 2.B 3.D 4.A 5.B 6.A 7.C 8.C 9.B 10.D 11.C 12.D 13.C 14.D
15.B
二、填空题
16.(每空2分,共13分,特殊标明除外)
Ⅰ.(1) (1分)(2) (3)符合
Ⅱ.(1) (2)
Ⅲ.3 无法将 和 分离
17.(每空2分,共16分)
(1)
(2)①负极②增大(3) 18
(3)①Cu、Ag(漏选1分,错选0分)减小
② 增大,电解液中 增大,阴极发生副反应: ,影响 放电,使铅
产率减小
18.(每空2分,共14分,特殊标明除外)
Ⅰ.(1)负极 (2)
Ⅱ.(1)
(2)①纯铜(1分)②D(1分)(3)>(4)e、j(漏选1分,错选0分)
19.(每空2分,共12分)
(1)AC(漏选1分,错选0分)(2)镀锡铁
(3)溶液酸性较强,铁发生析氢腐蚀生成氢气
(4) 蓝色沉淀(蓝色,沉淀各1分)
(5)
第10页