文档内容
湖北省随州市部分高中2024--2025学年下学期2月联考
高二化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
考试范围:
选择性必修2 物质结构与性质
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答
题卡上,并将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的
答案标号涂黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在
试卷、草稿纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符
合题意。
1、在宾馆、办公楼等公共场所,常使用一种电离式烟雾报警器,其主体是
一个放有镅-241(Am)放射源的电离室。Am原子核内中子数与核外电子数之差
是( )
A.241 B.146
C.95 D.51
2、X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结
构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上 s、p电子
数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M
层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是( )
A.X元素的氢化物的水溶液显碱性
B.Z元素的离子半径小于W元素的离子半径
C.Z元素的单质在一定条件下能与X元素的单质反应
D.基态Y原子的电子跃迁到较高能量的激发态时,会形成发射光谱
3、已知短周期主族元素X、Y、Z、W的原子序数依次增大,其中W和X原子的最外层电子数之差等于Z与Y原子的最外层电子数之差。它们形成的单
质和化合物之间转化的关系如图,常温下 d 是无色液体,液态 f 可用作制冷
剂。下列说法不正确的是( )
A.简单离子半径:Y>Z>W
B.第一电离能:Z>Y
C.电负性:Z>Y>X
D.X、Z形成的化合物中可能含有非极性键和极性键
4、前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量
最多的元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个
电子,W与Z处于同主族。下列说法错误的是( )
A.X能与多种元素形成共价键
B.X的第一电离能比同周期相邻元素的大
C.Y的电负性比Z的强
D.Z的简单气态氢化物的热稳定性比W的强
5、键长、键角和键能是描述共价键的三个重要参数,下列叙述正确的是(
)
A.键角是描述分子空间结构的重要参数
B.因为H—O键的键能小于H—F键的键能,所以O 、F 与H 反应的能力
2 2 2
逐渐减弱
C.AB 型分子的键角均为180°
2
D.H—O键的键能为462.8 kJ·mol-1,即18 g H O分解成H 和O 时,消
2 2 2
耗的能量为2×462.8 kJ
6、北京大学和中国科学院的化学工作者已成功研制出碱金属 K与C 形成
60
的球碳盐K C ,实验测知该物质为离子化合物,具有良好的超导性能。下列有
3 60
关分析正确的是( )
A.K C 中只含有离子键
3 60
B.K C 中既含有离子键又含有共价键
3 60C.该晶体在熔融状态下不能导电
D.C 与12C互为同素异形体
60
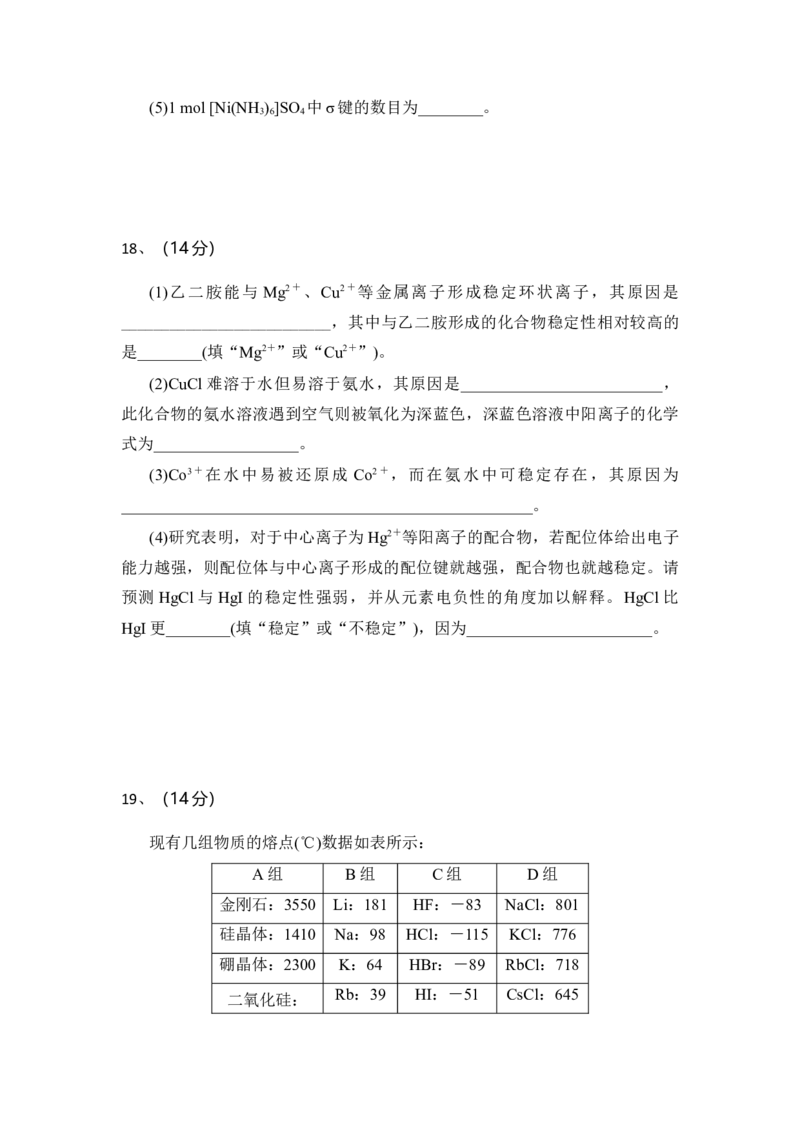
7、已知吡啶( )中含有与苯类似的π大π键,则吡啶中N原子的价层孤
电子对占据________(填标号)。
A.2s轨道 B.2p轨道
C.sp杂化轨道 D.sp2杂化轨道
8、下列关于BeF 和SF 的说法错误的是( )
2 2
A.BeF 分子中,中心原子Be的价层电子对数等于 2,成键电子对数也等
2
于2
B.BeF 分子的孤电子对数为0
2
C.SF 分子中,中心原子S的价层电子对数等于4,其空间结构为四面体
2
形,成键电子对数等于2,没有孤电子对
D.在气相中,BeF 是直线形而SF 是V形
2 2
9、下列关于超分子的说法中,不正确的是( )
A.超分子是由两种或两种以上的分子必须通过氢键相互作用形成的分子聚
集体
B.将C 加入一种空腔大小适配C 的“杯酚”中会形成超分子
60 60
C.碱金属离子虽然不是分子,但冠醚在识别碱金属离子时,形成的也是超
分子
D.超分子的重要特征是自组装和分子识别
10、液氨、液氯、清洗剂、萃取剂等重点品种使用企业和白酒企业,应加
强储罐区、危化品库房、危化品输送等的管理,确保化工生产安全。下列说法
正确的是( )
A.液氨中只存在范德华力
B.液氨分子间作用力强,所以其稳定性大于PH
3
C.液氯挥发导致人体吸入后中毒,是因为液氯分子中的共价键键能较小
D.萃取剂CCl 的沸点高于CH 的沸点
4 4
11、下列数据是对应物质的熔点(℃):
BCl Al O Na O NaCl AlF AlCl 干冰 SiO
3 2 3 2 3 3 2-107 2073 920 801 1291 190 -57 1723
据此做出的下列判断错误的是 ( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl 和干冰是分子晶体
3
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
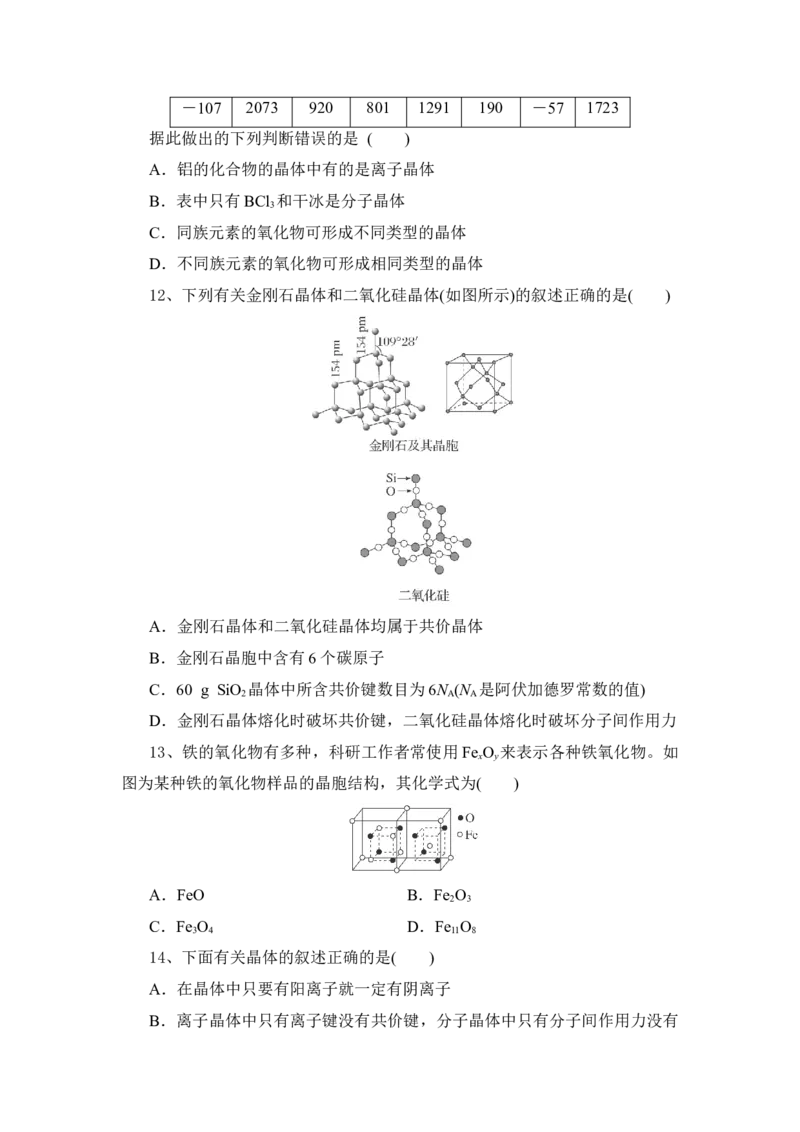
12、下列有关金刚石晶体和二氧化硅晶体(如图所示)的叙述正确的是( )
A.金刚石晶体和二氧化硅晶体均属于共价晶体
B.金刚石晶胞中含有6个碳原子
C.60 g SiO 晶体中所含共价键数目为6N (N 是阿伏加德罗常数的值)
2 A A
D.金刚石晶体熔化时破坏共价键,二氧化硅晶体熔化时破坏分子间作用力
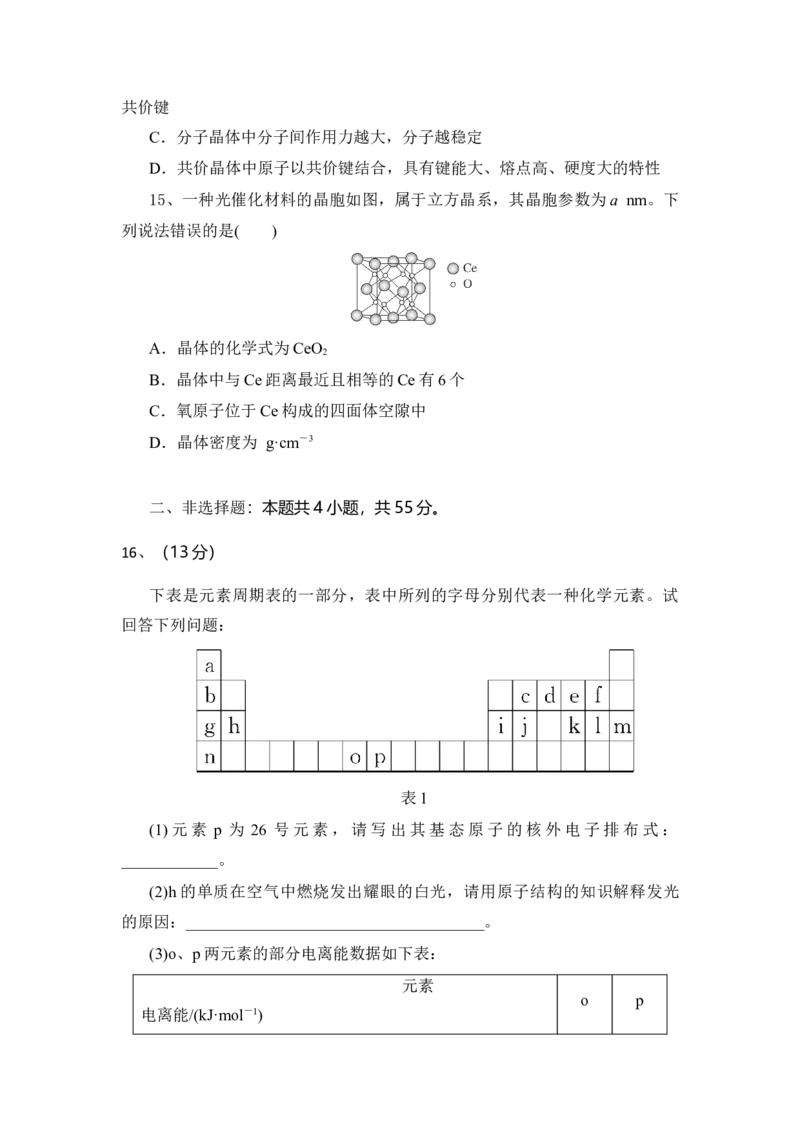
13、铁的氧化物有多种,科研工作者常使用Fe O 来表示各种铁氧化物。如
x y
图为某种铁的氧化物样品的晶胞结构,其化学式为( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe O
3 4 11 8
14、下面有关晶体的叙述正确的是( )
A.在晶体中只要有阳离子就一定有阴离子
B.离子晶体中只有离子键没有共价键,分子晶体中只有分子间作用力没有共价键
C.分子晶体中分子间作用力越大,分子越稳定
D.共价晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
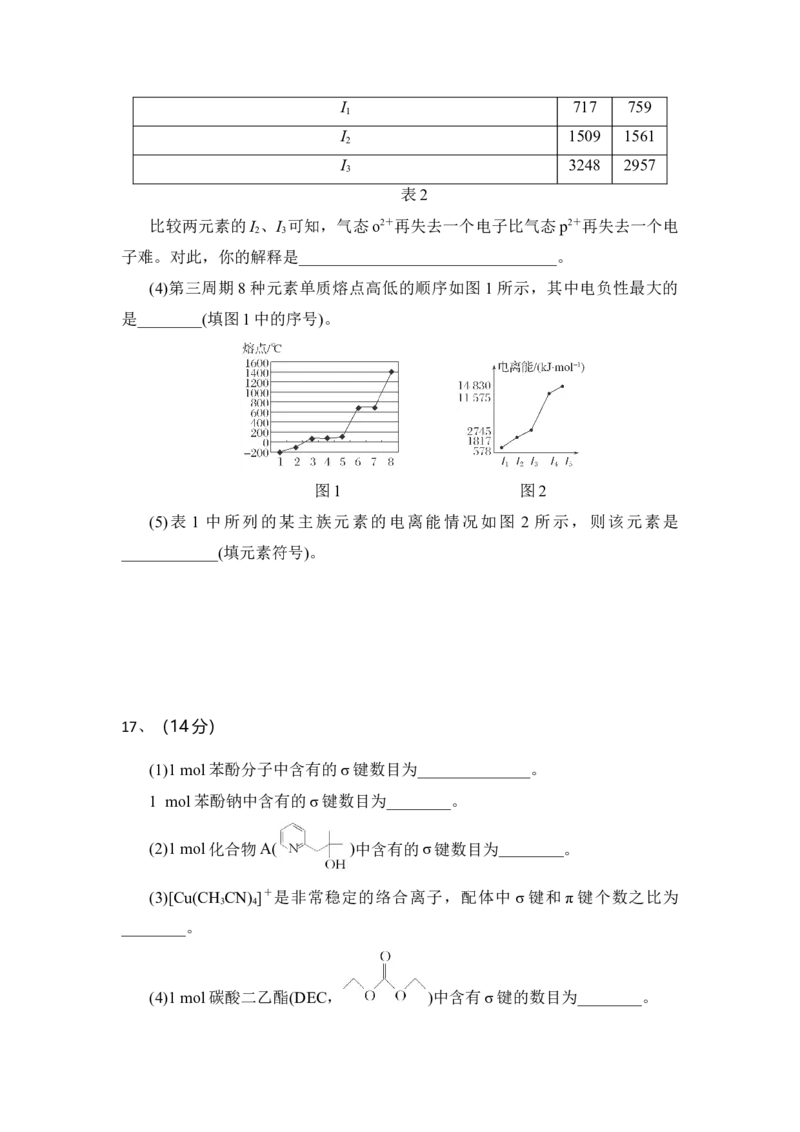
15、一种光催化材料的晶胞如图,属于立方晶系,其晶胞参数为a nm。下
列说法错误的是( )
A.晶体的化学式为CeO
2
B.晶体中与Ce距离最近且相等的Ce有6个
C.氧原子位于Ce构成的四面体空隙中
D.晶体密度为 g·cm-3
二、非选择题:本题共4小题,共55分。
16、(13分)
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试
回答下列问题:
表1
(1)元素 p 为 26 号元素,请写出其基态原子的核外电子排布式:
____________。
(2)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光
的原因:_____________________________________。
(3)o、p两元素的部分电离能数据如下表:
元素
o p
电离能/(kJ·mol-1)I 717 759
1
I 1509 1561
2
I 3248 2957
3
表2
比较两元素的I 、I 可知,气态o2+再失去一个电子比气态p2+再失去一个电
2 3
子难。对此,你的解释是________________________________。
(4)第三周期8种元素单质熔点高低的顺序如图 1所示,其中电负性最大的
是________(填图1中的序号)。
图1 图2
(5)表 1 中所列的某主族元素的电离能情况如图 2 所示,则该元素是
____________(填元素符号)。
17、(14分)
(1)1 mol苯酚分子中含有的σ键数目为______________。
1 mol苯酚钠中含有的σ键数目为________。
(2)1 mol化合物A( )中含有的σ键数目为________。
(3)[Cu(CH CN) ]+是非常稳定的络合离子,配体中 σ 键和 π 键个数之比为
3 4
________。
(4)1 mol碳酸二乙酯(DEC, )中含有σ键的数目为________。(5)1 mol [Ni(NH ) ]SO 中σ键的数目为________。
3 6 4
18、(14分)
(1)乙二胺能与 Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是
__________________________,其中与乙二胺形成的化合物稳定性相对较高的
是________(填“Mg2+”或“Cu2+”)。
(2)CuCl难溶于水但易溶于氨水,其原因是_________________________,
此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学
式为__________________。
(3)Co3+在水中易被还原成 Co2+,而在氨水中可稳定存在,其原因为
___________________________________________________。
(4)研究表明,对于中心离子为Hg2+等阳离子的配合物,若配位体给出电子
能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。请
预测 HgCl 与 HgI 的稳定性强弱,并从元素电负性的角度加以解释。HgCl 比
HgI更________(填“稳定”或“不稳定”),因为_______________________。
19、(14分)
现有几组物质的熔点(℃)数据如表所示:
A组 B组 C组 D组
金刚石:3550 Li:181 HF:-83 NaCl:801
硅晶体:1410 Na:98 HCl:-115 KCl:776
硼晶体:2300 K:64 HBr:-89 RbCl:718
Rb:39 HI:-51 CsCl:645
二氧化硅:1723
据此回答下列问题:
(1)A 组 属 于 ________ 晶 体 , 其 熔 化 时 克 服 的 微 粒 间 的 作 用 力 是
______________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性
④延展性
(3)C组中HF熔点反常是因为_______________________________。
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电
④熔融状态能导电