文档内容
赤峰第四中学 2024-2025 学年第二学期月考试题
高二化学
考试时间:75 分钟 满分:100 分
第Ⅰ卷 (选择题,共 45 分)
一、选择题(每小题只有一个正确选项,每小题 3 分)
1.对充有氖气的霓虹灯管通电,灯管发出红色光。这一现象的主要原因是
A.电子由激发态向基态跃迁时以红光的形式释放能量
B.电子由基态向激发态跃迁时吸收除红光以外的光线
C.氖原子获得电子后转变成发出红光的物质
D.在电流的作用下,氖原子与构成灯管的物质发生反应
2.下列有关叙述正确的是
A.π键是由两个 p 电子“头碰头”重叠形成的
B.电子云图中小黑点表示电子在原子核外出现的概率密度
C.同一原子中,1s、2s、3s 能级的轨道数依次增多
D.p 能级能量一定比 s 能级的能量高
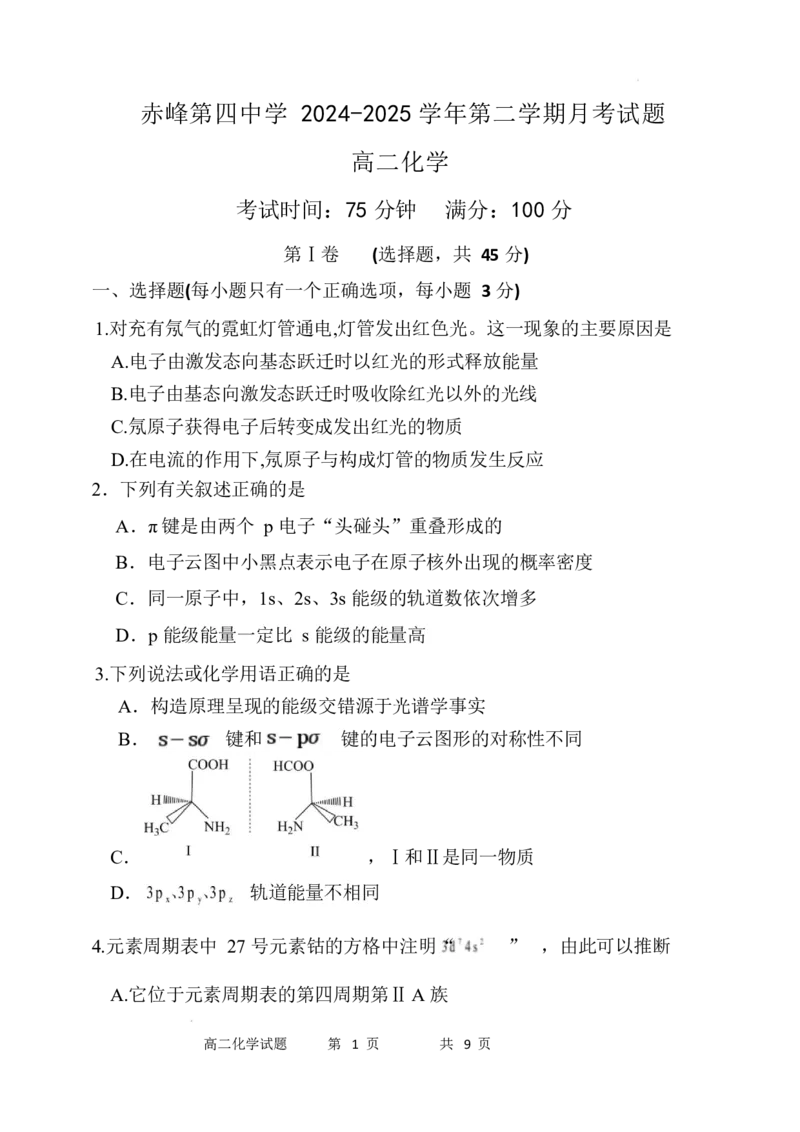
3.下列说法或化学用语正确的是
A.构造原理呈现的能级交错源于光谱学事实
B. 键和 键的电子云图形的对称性不同
C. ,Ⅰ和Ⅱ是同一物质
D. 轨道能量不相同
4.元素周期表中 27 号元素钴的方格中注明“ ” ,由此可以推断
A.它位于元素周期表的第四周期第ⅡA 族
高二化学试题 第 1 页 共 9 页B.它的基态原子核外电子排布式为
C. 的电子排布式为
D.Co 位于元素周期表中第 9 列
5. 下列有关分子的结构和性质的说法正确的是
A. H O 和 C H 均为直线形的非极性分子
2 2 2 2
B. CO 2- 和 SO 2- 的空间结构均为平面三角形
3 3
C.基态 Mn 原子核外有 25 种能量不同的电子
D. OF 和 NCl 均是极性分子,且 NCl 分子的键角较大
2 3 3
6.一氯乙烯 和一氯乙炔 都是烃的一氯代物,下列
有关说法错误的是
A.键长:
B. 是直线形分子
C. 中, 键与 键数目之比为 4:1
D.一氯乙烯中碳的杂化轨道类型为
7.短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示,其
中戊的非金属性最强且其基态原子的 p 轨道只有一个未成对电子。下列说法
错误的是( )
A.简单离子半径:丙>丁>戊 B.简单氢化物的沸点:丙<丁<戊
C.最高价含氧酸的酸性:丙>乙 D.第一电离能:甲<丁<丙
8.有关周期表和周期律的说法正确的是
A.第二周期元素,第一电离能介于 B 和 N 之间的元素有 1 种
高二化学试题 第 2 页 共 9 页B.周期表 p 区所有元素,电子最后填入的能级均为 p 能级
C.同一周期,第ⅡA 族元素电负性大于第ⅢA 族元素
D.周期表第 14 列元素形成化合物种类最多
9.下表列出了某短周期元素 R 的各级电离能数据(用 I1、I2……表示,单位
为 kJ·mol-1)。下列关于元素 R 的判断中一定正确的是
I I I I I ……
1 2 3 4
R 740 1 500 7 700 10 500
①R 的最高正价为+3 价 ②R 元素位于元素周期表中第ⅡA 族
③R 元素第一电离能大于同周期相邻元素
④R 元素基态原子的电子排布式为 1s22s2
A.②③ B.①② C.③④ D.①④
10.下列对一些实验事实的解释错误的是
选项 实验事实 解释
A 水加热到较高温度难以分解 水分子中共价键键能较大
甲基是推电子基团,使羧基中羟
B 甲酸酸性大于乙酸
基极性减小
C 的沸点高于 H-N 键的键长比 H-P 键的键长短
D 不存在稳定的 H 、H Cl 和 Cl 共价键具有饱和性
3 2 3
A.A B.B C.C D.D
11.类推是化学学习和研究中常用的思维方法。下列类推正确的是
A. 为直线形分子,则 也为直线形分子
高二化学试题 第 3 页 共 9 页B. 和 都为正四面体形, 中键角为 109°28′, 中键角也为 109°
28′
C.HF 分子间氢键强度大于水的分子间氢键,因此 HF 的沸点更高
D.基态 V 的价层电子排布式为 ,基态 Cr 的价层电子排布式为
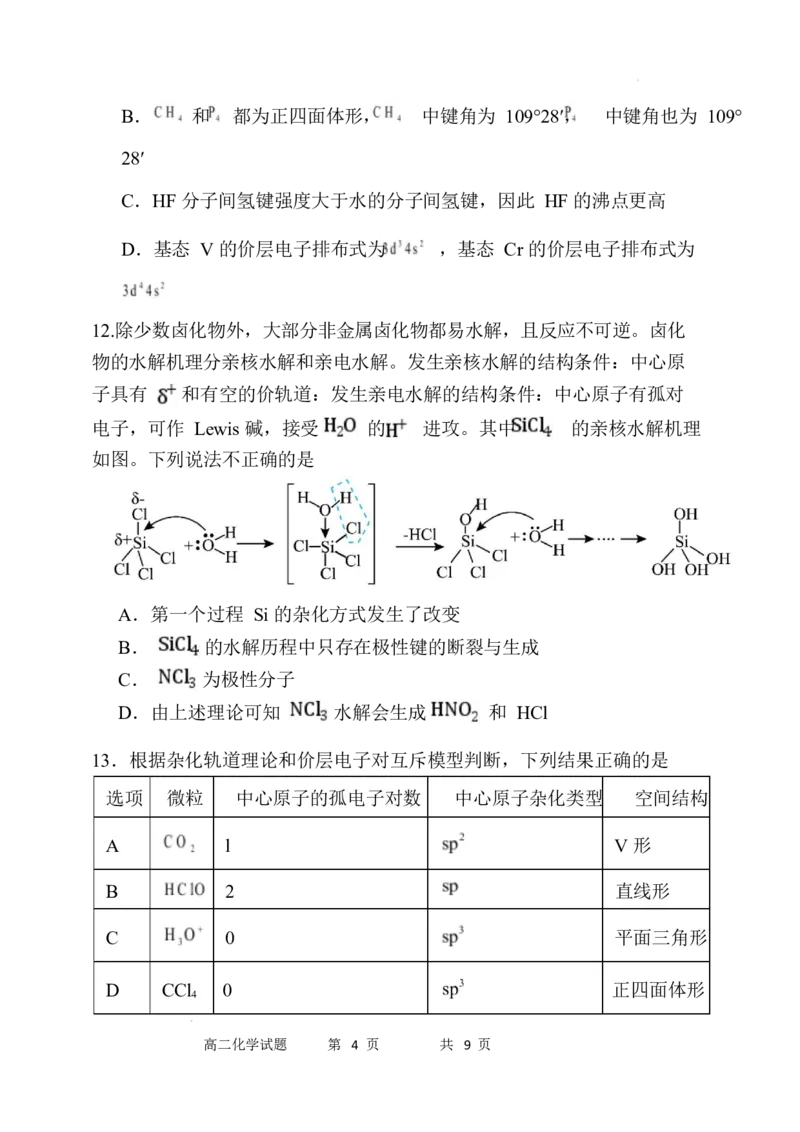
12.除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化
物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原
子具有 和有空的价轨道:发生亲电水解的结构条件:中心原子有孤对
电子,可作 Lewis 碱,接受 的 进攻。其中 的亲核水解机理
如图。下列说法不正确的是
A.第一个过程 Si 的杂化方式发生了改变
B. 的水解历程中只存在极性键的断裂与生成
C. 为极性分子
D.由上述理论可知 水解会生成 和 HCl
13.根据杂化轨道理论和价层电子对互斥模型判断,下列结果正确的是
选项 微粒 中心原子的孤电子对数 中心原子杂化类型 空间结构
A l V 形
B 2 直线形
C 0 平面三角形
D CCl 0 正四面体形
4
高二化学试题 第 4 页 共 9 页A.A B.B C.C D.D
14.现有如下各说法:①由非金属元素形成的单质中一定存在非极性键;②
活泼金属和活泼非金属化合时一般形成离子键;③非金属元素间形成的化合
物一定是共价化合物;④根据电离方程式 HCl=H +Cl-,判断 HCl 分子里存
+
在离子键;⑤冰的密度比水的密度小,这与氢键有关。上述说法中错误的是
A.①②⑤ B.①②④ C.①③④ D.③④⑤
15. 某电解质阴离子的结构如图。X、Y、Z、Q 为原子序数依序增大的同周
期元素,Z 的单质为空气的主要成分之一。下列说法错误的是
A. 第一电离能:
B. 最简单氢化物沸点:
C. 键长:
D. Y 的最高价氧化物对应水化物在水中电离:
第Ⅱ卷 (主观题,共 55 分)
二、填空题
16.(16 分)ⅥA 族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现
出多种氧化态,含ⅥA 族元素的化合物在研究和生产中有许多重要用途。请
回答下列问题:
高二化学试题 第 5 页 共 9 页(1)基态氧原子的轨道表示式为________,占据最高能级电子的电子云轮廓
图为________形。
(2) 分子的立体构型为 。 的三聚分子 常温下为固
体,其结构如图 , 原子的杂化方式为 ______ 。
(3)Se 原子的原子序数为 ,基态简化电子的排布式为 ;
(4) 的稳定性比 ___(填“强”或“弱”),原因为_________________。
(5)键角: _______(填“大于”或“小于”) ,原因为_________________
。
(6)乙硫醇 具有强烈的蒜臭味,常被少量加入煤气中作臭味指
示剂。常温下,乙硫醇微溶于水,而乙醇与水以任意比互溶,其主要原因
是 。
17.(12 分)Ⅰ.铝的化合物在化工、医药、材料等方面应用广泛。
回答下列问题:
(1)铝元素基态原子核外未成对电子数为 。
(2) 分子中心原子的杂化方式为 ,其空间结构为 。
(3) 的熔点低于 ,原因是 。
Ⅱ.S Cl 是一种黄红色溶液,常用作橡胶的低温硫化剂和粘结剂,其结构与
2 2
H O 相似。回答下列问题:
2 2
(4) H O 的电子式为 ,该分子为 (填“极性”或“非极
2 2
高二化学试题 第 6 页 共 9 页性”)分子。
(5)沸点:S Cl H O (填“>”“<”或“=”),理由是 。
2 2 2 2
(6) S Cl 遇水剧烈反应生成沉淀和气体,且气体能使品红溶液褪色,则 S Cl
2 2 2 2
的水解方程式为 。
18.(13 分)回答下列问题:
(1)下列状态的镁中电离最外层一个电子所需能量最大的是_______(填标
号)。
(2)在周期表中,与 Li 的化学性质最相似的邻族元素是________,该元素
基态原子核外 M 层电子的自旋状态________(填“相同”或“相反”)。
(3)Fe 成为阳离子时首先失去_______轨道电子,Fe2+基态核外电子排布
式为_________
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素是___,(填
元素名称),该元素的在周期表的位置是_________________。
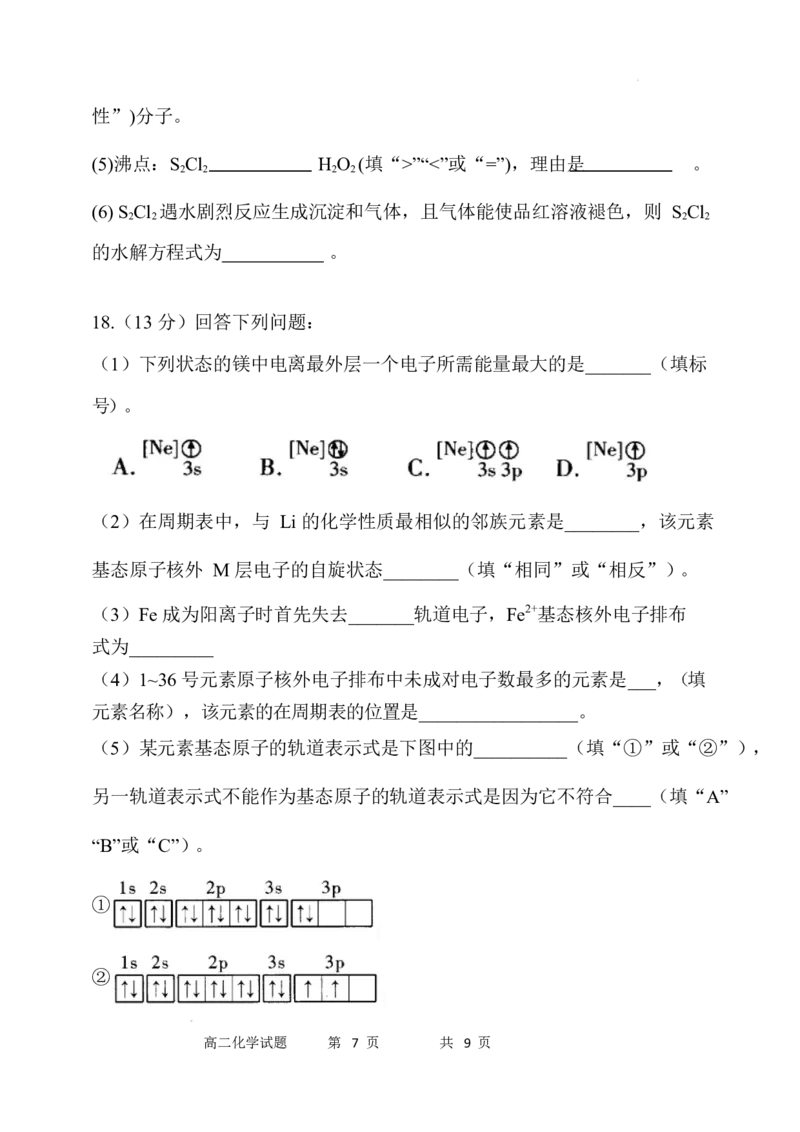
(5)某元素基态原子的轨道表示式是下图中的__________(填“①”或“②”),
另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合____(填“A”
“B”或“C”)。
①
②
高二化学试题 第 7 页 共 9 页A.能量最低原理 B.泡利原理 C.洪特规则
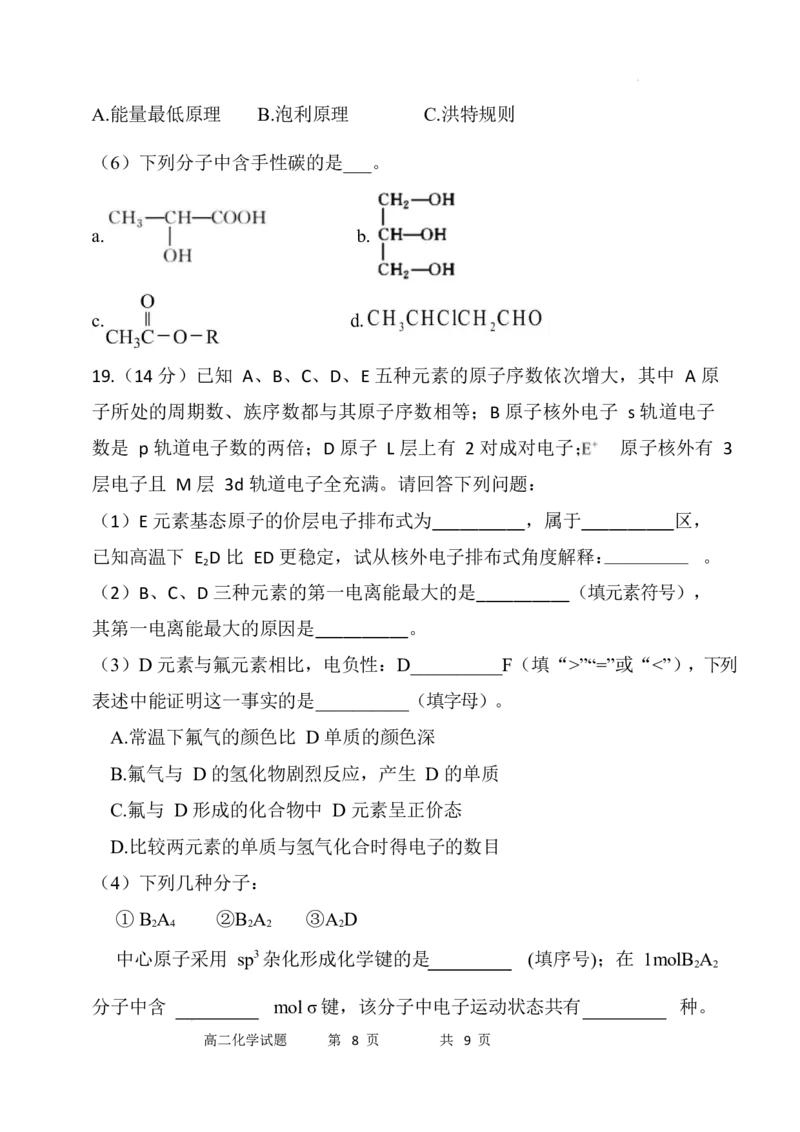
(6)下列分子中含手性碳的是___。
a. b.
c. d.
19.(14 分)已知 A、B、C、D、E 五种元素的原子序数依次增大,其中 A 原
子所处的周期数、族序数都与其原子序数相等;B 原子核外电子 s 轨道电子
数是 p 轨道电子数的两倍;D 原子 L 层上有 2 对成对电子; 原子核外有 3
层电子且 M 层 3d 轨道电子全充满。请回答下列问题:
(1)E 元素基态原子的价层电子排布式为__________,属于__________区,
已知高温下 E D 比 ED 更稳定,试从核外电子排布式角度解释: 。
2
(2)B、C、D 三种元素的第一电离能最大的是__________(填元素符号),
其第一电离能最大的原因是__________。
(3)D 元素与氟元素相比,电负性:D__________F(填“>”“=”或“<”),下列
表述中能证明这一事实的是__________(填字母)。
A.常温下氟气的颜色比 D 单质的颜色深
B.氟气与 D 的氢化物剧烈反应,产生 D 的单质
C.氟与 D 形成的化合物中 D 元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)下列几种分子:
① B A ②B A ③A D
2 4 2 2 2
中心原子采用 sp3 杂化形成化学键的是 (填序号);在 1molB A
2 2
分子中含 mol σ键,该分子中电子运动状态共有 种。
高二化学试题 第 8 页 共 9 页高二化学试题 第 9 页 共 9 页