文档内容
2024-2025 学年高二化学上学期第一次月考卷
一、选择题:本题共20个小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.工业上处理含CO、SO 烟道气的一种方法是将其在催化剂作用下转化为S和CO。已知:2CO(g)
2 2
+O (g)=2CO (g) ΔH=-566 kJ/mol; S(s)+O (g)=SO(g) ΔH=-296 kJ/mol;则该条件下2CO(g)
2 2 2 2
+SO(g)=S(s)+2CO (g)的ΔH等于
2 2
A.- 270 kJ/mol B.+26 kJ/mol C.-582 kJ/mol D.+270 kJ/mol
【答案】A
【详解】已知:①2CO(g)+O(g)=2CO (g) ΔH=-566 kJ/mol; ②S(s)+O (g)=SO(g) ΔH=-296 kJ/mol,根
2 2 2 2
据盖斯定律,将①-②,整理可得2CO(g)+SO (g)=S(s)+2CO (g) ΔH=- 270 kJ/mol,故合理选项是A。
2 2
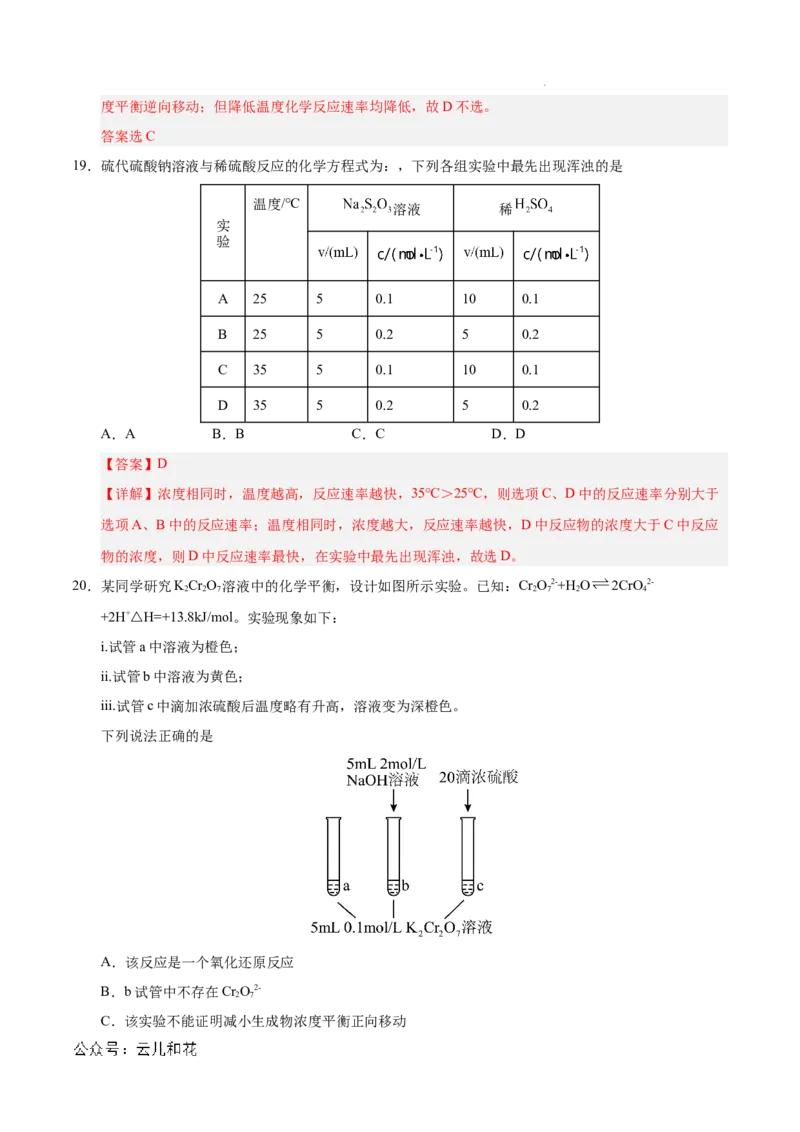
2.已知:2SO (g) + O(g) 2SO (g) ΔH,不同条件下反应过程能量变化如图所示。
2 2 3
下列说法中不正确的是
A.反应的ΔH<0
B.过程b使用了催化剂
C.使用催化剂不能提高活化分子百分数
D.过程b发生两步反应,第一步为吸热反应,且反应较慢
【答案】C
【详解】A.由图中信息可知,该反应的反应物的总能量高于生成物的总能量,故该反应为放热反应,
反应的ΔH<0,A正确;
B.使用催化剂可以降低反应的活化能,由图中信息可知,过程b的活化能比过程a的活化能低,因此
可以判断过程b使用了催化剂,B正确;
学科网(北京)股份有限公司C.催化剂可以降低反应的活化能,提高活化分子百分数从而加快反应速率,C错误;
D.过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,图中峰值越
小则活化能越小,决定总反应速率的是慢反应,活化能越大反应越慢;由图中信息可知,过程b发生两
步反应,第一步生成中间产物,中间产物的总能量高于反应物的总能量且活化能较第二步要大,因此
第一步为吸热反应且反应较慢,D正确;
故选C。
3.一定条件下,在2 L密闭容器中发生反应:2A(s)+3 B(g)=2 C(g)+4 D(g),测得5 min内,A的物质的量
减小了10 mol, 则0~5 min内该反应的平均速率为
A.v(A)=1.0 mol/(L·min) B.v(B)=1.5 mol/(L·min )
C.v(C)=2.0 mol/( L·min) D.v(D)=0.5 mol/(L·min)
【答案】B
【分析】根据反应方程式中各物质反应的量关系,变化量之比等于系数之比,推出速率之比等于各物
质的系数之比。
【详解】A.A是固体不能表示速率,故A不正确;
B.根据A的物质的量减少了10mol,B的物质的量减少了则是15mol,根据变化量之比等于系数比,
则 =1.5mol/(L·min ),故B正确;
C.根据A的物质的量减少了10mol,C的物质的量增加了则是10mol,根据变化量之比等于系数比,
= 1.0 mol/(L·min),故C不正确;
D.根据A的物质的量减少了10mol,D的物质的量增加了则是20mol,根据变化量之比等于系数比,
= 2.0 mol/(L·min),故D不正确;
故选答案B。
【点睛】根据速率之比等于化学反应方程式的计量数之比的实质进行分析,注意对于固体和纯液体不
能表示其速率。
4.。反应达平衡时,下列措施能提高N 转化率的是
2
①降温 ②恒压通入惰性气体 ③增加N 的浓度 ④加压 ⑤催化剂
2
A.①④ B.①② C.②⑤ D.③④
【答案】A
【详解】①合成氨反应为放热反应,降低温度,平衡向正反应方向移动,氮气转化率增大,故正确;
学科网(北京)股份有限公司②恒压条件下通入惰性气体相当于减小压强,该反应是气体体积减小的反应,减小压强,平衡向逆反
应方向进行,氮气转化率降低,故错误;
③增加氮气的浓度,衡向正反应方向移动,氢气转化率增大,但氮气转化率减小,故错误;
④该反应是气体体积减小的反应,增大压强,平衡向正反应方向移动,氮气转化率增大,故正确;
⑤使用催化剂,化学反应速率增大,但化学平衡不移动,氮气转化率不变,故错误;
①④正确,故选A。
5.为测定一定时间内锌和稀硫酸反应的速率,下列测量依据不可行的是
A. 的变化 B. 的变化 C. 的变化 D. 的变化
【答案】C
【详解】A. 的变化越快,锌和稀硫酸反应的速率越快,该测量依据可行,A项正确;
B. 的变化越快,锌和稀硫酸反应的速率越快,该测量依据可行,B项正确;
C.锌和稀硫酸反应的离子方程式为:Zn+2H+=Zn2++H ↑, 不参与该反应,所以测量 的变化无
2
法测得锌和稀硫酸反应的速率,C项错误;
D. 的变化越快,锌和稀硫酸反应的速率越快,该测量依据可行,D项正确;
答案选C。
6.对于反应2SO (g)+O(g) 2SO (g) ΔH<0,下列说法正确的是
2 2 3
A.使用VO 作催化剂,降低了反应的活化能,增大了单位体积内活化分子的数目
2 5
B.增加氧气的浓度,能够增大活化分子百分数
C.只要选择适宜的条件,SO 和O 就能全部转化为SO
2 2 3
D.升高温度能加快反应速率,提高SO 的平衡转化率
2
【答案】A
【详解】A.使用VO 作催化剂,降低了反应的活化能,增大了单位体积内活化分子的数目,增大了
2 5
活化分子百分数,故A正确;
B.增加氧气的浓度,增大了单位体积内活化分子数目,活化分子百分数不变,故B错误;
C.该反应为可逆反应,具有一定的反应限度,SO 和O 不能全部转化为SO ,故C错误;
2 2 3
D.该反应为放热反应,升高温度能加快反应速率,平衡往逆反应方向移动,降低了SO 的平衡转化率,
2
故D错误。
答案为A。
学科网(北京)股份有限公司7.在反应中,有关反应条件改变使反应速率增大的原因分析中,不正确的是
A.加入适宜的催化剂,可降低反应的活化能 B.增大 ,单位体积内活化分子数增大
C.升高温度,单位时间内有效碰撞次数增加 D.增大压强,活化分子的百分数增大
【答案】D
【详解】A.加入合适的催化剂,能降低反应的活化能,反应速率增大,A正确;
B.增大碘化氢的浓度,单位体积内活化分子数增多,反应速率增大,B正确;
C.升高温度,单位时间内有效碰撞次数增加,反应速率增大,C正确;
D.增大压强,单位体积内活化分子数增多,反应速率增大,但活化分子百分数不变,D错误;
答案选D。
8.一定温度下,溶液发生催化分解。不同时刻测得生成 的体积(已折算为标准状况)如下表,下列叙述
不正确的是(溶液体积变化忽略不计)
0 2 4 6 8 10
0.0 9.9 17.2 22.4 26.5 29.9
A. 的平均反应速率:
B. 的平均反应速率较 的平均反应速率更快
C.反应至 时,
D.反应至 时, 分解了50%
【答案】C
【详解】A. 生成氧气的物质的量为1×10-3mol,消耗HO 的物质的量为2×10-3mol,平均反应
2 2
速率: ,故A正确;
B. 内生成17.2mL氧气, 内生成9.3mL氧气,所以 的平均反应速率较
的平均反应速率更快,故B正确;
C.反应至 时,生成氧气的物质的量为1×10-3mol,消耗HO 的物质的量为2×10-3mol,
2 2
学科网(北京)股份有限公司,故C错误;
D.反应至 时,生成氧气的物质的量为1×10-3mol,消耗HO 的物质的量为2×10-3mol, 分解
2 2
率为 50%,故D正确;
选C。
9.已知分解1molH O 放出热量98 kJ,在含少量I-的溶液中,HO 分解的机理为:
2 2 2 2
第一步:HO+I-→HO+IO- 慢
2 2 2
第二步:HO+IO-→HO+O+I- 快
2 2 2 2
下列有关该反应的说法正确的是
A.I-的浓度大小决定反应速率的大小
B.IO-是该反应的催化剂
C.v(H O)=v(H O)=v(O )
2 2 2 2
D.HO 分解的热化学方程式为2HO(l)=2H O(l)+O(g) ΔH=-98kJ·mol-1
2 2 2 2 2 2
【答案】A
【详解】A.I-是第一步反应的反应物, I-的浓度大小决定第一步反应速率,第一步是慢反应,慢反应
决定总反应速率,所以I-决定反应速率的大小,故A正确;
B.IO-是第一步反应的生成物,IO-是第二步反应的反应物,所以IO-是该反应的中间产物,故B错误;
C.v(H O)是纯液体,不能用水的浓度变化表示反应速率,故C错误;
2
D.1molH O 放出热量98kJ,HO 分解的热化学方程式为2HO(l)=2H O(l)+O(g) ΔH=-196kJ·mol-1,故
2 2 2 2 2 2 2 2
D错误;
选A。
10.NH 原NO,其反应过程与能量关系如图1所示;有氧条件下,Fe3+催化NH 还原NO的反应历程如图
3 3
2所示。下列说法正确的是
学科网(北京)股份有限公司A.图1所示热化学方程式为
B.图1所示反应产物中氧化产物与还原产物物质的量之比为2:3
C.图2所示过程中 的物质的量减少
D.图2所示过程生成1mol氮气,转移电子的数目为2.4mol
【答案】B
【详解】A.热化学方程式为4NH (g)+6NO(g)═5N(g)+6HO(g)ΔH=正反应活化能-逆反应活化能=(a-
3 2 2
b)kJ/mol,A错误;
B.图1所示反应方程式为:4NH (g)+6NO(g)═5N(g)+6HO(g),反应产物中氧化产物与还原产物为
3 2 2
N,其中有4个N被氧化,6个N被还原,故氧化产物与还原产物物质的量之比为2:3,B正确;
2
C.由题干图示信息可知,图2所示过程中 作催化剂,故其物质的量在反应前后保持不变,C错误;
D.由题干图示信息可知,图2所示过程发生的总反应为:4NH +4NO+O 4N+6H O,故生成
3 2 2 2
1mol氮气,转移电子的数目为3mol,D错误;
故答案为:B。
11.一定条件下,一定容积的密闭容器中,反应达到平衡状态的标志是
A.压强不随时间变化
B.气体平均相对分子质量不随时间变化
C.气体密度不随时间变化
D.单位时间内生成nmolA ,同时生成2nmolAB
2
【答案】D
【详解】A.该反应是气体体积不变的反应,反应中气体压强始终不变,则压强不随时间变化不能说
学科网(北京)股份有限公司明正逆反应速率相等,无法判断反应是否达到平衡,故A错误;
B.由质量守恒定律可知,反应前后气体的质量相等,该反应是气体体积不变的反应,反应中气体平
均相对分子质量始终不变,则气体平均相对分子质量不随时间变化不能说明正逆反应速率相等,无法
判断反应是否达到平衡,故B错误;
C.由质量守恒定律可知,反应前后气体的质量相等,在恒容密闭容器中混合气体的密度始终不变,
则混合气体的密度保持不变不能说明正逆反应速率相等,无法判断反应是否达到平衡,故C错误;
D.由方程式可知,单位时间内生成nmolA ,同时生成2nmolAB说明正逆反应速率相等,反应已达到
2
平衡,故D正确;
故选D。
12.下列事实不能用勒夏特列原理解释的是
A.加水稀释0.1 mol∙L−1CHCOOH溶液,其电离程度增大
3
B.NO 和NO 的混合气体升温后红棕色加深
2 2 4
C.SO 催化氧化成SO 的反应,往往需要使用催化剂
2 3
D.向水中加入少量NaOH(s)后恢复至常温,溶液的pH增大
【答案】C
【详解】A.加水稀释0.1 mol∙L−1CHCOOH溶液,平衡正向移动,醋酸又电离,因此醋酸电离程度增
3
大,能用勒夏特列原理解释,故A不符合题意;
B.2NO NO 是吸热反应,NO 和NO 的混合气体升温,平衡逆向移动,气体红棕色加深,能
2 2 4 2 2 4
用勒夏特列原理解释,故B不符合题意;
C.SO 催化氧化成SO 的反应,往往需要使用催化剂,反应速率加快,平衡不移动,不能用勒夏特列
2 3
原理解释,故C符合题意;
D.向水中加入少量NaOH(s)后恢复至常温,氢氧根浓度增大,抑制水的电离,溶液的pH增大,能用
勒夏特列原理解释,故D不符合题意。
综上所述,答案为C。
13.将2mol 和1mol 分别置于相同温度下相同体积的甲乙两密闭容器中发生反应:
并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说
法不正确的是
A.平衡时 的百分含量:乙<甲 B. 的转化率:乙>甲
学科网(北京)股份有限公司C.反应速率:乙>甲 D.平衡时容器的压强:乙>甲
【答案】A
【详解】A.该反应气体分子数减小,甲容器在恒温恒容下建立平衡则压强减小,乙容器在恒温恒压
下建立平衡则体积减小而维持压强不变,平衡时的压强:乙容器>甲容器,压强越大越有利于平衡正
移,平衡时 的百分含量更大,A错误;
B.平衡时乙容器压强大, 的转化率高,B正确;
C.温度相同时,乙容器的压强大,乙的反应速率快,C正确;
D.平衡时乙容器压强大于甲容器,D正确;
答案选A。
14.乙烯气相直接水合反应制备乙醇:。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,
,容器体积为 )。下列分析不正确的是
A.乙烯气相直接水合反应的 B.图中压强的大小关系为:
C.图中a点对应的平衡常数 D.达到平衡状态a、b所需要的时间:
【答案】C
【详解】A.如图,温度越高,乙烯的转化率越低,平衡逆向移动,该反应的放热反应, ,A
正确;
B.由图可知,压强越大,平衡正向移动,乙烯的平衡转化率越大,所以 ,B正确;
C.a点时,乙烯转化率为20%,根据三段式: ,
学科网(北京)股份有限公司,C错误;
D.与a点相比,b点温度高,压强大,反应速率较慢,达平衡所需时间较短,D正确;
故选C。
15.在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T、T 下X的物质的量浓度c(X)随时间t变化
1 2
的曲线如图所示,下列叙述正确的是
A.M点的正反应速率υ 小于N点的逆反应速率υ
正 逆
B.T 下,在0~t 时间内,υ(Y)= mol/(L·min)
2 1
C.M点时再加入一定量X,平衡后X的转化率减小
D.该反应进行到M点放出的热量小于进行到W点放出的热量
【答案】D
【详解】分析:用“先拐后平”法,T 优先T 出现拐点,T 达到平衡时间短、速率快,则T T;T
1 2 1 1 2 2
平衡时c(X)小于T,升高温度平衡向逆反应方向移动,该反应的ΔH 0;利用图象上的数据和速率
1
之比等于化学计量数之比计算υ(Y);平衡后再加入一定量X,相当于增大压强,平衡向正反应方向
移动,X的平衡转化率增大。
详解:用“先拐后平”法,T 优先T 出现拐点,T 达到平衡时间短、速率快,其它条件不变时升高温
1 2 1
度化学反应速率加快,则T T;T 平衡时c(X)小于T,升高温度平衡向逆反应方向移动,逆反应
1 2 2 1
为吸热反应,该反应的ΔH 0。A项,M点是T 时的平衡点,υ (M)=υ (M),N点是T 时的不
1 正 逆 2
平衡点,N点时的逆反应速率小于T 平衡时的逆反应速率,由于T T,T 平衡时的反应速率小于T
2 1 2 2 1
平衡时的反应速率,M点的正反应速率υ 大于N点的逆反应速率υ ,A项错误;B项,T 下,0~t
正 逆 2 1
时间内υ(X)= = = mol/(L·min),不同物质表示的化学反应速率之比等于
学科网(北京)股份有限公司化学计量数之比,υ(Y)= υ(X)= mol/(L·min),B项错误;C项,M点时再加入一定量
X,相当于增大压强,平衡向正反应方向移动,平衡后X的转化率增大,C项错误;D项,该反应的
正反应为放热反应,W点消耗X的物质的量大于M点,该反应进行到M点放出的热量小于进行到W
点放出的热量,D项正确;答案选D。
点睛:本题考查化学平衡的图象分析、化学反应速率的计算、外界条件对化学反应速率和化学平衡的
影响。观察图象时先看纵横坐标的含义,根据关键点和曲线的变化趋势,联想外界条件对化学反应速
率和化学平衡影响的规律进行判断。注意:在恒容容器中增加反应物浓度,平衡向正反应方向移动;
若反应物只有一种,平衡时反应物转化率的变化,利用增大压强对平衡的影响判断。
16.下列关于化学反应速率的说法正确的是
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④ 的反应速率一定比 的反应速率大
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子数,从
而使反应速率增大
⑥增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
A.②⑥ B.②⑤ C.①②③⑤ D.①②④⑤
【答案】B
【详解】①恒温时,增大压强,如没有气体参加反应,化学反应速率不加快,故错误;
②其他条件不变,温度升高,增大活化分子百分数,化学反应速率越快,故正确;
③使用催化剂不能改变反应热,故错误;
④没有指定反应,也没有指定反应速率用方程式中的哪种物质表示,所以无法比较3mol/(L▪s)和1mol/
(L▪s)的反应速率的快慢,故错误;
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),活化分子百分数不变,增加了单
位体积内活化分子数,故正确;
⑥增大反应物浓度,活化分子的百分数不变,增加的是单位体积内活化分子数,故错误;
②⑤正确,故答案选B。
17.我国科研人员提出了由和 转化为高附加值产品 的催化反应历程,该历程示意图如下所
示。下列说法正确的是
学科网(北京)股份有限公司A.①→②的过程中吸收能量
B. → 过程中,C—H键全部发生断裂
C.生成 总反应的原子利用率为100%
D.该催化剂可有效提高反应物的平衡转化率
【答案】C
【详解】A.据图可知①→②的焓值降低,过程为放热过程,故A错误;
B.该过程中反应物为CO 和CH,生成的产物为CHCOOH,CH 生成-CH,有C-H键发生断裂但不
2 4 3 4 3
是全部断裂,故B错误;
C.图中分析,1molCH 和1molCO 反应元素全部生成1molCH COOH,生成CHCOOH总反应的原子
4 2 3 3
利用率为100%,故C正确;
D.催化剂只能改变反应速率,不影响化学平衡,不影响转化率,故D错误;
故选C。
18.汽车尾气净化器中发生可逆反应:2NO(g) +2CO(g)N (g) +2CO (g) ΔH = -746.8 kJ·mol-1下列有关说法正
2 2
确的是
A.加入催化剂,上述反应的反应热ΔH小于-746.8 kJ ·mol-1
B.增大NO浓度,平衡正向移动,平衡常数增大
C.加入催化剂,有利于提高平衡前单位时间内NO的转化率
D.降低温度,平衡正向移动,v 增大,v 减小
正 逆
【答案】C
【详解】A.催化剂只能将改变反应的活化能,并不能改变焓变,故A不选;
B.增大NO浓度,平衡正向移动;但平衡常数只与温度有关,与反应物浓度无关,故B不选;
C.加入催化剂,化学反应速率增大,有利于提高平衡前单位时间内NO的转化率,故选C;
D.由反应2NO(g) +2CO(g) N(g) +2CO (g) ΔH = -746.8 kJ·mol-1可知,该反应为放热反应,降低温
2 2
学科网(北京)股份有限公司度平衡逆向移动;但降低温度化学反应速率均降低,故D不选。
答案选C
19.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:,下列各组实验中最先出现浑浊的是
温度/℃
溶液 稀
实
验
A 25 5 0.1 10 0.1
B 25 5 0.2 5 0.2
C 35 5 0.1 10 0.1
D 35 5 0.2 5 0.2
A.A B.B C.C D.D
【答案】D
【详解】浓度相同时,温度越高,反应速率越快,35℃>25℃,则选项C、D中的反应速率分别大于
选项A、B中的反应速率;温度相同时,浓度越大,反应速率越快,D中反应物的浓度大于C中反应
物的浓度,则D中反应速率最快,在实验中最先出现浑浊,故选D。
20.某同学研究KCr O 溶液中的化学平衡,设计如图所示实验。已知:Cr O2-+H O 2CrO2-
2 2 7 2 7 2 4
+2H+△H=+13.8kJ/mol。实验现象如下:
i.试管a中溶液为橙色;
ii.试管b中溶液为黄色;
iii.试管c中滴加浓硫酸后温度略有升高,溶液变为深橙色。
下列说法正确的是
A.该反应是一个氧化还原反应
B.b试管中不存在Cr O2-
2 7
C.该实验不能证明减小生成物浓度平衡正向移动
学科网(北京)股份有限公司D.试管c中影响平衡的主要因素是温度
【答案】C
【详解】A.反应前后元素的化合价不变,该反应是一个非氧化还原反应,故A错误;
B.Cr O2-+H O 2CrO2-+2H+,是可逆反应,转化率不可能达到100%,b试管中存在Cr O2-,故B
2 7 2 4 2 7
错误;
C.滴加浓硫酸,放出热量,温度、浓度均影响平衡移动,则该实验不能证明减小生成物浓度,平衡
正向移动,可能升高温度平衡正向移动,故C正确;
D.试管c中温度、氢离子浓度均变化,则c中的现象不能说明影响平衡的主要因素是温度,故D错
误;
故选C。
【点睛】本题考查化学平衡的影响因素,把握可逆反应的特点、温度和浓度对平衡移动的影响为解答
的关键,侧重分析与应用能力的考查,注意判断存在的变量,易错点C,注意滴加浓硫酸,放出热量,
温度、浓度均影响平衡移动,有多种变量。
第 II 卷(非选择题 共 40 分)
二、填空题
21.(9分)工业合成氨反应原理为 。
(1)T℃时,向有催化剂、容积为1.0L的恒容密闭容器中充入3mol 、1mol ,10min时反应达到平
衡,测得 。
①0~10min,用 表示的平均反应速率 。
②化学平衡常数 。
(2)T℃时,向有催化剂的恒容密闭容器中充入 和 。下图为X的平衡转化率随不同投料比值
的变化曲线。
学科网(北京)股份有限公司X是 (填“ ”或“ ”),判断依据是 。
(3)其他条件相同时,如下图所示为合成氨反应在不同压强、不同温度下达到平衡状态时,测得的
平衡转化率的变化曲线。
L表示 ,其中 (填“>”或“<”) 。
【答案】 0.18 2.08 增大 的浓度可以提高 的转化率,但 的转化率降低
压强 <
【分析】(1)①根据速率等于浓度改变量除以时间②将平衡时每种物质的浓度计算出来,再根据平衡常
数公式计算。
(2)假设 ,投料比值 增大时,即 增大时,X的平衡转化率增大,而
增大 的浓度可以提高 的转化率,但 的转化率降低。
(3)该反应是放热反应,也是气体体积减小的反应,利用平衡移动原理进行分析。
【详解】(1)① ;故答案为:0.18。
学科网(北京)股份有限公司②平衡时, , ,
,则 ,
,则 ,则
;故答案为:2.08。
(2)假设 ,投料比值 增大时,即 增大时,X的平衡转化率增大,而
增大 的浓度可以提高 的转化率,但 的转化率降低,则X为 ;故答案为: ;增大 的
浓度可以提高 的转化率,但 的转化率降低。
(3)该反应是放热反应,也是气体体积减小的反应,若L为温度,则随着温度升高,平衡逆向移动,
的平衡转化率减小,所以L不是温度,而是压强; 、 代表温度,保持压强不变, 下 的
平衡转化率比 下的大,说明平衡正向移动,而降低温度,该平衡正向移动,则 ;故答案为:
压强;<。
【点睛】分析图象时,常采用 “定一论二”思想分析,先看其中一条曲线,分析平衡移动,再作一
条与y轴相平的平行线,再根据平衡移动原理分析。
22.(9分)氢能是一种极具发展潜力的清洁能源。以下反应是目前大规模制取氢气的重要方法之一、
(1)欲提高CO的平衡转化率,理论上可以采取的措施为 。
A.增大压强 B.升高温度 C.加入催化剂 D.通入过量水蒸气
(2)800C时,该反应的平衡常数 ,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中
CO、 、 、 的物质的量分别为1mol、3mol、1mol、1mol。
学科网(北京)股份有限公司①写出该反应的平衡常数表达式 。
②该时刻反应 (填“正向进行”或“逆向进行”或“达平衡”)。
(3)830℃时,该反应的平衡常数 ,在容积为1L的密闭容器中,将2mol CO与2mol 混合加热
到830℃。反应达平衡时CO的转化率为 。
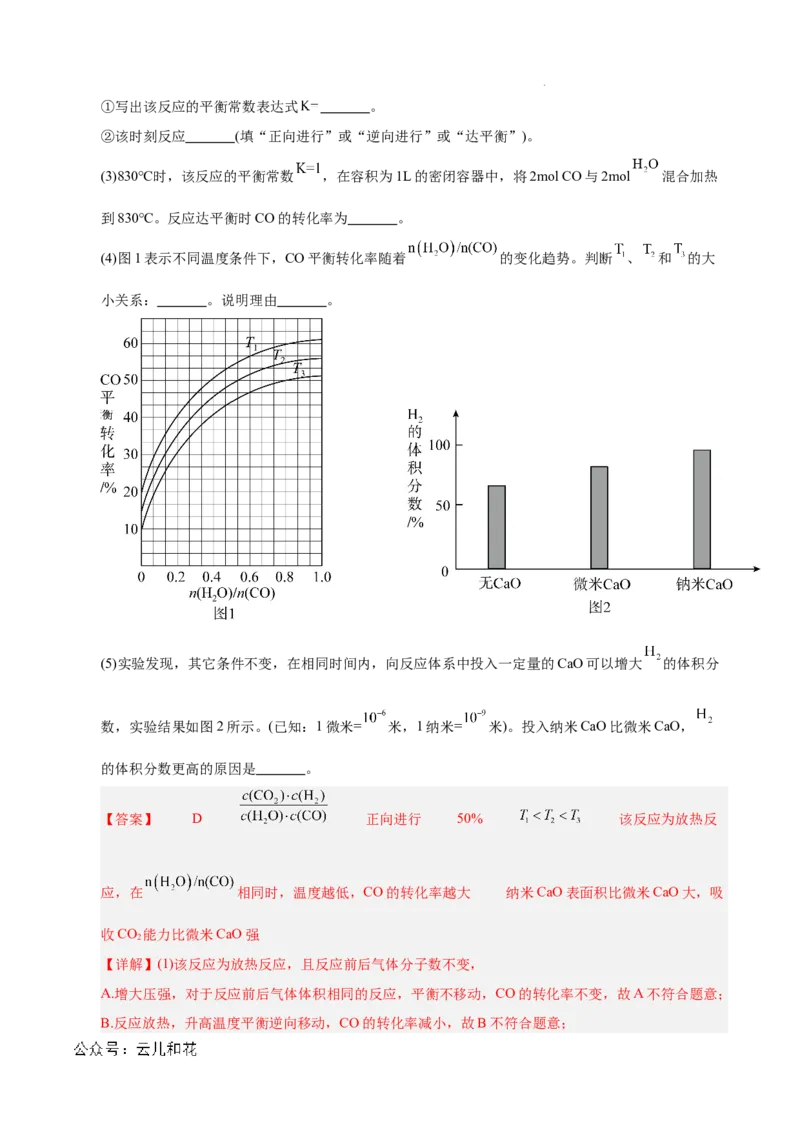
(4)图1表示不同温度条件下,CO平衡转化率随着 的变化趋势。判断 、 和 的大
小关系: 。说明理由 。
(5)实验发现,其它条件不变,在相同时间内,向反应体系中投入一定量的CaO可以增大 的体积分
数,实验结果如图2所示。(已知:1微米= 米,1纳米= 米)。投入纳米CaO比微米CaO,
的体积分数更高的原因是 。
【答案】 D 正向进行 50% 该反应为放热反
应,在 相同时,温度越低,CO的转化率越大 纳米CaO表面积比微米CaO大,吸
收CO 能力比微米CaO强
2
【详解】(1)该反应为放热反应,且反应前后气体分子数不变,
A.增大压强,对于反应前后气体体积相同的反应,平衡不移动,CO的转化率不变,故A不符合题意;
B.反应放热,升高温度平衡逆向移动,CO的转化率减小,故B不符合题意;
学科网(北京)股份有限公司C.催化剂只影响反应速率,不影响平衡状态,故C不符合题意;
D.通入过量水蒸气,提高反应的浓度使平衡正向移动,增大CO的转化率,故D符合题意;
故答案为:D。
(2)①由反应可知该反应的平衡常数为:K= ,CO、 、 、 的物质的量分别为
1mol、3mol、1mol、1mol时, <
(4) 强于 猜想1
(5) 蒸馏水 2.8mL
(6)在实验2-2中与 完全反应后的溶液中, 也高于实验2-1中的起始 ,溶液立
即变成蓝色,所以猜想1不成立
(7)BC
(8)
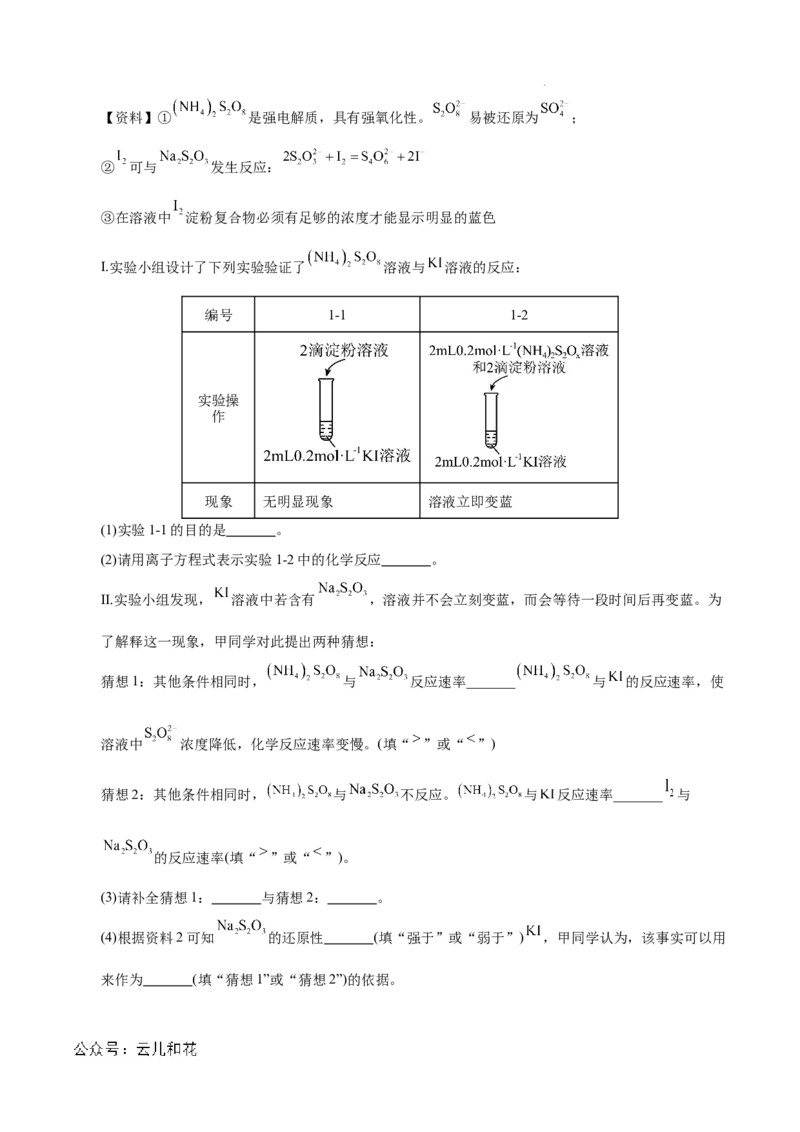
学科网(北京)股份有限公司【详解】(1)实验1-1的目的是对比实验,证明 溶液与 溶液反应将其氧化为碘单质而
使淀粉溶液变蓝色,排除氧气氧化碘离子的干扰;
(2)实验1-2中 溶液与 溶液反应生成碘单质而使淀粉溶液变蓝色,反应的离子方程式
为: ;
(3) 溶液中若含有 ,溶液并不会立刻变蓝,而会等待一段时间后再变蓝,可能的原因为:
猜想1: 与 反应速率大于 与 的反应速率,使溶液中 浓度降低,
化学反应速率变慢;猜想2:其他条件相同时, 与 不反应,而 与 反应
速率小于 与 的反应速率,所以溶液并不会立刻变蓝;
(4)根据资料② 可与 发生反应: ,还原剂的还原性强于还原产物,
所以 的还原性强于 ;所以猜想1:其他条件相同时, 与 反应速率大于
与 的反应速率,使溶液中 浓度降低,化学反应速率变慢成立;
(5)表格中①为蒸馏水,根据控制变量法,为了使溶液的总体积相同,②为加入2.8mL蒸馏水;
(6)在实验2-2中与 完全反应后的溶液中, 也高于实验2-1中的起始 ,溶液
立即变成蓝色,所以猜想1不成立;
(7)A. 由实验2-1和2-1对比,实验2-2增加溶液中 浓度,溶液变蓝的时间长,初始反应速
率较慢,A错误;
B. 由实验2-2可知,增加溶液中 浓度,溶液变蓝时间可能增加,B正确;
C. 增加溶液中 浓度,将生成的碘单质完全反应,溶液可能无法变蓝,C正确;
D. 升高溶液温度,反应速率加快,溶液开始变蓝时间可能减小,D错误;
学科网(北京)股份有限公司故选BC;
(8)根据反应 和 得到关系式: ,所以
, 。
学科网(北京)股份有限公司