文档内容
南充高中 2024-2025 学年度下学期第二次月考
4. 为阿伏加德罗常数的值。下列说法正确的是
高2023级化学试卷
A. 所含的电子总数为
(时间:120分钟 总分:150分 )
B. 中含有的 键数目为
可能用到的相对原子质量:
H 1 C 12 O 16 P 31 Zn 65 Cu 64
C. 白磷( )中共价键的数目为
一、单选题(本题共14小题,每小题3分,合计42分。每小题给出的四个选项中,只有一项符
合题目要求。)
D. 中 键数目为3N
A
1.科技是第一生产力,我国科学家在诸多领域取得了重大成就。下列说法正确的是
5.由六种元素形成的某种抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增
A.红外光谱图能确定有机化合物所含官能团的种类和数目
大的短周期主族元素,W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。
下列叙述错误的是
B.“神舟十七号”发动机的耐高温结构材料 属于分子晶体
A.W的最简单氢化物与Z的单质混合后可产生白烟
B.最高价氧化物水化物的酸性:Y<W<Z
C.飞船火箭使用偏二甲肼[ ]作燃料, 属于烃类 C.原子半径大小:Z<Y<X<W
D.化合物ZX 可用于自来水消毒
2
D.量子计算机“悟空”即将面世,其传输信号的光纤主要成分为SiO 6.我国科学家研究出一种新型的可充电水系 电池,放电时 装
2
2.下列化学用语表述正确的是 置如下图所示,其中双极膜间的 电离出的 和 可以分别通过膜移向两极,下列说法正
确的是
A. 的价层电子对互斥 模型:
B.P-P 键形成的轨道重叠示意图:
C. 溶液中的水合离子(各离子周围水分子数无误):
A.放电时,双极膜间的 电离出 移向右室
B.放电时, 极的电极反应式为
D.基态 原子的价层电子轨道表示式为: C.充电时, 极接外接电源正极,实现电能转化为化学能
D.充电时,当电路中转移 电子时,理论上沉积
7.物质结构决定性质。下列性质差异与结构因素匹配错误的是
3.下列有关原子的结构与性质说法中,正确的是
选项 性质差异 结构因素
A.氮原子的电子排布式由 释放能量产生发射光谱
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B.基态O原子的核外电子的空间运动状态有8种
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C.微粒半径大小:
C 酸性: ( )远强于 ( ) 羟基极性
D.Be和Al两种元素因处于元素周期表的对角线位置,且都属于p区元素,所以有些性质相似
高2023级化学试题 第19页 共510页 高2023级化学试题 第110页 共510页D 溶解性:小分子的醇,醛,酸极易溶解在水中 范德华力
A.A B.B C.C D.D
8.分子式为C HClO,加入金属钠能产生气体,符合条件的同分异构体数目为(不考虑空间异
3 7
构)
A.5 种 B.4 种 C.3 种 D.2 种
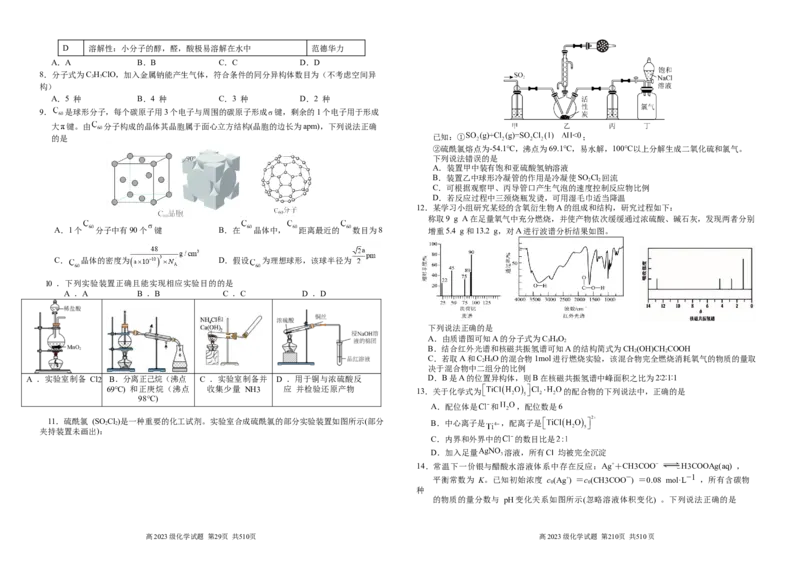
9. 是球形分子,每个碳原子用3个电子与周围的碳原子形成 键,剩余的1个电子用于形成
大 键。由 分子构成的晶体其晶胞属于面心立方结构(晶胞的边长为apm),下列说法正确
的是 已知:① ;
②硫酰氯熔点为-54.1℃,沸点为69.1℃,易水解,100℃以上分解生成二氧化硫和氯气。
下列说法错误的是
A.装置甲中装有饱和亚硫酸氢钠溶液
B.装置乙中球形冷凝管的作用是冷凝使SO Cl 回流
2 2
C.可根据观察甲、丙导管口产生气泡的速度控制反应物比例
D.若反应过程中三颈烧瓶发烫,可用湿毛巾适当降温
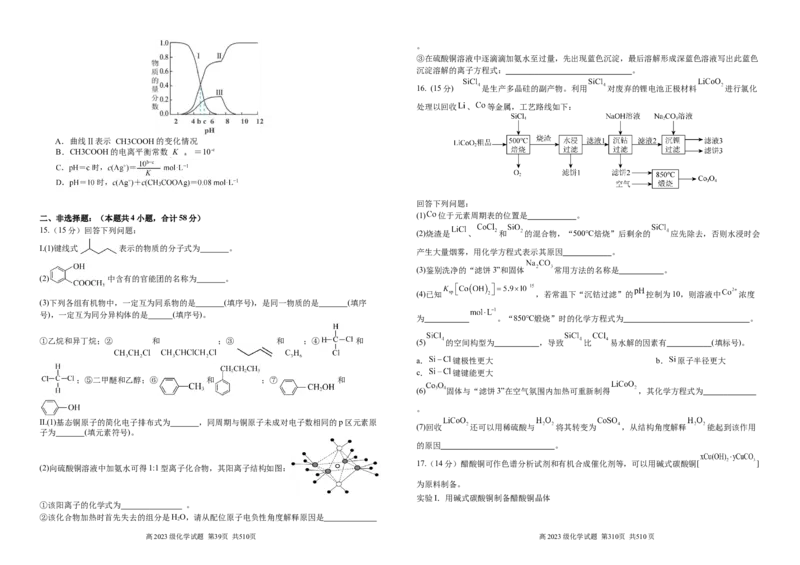
12.某学习小组研究某烃的含氧衍生物A的组成和结构,研究过程如下:
称取9 g A在足量氧气中充分燃烧,并使产物依次缓缓通过浓硫酸、碱石灰,发现两者分别
A.1个 分子中有90个 键 B.在 晶体中, 距离最近的 数目为8 增重5.4 g和13.2 g,对A进行波谱分析结果如图。
C. 晶体的密度为 D.假设 为理想球形,该球半径为
10 .下列实验装置正确且能实现相应实验目的的是
A .A B .B C .C D .D
下列说法正确的是
A.由质谱图可知A的分子式为C HO
3 6 2
B.结合红外光谱和核磁共振氢谱可知A的结构简式为CH(OH)CHCOOH
2 2
C.若取A和C HO的混合物1mol进行燃烧实验,该混合物完全燃烧消耗氧气的物质的量取
2 6
决于混合物中二组分的比例
A .实验室制备 Cl2 B.分离正己烷(沸点 C .实验室制备并 D .用于铜与浓硫酸反 D.B是A的位置异构体,则B在核磁共振氢谱中峰面积之比为2∶2∶1∶1
69℃) 和正庚烷(沸点 收集少量 NH3 应 并检验还原产物 13.关于化学式为 的配合物的下列说法中,正确的是
98℃)
A.配位体是 和 ,配位数是6
11.硫酰氯 (SO 2 Cl 2 )是一种重要的化工试剂。实验室合成硫酰氯的部分实验装置如图所示(部分 B.中心离子是 ,配离子是
夹持装置未画出):
C.内界和外界中的 的数目比是
D.加入足量 溶液,所有 均被完全沉淀
14.常温下一价银与醋酸水溶液体系中存在反应:Ag++CH3COO− CH3COOAg(aq) ,
平衡常数为 K。已知初始浓度 c (Ag+) =c (CH3COO − ) =0.08 mol·L −1 ,所有含碳物
0 0
种
的物质的量分数与 pH变化关系如图所示(忽略溶液体积变化) 。下列说法正确的是
高2023级化学试题 第29页 共510页 高2023级化学试题 第210页 共510页。
③在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液写出此蓝色
沉淀溶解的离子方程式: 。
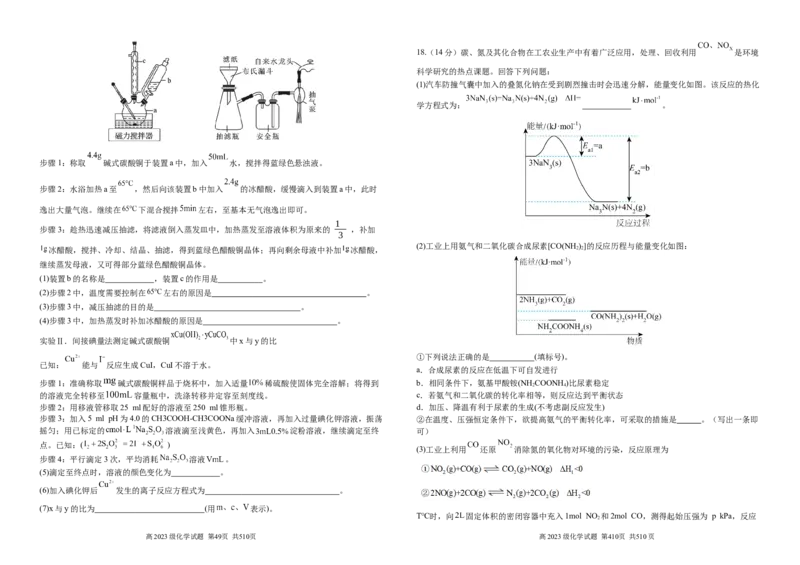
16. (15分) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯化
处理以回收 、 等金属,工艺路线如下:
A.曲线Ⅱ表示 CH3COOH的变化情况
B.CH3COOH的电离平衡常数 K =10-c
a
回答下列问题:
(1) 位于元素周期表的位置是 。
二、非选择题:(本题共4小题,合计58分)
15.(15分)回答下列问题:
(2)烧渣是 、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会
Ⅰ.(1)键线式 表示的物质的分子式为 。
产生大量烟雾,用化学方程式表示其原因 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是 。
(2) 中含有的官能团的名称为 。
(4)已知 ,若常温下“沉钴过滤”的 控制为10,则溶液中 浓度
(3)下列各组有机物中,一定互为同系物的是 (填序号),是同一物质的是 (填序
号),一定互为同分异构体的是 (填序号)。
为 。“850℃煅烧”时的化学方程式为 。
①乙烷和异丁烷;② 和 ;③ 和 ;④ 和 (5) 的空间构型为 ,导致 比 易水解的因素有 (填标号)。
a. 键极性更大 b. 原子半径更大
c. 键键能更大
;⑤二甲醚和乙醇;⑥ 和 ;⑦ 和
(6) 固体与“滤饼3”在空气氛围内加热可重新制得 ,其化学方程式为
。
Ⅱ.(1)基态铜原子的简化电子排布式为 ,同周期与铜原子未成对电子数相同的p区元素原
(7)回收 还可以用稀硫酸与 将其转变为 ,从结构角度解释 能起到该作用
子为 (填元素符号)。
的原因 。
17.(14分)醋酸铜可作色谱分析试剂和有机合成催化剂等,可以用碱式碳酸铜[ ]
(2)向硫酸铜溶液中加氨水可得1:1型离子化合物,其阳离子结构如图:
为原料制备。
实验I.用碱式碳酸铜制备醋酸铜晶体
①该阳离子的化学式为 。
②该化合物加热时首先失去的组分是HO,请从配位原子电负性角度解释原因是
2
高2023级化学试题 第39页 共510页 高2023级化学试题 第310页 共510页18.(14分)碳、氮及其化合物在工农业生产中有着广泛应用,处理、回收利用 是环境
科学研究的热点课题。回答下列问题:
(1)汽车防撞气囊中加入的叠氮化钠在受到剧烈撞击时会迅速分解,能量变化如图。该反应的热化
学方程式为: 。
步骤1:称取 碱式碳酸铜于装置a中,加入 水,搅拌得蓝绿色悬浊液。
步骤2:水浴加热a至 ,然后向该装置b中加入 的冰醋酸,缓慢滴入到装置a中,此时
逸出大量气泡。继续在 下混合搅拌 左右,至基本无气泡逸出即可。
1
步骤3:趁热迅速减压抽滤,将滤液倒入蒸发皿中,加热蒸发至溶液体积为原来的 ,补加
3
(2)工业上用氨气和二氧化碳合成尿素[CO(NH)]的反应历程与能量变化如图:
冰醋酸,搅拌、冷却、结晶、抽滤,得到蓝绿色醋酸铜晶体;再向剩余母液中补加 冰醋酸, 2 2
继续蒸发母液,又可得部分蓝绿色醋酸铜晶体。
(1)装置b的名称是 ,装置c的作用是 。
(2)步骤2中,温度需要控制在 左右的原因是 。
(3)步骤3中,减压抽滤的目的是 。
(4)步骤3中,加热蒸发时补加冰醋酸的原因是 。
实验Ⅱ.间接碘量法测定碱式碳酸铜 中x与y的比
①下列说法正确的是 (填标号)。
已知: 能与 反应生成CuI,CuI不溶于水。
a.合成尿素的反应在低温下可自发进行
步骤1:准确称取 碱式碳酸铜样品于烧杯中,加入适量 稀硫酸使固体完全溶解;将得到 b.相同条件下,氨基甲酸铵(NH COONH)比尿素稳定
2 4
的溶液完全转移至 容量瓶中,洗涤转移并定容至刻度线。 c.若氨气和二氧化碳的转化率相等,则反应达到平衡状态
步骤2:用移液管移取25 ml配好的溶液至250 ml锥形瓶。 d.加压、降温有利于尿素的生成(不考虑副反应发生)
步骤3:加入5 ml pH为4.0的CH3COOH-CH3COONa缓冲溶液,再加入过量碘化钾溶液,振荡 ②在温度、压强恒定条件下,欲提高氨气的平衡转化率,可采取的措施是 。(写出一条即
摇匀;用已标定的 溶液滴至浅黄色,再加入 淀粉溶液,继续滴定至终 可)
点。已知:( )
(3)工业上利用 还原 消除氮的氧化物对环境的污染,反应原理为
步骤4:平行滴定3次,平均消耗 溶液 。
(5)滴定至终点时,溶液的颜色变化为 。
(6)加入碘化钾后 发生的离子反应方程式为 。
(7)x与y的比为 (用 表示)。
T℃时,向 固定体积的密闭容器中充入1mol NO 和2mol CO,测得起始压强为 p kPa,反应
2
高2023级化学试题 第49页 共510页 高2023级化学试题 第410页 共510页后达到平衡,测得 转化率为80%,N 占总气体物质的量分数为 ,用CO表示从反应
2
开始到达平衡时的平均反应速率v(CO)= ;该温度下反应②的正反应平
衡常数K = 。(用分数表示)
p
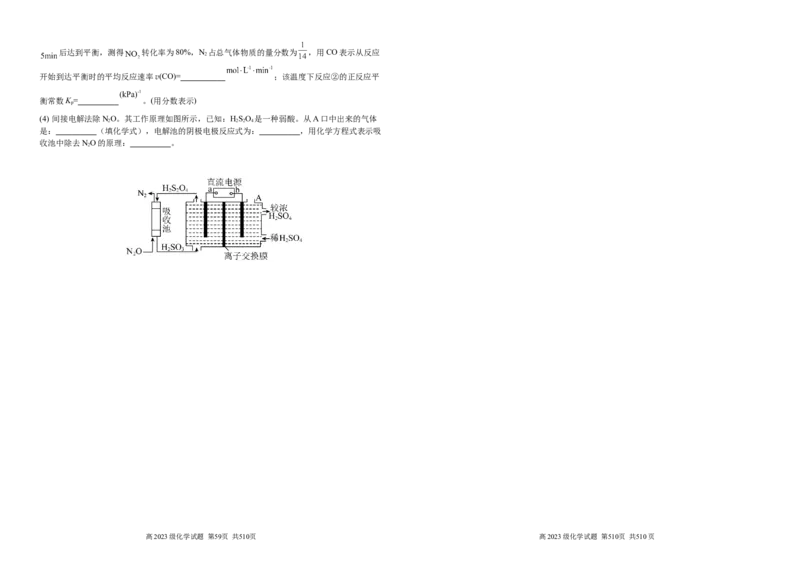
(4) 间接电解法除NO。其工作原理如图所示,已知:HSO 是一种弱酸。从A口中出来的气体
2 2 2 4
是: (填化学式),电解池的阴极电极反应式为: ,用化学方程式表示吸
收池中除去NO的原理: 。
2
高2023级化学试题 第59页 共510页 高2023级化学试题 第510页 共510页