文档内容
运城中学 2025-2026 学年第一学期高二年级期中考试
化 学 试 题
一、选择题:本题共14小题,每小题3分,共42分.每题所给的答案中,只有一个是正确
考生请注意:
1. 本试卷共5页,满分100分,考试时间75分钟。考试结束后,交回答题纸;
2. 答题前,请务必将自己的姓名、考生号用0.5毫米黑色中性笔或碳素笔在答题纸
上进行书写;
3. 作答选择题,必须用2B铅笔将答题纸上的对应题目的答题标号涂黑涂满;如需
改动,请用橡皮擦干净后,再更正其它的答案。未在答题纸上作答的、在答题
纸规定区域以外答题的一律无效;
4. 如有作图需要,请使用2B铅笔作图,并加黑加粗,描写清楚。
选项.
1.下列反应为吸热反应的是
A.反应物总能量高于生成物总能量的反应 B.需要加热的反应
C.八水合氢氧化钡与氯化铵晶体的反应 D.铝热反应
2.下列方程式与所给事实不相符的是
A.用 溶液“腐蚀”覆铜板:
B. 在强碱性溶液中制备 :
C.海水提溴中,用二氧化硫的水溶液吸收溴:
D.灭火时,将泡沫灭火器中的 浓溶液和 浓溶液混合:
3.下列表示不正确的是
A.中子数为10的氧原子:B. 的价层电子对互斥(VSEPR)模型:
C.用电子式表示 的形成过程:
D. 的名称:2-甲基-4-乙基戊烷
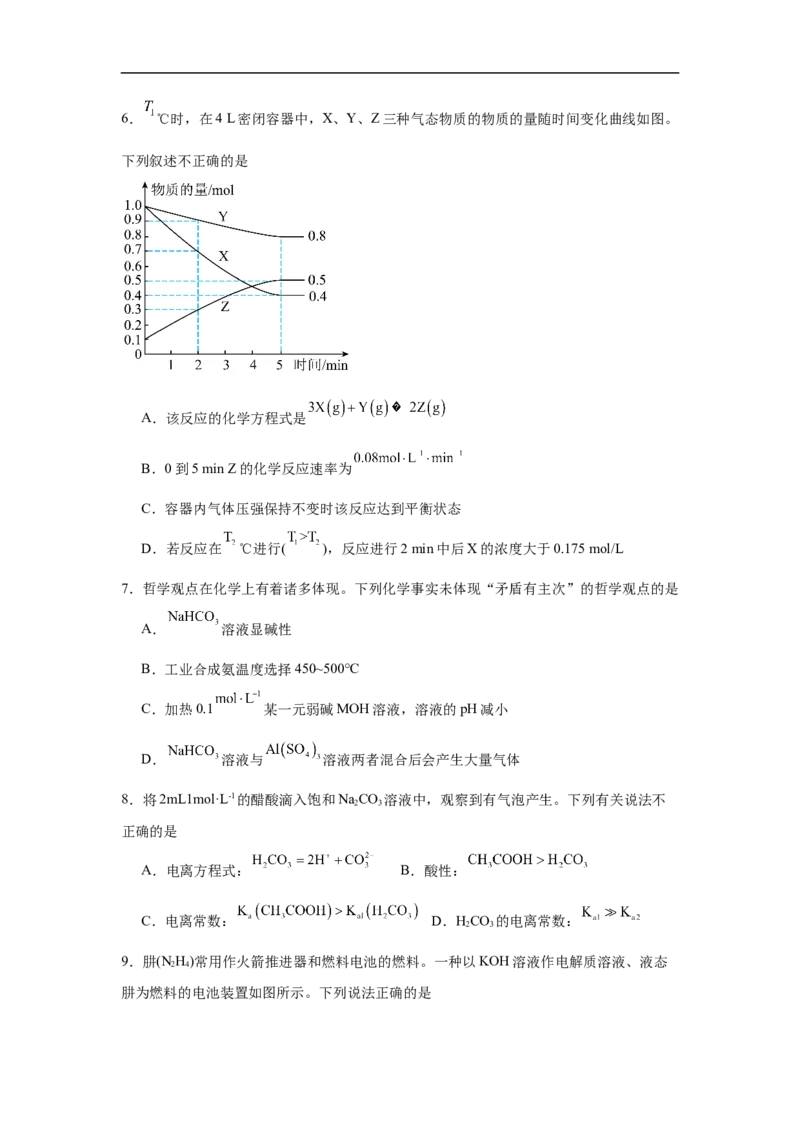
4.某研究小组利用软锰矿(主要成分为 ,另含少量铁、铝、铜、镍的化合物)作脱硫
剂,通过如图简化流程,既脱除燃煤尾气中的 ,又制得 。下列叙述错误的是
A.“还原酸浸”步骤的主要化学方程式为
B.X可能是
C.若滤渣2是CuS和NiS,则Y一定是
D.“氧化”步骤氧化剂与还原剂的物质的量之比为2:3
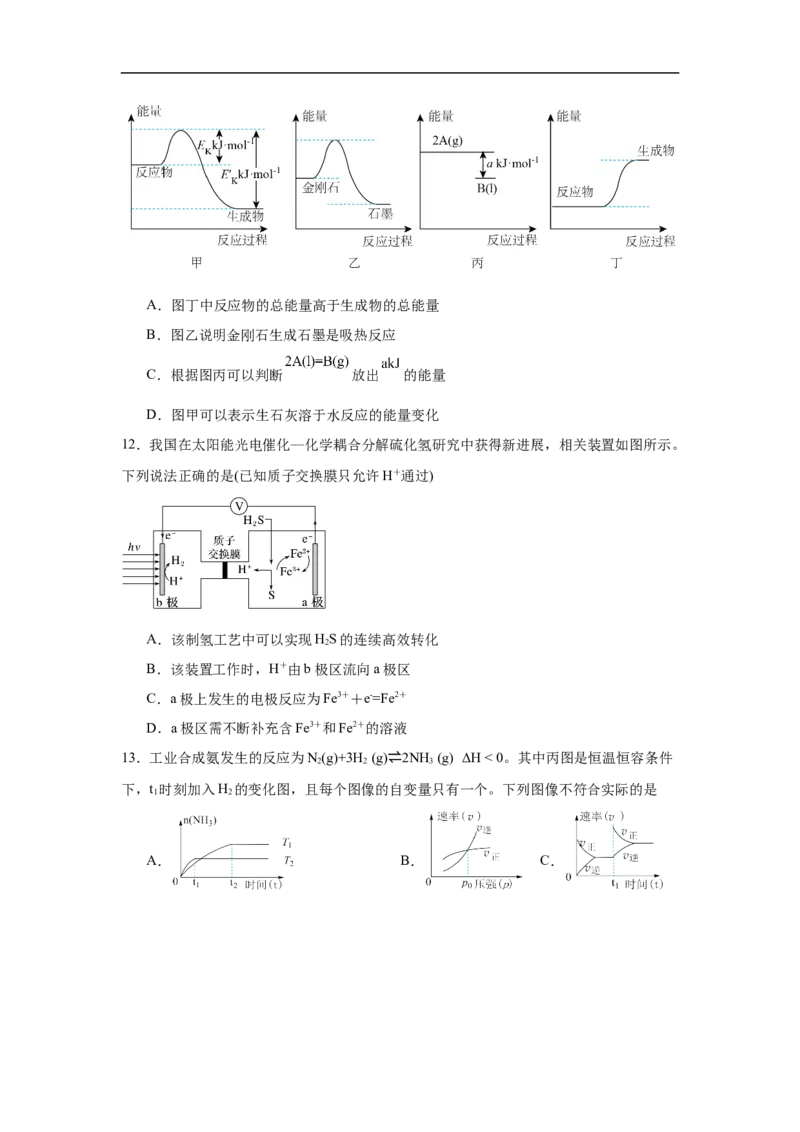
5.假设反应体系的始态为甲,中间态为乙,终态为丙,它们之间的变化如图所示,则下列
说法不正确的是
A. B.
C. D.甲→丙的
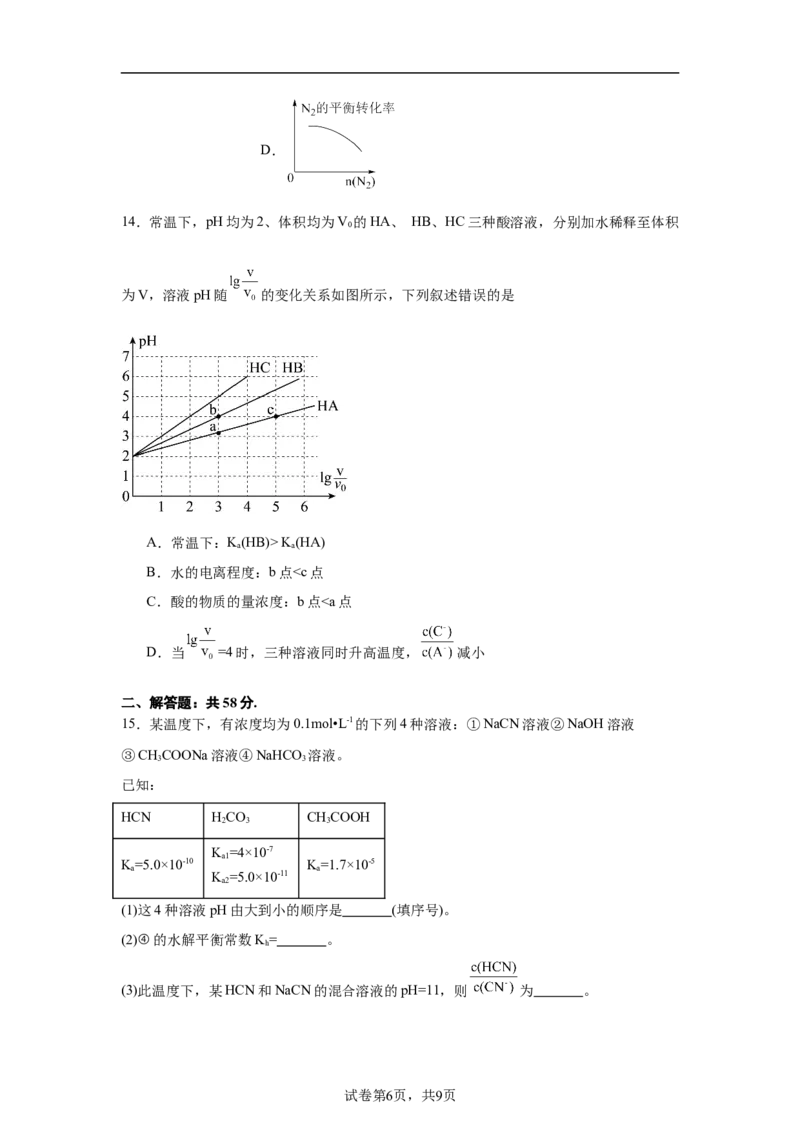
试卷第2页,共9页6. ℃时,在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
下列叙述不正确的是
A.该反应的化学方程式是
B.0到5 min Z的化学反应速率为
C.容器内气体压强保持不变时该反应达到平衡状态
D.若反应在 ℃进行( ),反应进行2 min中后X的浓度大于0.175 mol/L
7.哲学观点在化学上有着诸多体现。下列化学事实未体现“矛盾有主次”的哲学观点的是
A. 溶液显碱性
B.工业合成氨温度选择450~500℃
C.加热0.1 某一元弱碱MOH溶液,溶液的pH减小
D. 溶液与 溶液两者混合后会产生大量气体
8.将2mL1mol·L-1的醋酸滴入饱和NaCO 溶液中,观察到有气泡产生。下列有关说法不
2 3
正确的是
A.电离方程式: B.酸性:
C.电离常数: D.HCO 的电离常数:
2 3
9.肼(N H)常用作火箭推进器和燃料电池的燃料。一种以KOH溶液作电解质溶液、液态
2 4
肼为燃料的电池装置如图所示。下列说法正确的是A.放电时,b电极的电极电势比a电极高
B.放电时,电子从b电极经负载流向a电极
C.离子交换膜为阳离子交换膜
D.a电极反应式为NH + 4OH-+ 4e- =N ↑ + 4H O
2 4 2 2
10.下列实验方案设计、现象和结论都正确的是
方案设计 现象 结论
向恒温恒容密闭玻璃
容器中充入 气体颜 对于反应前后气体分子数不变的可逆反应,改变
A
气体,分解达到平衡 色不变 压强平衡不移动
后再充入
将一支盛有 溶液颜
色由蓝
B 溶液的试管水浴加热 变黄绿
片刻,取出置于冷水 后再变
中 蓝
向盛有 和
溶液颜
C 混合溶液的试管中加 平衡向左移动
色变浅
入少量 固体
分别向两支盛有
水溶液的 滴加
试管中滴3滴
溶液的
D 的 对 分解反应, 的催化能力优于
试管产
溶液和
生气泡
溶 快
液
A.A B.B C.C D.D
11.下列图像均表示化学反应中的能量变化,其中描述正确的是
试卷第4页,共9页A.图丁中反应物的总能量高于生成物的总能量
B.图乙说明金刚石生成石墨是吸热反应
C.根据图丙可以判断 放出 的能量
D.图甲可以表示生石灰溶于水反应的能量变化
12.我国在太阳能光电催化—化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。
下列说法正确的是(已知质子交换膜只允许H+通过)
A.该制氢工艺中可以实现HS的连续高效转化
2
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
13.工业合成氨发生的反应为N(g)+3H (g)⇌2NH (g) ΔH < 0。其中丙图是恒温恒容条件
2 2 3
下,t 时刻加入H 的变化图,且每个图像的自变量只有一个。下列图像不符合实际的是
1 2
A. B. C.D.
14.常温下,pH均为2、体积均为V 的HA、 HB、HC三种酸溶液,分别加水稀释至体积
0
为V,溶液pH随 的变化关系如图所示,下列叙述错误的是
A.常温下:K(HB)> K(HA)
a a
B.水的电离程度:b点”)。
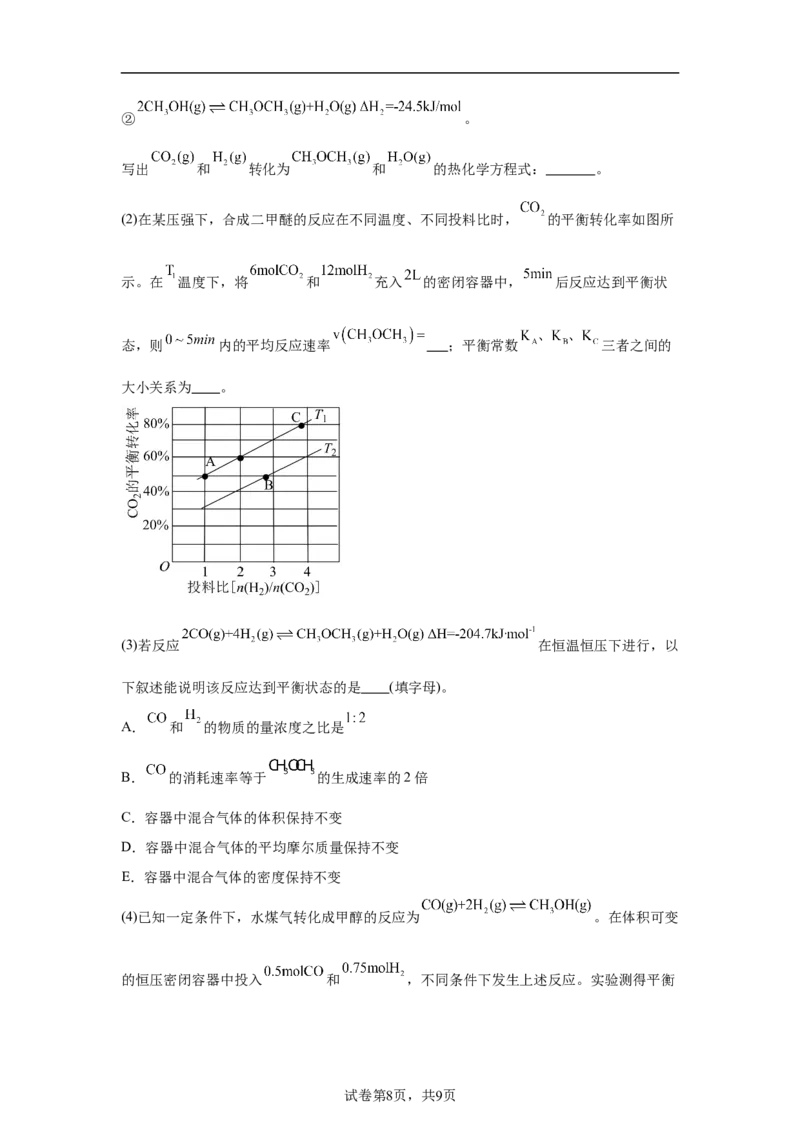
②M点对应的平衡混合气体的体积为 ,则 时,该反应的平衡常数 , 的
转化率为 (计算结果保留1位小数)。
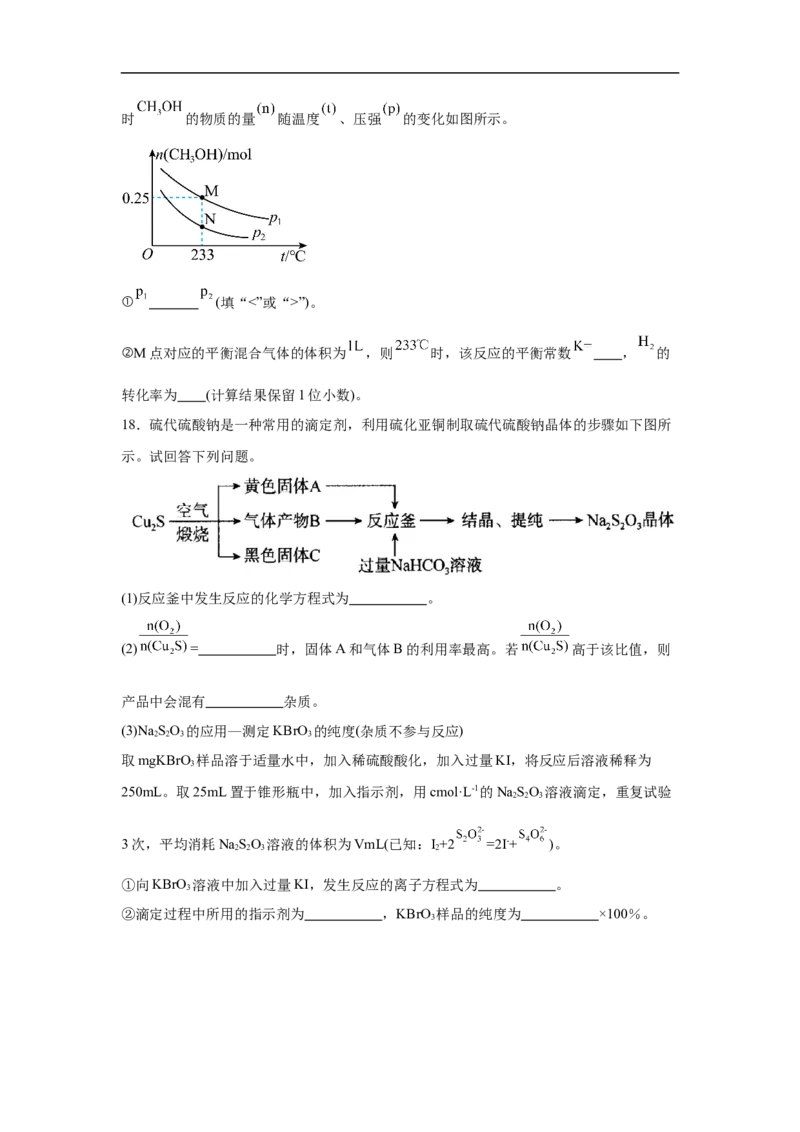
18.硫代硫酸钠是一种常用的滴定剂,利用硫化亚铜制取硫代硫酸钠晶体的步骤如下图所
示。试回答下列问题。
(1)反应釜中发生反应的化学方程式为 。
(2) = 时,固体A和气体B的利用率最高。若 高于该比值,则
产品中会混有 杂质。
(3)Na SO 的应用—测定KBrO 的纯度(杂质不参与反应)
2 2 3 3
取mgKBrO 样品溶于适量水中,加入稀硫酸酸化,加入过量KI,将反应后溶液稀释为
3
250mL。取25mL置于锥形瓶中,加入指示剂,用cmol·L-1的NaSO 溶液滴定,重复试验
2 2 3
3次,平均消耗NaSO 溶液的体积为VmL(已知:I+2 =2I-+ )。
2 2 3 2
①向KBrO 溶液中加入过量KI,发生反应的离子方程式为 。
3
②滴定过程中所用的指示剂为 ,KBrO 样品的纯度为 ×100%。
3