文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
题号 1 2 3 4 5 6 7
答案 A A C B A B B
题号 8 9 10 11 12 13 14
答案 C D B B D D D
【解析】
1.木材中的纤维素转化为炭黑制作墨水不涉及同素异形体的转化,同素异形体是同种元素的
不同单质,A错误。
2.HCl分子中键的形成为s和p轨道重叠后形成s−p键,A正确。2p能级中最后一个轨
道应该满足泡利原理,B错误。基态As原子的简化电子排布式:[Ar]3d104s24p3,C正确。
CH CH(CH CH )CH CH 的名称为3−甲基戊烷,D错误。
3 2 3 2 3
3.工业生产Si单质,用石英砂和碳高温反应生成Si和CO,A错误。给橘子树喷洒波尔多液
能起到杀菌作用,原因是铜离子能使蛋白质变性,B错误。用硫粉处理打碎的水银温度计,
S+Hg=HgS,S 体现氧化性,C 正确。工业合成氨采用高温作条件,因为单位时间内
生成NH 的量更多,该反应为放热反应,低温有利于提高平衡转化率,D错误。
3
4.用NaOH溶液吸收NO 气体的离子方程式为2NO +2OH−=NO+NO+H O,A正确。
2 2 3 2 2
SO 通入漂白液中,发生氧化还原反应SO +H O+3ClO−=SO2+Cl−+2HClO,B错误。
2 2 2 4
向饱和碳酸钠溶液中通入足量CO ,发生反应2Na++CO2+H O+CO =2NaHCO ↓,析
2 3 2 2 3
出 NaHCO 沉 淀 , C 正 确 。 甲 烷 燃 烧 热 的 热 化 学 方 程 式 : CH (g)+2O (g)
3 4 2
=CO (g)+2H O(l) ΔH=−890.3kJ·mol−1,D正确。
2 2
5.浓氨水滴在生石灰上可快速生成氨气,生成的氨气用碱石灰干燥,然后用向下排空气法收
集,A正确。NH 能溶于水,不能用排水法测体积,B错误。用Na CO 标准溶液滴定锥形
3 2 3
瓶中的盐酸,Na CO 溶液应盛放在碱式滴定管中,仪器的使用不合理,C错误。铁和水蒸
2 3
气在高温时发生反应生成 Fe O 和氢气,氢气被肥皂泡收集,可以用点燃肥皂泡的方法检
3 4
验氢气,但Fe O 为黑色固体,D错误。
3 4
化学参考答案·第1页(共7页)6.六氟合铂酸氙[XeF]+[Pt F ]-含有阴、阳离子,因此六氟合铂酸氙是离子化合物,A正确。
2 11
根据图中分析,上述制备过程的催化剂是F−,PtF不是催化剂,B错误。反应②中Xe元
7
素化合价升高,Pt 元素化合价降低,反应③中 Xe 元素化合价升高,Pt 元素化合价降低,
因此上述制备过程中属于氧化还原反应的有②③,C 正确。六氟合铂酸氙中含有[XeF]+,
则Xe元素的化合价为+2价,说明Xe被氧化,每生成1mol产物,转移2mol e−,D正确。
7.6.0g SiO 晶体中所含O—Si键的数目为0.4N ,A错误。常温下,1L pH=10的CH COONa
2 A 3
溶液中,由水电离的 OH−的数目为 10−4N ,故由水电离的 H+的数目为 10−4N ,B 正确。
A A
工业合成氨的反应为可逆反应,1mol N 与3mol H 充分反应生成NH 的分子数小于2N ,
2 2 3 A
C错误。标况下2.24L Cl 通入H O中充分反应,氯绝大多数以Cl 分子的形式存在,根据
2 2 2
原子守恒,Cl−、ClO−和HClO的数目小于0.2N ,D错误。
A
8.X中苯环和氢气以1∶3发生加成反应,碳碳双键1∶1加成,酯基中碳氧双键和氢气不发
生加成反应,1molX 只可与 4mol H 发生加成反应,A 错误。Y 相当于乙烯分子中的 4 个
2
氢原子被羧基取代,B 错误。含有酚羟基的有机物能和氯化铁溶液发生显色反应,X 能和
氯化铁溶液发生显色反应,X 和碳酸氢钠溶液不反应,所以可用 FeCl 溶液或 NaHCO 溶
3 3
液鉴别X和Y,C正确。酚羟基、酯基水解生成的羧基和酚羟基都能与NaOH反应,故1mol
M与6mol NaOH溶液反应,D错误。
9.海绵铜中加入硝酸铵、水和硫酸,硝酸根离子和氢离子构成硝酸,故反应生成铜离子、一
氧化氮,过滤后滤液中加入亚硫酸铵和氯化铵,此时铜离子与亚硫酸根离子、氯离子反应
生成 CuCl,过滤得到 CuCl,再洗涤烘干得到氯化亚铜粗产品。“溶解”过程中硫酸的作
用是提供酸性环境,硝酸铵中的硝酸根离子与硫酸电离出的氢离子构成硝酸,将铜氧化,
离子方程式是3Cu+8H++2NO=3Cu2++2NO↑+4H O,A错误。从后续操作看,“反应”
3 2
过程生成CuCl,则溶液中的Cu2+被SO2还原,发生反应的离子方程式是2Cu2++SO2+2Cl−
3 3
+H O=2CuCl↓+SO2+2H+,B错误。“溶解”过程中,若硫酸用浓盐酸代替,则“反
2 4
应”过程中生成的 CuCl 会被 Cl-溶解,难以得到 CuCl 沉淀,C 错误。“烘干”时,CuCl
易被空气中的氧气氧化,所以需在隔绝空气的环境中进行,D正确。
10.物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原
子序数的关系如图所示,X位于第一周期,为H,Y位于第二周期,M、N位于第三周期;
实验室中常用 CS 洗涤残留在试管壁上的 N 单质,则 N 为 S;Y 形成 4 个共价键,Z 形
2
成2个共价键,M形成+1价离子,则Y为C,Z为O,M为Na。Y、Z形成的阴离子为
化学参考答案·第2页(共7页)CO2,根据价层电子对互斥理论可知,该离子的空间构型为平面三角形,A正确。Na O
3 2 2
可作呼吸面具的供氧剂,当反应生成标况下22.4L O 时,转移电子的物质的量为2mol,
2
B错误。Y的氢化物为烃,Z的氢化物为水、双氧水,碳原子数较多的烃常温下为固态,
其沸点大于水和双氧水,Z 的氢化物的沸点不一定大于 Y 的氢化物的沸点,C 正确。W
分子中含有H—O—O—H结构,结合过氧化氢的性质可知,化合物W具有强氧化性,可
用作氧化剂,但过氧化氢不稳定,该物质不宜在高温下使用,D正确。
11.反应Ⅰ、Ⅲ为放热反应,相同物质的量的反应物,反应Ⅰ放出的热量小于反应Ⅱ放出的热
量,反应放出的热量越多,其焓变越小,因此反应焓变:反应Ⅰ>反应Ⅱ,A错误。短时
间里反应Ⅰ得到的产物比反应Ⅱ得到的产物多,说明反应Ⅰ的速率比反应Ⅱ的速率快,速
率越快,其活化能越小,则反应活化能:反应Ⅰ<反应Ⅱ,B正确。产物Ⅰ和产物Ⅱ存在
可逆反应,则产物Ⅱ和产物Ⅰ的比值即该可逆反应的平衡常数K,由于平衡常数只与温度
有关,所以选择合适的催化剂平衡时产物Ⅱ和产物Ⅰ的比例不变,C错误。根据图中信息,
选择相对较长的反应时间,能提高反应Ⅱ的产率,但是根据反应Ⅰ和Ⅲ为放热反应可知,
反应Ⅱ也为放热反应,反应Ⅱ和Ⅲ均为放热反应,所以降低温度才能提高反应Ⅱ的产率,
D错误。
12.石墨电极Y上的丙烯腈得电子变为己二腈,A错误。阳极是水电离出的氢氧根离子放电,
反应是为4OH−−4e−=2H O+O ↑,生成氢离子通过质子交换膜进入阴极室,电解过程
2 2
中阳极室溶剂减少,硫酸的物质的量不变,因此电解过程中稀硫酸的浓度逐渐增大,B错
误 。 丙 烯 腈 在 阴 极 得 到 电 子 生 成 己 二 腈 , 生 成 己 二 腈 的 电 极 反 应 式 为
2CH =CHCN+2e−+2H+――→NC(CH ) CN,C 错误。生成丙腈的电极反应式为
2 2 4
CH =CHCN+2e−+2H+――→CH CH CN,季铵盐的浓度为1.5×10−2mol/L时,己二腈和丙
2 3 2
腈的生成速率分别为3.4×10−3mol·h−1和0.8×10−3 mol·h−1,则每小时通过质子交换膜的
氢离子的物质的量最少为 3.4×10−3 mol·h−1×1h×2+0.8×10−3 mol·h−1×1h×2=
8.4×10−3,D正确。
28.8g
13.根据题意可知,n(Cu O)= =0.2mol,在反应中,Cu O中的Cu元素由+1价升高到
2 2
144g/mol
+2 价,则反应中转移电子的数目为 0.4N ,这些电子最终被 O 获得,因此标况下消耗
A 2
1000w
O 的体积为2.24L,A正确。根据计算公式c 可知,硝酸的c=12mol·L−1,B
2
M
正确。由 A 项可知,反应中转移电子的数目为 0.4N ,又根据题目可知
A
化学参考答案·第3页(共7页)4.48L
n(NO )= =0.2mol,在反应中,HNO 中生成NO 的N元素由+5价降低为+2x价,
x 3 x
22.4L/mol
依据得失电子守恒可得:0.4mol=0.2mol×(5−2x),x=1.5,C正确。向反应后的溶液中加入
4.00mol·L−1NaOH 溶液,当沉淀质量达到最大时,Cu(NO ) 及过量 HNO 刚好与 NaOH
3 2 3
完全反应,生成 NaNO 等,则 n(NaOH)=n(NO),从而得出 4.00mol·L−1×V(NaOH)=
3 3
n(HNO )−n(NO )= 0.100L×12.0mol·L−1−0.2mol,V(NaOH)=0.25L,D错误。
3 x
1 3 a3
14.根据题给信息,反应i的化学平衡常数K
i
=p(NH
3
)p(H
2
O)p(SO
2
)= a ,反应ii的化
3 27
1 2 b2
学平衡常数 K
ii
=p(H
2
O)p(SO
2
)= b ,在该温度下,将一定质量的 NH
4
HSO
3
与
2 4
NaHSO 加入某一密闭容器中达平衡,三种固体均存在。由于平衡i和ii,反应生成的H O
3 2
和SO 的量始终相等,则可设达平衡时H O和SO 的分压为xPa,NH 的分压为yPa,则
2 2 2 3
a3 b2 b 4a3
K x2y ,K x2 ,解得x Pa,y Pa,据此分析解答。反应 i 的化
i 27 ii 4 2 27b2
1 3 a3
学平衡常数 K
i
=p(NH
3
)p(H
2
O)p(SO
2
)= a ,A 正确。反应 ii 的化学平衡常数
3 27
1 2 b2
K
ii
=p(H
2
O)p(SO
2
)= b ,在该温度下,将一定质量的 NH
4
HSO
3
与 NaHSO
3
加入某
2 4
一密闭容器中达平衡,三种固体均存在。由于平衡i和ii,反应生成的H O和SO 的量始
2 2
a3
终相等,则可设达平衡时H O和SO 的分压为xPa,NH 的分压为yPa,则K=x2y= ,
2 2 3 i
27
b2 b 4a3
K =x2= ,解得x Pa,y Pa,B正确。保持恒温、恒容,若再通入少量NH ,
ii 4 2 27b2 3
平衡逆向移动,温度不变,平衡常数不变,再次平衡时体系的总压强不变,C正确。保持
恒温、恒压,若再通入少量 NH ,相当于扩大体积,平衡正向移动,由于温度不变 K 不
3
变,再次达平衡时,反应 ii 中 H O和 SO 的分压仍为 xPa,由此可知反应i中NH 的分
2 2 3
压仍为yPa,即再次平衡时容器内H O的物质的量增大,D错误。
2
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共15分)
(1)四(或4),ⅦB(2分,2个全对得分,见错不得分)
化学参考答案·第4页(共7页)(2)将MnO 还原为Mn2+(1分) SiO 、PbSO (2分,1个1分,见错不得分)
2 2 4
(3)2H SO +2FeSO +MnO =Fe (SO ) +MnSO +2H O
2 4 4 2 2 4 3 4 2
(4)Mn2++2HCO=MnCO ↓+CO ↑+H O
3 3 2 2
(5)取最后一次洗涤液,先加稀盐酸再加BaCl ,无白色沉淀产生
2
9.2cd
(6) %
b
4 4
πx32 πy341030
4πN (x2 2y3) 3 3
(7) A %(或 100%)
3M 1028 2M
N
A
【解析】(6)由MnO ~ Fe2+
4
1 5
n cd×10−3
cd cd
则n 103mol,m(MnCO ) 103411592cd103g,
5 3 5
92cd103 9.2cd
则w(MnCO ) 100% %。
3 b b
2M 2M
(7)由 得V cm3,
V N 晶胞 N
A A
4 4 8
V πx32 πy34 π(x3 2y3)pm3
球 3 3 3
代入计算即可。
16.(每空2分,共14分)
(1)圆底烧瓶
(2)f→g→b→c→e→d
(3)2HNO +4SnCl +8HCl=4SnCl +N O↑+5H O
3 2 4 2 2
(4)锡粒/Sn
(5)2N+ClO−+H O=3N ↑+Cl−+2OH−
3 2 2
(6)减小因液体进入圆底烧瓶引起的气体体积测量误差
13(V V )
(7) 1 2
3nV
m
化学参考答案·第5页(共7页)【解析】(2)氨基钠溶液易水解且容易被氧化,因此A中产生的N O中的HNO 和H O
2 3 2
需要通过碱石灰干燥除杂后进入B中,通入E之前需要再次干燥。
(4)类比FeCl 易被氧化用Fe单质防氧化。
2
(6)若无侧管,滴加液体时会将一部分空气挤入,导致气体测量体积偏大。
17.(除特殊标注外,每空2分,共16分)
(1)−2(x+y)
(2)BD(2分,1个1分,见错不得分)
(3)①d(1分)
②主副反应均为放热反应,升温平衡均逆移(1分),主反应逆移程度大于副反应(1分)
③加压或选用主反应选择性大的催化剂(1分)
(4)0.5 2(mol/L)−1
(5)①C H O −20e−+6H O=4CO ↑+20H+ ②18
4 8 2 2 2
【解析】(4)CH COOH + 2H ――→CH CH OH + H O
3 2 3 2 2
初/mol 1 2
Δ/mol x 2x x x
平/mol 1−x 2−2x x x
CH COOH + CH CH OHCH COOC H + H O
3 3 2 3 2 5 2
初/mol 1
Δ/mol y y y y
平/mol y
x y0.8
x0.6
则3x ,V 0.8L
0.8 y0.2 容
3
0.8 0.4
0.4 0.8 0.8
则:c(CH CH OH)= =0.5mol/L,K 2(mol/L)1。
3 2 0.8 0.8 2 0.2
0.8 0.8
(5) 、
化学参考答案·第6页(共7页)由C H O −20e−+6H O=4CO ↑+20H+
4 8 2 2 2
则20e−~20H+~5O
2
m=5×32+20=180g
则2mol e −时,m18g。
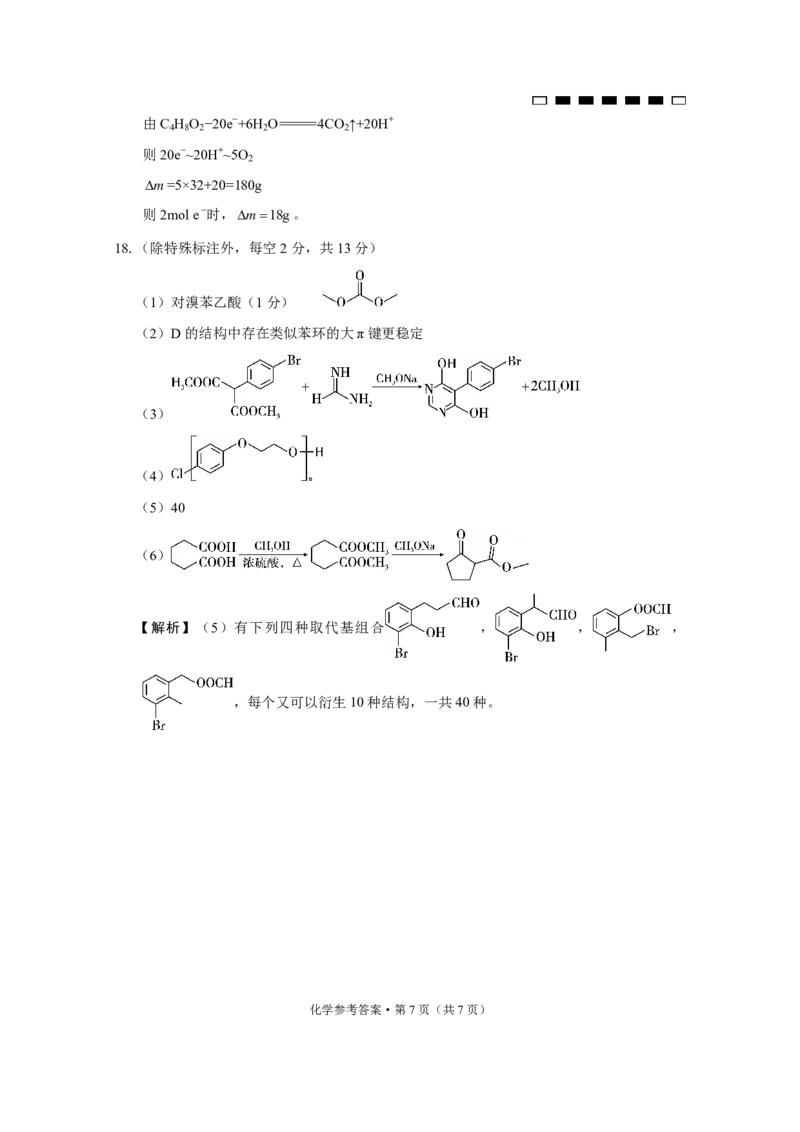
18.(除特殊标注外,每空2分,共13分)
(1)对溴苯乙酸(1分)
(2)D的结构中存在类似苯环的大π键更稳定
(3)
(4)
(5)40
(6)
【解析】(5)有下列四种取代基组合 , , ,
,每个又可以衍生10种结构,一共40种。
化学参考答案·第7页(共7页)