文档内容
2020年江苏省南通市中考化学试卷解析
一、选择题(本题共10个小题)
1.(2020•南通)垃圾分类回收有利于保护环境、节约资源。下列可回收垃圾中属于金属
材料的是( )
A.玻璃瓶 B.塑料袋 C.易拉罐 D.废报纸
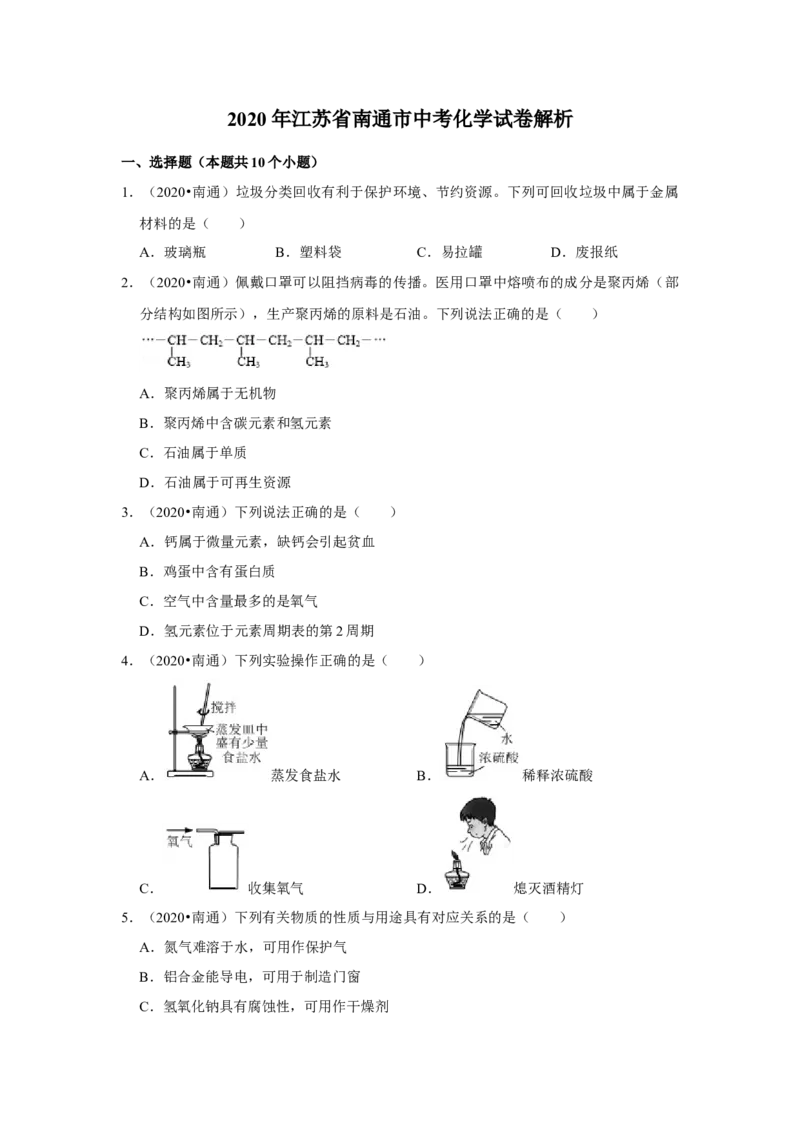
2.(2020•南通)佩戴口罩可以阻挡病毒的传播。医用口罩中熔喷布的成分是聚丙烯(部
分结构如图所示),生产聚丙烯的原料是石油。下列说法正确的是( )
A.聚丙烯属于无机物
B.聚丙烯中含碳元素和氢元素
C.石油属于单质
D.石油属于可再生资源
3.(2020•南通)下列说法正确的是( )
A.钙属于微量元素,缺钙会引起贫血
B.鸡蛋中含有蛋白质
C.空气中含量最多的是氧气
D.氢元素位于元素周期表的第2周期
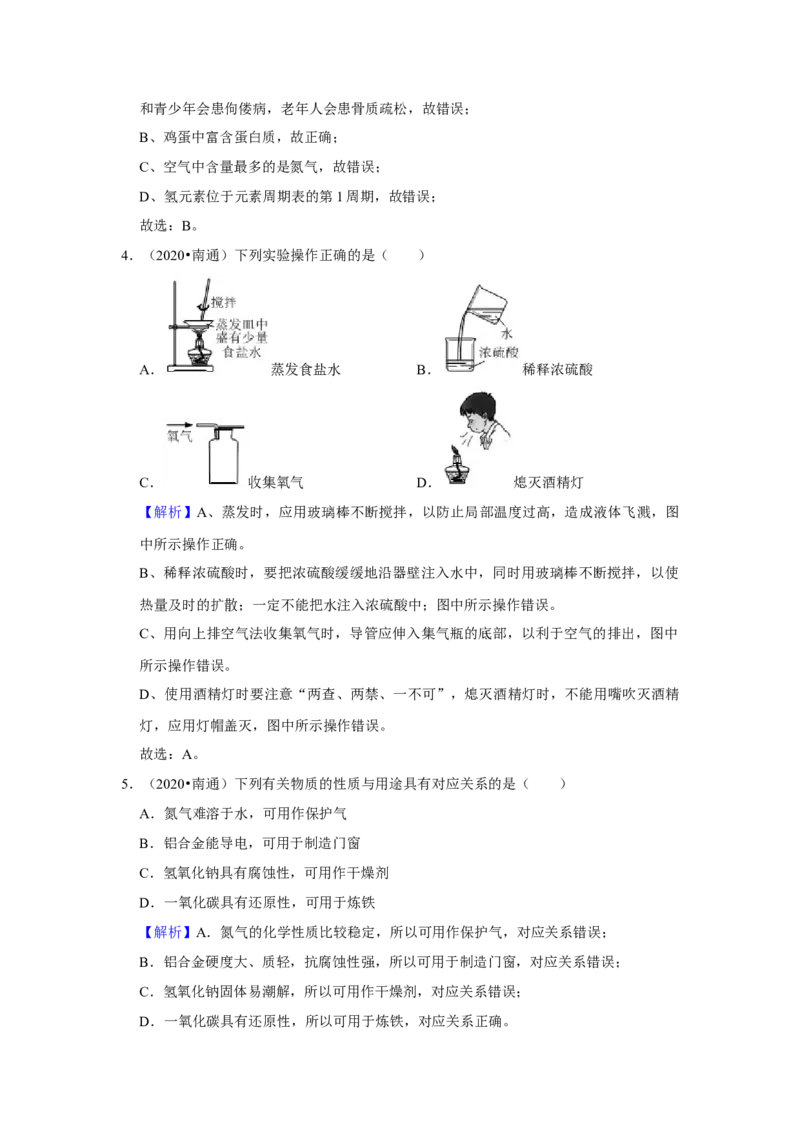
4.(2020•南通)下列实验操作正确的是( )
A. 蒸发食盐水 B. 稀释浓硫酸
C. 收集氧气 D. 熄灭酒精灯
5.(2020•南通)下列有关物质的性质与用途具有对应关系的是( )
A.氮气难溶于水,可用作保护气
B.铝合金能导电,可用于制造门窗
C.氢氧化钠具有腐蚀性,可用作干燥剂D.一氧化碳具有还原性,可用于炼铁
6.(2020•南通)“低碳”生活减少了二氧化碳的排放。下列说法正确的是( )
A.实验室用NaCl溶液检验CO
2
B.过多排放二氧化碳会造成温室效应
C.燃煤发电比太阳能发电有利于减少二氧化碳的排放
D.CO 通入滴有紫色石蕊试液的蒸馏水中,溶液颜色变蓝
2
7.(2020•南通)我国南海海底含大量的“可燃冰”。“可燃冰”外形似冰、可以燃烧,
其中主要含有甲烷水合物。下列说法正确的是( )
A.“可燃冰”可作为能源
B.“可燃冰”燃烧时只生成水
C.“可燃冰”燃烧属于物理变化
D.“可燃冰”能燃烧,说明水具有可燃性
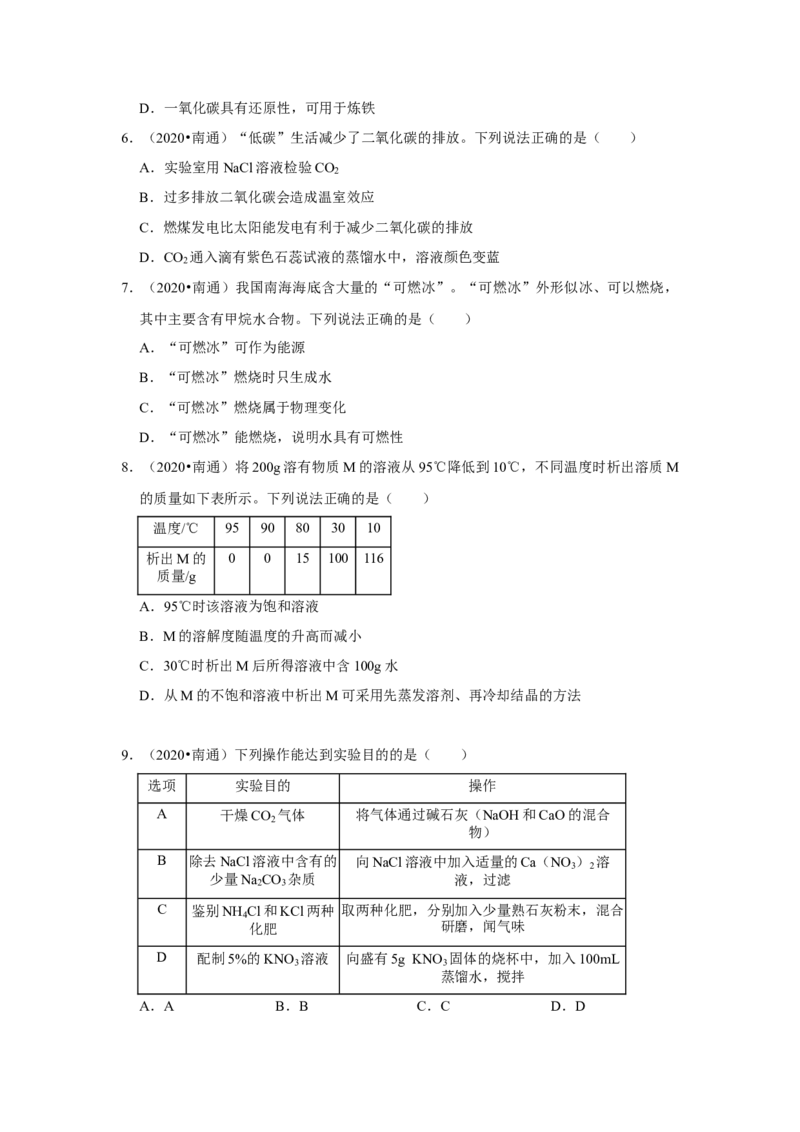
8.(2020•南通)将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M
的质量如下表所示。下列说法正确的是( )
温度/℃ 95 90 80 30 10
析出M的 0 0 15 100 116
质量/g
A.95℃时该溶液为饱和溶液
B.M的溶解度随温度的升高而减小
C.30℃时析出M后所得溶液中含100g水
D.从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法
9.(2020•南通)下列操作能达到实验目的的是( )
选项 实验目的 操作
A 干燥CO 气体 将气体通过碱石灰(NaOH和CaO的混合
2
物)
B 除去NaCl溶液中含有的 向NaCl溶液中加入适量的Ca(NO ) 溶
3 2
少量Na CO 杂质 液,过滤
2 3
C 鉴别NH Cl和KCl两种 取两种化肥,分别加入少量熟石灰粉末,混合
4
化肥 研磨,闻气味
D 配制5%的KNO 溶液 向盛有5g KNO 固体的烧杯中,加入100mL
3 3
蒸馏水,搅拌
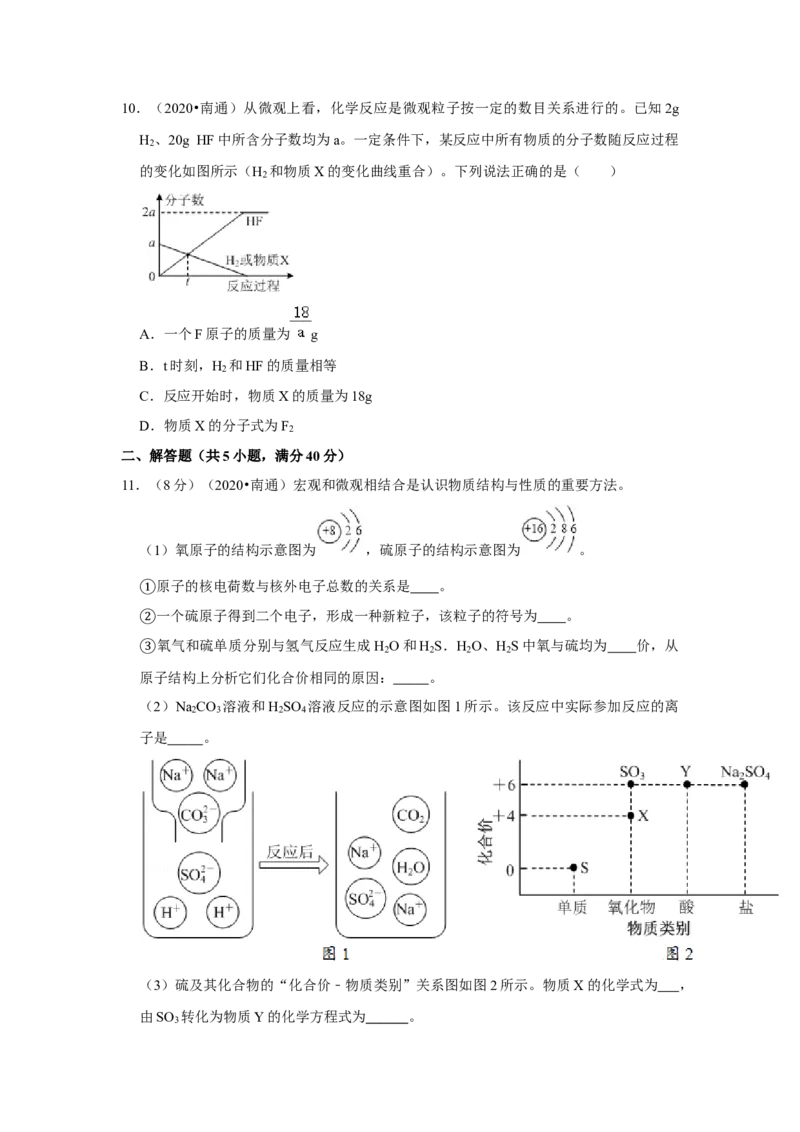
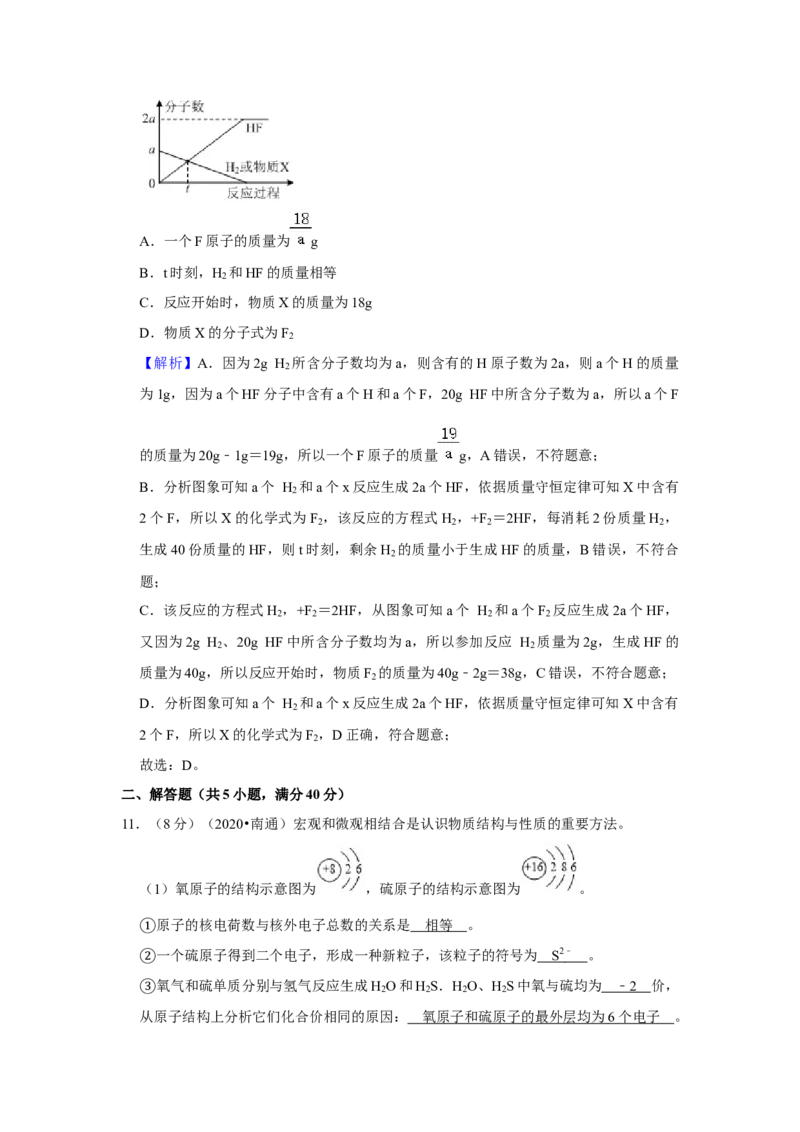
A.A B.B C.C D.D10.(2020•南通)从微观上看,化学反应是微观粒子按一定的数目关系进行的。已知2g
H 、20g HF中所含分子数均为a。一定条件下,某反应中所有物质的分子数随反应过程
2
的变化如图所示(H 和物质X的变化曲线重合)。下列说法正确的是( )
2
A.一个F原子的质量为 g
B.t时刻,H 和HF的质量相等
2
C.反应开始时,物质X的质量为18g
D.物质X的分子式为F
2
二、解答题(共5小题,满分40分)
11.(8分)(2020•南通)宏观和微观相结合是认识物质结构与性质的重要方法。
(1)氧原子的结构示意图为 ,硫原子的结构示意图为 。
原子的核电荷数与核外电子总数的关系是 。
①一个硫原子得到二个电子,形成一种新粒子,该粒子的符号为 。
②氧气和硫单质分别与氢气反应生成H
2
O和H
2
S.H
2
O、H
2
S中氧与硫均为 价,从
③原子结构上分析它们化合价相同的原因: 。
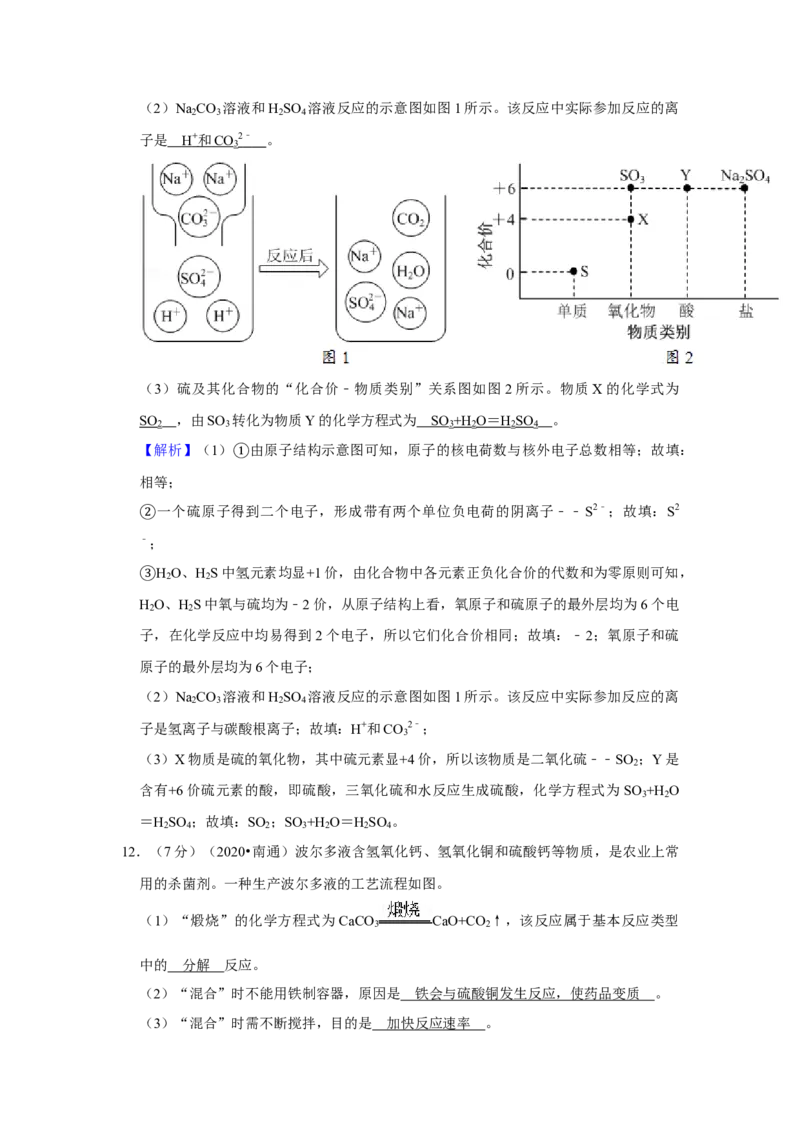
(2)Na CO 溶液和H SO 溶液反应的示意图如图1所示。该反应中实际参加反应的离
2 3 2 4
子是 。
(3)硫及其化合物的“化合价﹣物质类别”关系图如图2所示。物质X的化学式为 ,
由SO 转化为物质Y的化学方程式为 。
312.(7分)(2020•南通)波尔多液含氢氧化钙、氢氧化铜和硫酸钙等物质,是农业上常
用的杀菌剂。一种生产波尔多液的工艺流程如图。
(1)“煅烧”的化学方程式为CaCO CaO+CO ↑,该反应属于基本反应类型
3 2
中的 反应。
(2)“混合”时不能用铁制容器,原因是 。
(3)“混合”时需不断搅拌,目的是 。
(4)“混合”过程中硫酸铜和氢氧化钙反应生成氢氧化铜的化学方程式为 。
(5)“混合”后得到的波尔多液温度明显高于室温,原因是 。
(6)用 可以测定波尔多液酸碱度。
13.(8分)(2020•南通)中国画历史悠久、风格多样,是我国的文化艺术瑰宝。
(1)“文房四宝”之一的墨是中国传统水墨画的绘画材料。
墨由炭黑中加入天然胶等制成。墨属于 (填“混合物”或“纯净物”)。水墨
①画能长时间保存,是因为墨汁中的炭黑 。
宋代《墨经》记载“立窑烧烟法”的示意图如图1所示,炉膛口较小,松木置于炉膛
②中燃烧,瓮中收集的烟可用于制墨。“立窑烧烟法”利用了松木的 (填“完全”
或“不完全”)燃烧。
(2)敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu (OH) (CO )
3 2 3
].石青中铜元素(+2价)与碳元素的质量比为 (用不含x的比值表示)。
x
(3)油画促进了中国绘画的多元化发展。长期放置的油画色彩变暗,是因为生成了黑
色的PbS.油画修复的方法是用H O 将PbS变为白色的PbSO (另一产物为H O),修
2 2 4 2
复的化学方程式 。
(4)化学能拓展绘画表现形式。在图2中未着色的“葡萄画”上滴加酚酞试剂,“葡
萄”变为 色,打开装有 (填“浓氨水”、“浓盐酸”或“浓硫酸”)的试剂
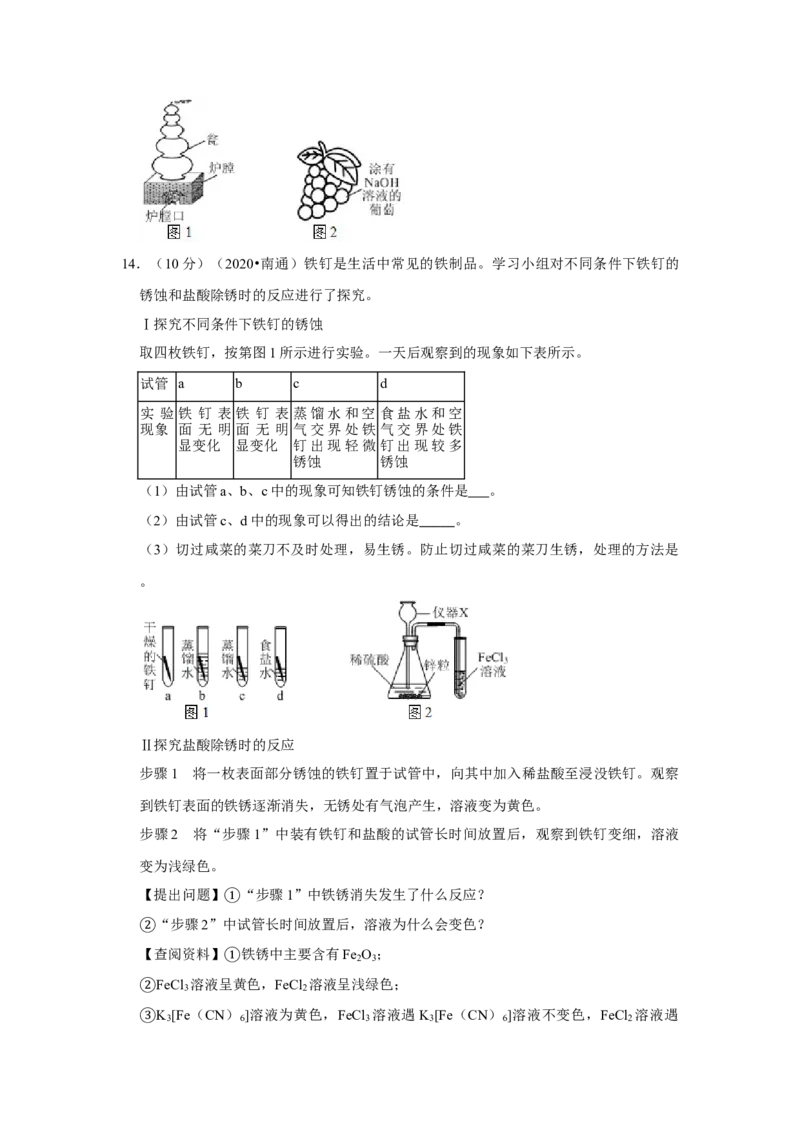
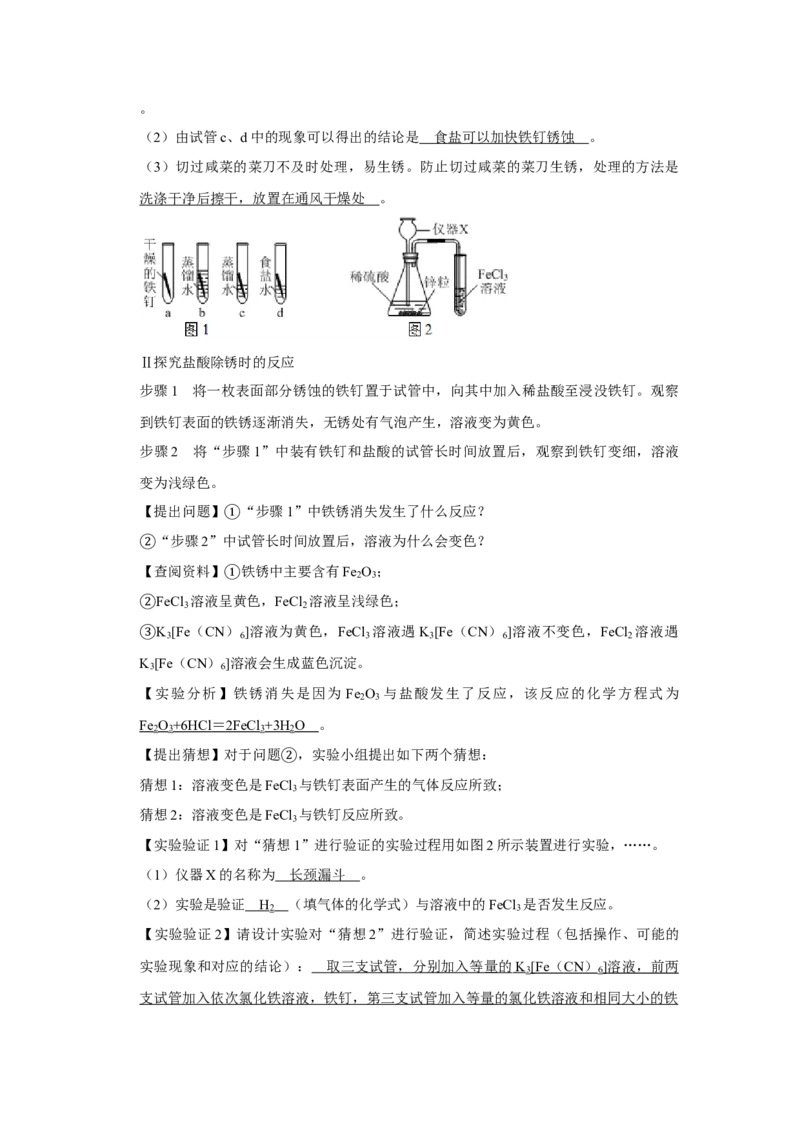
瓶,将瓶口靠近“葡萄”,“葡萄”颜色消失。14.(10分)(2020•南通)铁钉是生活中常见的铁制品。学习小组对不同条件下铁钉的
锈蚀和盐酸除锈时的反应进行了探究。
Ⅰ探究不同条件下铁钉的锈蚀
取四枚铁钉,按第图1所示进行实验。一天后观察到的现象如下表所示。
试管 a b c d
实 验铁 钉 表铁 钉 表蒸馏水和空 食盐水和空
现象 面 无 明 面 无 明气交界处铁 气交界处铁
显变化 显变化 钉出现轻微 钉出现较多
锈蚀 锈蚀
(1)由试管a、b、c中的现象可知铁钉锈蚀的条件是 。
(2)由试管c、d中的现象可以得出的结论是 。
(3)切过咸菜的菜刀不及时处理,易生锈。防止切过咸菜的菜刀生锈,处理的方法是
。
Ⅱ探究盐酸除锈时的反应
步骤1 将一枚表面部分锈蚀的铁钉置于试管中,向其中加入稀盐酸至浸没铁钉。观察
到铁钉表面的铁锈逐渐消失,无锈处有气泡产生,溶液变为黄色。
步骤2 将“步骤1”中装有铁钉和盐酸的试管长时间放置后,观察到铁钉变细,溶液
变为浅绿色。
【提出问题】 “步骤1”中铁锈消失发生了什么反应?
“步骤2”中①试管长时间放置后,溶液为什么会变色?
②【查阅资料】 铁锈中主要含有Fe
2
O
3
;
FeCl
3
溶液呈①黄色,FeCl
2
溶液呈浅绿色;
②K
3
[Fe(CN)
6
]溶液为黄色,FeCl
3
溶液遇K
3
[Fe(CN)
6
]溶液不变色,FeCl
2
溶液遇
③K [Fe(CN) ]溶液会生成蓝色沉淀。
3 6
【实验分析】铁锈消失是因为Fe O 与盐酸发生了反应,该反应的化学方程式为 。
2 3
【提出猜想】对于问题 ,实验小组提出如下两个猜想:
猜想1:溶液变色是FeC②l
3
与铁钉表面产生的气体反应所致;
猜想2:溶液变色是FeCl 与铁钉反应所致。
3
【实验验证1】对“猜想1”进行验证的实验过程用如图2所示装置进行实验,……。
(1)仪器X的名称为 。
(2)实验是验证 (填气体的化学式)与溶液中的FeCl 是否发生反应。
3
【实验验证2】请设计实验对“猜想2”进行验证,简述实验过程(包括操作、可能的
实验现象和对应的结论): 。(实验中必须用到K [Fe(CN) ]溶液、FeCl 溶液
3 6 3
和铁钉)
15.(7分)(2020•南通)南通滨临长江,将长江水净化处理可成为居民生活用水。
(1)水净化时先加入絮凝剂,沉降过滤后,通过活性炭。活性炭的作用是 。
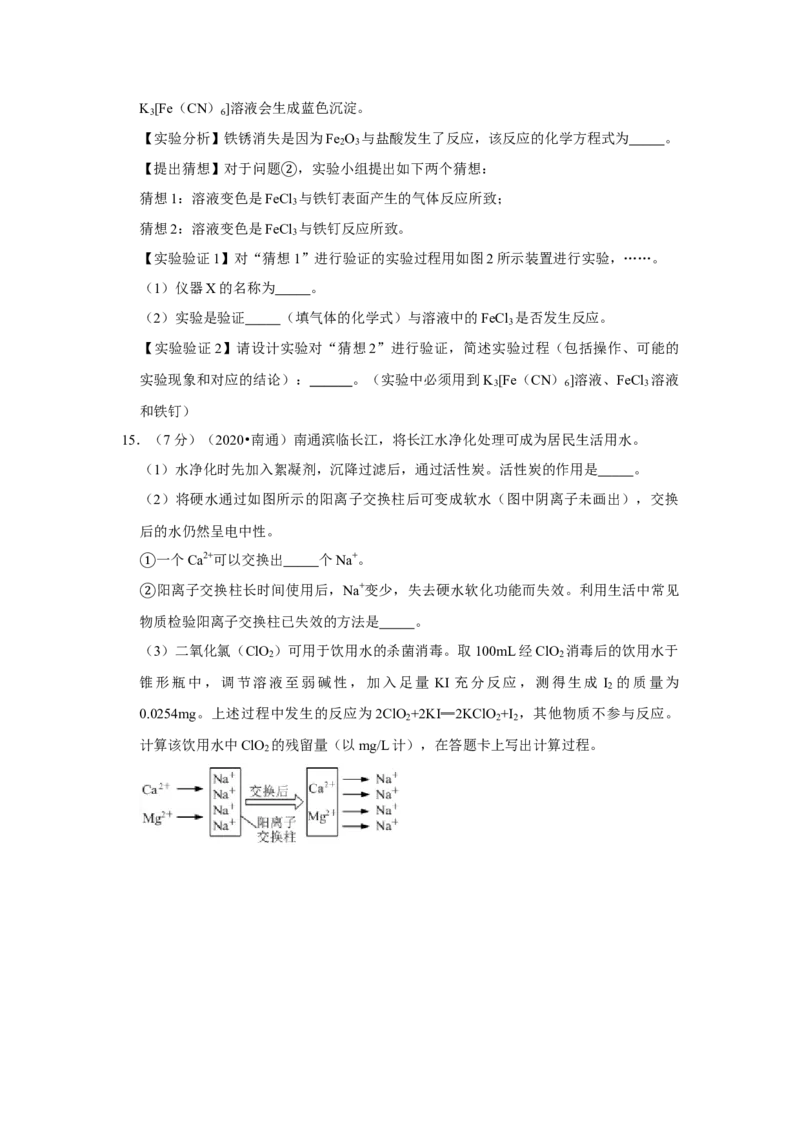
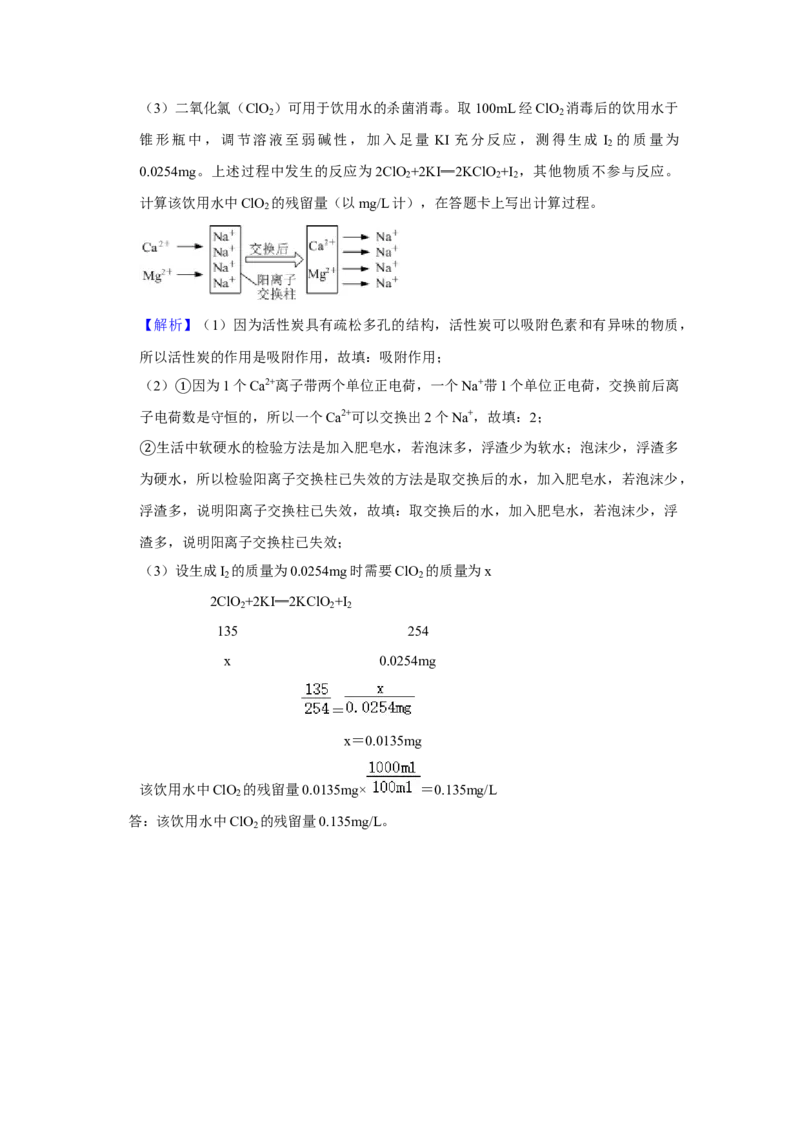
(2)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换
后的水仍然呈电中性。
一个Ca2+可以交换出 个Na+。
①阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见
②物质检验阳离子交换柱已失效的方法是 。
(3)二氧化氯(ClO )可用于饮用水的杀菌消毒。取100mL经ClO 消毒后的饮用水于
2 2
锥形瓶中,调节溶液至弱碱性,加入足量 KI 充分反应,测得生成 I 的质量为
2
0.0254mg。上述过程中发生的反应为2ClO +2KI═2KClO +I ,其他物质不参与反应。
2 2 2
计算该饮用水中ClO 的残留量(以mg/L计),在答题卡上写出计算过程。
22020年江苏省南通市中考化学试卷解析
一、选择题(本题共10个小题)
1.(2020•南通)垃圾分类回收有利于保护环境、节约资源。下列可回收垃圾中属于金属
材料的是( )
A.玻璃瓶 B.塑料袋 C.易拉罐 D.废报纸
【解析】A.玻璃瓶是由玻璃制成的,属于无机非金属材料,不合题意;
B.塑料属于有机合成材料,不合题意;
C.易拉罐是由铝制成的,属于金属材料,符合题意;
D.报纸含有的成分是天然的纤维素,不是金属材料,不合题意。
故选:C。
2.(2020•南通)佩戴口罩可以阻挡病毒的传播。医用口罩中熔喷布的成分是聚丙烯(部
分结构如图所示),生产聚丙烯的原料是石油。下列说法正确的是( )
A.聚丙烯属于无机物
B.聚丙烯中含碳元素和氢元素
C.石油属于单质
D.石油属于可再生资源
【解析】A、由图可知,聚丙烯是含碳的化合物,属于有机物,故选项错误;
B、由图可知,聚丙烯中含碳元素和氢元素,故选项正确;
C、石油中含有多种物质,属于混合物,故选项错误;
D、煤石油天然气等化石燃料都属于不可再生资源,故选项错误;
故选:B。
3.(2020•南通)下列说法正确的是( )
A.钙属于微量元素,缺钙会引起贫血
B.鸡蛋中含有蛋白质
C.空气中含量最多的是氧气
D.氢元素位于元素周期表的第2周期
【解析】A、钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏幼儿和青少年会患佝偻病,老年人会患骨质疏松,故错误;
B、鸡蛋中富含蛋白质,故正确;
C、空气中含量最多的是氮气,故错误;
D、氢元素位于元素周期表的第1周期,故错误;
故选:B。
4.(2020•南通)下列实验操作正确的是( )
A. 蒸发食盐水 B. 稀释浓硫酸
C. 收集氧气 D. 熄灭酒精灯
【解析】A、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图
中所示操作正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使
热量及时的扩散;一定不能把水注入浓硫酸中;图中所示操作错误。
C、用向上排空气法收集氧气时,导管应伸入集气瓶的底部,以利于空气的排出,图中
所示操作错误。
D、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时,不能用嘴吹灭酒精
灯,应用灯帽盖灭,图中所示操作错误。
故选:A。
5.(2020•南通)下列有关物质的性质与用途具有对应关系的是( )
A.氮气难溶于水,可用作保护气
B.铝合金能导电,可用于制造门窗
C.氢氧化钠具有腐蚀性,可用作干燥剂
D.一氧化碳具有还原性,可用于炼铁
【解析】A.氮气的化学性质比较稳定,所以可用作保护气,对应关系错误;
B.铝合金硬度大、质轻,抗腐蚀性强,所以可用于制造门窗,对应关系错误;
C.氢氧化钠固体易潮解,所以可用作干燥剂,对应关系错误;
D.一氧化碳具有还原性,所以可用于炼铁,对应关系正确。故选:D。
6.(2020•南通)“低碳”生活减少了二氧化碳的排放。下列说法正确的是( )
A.实验室用NaCl溶液检验CO
2
B.过多排放二氧化碳会造成温室效应
C.燃煤发电比太阳能发电有利于减少二氧化碳的排放
D.CO 通入滴有紫色石蕊试液的蒸馏水中,溶液颜色变蓝
2
【解析】A.二氧化碳与氯化钠溶液不反应,检验二氧化碳要用澄清的石灰水,选项说
法错误;
B.过多排放二氧化碳会造成温室效应,选项说法正确;
C.燃煤发电过程中会产生大量的二氧化碳,选项说法错误;
D.CO 通入滴有紫色石蕊试液的蒸馏水中,二氧化碳与水反应生成碳酸,碳酸能使紫
2
色的石蕊试液变红,选项说法错误。
故选:B。
7.(2020•南通)我国南海海底含大量的“可燃冰”。“可燃冰”外形似冰、可以燃烧,
其中主要含有甲烷水合物。下列说法正确的是( )
A.“可燃冰”可作为能源
B.“可燃冰”燃烧时只生成水
C.“可燃冰”燃烧属于物理变化
D.“可燃冰”能燃烧,说明水具有可燃性
【解析】A、“可燃冰”可以燃烧,可作为能源,故正确;
B、“可燃冰”主要含有甲烷水合物,所以燃烧会生成二氧化碳和水等,故错误;
C、“可燃冰”燃烧有新物质生成,属于化学变化,故错误;
D、“可燃冰”主要含有甲烷水合物,具有可燃性,但是水没有可燃性,故错误;
故选:A。
8.(2020•南通)将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M
的质量如下表所示。下列说法正确的是( )
温度/℃ 95 90 80 30 10
析出M的 0 0 15 100 116
质量/g
A.95℃时该溶液为饱和溶液
B.M的溶解度随温度的升高而减小
C.30℃时析出M后所得溶液中含100g水D.从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法
【解析】A、将200g溶有物质M的溶液从95℃降低到90℃,没有晶体析出,说明95℃
时该溶液为不饱和溶液,故选项说法错误。
B、将200g溶有物质M的溶液从95℃降低到10℃的过程中,逐渐析出晶体,说明M的
溶解度随温度的升高而增大,随温度的降低而减小,故选项说法错误。
C、30℃时析出M后析出100gM,所得溶液的质量为100g,故选项说法错误。
D、M的溶解度随温度的降低而减小,从M的不饱和溶液中析出M可采用先蒸发溶剂
再冷却结晶的方法,故选项说法正确。
故选:D。
9.(2020•南通)下列操作能达到实验目的的是( )
选项 实验目的 操作
A 干燥CO 气体 将气体通过碱石灰(NaOH和CaO的混合
2
物)
B 除去NaCl溶液中含有的 向NaCl溶液中加入适量的Ca(NO ) 溶
3 2
少量Na CO 杂质 液,过滤
2 3
C 鉴别NH Cl和KCl两种 取两种化肥,分别加入少量熟石灰粉末,混合
4
化肥 研磨,闻气味
D 配制5%的KNO 溶液 向盛有5g KNO 固体的烧杯中,加入100mL
3 3
蒸馏水,搅拌
A.A B.B C.C D.D
【解析】A、二氧化碳能被氢氧化钠吸收,该选项不能达到实验目的;
B、碳酸钠和硝酸钙反应生成碳酸钙沉淀和硝酸钠,除去碳酸钠带入硝酸钠,该选项不
能达到实验目的;
C、分别加入少量熟石灰粉末,混合研磨,产生刺激性气味的是氯化铵,是因为氯化铵
和氢氧化钙反应生成氯化钙、水和氨气,氨气有刺激性气味,该选项能够达到实验目的;
D、向盛有5g KNO 固体的烧杯中,加入100mL蒸馏水,搅拌,形成溶液的溶质质量
3
分数= ×100%=4.8%,该选项不能达到实验目的。
故选:C。
10.(2020•南通)从微观上看,化学反应是微观粒子按一定的数目关系进行的。已知2g
H 、20g HF中所含分子数均为a。一定条件下,某反应中所有物质的分子数随反应过程
2
的变化如图所示(H 和物质X的变化曲线重合)。下列说法正确的是( )
2A.一个F原子的质量为 g
B.t时刻,H 和HF的质量相等
2
C.反应开始时,物质X的质量为18g
D.物质X的分子式为F
2
【解析】A.因为2g H 所含分子数均为a,则含有的H原子数为2a,则a个H的质量
2
为1g,因为a个HF分子中含有a个H和a个F,20g HF中所含分子数为a,所以a个F
的质量为20g﹣1g=19g,所以一个F原子的质量 g,A错误,不符题意;
B.分析图象可知a个 H 和a个x反应生成2a个HF,依据质量守恒定律可知X中含有
2
2个F,所以X的化学式为F ,该反应的方程式H ,+F =2HF,每消耗2份质量H ,
2 2 2 2
生成40份质量的HF,则t时刻,剩余H 的质量小于生成HF的质量,B错误,不符合
2
题;
C.该反应的方程式H ,+F =2HF,从图象可知a个 H 和a个F 反应生成2a个HF,
2 2 2 2
又因为2g H 、20g HF中所含分子数均为a,所以参加反应 H 质量为2g,生成HF的
2 2
质量为40g,所以反应开始时,物质F 的质量为40g﹣2g=38g,C错误,不符合题意;
2
D.分析图象可知a个 H 和a个x反应生成2a个HF,依据质量守恒定律可知X中含有
2
2个F,所以X的化学式为F ,D正确,符合题意;
2
故选:D。
二、解答题(共5小题,满分40分)
11.(8分)(2020•南通)宏观和微观相结合是认识物质结构与性质的重要方法。
(1)氧原子的结构示意图为 ,硫原子的结构示意图为 。
原子的核电荷数与核外电子总数的关系是 相等 。
①一个硫原子得到二个电子,形成一种新粒子,该粒子的符号为 S 2 ﹣ 。
②氧气和硫单质分别与氢气反应生成H
2
O和H
2
S.H
2
O、H
2
S中氧与硫均为 ﹣ 2 价,
③从原子结构上分析它们化合价相同的原因: 氧原子和硫原子的最外层均为 6 个电子 。(2)Na CO 溶液和H SO 溶液反应的示意图如图1所示。该反应中实际参加反应的离
2 3 2 4
子是 H + 和 CO 2 ﹣ 。
3
(3)硫及其化合物的“化合价﹣物质类别”关系图如图2所示。物质X的化学式为
SO ,由SO 转化为物质Y的化学方程式为 SO +H O = H SO 。
2 3 3 2 2 4
【解析】(1) 由原子结构示意图可知,原子的核电荷数与核外电子总数相等;故填:
相等; ①
一个硫原子得到二个电子,形成带有两个单位负电荷的阴离子﹣﹣S2﹣;故填:S2
②﹣;
H O、H S中氢元素均显+1价,由化合物中各元素正负化合价的代数和为零原则可知,
2 2
③H O、H S中氧与硫均为﹣2价,从原子结构上看,氧原子和硫原子的最外层均为6个电
2 2
子,在化学反应中均易得到2个电子,所以它们化合价相同;故填:﹣2;氧原子和硫
原子的最外层均为6个电子;
(2)Na CO 溶液和H SO 溶液反应的示意图如图1所示。该反应中实际参加反应的离
2 3 2 4
子是氢离子与碳酸根离子;故填:H+和CO 2﹣;
3
(3)X物质是硫的氧化物,其中硫元素显+4价,所以该物质是二氧化硫﹣﹣SO ;Y是
2
含有+6价硫元素的酸,即硫酸,三氧化硫和水反应生成硫酸,化学方程式为SO +H O
3 2
=H SO ;故填:SO ;SO +H O=H SO 。
2 4 2 3 2 2 4
12.(7分)(2020•南通)波尔多液含氢氧化钙、氢氧化铜和硫酸钙等物质,是农业上常
用的杀菌剂。一种生产波尔多液的工艺流程如图。
(1)“煅烧”的化学方程式为CaCO CaO+CO ↑,该反应属于基本反应类型
3 2
中的 分解 反应。
(2)“混合”时不能用铁制容器,原因是 铁会与硫酸铜发生反应,使药品变质 。
(3)“混合”时需不断搅拌,目的是 加快反应速率 。(4)“混合”过程中硫酸铜和氢氧化钙反应生成氢氧化铜的化学方程式为 CuSO +Ca
4
( OH ) = CaSO +Cu ( OH ) ↓ 。
2 4 2
(5)“混合”后得到的波尔多液温度明显高于室温,原因是 氧化钙和水的反应属于
放热反应 。
(6)用 pH 试纸 可以测定波尔多液酸碱度。
【解析】(1)碳酸钙在高温的条件下生成氧化钙和二氧化碳,该反应是一种物质生成
了两种物质,属于分解反应;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,所以“混合”时不能用铁制容器;
(3)“混合”时需不断搅拌,目的是:加快反应速率;
(4)硫酸铜和氢氧化钙反应生成氢氧化铜沉淀和硫酸钙,化学方程式为:CuSO +Ca
4
(OH) =CaSO +Cu(OH) ↓;
2 4 2
(5)氧化钙和水的反应属于放热反应,所以“混合”后得到的波尔多液温度明显高于
室温;
(6)用pH试纸可以测定波尔多液酸碱度。
故答案为:(1)分解;
(2)铁会与硫酸铜发生反应,使药品变质;
(3)加快反应速率;
(4)CuSO +Ca(OH) =CaSO +Cu(OH) ↓;
4 2 4 2
(5)氧化钙和水的反应属于放热反应;
(6)pH试纸。
13.(8分)(2020•南通)中国画历史悠久、风格多样,是我国的文化艺术瑰宝。
(1)“文房四宝”之一的墨是中国传统水墨画的绘画材料。
墨由炭黑中加入天然胶等制成。墨属于 混合物 (填“混合物”或“纯净物”)。
①水墨画能长时间保存,是因为墨汁中的炭黑 化学性质不活泼 。
宋代《墨经》记载“立窑烧烟法”的示意图如图1所示,炉膛口较小,松木置于炉膛
②中燃烧,瓮中收集的烟可用于制墨。“立窑烧烟法”利用了松木的 不充分 (填“完
全”或“不完全”)燃烧。
(2)敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu (OH) (CO )
3 2 3
].石青中铜元素(+2价)与碳元素的质量比为 8 : 1 (用不含x的比值表示)。
x(3)油画促进了中国绘画的多元化发展。长期放置的油画色彩变暗,是因为生成了黑
色的PbS.油画修复的方法是用H O 将PbS变为白色的PbSO (另一产物为H O),修
2 2 4 2
复的化学方程式 PbS+4H O ═ PbSO +4H O 。
2 2 4 2
(4)化学能拓展绘画表现形式。在图2中未着色的“葡萄画”上滴加酚酞试剂,“葡
萄”变为 红 色,打开装有 浓盐酸 (填“浓氨水”、“浓盐酸”或“浓硫酸”)
的试剂瓶,将瓶口靠近“葡萄”,“葡萄”颜色消失。
【解析】(1) 墨由炭黑中加入天然胶等制成。墨属于混合物。水墨画能长时间保存,
是因为墨汁中的①炭黑化学性质不活泼;故填:混合物;化学性质不活泼;
“立窑烧烟法”利用了松木的不完全燃烧产生的炭黑;故填:不充分;
②(2)化合物中各元素正负化合价的代数和为零,即:(+2)×3++(﹣1)×2+(﹣2)
×x=0,x=2;则石青中铜元素(+2价)与碳元素的质量比为:(64×3):(12×2)=
8:1;故填:8:1;
(3)用H O 来“清洗”,则可将PbS转化为白色PbSO ,过氧化氢被还原为水,反应
2 2 4
为PbS+4H O ═PbSO +4H O,故填:PbS+4H O ═PbSO +4H O;
2 2 4 2 2 2 4 2
(4)氢氧化钠溶液显碱性,能使无色酚酞试液变红色,浓盐酸具有挥发性,挥发出来
的氯化氢气体溶于水形成盐酸,盐酸与氢氧化钠反应生成氯化钠和水,当氢氧化钠被完
全反应后,红色消失;故填:红;浓盐酸。
14.(10分)(2020•南通)铁钉是生活中常见的铁制品。学习小组对不同条件下铁钉的
锈蚀和盐酸除锈时的反应进行了探究。
Ⅰ探究不同条件下铁钉的锈蚀
取四枚铁钉,按第图1所示进行实验。一天后观察到的现象如下表所示。
试管 a b c d
实 验铁 钉 表铁 钉 表蒸馏水和空 食盐水和空
现象 面 无 明 面 无 明气交界处铁 气交界处铁
显变化 显变化 钉出现轻微 钉出现较多
锈蚀 锈蚀
(1)由试管a、b、c中的现象可知铁钉锈蚀的条件是 铁钉生锈需要与水和空气接触。
(2)由试管c、d中的现象可以得出的结论是 食盐可以加快铁钉锈蚀 。
(3)切过咸菜的菜刀不及时处理,易生锈。防止切过咸菜的菜刀生锈,处理的方法是
洗涤干净后擦干,放置在通风干燥处 。
Ⅱ探究盐酸除锈时的反应
步骤1 将一枚表面部分锈蚀的铁钉置于试管中,向其中加入稀盐酸至浸没铁钉。观察
到铁钉表面的铁锈逐渐消失,无锈处有气泡产生,溶液变为黄色。
步骤2 将“步骤1”中装有铁钉和盐酸的试管长时间放置后,观察到铁钉变细,溶液
变为浅绿色。
【提出问题】 “步骤1”中铁锈消失发生了什么反应?
“步骤2”中①试管长时间放置后,溶液为什么会变色?
②【查阅资料】 铁锈中主要含有Fe
2
O
3
;
FeCl
3
溶液呈①黄色,FeCl
2
溶液呈浅绿色;
②K
3
[Fe(CN)
6
]溶液为黄色,FeCl
3
溶液遇K
3
[Fe(CN)
6
]溶液不变色,FeCl
2
溶液遇
③K [Fe(CN) ]溶液会生成蓝色沉淀。
3 6
【实验分析】铁锈消失是因为 Fe O 与盐酸发生了反应,该反应的化学方程式为
2 3
Fe O +6HCl = 2FeCl +3H O 。
2 3 3 2
【提出猜想】对于问题 ,实验小组提出如下两个猜想:
猜想1:溶液变色是FeC②l
3
与铁钉表面产生的气体反应所致;
猜想2:溶液变色是FeCl 与铁钉反应所致。
3
【实验验证1】对“猜想1”进行验证的实验过程用如图2所示装置进行实验,……。
(1)仪器X的名称为 长颈漏斗 。
(2)实验是验证 H (填气体的化学式)与溶液中的FeCl 是否发生反应。
2 3
【实验验证2】请设计实验对“猜想2”进行验证,简述实验过程(包括操作、可能的
实验现象和对应的结论): 取三支试管,分别加入等量的 K [Fe ( CN ) ] 溶液,前两
3 6
支试管加入依次氯化铁溶液,铁钉,第三支试管加入等量的氯化铁溶液和相同大小的铁钉,前两支试管不发生变色,第三支试管变色并有蓝色沉淀生成,说明溶液变色是
FeCl 与铁钉反应所致 。(实验中必须用到K [Fe(CN) ]溶液、FeCl 溶液和铁钉)
3 3 6 3
【解析】Ⅰ(1)a和b与c相比变量为空气和水,因此得出铁生锈与空气和水有关;
故答案为:铁钉生锈需要与水和空气接触。
(2)c和d相比,铁钉生锈出现的多,说明氯化钠可以加快铁钉生锈速率;
故答案为:食盐可以加快铁钉锈蚀。
(3)菜刀上存留有氯化钠,为了去了氯化钠,需要清洗,另外不能与水和空气同时接
触,因此需要擦干,然后通风干燥保存;
故答案为:洗涤干净后擦干,放置在通风干燥处。
Ⅱ【实验分析】氧化铁与盐酸反应生成氯化铁和水,书写化学方程式注意配平,所以化
学方程式为Fe O +6HCl=2FeCl +3H O;
2 3 3 2
故答案为:Fe O +6HCl=2FeCl +3H O。
2 3 3 2
【实验验证1】(1)X为加入液体的长颈漏斗;
故答案为:长颈漏斗。
(2)锌与硫酸反应生成氢气和硫酸锌,所以气体为氢气;
故答案为:H 。
2
【实验验证2】根据K [Fe(CN) ]溶液为黄色,FeCl 溶液遇K [Fe(CN) ]溶液不变
3 6 3 3 6
色,FeCl 溶液遇K [Fe(CN) ]溶液会生成蓝色沉淀的现象,设计实验得出实验结论溶
2 3 6
液变色是FeCl 与铁钉反应所致;
3
故答案为:取三支试管,分别加入等量的K [Fe(CN) ]溶液,前两支试管加入依次氯
3 6
化铁溶液,铁钉,第三支试管加入等量的氯化铁溶液和相同大小的铁钉,前两支试管不
发生变色,第三支试管变色并有蓝色沉淀生成,说明溶液变色是FeCl 与铁钉反应所致。
3
15.(7分)(2020•南通)南通滨临长江,将长江水净化处理可成为居民生活用水。
(1)水净化时先加入絮凝剂,沉降过滤后,通过活性炭。活性炭的作用是 吸附作用
。
(2)将硬水通过如图所示的阳离子交换柱后可变成软水(图中阴离子未画出),交换
后的水仍然呈电中性。
一个Ca2+可以交换出 2 个Na+。
①阳离子交换柱长时间使用后,Na+变少,失去硬水软化功能而失效。利用生活中常见
②物质检验阳离子交换柱已失效的方法是 取交换后的水,加入肥皂水,若泡沫少,浮渣
多,说明阳离子交换柱已失效 。(3)二氧化氯(ClO )可用于饮用水的杀菌消毒。取100mL经ClO 消毒后的饮用水于
2 2
锥形瓶中,调节溶液至弱碱性,加入足量 KI 充分反应,测得生成 I 的质量为
2
0.0254mg。上述过程中发生的反应为2ClO +2KI═2KClO +I ,其他物质不参与反应。
2 2 2
计算该饮用水中ClO 的残留量(以mg/L计),在答题卡上写出计算过程。
2
【解析】(1)因为活性炭具有疏松多孔的结构,活性炭可以吸附色素和有异味的物质,
所以活性炭的作用是吸附作用,故填:吸附作用;
(2) 因为1个Ca2+离子带两个单位正电荷,一个Na+带1个单位正电荷,交换前后离
子电荷①数是守恒的,所以一个Ca2+可以交换出2个Na+,故填:2;
生活中软硬水的检验方法是加入肥皂水,若泡沫多,浮渣少为软水;泡沫少,浮渣多
②为硬水,所以检验阳离子交换柱已失效的方法是取交换后的水,加入肥皂水,若泡沫少,
浮渣多,说明阳离子交换柱已失效,故填:取交换后的水,加入肥皂水,若泡沫少,浮
渣多,说明阳离子交换柱已失效;
(3)设生成I 的质量为0.0254mg时需要ClO 的质量为x
2 2
2ClO +2KI═2KClO +I
2 2 2
135 254
x 0.0254mg
=
x=0.0135mg
该饮用水中ClO 的残留量0.0135mg× =0.135mg/L
2
答:该饮用水中ClO 的残留量0.135mg/L。
2