文档内容
湛江市第二十一中学2024-2025 学年第二学期4月考·高一
化学
考试时间:75分钟,满分:100分
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号、考场号和座位号填写在答题卡
上,并将考号条形码粘贴在答题卡上的指定位置。
2作答选择题时,选出每小题答案后,用2铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,
用橡皮擦干净后,再选涂其他答案。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;
如需改动,先划掉原来的答案,然后再写上新的答案。
4.不准使用铅笔和涂改液。不按以上要求作答的答案无效。
可能用到的相对原子质量:H:1 N:14 O:16 Na:23 Si:28 S:32 Cl:35.5 Fe:56 Cu:64
第I卷选择题(共44分)
一、选择题: 本题共16小题,共44分,第1--10小题,每小题2分;第11--16小题,每小题4分。在每
小题给出的四个选项中,只有一项符合题目要求的。
1.生活与能量转化息息相关,下列能量转化是由化学能直接转化为电能的是( )
A.燃料电池电动车 B.风力发电 C.使用天然气燃气灶 D.火力发电
2. 第19届杭州亚运会是一次充满未来感和科技感的盛会。下列有关说法错误的是( )
A. 亚运火炬“薪火”燃料为再生的绿色甲醇,甲醇是一种清洁燃料
B. 杭州亚运会夜空中美丽 的探照灯光束,其原理是丁达尔效应
C. “杭州伞”以钢管为基础构建,钢是用量最大、用途最广的合金
D. 开幕式上五彩缤纷的烟花,其焰色原理的本质是一种化学变化
3.在四个不同的容器中,不同条件下进行的合成氨反应N+3H 2NH,其中生成氨气速率最快的是(
2 2 3
)
A.v(N)=0.3 mol·L-1·min-1 B.v(NH)=0.5 mol·L-1·min-1
2 3
C.v(H)=0.01 mol·L-1·s-1 D.v(N)=0.2 mol·L-1·min-1
2 2
4.下列化学用语表示正确的是( )
A.氢化钠(NaH)中H的化合价:-1 B.小苏打的化学式:NaCO
2 3C.氯离子的结构示意图: D.NaClO的电离方程式:NaClO Na++Cl-+O2-
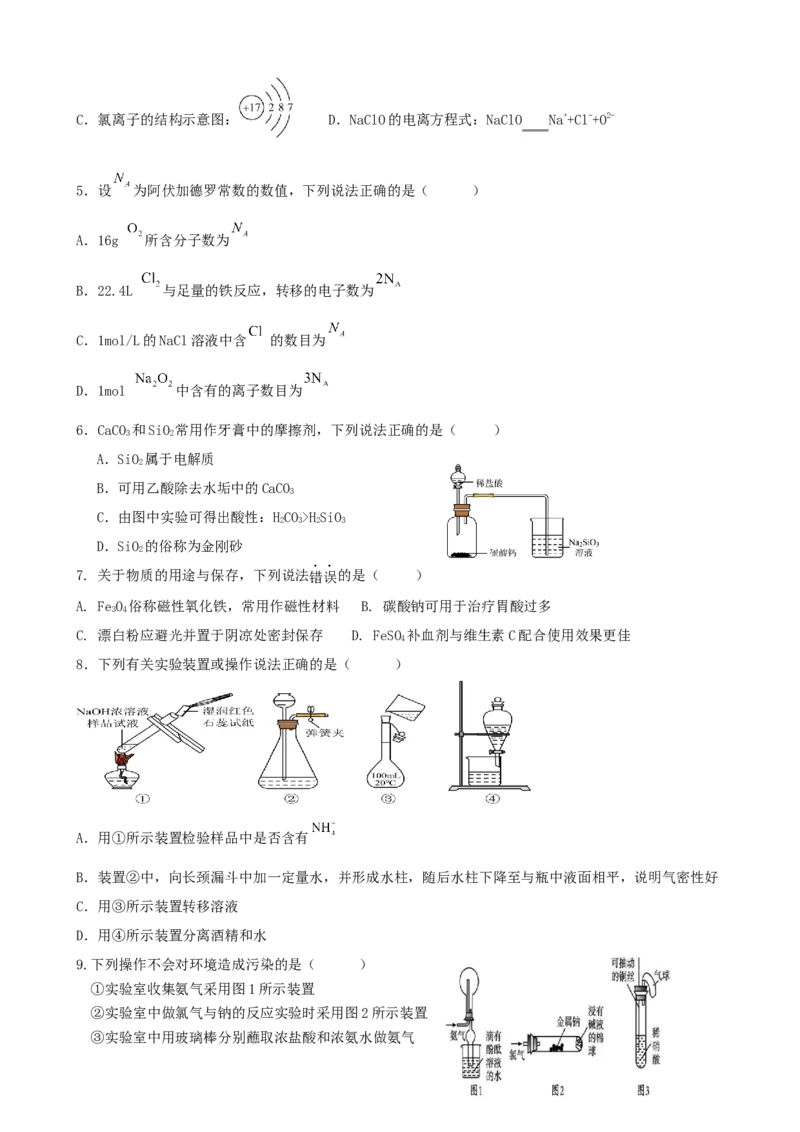
5.设 为阿伏加德罗常数的数值,下列说法正确的是( )
A.16g 所含分子数为
B.22.4L 与足量的铁反应,转移的电子数为
C.1mol/L的NaCl溶液中含 的数目为
D.1mol 中含有的离子数目为
6.CaCO 和SiO 常用作牙膏中的摩擦剂,下列说法正确的是( )
3 2
A.SiO 属于电解质
2
B.可用乙酸除去水垢中的CaCO
3
C.由图中实验可得出酸性:HCO>HSiO
2 3 2 3
D.SiO 的俗称为金刚砂
2
7. 关于物质的用途与保存,下列说法错误的是( )
A. FeO 俗称磁性氧化铁,常用作磁性材料 B. 碳酸钠可用于治疗胃酸过多
3 4
C. 漂白粉应避光并置于阴凉处密封保存 D. FeSO 补血剂与维生素C配合使用效果更佳
4
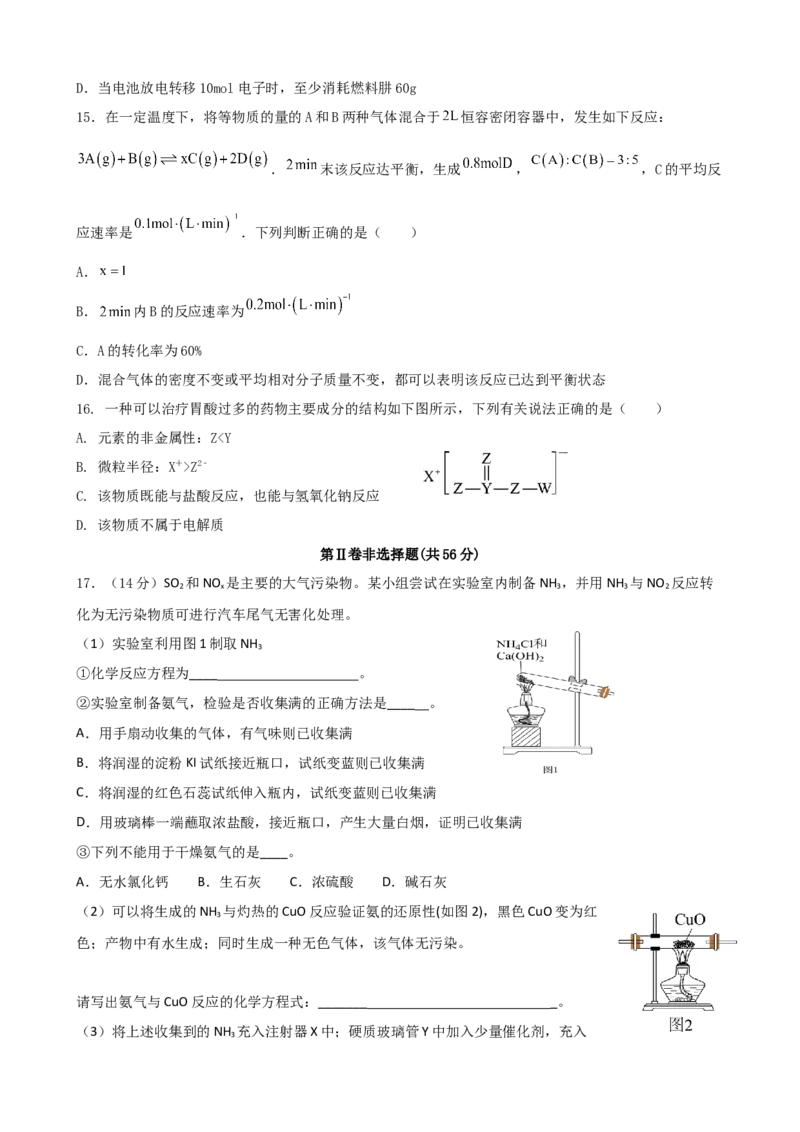
8.下列有关实验装置或操作说法正确的是( )
A.用①所示装置检验样品中是否含有
B.装置②中,向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性好
C.用③所示装置转移溶液
D.用④所示装置分离酒精和水
9.下列操作不会对环境造成污染的是( )
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠的反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸反应生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
A. ①③ B. ①④ C. ②③ D.③④
10. 中国化学遴选了118名青年化学家作为“元素代言人”组成“中国青年化学家元素周期表”。元素
Po(钋)与S同主族,由暨南大学陈填烽代言,其原子序数为84.下列说法正确的是( )
A. Po位于元素周期表的第4周期 B. 原子半径:PoZ2﹣
C. 该物质既能与盐酸反应,也能与氢氧化钠反应
D. 该物质不属于电解质
第Ⅱ卷非选择题(共56分)
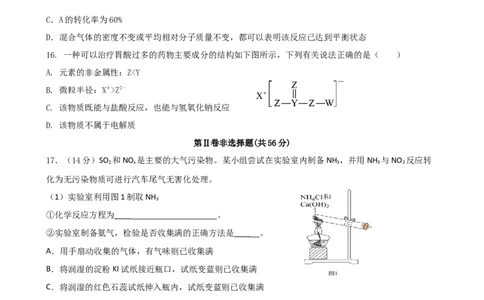
17.(14分)SO 和NO 是主要的大气污染物。某小组尝试在实验室内制备NH ,并用NH 与NO 反应转
2 x 3 3 2
化为无污染物质可进行汽车尾气无害化处理。
(1)实验室利用图1制取NH
3
①化学反应方程为____ 。
②实验室制备氨气,检验是否收集满的正确方法是____ 。
A.用手扇动收集的气体,有气味则已收集满
B.将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满
C.将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满
D.用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满
③下列不能用于干燥氨气的是____。
A.无水氯化钙 B.生石灰 C.浓硫酸 D.碱石灰
(2)可以将生成的NH 与灼热的CuO反应验证氨的还原性(如图2),黑色CuO变为红
3
色;产物中有水生成;同时生成一种无色气体,该气体无污染。
请写出氨气与CuO反应的化学方程式:_______ _。
(3)将上述收集到的NH 充入注射器X中;硬质玻璃管Y中加入少量催化剂,充入
3NO (两端用夹子K 、K 夹好)。在一定温度下按图所示装置进行实验(加热装置和夹持装置省略)。
2 1 2
①打开K ,推动注射器活塞,使X中的气体缓慢通入Y管中,可观察到Y管中_____,Y管中反应的化学方
1
程式为:______ 。
②Z的作用为_____ _。
18.(14分)下表为元素周期表的一部分,参照元素①~⑪在表中的位置,回答下列问题:
(1)已知元素⑪的一种核素,其中子数为45,用原子符号表示该核素为 (用 的形式表示)。
(2)②、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为 (用化学式表示)。
(3)写出③和⑤两元素形成的具有较强氧化性的化合物的电子式 ,该物质中含有的化学键类型
为 。用电子式表示⑥和⑩两元素组成的化合物的形成过程 。
(4)下列事实中不能说明非金属性⑩>⑨的是 (填标号)。
a.⑨和⑩两元素的简单氢化物受热分解,后者的分解温度高
b.元素⑩的单质能将 氧化成三价铁,而元素⑨的单质只能将铁氧化成二价铁
c.元素⑩的单质与⑨的氢化物的水溶液反应,产生元素⑨的单质
d.元素⑩的氢化物的水溶液的酸性比元素⑨的氢化物的水溶液的酸性强
(5)写出⑦的单质与⑤的最高价氧化物的水化物反应的离子方程式 。
19. (14分)利用金属矿渣(含有FeS、SiO 及CuO)制备FeCO 的实验流程如下。已知煅烧过程中FeS 和
2 2 2 3 2
CuO转化为FeO 和CuO。
2 2 3
(1)滤渣1的主要成分为:______(写化学式)。
(2)FeS 在空气中煅烧的化学方程式为______。
2
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将 转化为 外,还能______。若将6 g铁粉加入200 mL Fe(SO) 和CuSO 的混合溶液中,充分反应得到200 mL 0.5mol.L-1FeSO 溶液和
2 4 3 4 4
5.2 g固体沉淀物。
①5.2 g固体沉淀物的成份为_______(写化学式)。
②原Fe(SO) 溶液的物质的量浓度是_______。
2 4 3
(4)检验Fe3+是否完全被还原的实验操作是_______。
(5)制备FeCO,写出“沉铁”步骤发生反应的离子方程式:_______。
3
20.(14分)I .(1).为防止氮的氧化物污染空气,可用活性炭或一氧化碳还原氮氧化物。 请回答问题:
消除 NO 污染物,可在一定条件下,用 CO 与 NO 反应生成CO 和N ,反应的化学方程式:2CO(g)
2 2
+2NO(g) N(g)+2CO(g)。
2 2
①为提高此反应的速率,下列措施可行的是 (填字母代号)。
A.增大压强 B.降低温度 C.使用适合催化剂 D.移出 CO
2
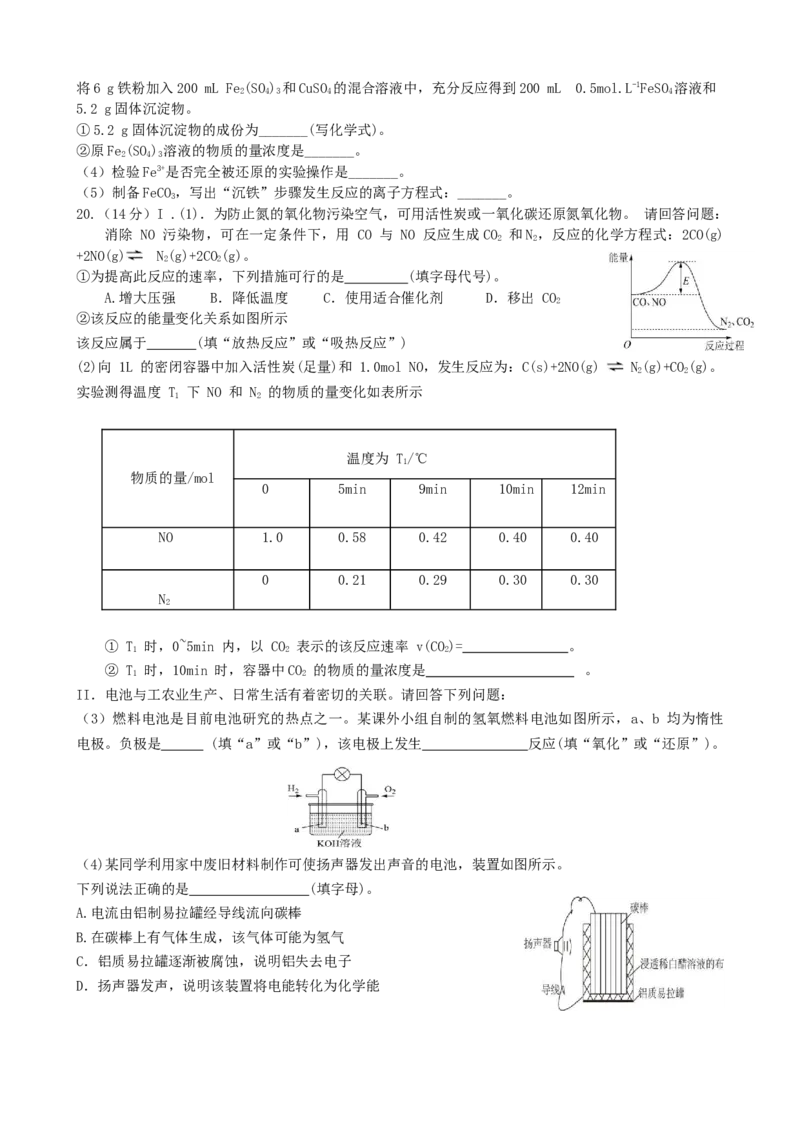
②该反应的能量变化关系如图所示
该反应属于 (填“放热反应”或“吸热反应”)
(2)向 1L 的密闭容器中加入活性炭(足量)和 1.0mol NO,发生反应为:C(s)+2NO(g) N(g)+CO(g)。
2 2
实验测得温度 T 下 NO 和 N 的物质的量变化如表所示
1 2
温度为 T/℃
1
物质的量/mol
0 5min 9min 10min 12min
NO 1.0 0.58 0.42 0.40 0.40
0 0.21 0.29 0.30 0.30
N
2
① T 时,0~5min 内,以 CO 表示的该反应速率 v(CO)= 。
1 2 2
② T 时,10min 时,容器中CO 的物质的量浓度是 。
1 2
II.电池与工农业生产、日常生活有着密切的关联。请回答下列问题:
(3)燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b 均为惰性
电极。负极是 (填“a”或“b”),该电极上发生 反应(填“氧化”或“还原”)。
(4)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如图所示。
下列说法正确的是 (填字母)。
A.电流由铝制易拉罐经导线流向碳棒
B.在碳棒上有气体生成,该气体可能为氢气
C.铝质易拉罐逐渐被腐蚀,说明铝失去电子
D.扬声器发声,说明该装置将电能转化为化学能