文档内容
化学部分
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Fe-56 Cu-64 Zn-65
一、选择题(共10小题,每小题2分,计20分。每题只有一个选项符合题意)
1. 下列变化过程中,不属于缓慢氧化的是
A. 塑料老化 B. 食物腐败 C. 镁条燃烧 D. 动植物呼吸
【答案】C
【解析】
【详解】A、塑料老化是塑料与氧气发生的缓慢氧化,不符合题意;
B、食物腐败进行的很慢,属于缓慢氧化,不符合题意;
C、镁条燃烧是剧烈的氧化反应,符合题意;
D、动植物呼吸进行的很慢,属于缓慢氧化,不符合题意。
故选C。
2. 下列物质溶于水,会导致溶液温度明显降低的是
A. 硝酸铵 B. 蔗糖 C. 浓硫酸 D. 氢氧化钠
【答案】A
【解析】
【详解】A、硝酸铵溶于水吸热, 溶液温度明显降低,符合题意;
B、蔗糖溶于水,温度变化不大,不符合题意;
C、浓硫酸溶于水,放出大量的热,溶液温度升高,不符合题意;
D、氢氧化钠溶于水,放出大量的热,溶液温度升高,不符合题意。
故选A。
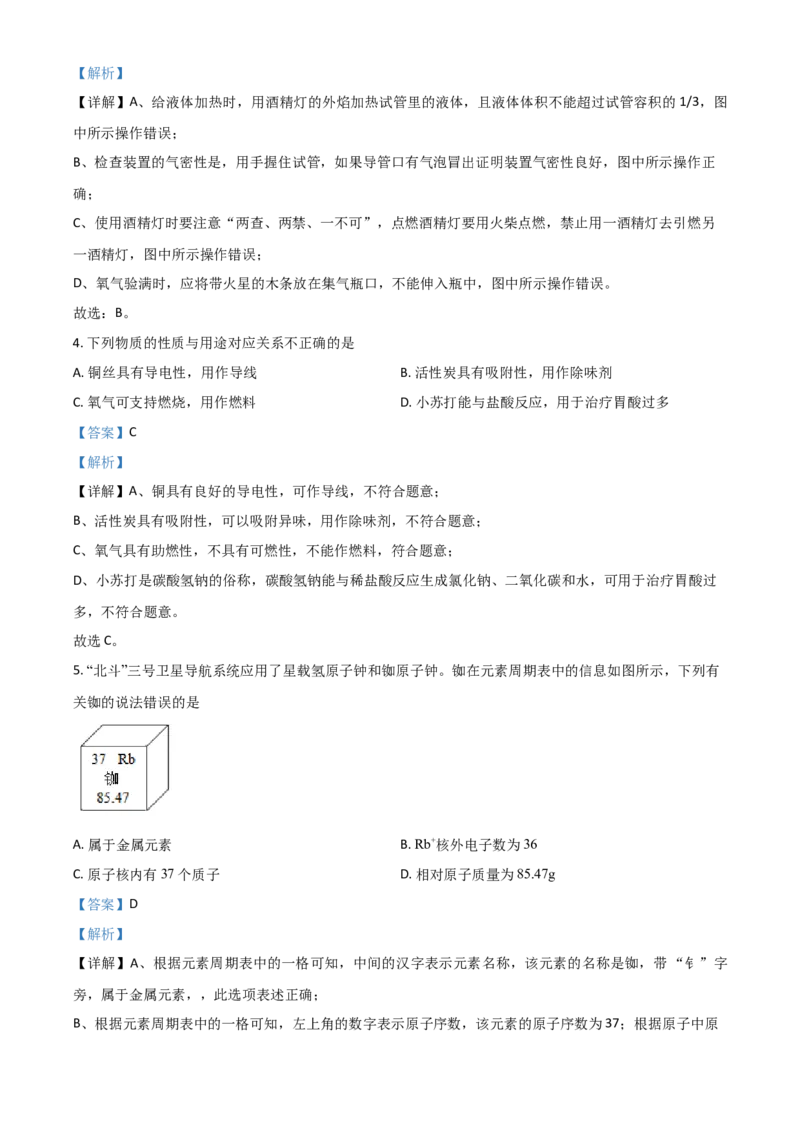
3. 下列实验操作正确的是
A. 加热液体 B. 检查气密性
C. 点燃酒精灯 D. 氧气验满
【答案】B【解析】
【详解】A、给液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的1/3,图
中所示操作错误;
B、检查装置的气密性是,用手握住试管,如果导管口有气泡冒出证明装置气密性良好,图中所示操作正
确;
C、使用酒精灯时要注意“两查、两禁、一不可”,点燃酒精灯要用火柴点燃,禁止用一酒精灯去引燃另
一酒精灯,图中所示操作错误;
D、氧气验满时,应将带火星的木条放在集气瓶口,不能伸入瓶中,图中所示操作错误。
故选:B。
4. 下列物质的性质与用途对应关系不正确的是
A. 铜丝具有导电性,用作导线 B. 活性炭具有吸附性,用作除味剂
C. 氧气可支持燃烧,用作燃料 D. 小苏打能与盐酸反应,用于治疗胃酸过多
【答案】C
【解析】
【详解】A、铜具有良好的导电性,可作导线,不符合题意;
B、活性炭具有吸附性,可以吸附异味,用作除味剂,不符合题意;
C、氧气具有助燃性,不具有可燃性,不能作燃料,符合题意;
D、小苏打是碳酸氢钠的俗称,碳酸氢钠能与稀盐酸反应生成氯化钠、二氧化碳和水,可用于治疗胃酸过
多,不符合题意。
故选C。
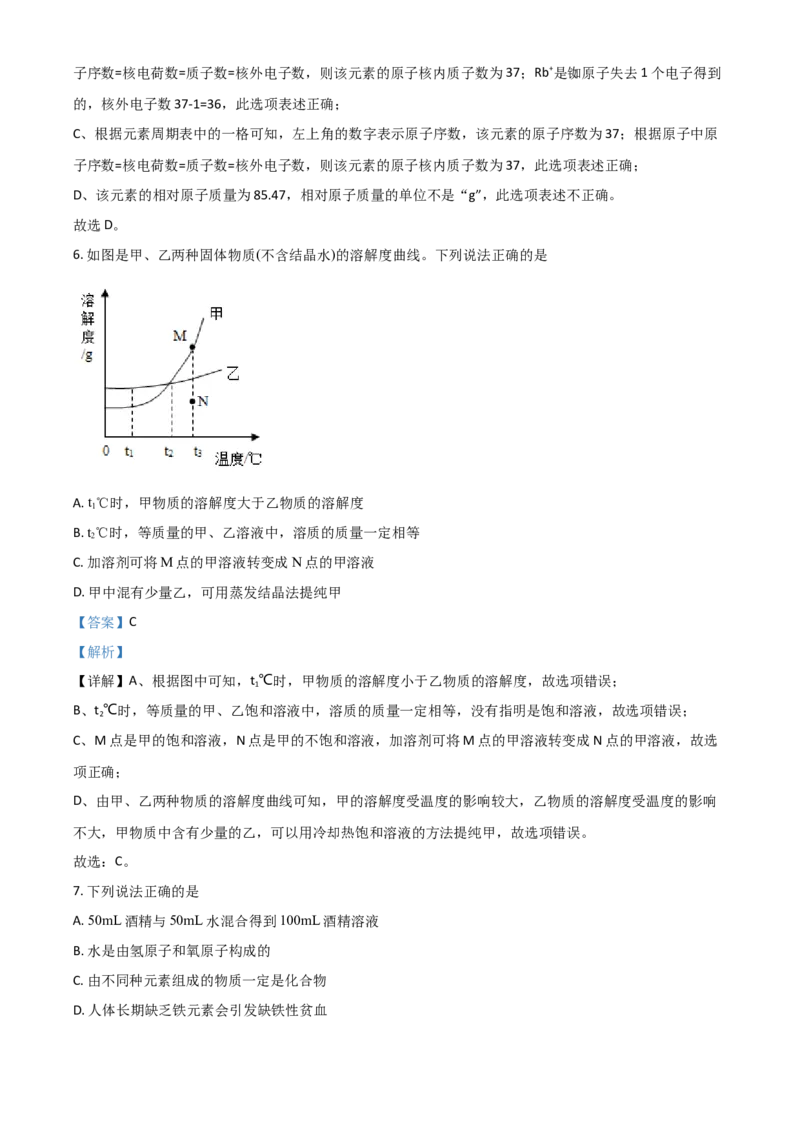
5. “北斗”三号卫星导航系统应用了星载氢原子钟和铷原子钟。铷在元素周期表中的信息如图所示,下列有
关铷的说法错误的是
A. 属于金属元素 B. Rb+核外电子数为36
C. 原子核内有37个质子 D. 相对原子质量为85.47g
【答案】D
【解析】
【详解】A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是铷,带“钅”字
旁,属于金属元素,,此选项表述正确;
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为37;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为37;Rb+是铷原子失去1个电子得到
的,核外电子数37-1=36,此选项表述正确;
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为37;根据原子中原
子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为37,此选项表述正确;
D、该元素的相对原子质量为85.47,相对原子质量的单位不是“g”,此选项表述不正确。
故选D。
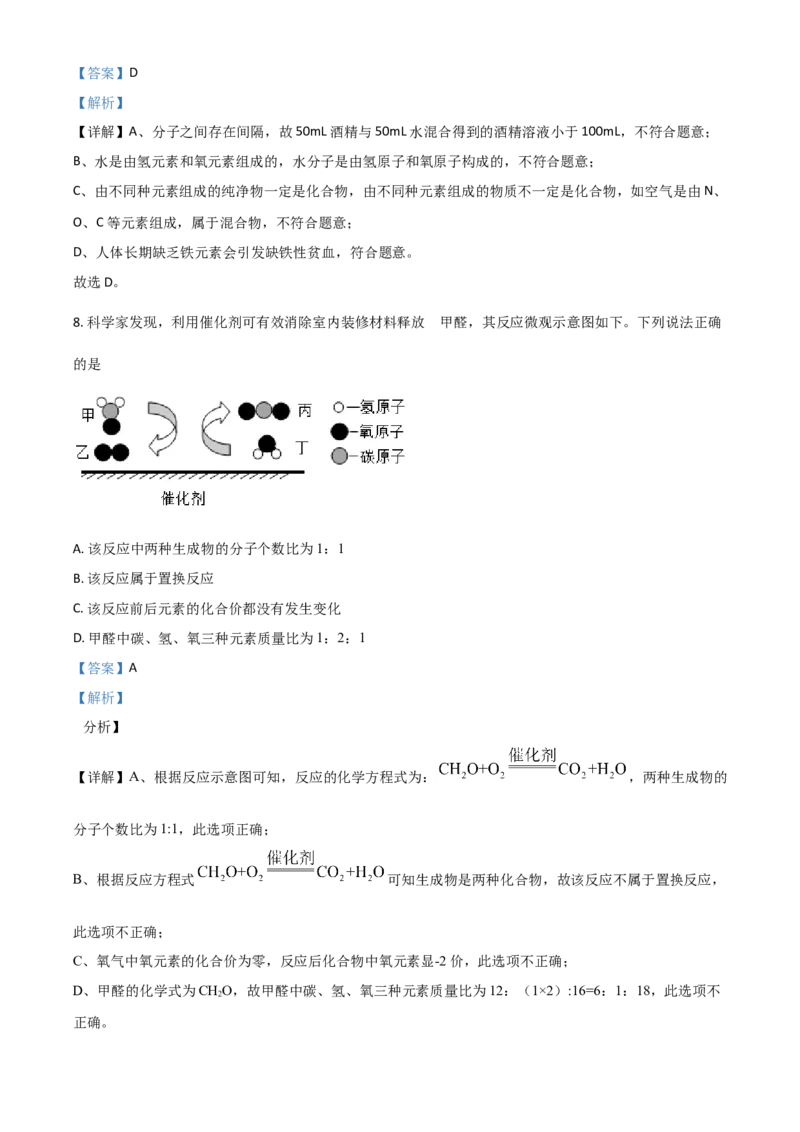
6. 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线。下列说法正确的是
A. t℃时,甲物质的溶解度大于乙物质的溶解度
1
B. t℃时,等质量的甲、乙溶液中,溶质的质量一定相等
2
C. 加溶剂可将M点的甲溶液转变成N点的甲溶液
D. 甲中混有少量乙,可用蒸发结晶法提纯甲
【答案】C
【解析】
【详解】A、根据图中可知,t ℃时,甲物质的溶解度小于乙物质的溶解度,故选项错误;
1
B、t ℃时,等质量的甲、乙饱和溶液中,溶质的质量一定相等,没有指明是饱和溶液,故选项错误;
2
C、M点是甲的饱和溶液,N点是甲的不饱和溶液,加溶剂可将M点的甲溶液转变成N点的甲溶液,故选
项正确;
D、由甲、乙两种物质的溶解度曲线可知,甲的溶解度受温度的影响较大,乙物质的溶解度受温度的影响
不大,甲物质中含有少量的乙,可以用冷却热饱和溶液的方法提纯甲,故选项错误。
故选:C。
7. 下列说法正确的是
A. 50mL酒精与50mL水混合得到100mL酒精溶液
B. 水是由氢原子和氧原子构成的
C. 由不同种元素组成的物质一定是化合物
D. 人体长期缺乏铁元素会引发缺铁性贫血【答案】D
【解析】
【详解】A、分子之间存在间隔,故50mL酒精与50mL水混合得到的酒精溶液小于100mL,不符合题意;
B、水是由氢元素和氧元素组成的,水分子是由氢原子和氧原子构成的,不符合题意;
C、由不同种元素组成的纯净物一定是化合物,由不同种元素组成的物质不一定是化合物,如空气是由N、
O、C等元素组成,属于混合物,不符合题意;
D、人体长期缺乏铁元素会引发缺铁性贫血,符合题意。
故选D。
的
8. 科学家发现,利用催化剂可有效消除室内装修材料释放 甲醛,其反应微观示意图如下。下列说法正确
的是
A. 该反应中两种生成物的分子个数比为1:1
B. 该反应属于置换反应
C. 该反应前后元素的化合价都没有发生变化
D. 甲醛中碳、氢、氧三种元素质量比为1:2:1
【答案】A
【解析】
【分析】
【详解】A、根据反应示意图可知,反应的化学方程式为: ,两种生成物的
分子个数比为1:1,此选项正确;
B、根据反应方程式 可知生成物是两种化合物,故该反应不属于置换反应,
此选项不正确;
C、氧气中氧元素的化合价为零,反应后化合物中氧元素显-2价,此选项不正确;
D、甲醛的化学式为CHO,故甲醛中碳、氢、氧三种元素质量比为12:(1×2):16=6:1:18,此选项不
2
正确。故选A。
9. 将X、Z两种金属分别放入Y(NO) 的溶液中,仅X的表面有Y单质析出,则X、Y、Z三种金属的活动
3 2
性顺序是
A. Z>X>Y B. X>Y>Z C. X>Z>Y D. Y>X>Z
【答案】B
【解析】
【详解】将X、Z两种金属分别放入Y(NO ) 的溶液中,仅X的表面有Y单质析出,说明X能将Y从其盐溶液
3 2
中置换出来,X比Y活泼,Z与Y(NO ) 不反应,说明Y比Z活泼,故三种金属的活动性顺序是:X>Y>Z。
3 2
故选B。
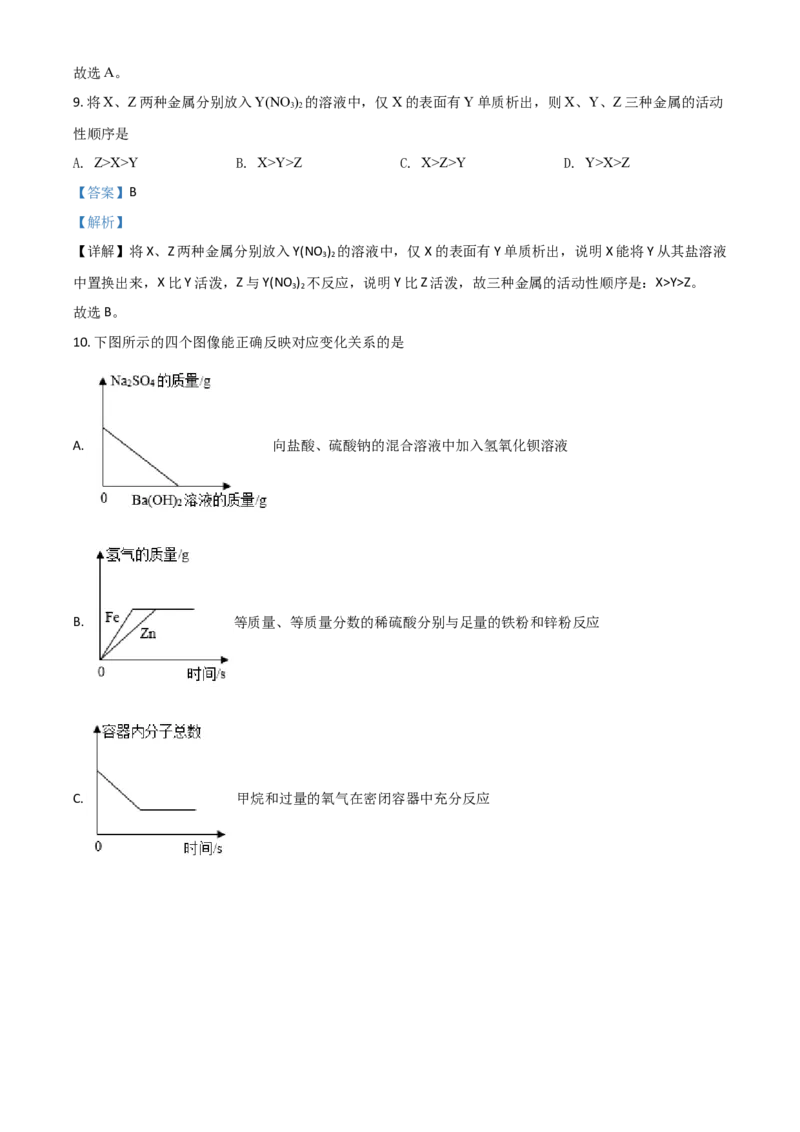
10. 下图所示的四个图像能正确反映对应变化关系的是
A. 向盐酸、硫酸钠的混合溶液中加入氢氧化钡溶液
B. 等质量、等质量分数的稀硫酸分别与足量的铁粉和锌粉反应
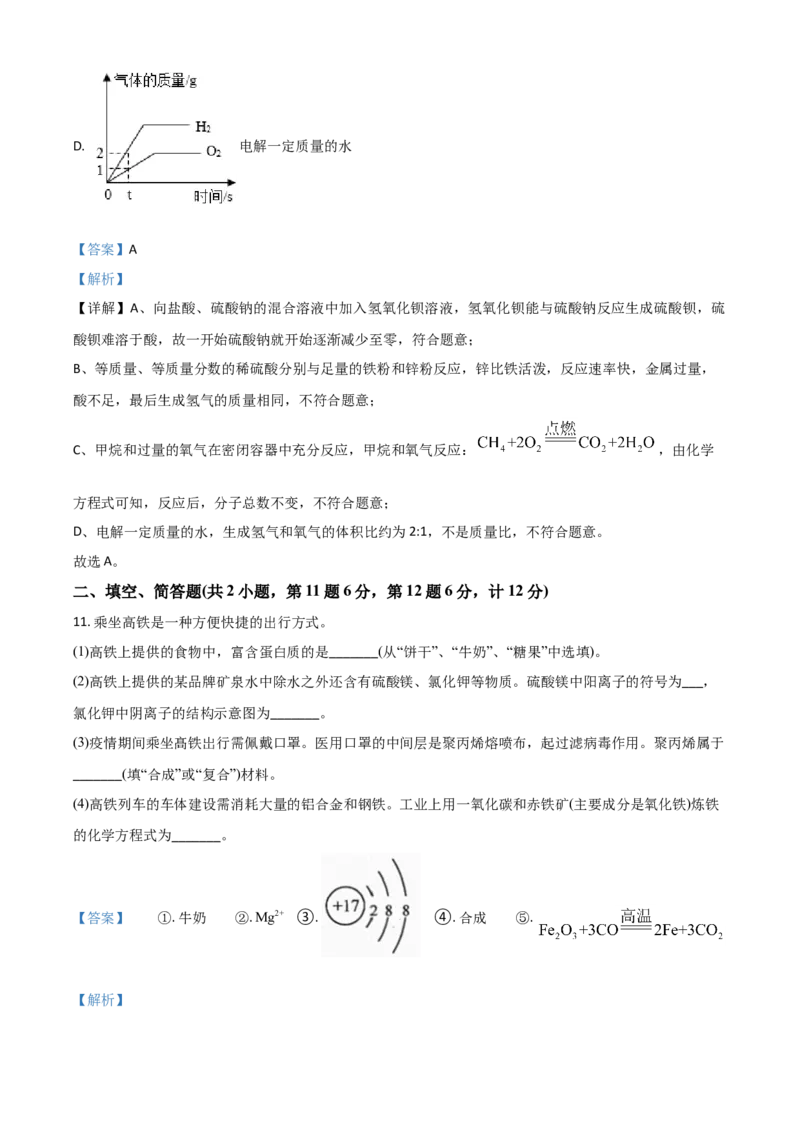
C. 甲烷和过量的氧气在密闭容器中充分反应D. 电解一定质量的水
【答案】A
【解析】
【详解】A、向盐酸、硫酸钠的混合溶液中加入氢氧化钡溶液,氢氧化钡能与硫酸钠反应生成硫酸钡,硫
酸钡难溶于酸,故一开始硫酸钠就开始逐渐减少至零,符合题意;
B、等质量、等质量分数的稀硫酸分别与足量的铁粉和锌粉反应,锌比铁活泼,反应速率快,金属过量,
酸不足,最后生成氢气的质量相同,不符合题意;
C、甲烷和过量的氧气在密闭容器中充分反应,甲烷和氧气反应: ,由化学
方程式可知,反应后,分子总数不变,不符合题意;
D、电解一定质量的水,生成氢气和氧气的体积比约为2:1,不是质量比,不符合题意。
故选A。
二、填空、简答题(共2小题,第11题6分,第12题6分,计12分)
11. 乘坐高铁是一种方便快捷的出行方式。
(1)高铁上提供的食物中,富含蛋白质的是_______(从“饼干”、“牛奶”、“糖果”中选填)。
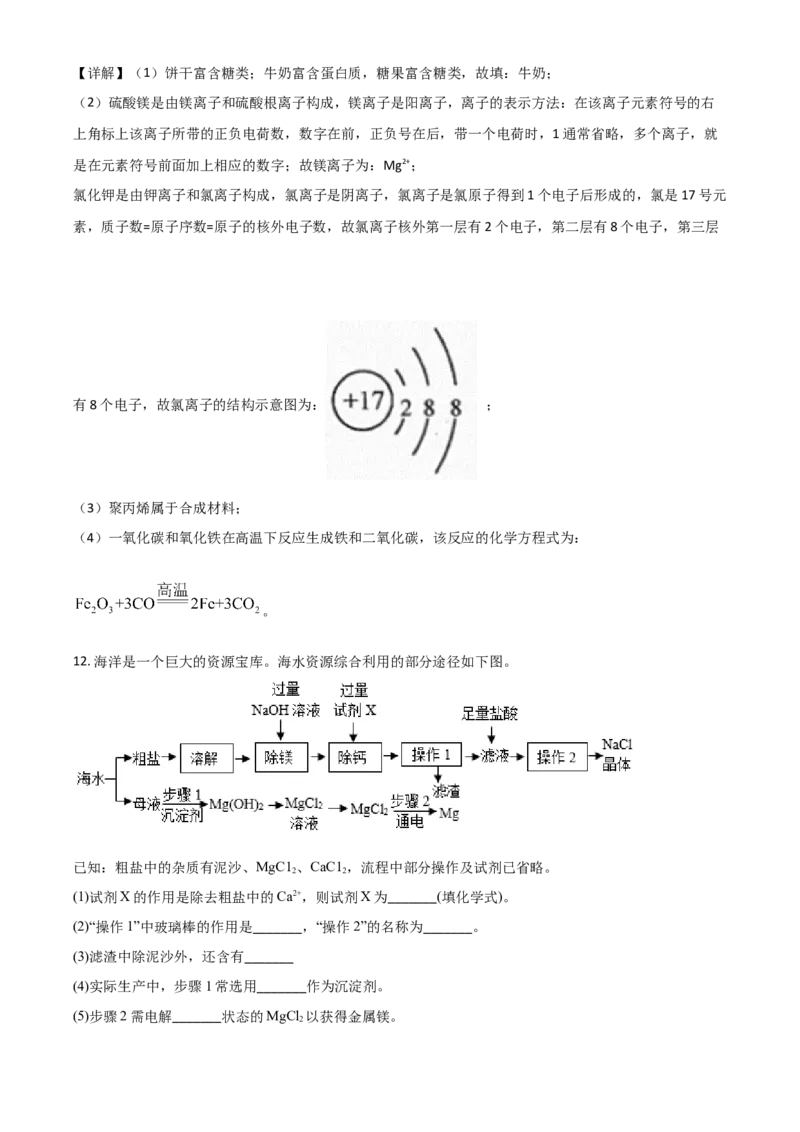
(2)高铁上提供的某品牌矿泉水中除水之外还含有硫酸镁、氯化钾等物质。硫酸镁中阳离子的符号为___,
氯化钾中阴离子的结构示意图为_______。
(3)疫情期间乘坐髙铁岀行需佩戴口罩。医用口罩的中间层是聚丙烯熔喷布,起过滤病毒作用。聚丙烯属于
_______(填“合成”或“复合”)材料。
(4)高铁列车的车体建设需消耗大量的铝合金和钢铁。工业上用一氧化碳和赤铁矿(主要成分是氧化铁)炼铁
的化学方程式为_______。
【答案】 ①. 牛奶 ②. Mg2+ ③. ④. 合成 ⑤.
【解析】【详解】(1)饼干富含糖类;牛奶富含蛋白质,糖果富含糖类,故填:牛奶;
(2)硫酸镁是由镁离子和硫酸根离子构成,镁离子是阳离子,离子的表示方法:在该离子元素符号的右
上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就
是在元素符号前面加上相应的数字;故镁离子为:Mg2+;
氯化钾是由钾离子和氯离子构成,氯离子是阴离子,氯离子是氯原子得到1个电子后形成的,氯是17号元
素,质子数=原子序数=原子的核外电子数,故氯离子核外第一层有2个电子,第二层有8个电子,第三层
有8个电子,故氯离子的结构示意图为: ;
(3)聚丙烯属于合成材料;
(4)一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:
。
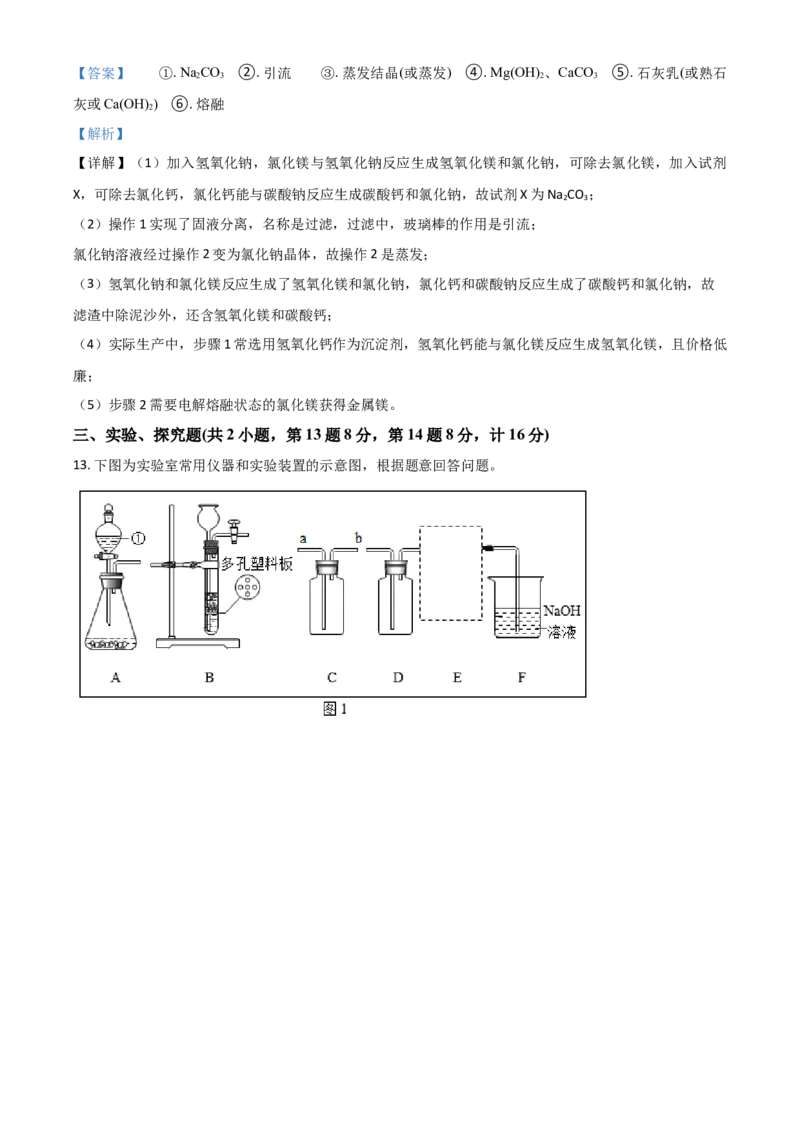
12. 海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如下图。
已知:粗盐中的杂质有泥沙、MgC1 、CaC1 ,流程中部分操作及试剂已省略。
2 2
(1)试剂X的作用是除去粗盐中的Ca2+,则试剂X为_______(填化学式)。
(2)“操作1”中玻璃棒的作用是_______,“操作2”的名称为_______。
。
(3)滤渣中除泥沙外,还含有_______
(4)实际生产中,步骤1常选用_______作为沉淀剂。
(5)步骤2需电解_______状态的MgCl 以获得金属镁。
2【答案】 ①. NaCO ②. 引流 ③. 蒸发结晶(或蒸发) ④. Mg(OH) 、CaCO ⑤. 石灰乳(或熟石
2 3 2 3
灰或Ca(OH) ) ⑥. 熔融
2
【解析】
【详解】(1)加入氢氧化钠,氯化镁与氢氧化钠反应生成氢氧化镁和氯化钠,可除去氯化镁,加入试剂
X,可除去氯化钙,氯化钙能与碳酸钠反应生成碳酸钙和氯化钠,故试剂X为Na CO ;
2 3
(2)操作1实现了固液分离,名称是过滤,过滤中,玻璃棒的作用是引流;
氯化钠溶液经过操作2变为氯化钠晶体,故操作2是蒸发;
(3)氢氧化钠和氯化镁反应生成了氢氧化镁和氯化钠,氯化钙和碳酸钠反应生成了碳酸钙和氯化钠,故
滤渣中除泥沙外,还含氢氧化镁和碳酸钙;
(4)实际生产中,步骤1常选用氢氧化钙作为沉淀剂,氢氧化钙能与氯化镁反应生成氢氧化镁,且价格低
廉;
(5)步骤2需要电解熔融状态的氯化镁获得金属镁。
三、实验、探究题(共2小题,第13题8分,第14题8分,计16分)
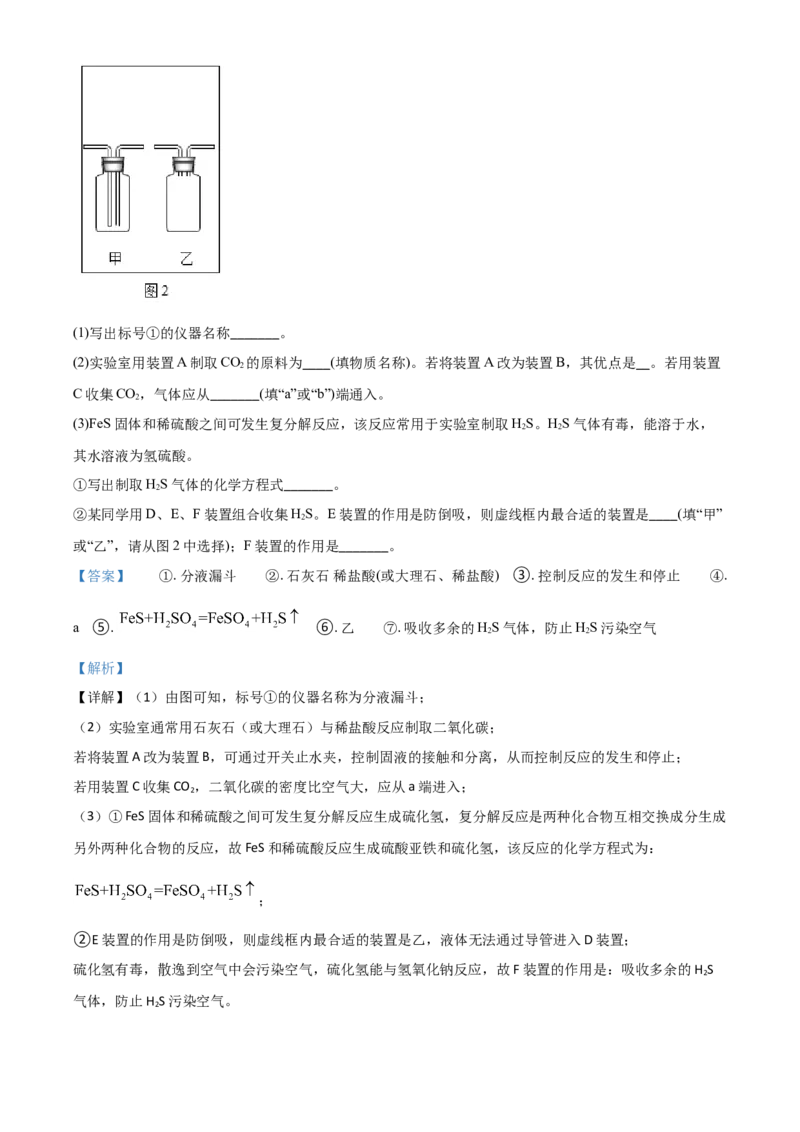
13. 下图为实验室常用仪器和实验装置的示意图,根据题意回答问题。(1)写出标号①的仪器名称_______。
(2)实验室用装置A制取CO 的原料为____(填物质名称)。若将装置A改为装置B,其优点是__。若用装置
2
C收集CO,气体应从_______(填“a”或“b”)端通入。
2
(3)FeS固体和稀硫酸之间可发生复分解反应,该反应常用于实验室制取HS。HS气体有毒,能溶于水,
2 2
其水溶液为氢硫酸。
①写出制取HS气体的化学方程式_______。
2
②某同学用D、E、F装置组合收集HS。E装置的作用是防倒吸,则虚线框内最合适的装置是____(填“甲”
2
或“乙”,请从图2中选择);F装置的作用是_______。
【答案】 ①. 分液漏斗 ②. 石灰石 稀盐酸(或大理石、稀盐酸) ③. 控制反应的发生和停止 ④.
a ⑤. ⑥. 乙 ⑦. 吸收多余的HS气体,防止HS污染空气
2 2
【解析】
【详解】(1)由图可知,标号①的仪器名称为分液漏斗;
(2)实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳;
若将装置A改为装置B,可通过开关止水夹,控制固液的接触和分离,从而控制反应的发生和停止;
若用装置C收集CO ,二氧化碳的密度比空气大,应从a端进入;
2
(3)①FeS固体和稀硫酸之间可发生复分解反应生成硫化氢,复分解反应是两种化合物互相交换成分生成
另外两种化合物的反应,故FeS和稀硫酸反应生成硫酸亚铁和硫化氢,该反应的化学方程式为:
;
②E装置的作用是防倒吸,则虚线框内最合适的装置是乙,液体无法通过导管进入D装置;
硫化氢有毒,散逸到空气中会污染空气,硫化氢能与氢氧化钠反应,故F装置的作用是:吸收多余的H S
2
气体,防止H S污染空气。
214. 某化学课堂围绕“酸碱中和反应”,将学生分成若干个小组展开探究。以下是教学片断,请你参加学习并
填写空格。
【演示实验】将一定质量的稀盐酸加入盛有NaOH溶液的小烧杯中。
【提出问题】实验中未观察到明显现象,某同学提出疑问:反应后溶液中溶质是什么?
【猜憲与假设】针对疑问,大家纷纷提岀猜想。甲组同学的猜想如下,请补上猜想二、
猜想一:只有NaCl 猜想二:_______
猜想三:NaC1和HC1 猜想四:NaC1、NaOH和HC1
乙组同学认为有一种猜想不合理,不合理的猜想是_______,理由是_______。
【实验探究】
(1)丙组同学取烧杯中的溶液少许于试管中,滴加几滴CuCl 溶液,_______(填实验现象),证明溶液中一定
2
没有NaOH。
(2)为了验证其余猜想,各学习小组利用浇杯中的溶液,并选用了老师提供的pH试纸、KCO 溶液、AgNO
2 3 3
溶液,进行如下三个方案的探究。
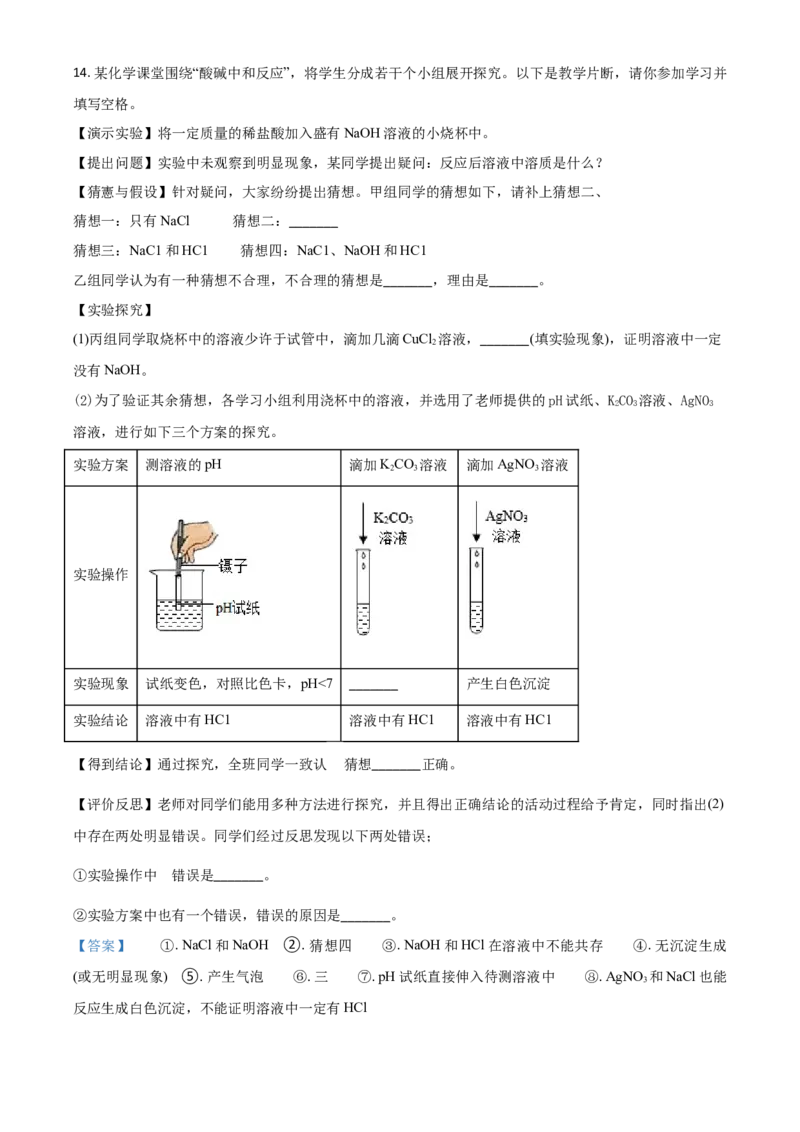
实验方案 测溶液的pH 滴加KCO 溶液 滴加AgNO 溶液
2 3 3
实验操作
实验现象 试纸变色,对照比色卡,pH<7 _______ 产生白色沉淀
实验结论 溶液中有HC1 溶液中有HC1 溶液中有HC1
为
【得到结论】通过探究,全班同学一致认 猜想_______正确。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论的活动过程给予肯定,同时指出(2)
中存在两处明显错误。同学们经过反思发现以下两处错误;
的
①实验操作中 错误是_______。
②实验方案中也有一个错误,错误的原因是_______。
【答案】 ①. NaCl和NaOH ②. 猜想四 ③. NaOH和HCl在溶液中不能共存 ④. 无沉淀生成
(或无明显现象) ⑤. 产生气泡 ⑥. 三 ⑦. pH试纸直接伸入待测溶液中 ⑧. AgNO 和NaCl也能
3
反应生成白色沉淀,不能证明溶液中一定有HCl【解析】
【详解】猜想与假设:氢氧化钠和稀盐酸反应生成氯化钠和水,如果恰好完全反应,则溶质为:NaCl,如
果氢氧化钠过量,则溶质为:NaOH、NaCl,如果稀盐酸过量,则溶质为:NaCl、HCl,故猜想二:NaCl、
NaOH;
猜想四不合理,因为氢氧化钠能与盐酸反应生成氯化钠和水,不能共存;
实验探究:(1)氯化铜能与氢氧化钠反应生成氢氧化铜和氯化钠,故滴入氯化铜溶液,无明显现象,说
明不含氢氧化钠;
(2)结论为:溶液中有HCl,碳酸钾能与盐酸反应生成氯化钾、二氧化碳和水,现象为:产生气泡;
得到结论:溶液pH<7,加入碳酸钾,产生气泡,说明溶液中含HCl,故溶质为:NaCl、HCl,故猜想三成
立;
评价反思:①测定溶液的pH值,应用洁净、干燥的玻璃棒蘸取待测液点在pH试纸上,观察颜色的变化,
然后与标准比色卡对照,不能直接伸入待测液中,故操作中的错误是:pH试纸直接伸入待测溶液中;
②硝酸银和氯化钠、氯化氢均能反应生成氯化银,故产生白色沉淀,不能说明溶液中一定含有HCl。
四、推理、计算题(共2小题,第15题6分,第16题6分,计12分)
15. 有一包白色固体混合物,可能由NaCl、CuSO 、NaCO、NaSO 、BaCl 、NaOH中的一种或几种组成,
4 2 3 2 4 2
为确定其组成,兴趣小组同学进行下列实验:
(1)取少量固体溶于足量的水过滤得到白色固体A和无色滤液B,则原固体中一定不含有_______。
(2)向白色固体A中加入足量的稀盐酸,固体全部溶解,且有气泡生成,则原固体中一定有_______,一定
不含有_______。
(3)小红同学取少量滤液B,滴加无色酚酞试液,溶液变红,她认为原固体中一定含有NaOH。你同意小红
的观点吗?_______(填“是”或“否”)。
(4)小雪同学另取一份滤液B,加入足量的BaCl 溶液,观察到有白色沉淀生成,再向上层清液中滴加无色
2
酚酞试液,溶液变红,则原固体中一定含有_______。
(5)以上实验不能确定的物质是_______。
【答案】 ①. CuSO ②. NaCO、BaCl ③. NaSO ④. 否 ⑤. NaOH ⑥. NaCl
4 2 3 2 2 4
【解析】
【详解】(1)取少量固体溶于足量的水过滤得到白色固体 A和无色滤液B,则原固体中一定不含有
CuSO ,因为硫酸铜溶液是蓝色的,且形成蓝色沉淀;
4
(2)向白色固体A中加入足量的稀盐酸,固体全部溶解,且有气泡生成,故白色固体A为氯化钡和碳酸
钠反应生成的碳酸钡,原固体中一定含有BaCl 、Na CO ,一定不含Na SO ,因为硫酸钠与氯化钡反应生成
2 2 3 2 4
的硫酸钡不溶于酸;
(3)取少量滤液B,滴加无色酚酞试液,溶液变红,不一定含氢氧化钠,因为溶液中可能含碳酸钠,碳酸钠显碱性,也能使无色酚酞试液变红,故填:否;
(4)另取一份滤液B,加入足量的BaCl 溶液,观察到有白色沉淀生成,说明滤液B中含碳酸钠,碳酸钠
2
和氯化钡反应生成碳酸钡和氯化钠,且能将碳酸钠除尽,再向上层清液中滴加无色酚酞试液,溶液变红,
说明滤液B中含氢氧化钠,原固体中一定含NaOH;
(5)以上实验,无法确定是否含NaCl,没有关于氯化钠的验证。
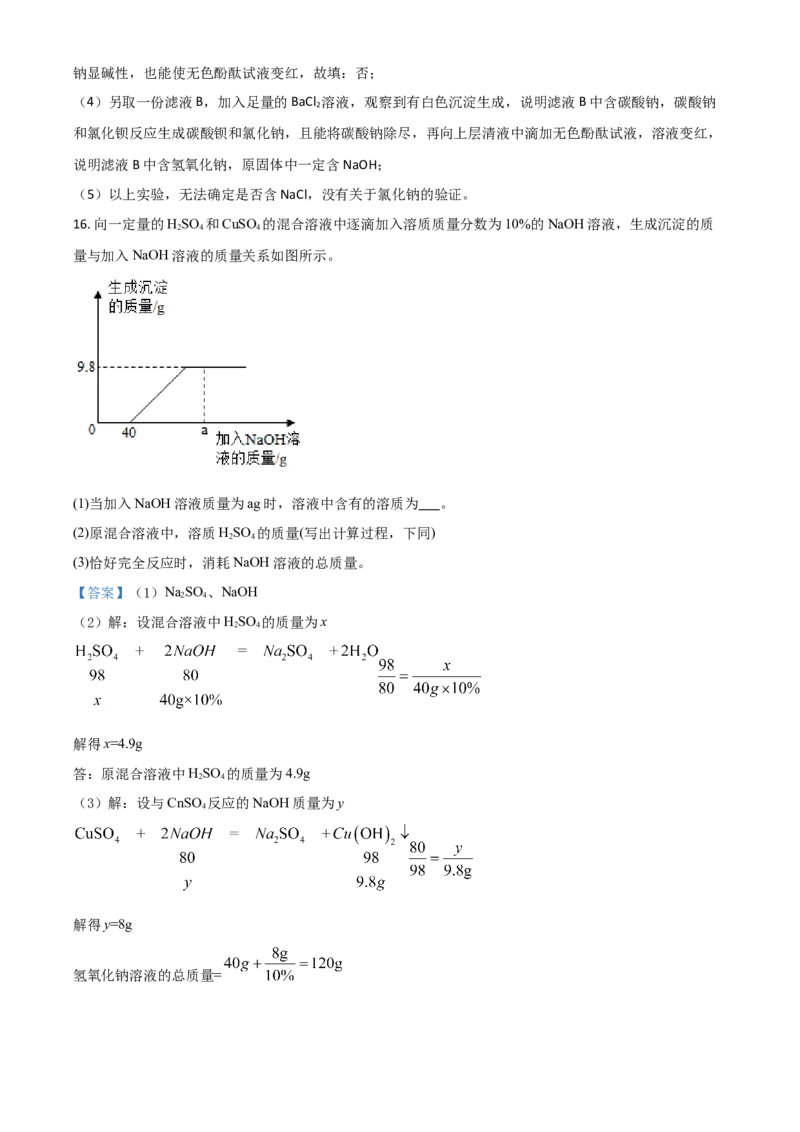
16. 向一定量的HSO 和CuSO 的混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质
2 4 4
量与加入NaOH溶液的质量关系如图所示。
(1)当加入NaOH溶液质量为ag时,溶液中含有的溶质为 。
(2)原混合溶液中,溶质HSO 的质量(写出计算过程,下同)
2 4
(3)恰好完全反应时,消耗NaOH溶液的总质量。
【答案】(1)NaSO 、NaOH
2 4
(2)解:设混合溶液中HSO 的质量为x
2 4
解得x=4.9g
答:原混合溶液中HSO 的质量为4.9g
2 4
(3)解:设与CnSO 反应的NaOH质量为y
4
解得y=8g
氢氧化钠溶液的总质量=答:恰好完全反应时,消耗NaOH溶液的质量为120g。
【解析】
【详解】(1)氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,
所以反应后溶液中的溶质一定含有氯化钠,a点时氢氧化钠过量,所以溶质中还含有氢氧化钠,故填:
Na SO 、NaOH;
2 4
(2)见答案;
(3)见答案。