文档内容
荆州市2015年中考化学试题
(满分:60分 考试时间:50分钟)
可能要用到的相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5
一、单项选择题(本大题包括12个小题,共24分)
1、以下过程属于化学变化的是(▲)
A.水蒸气凝结 B.钢铁生锈 C.酒精挥发 D.干冰升华
2、下列物质中,属于纯净物的是(▲)
A.洁净的空气 B.纯净的食盐水 C.pH= 7的溶液 D.四氧化三铁
3、在下列类型的化学反应中,各元素的化合价一定不会发生变化的是(▲)
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
4、原子核中一定含有的粒子是(▲)
A.中子 B.质子 C.电子 D.质子和中子
5、日常生活里常见的下列饮品中,可能不含有机物的是(▲)
A.果汁 B.牛奶 C.矿泉水 D.啤酒
6、下面所列各项中,与元素的化学性质的关系最为密切的是(▲)
A.元素的相对原子质量 B.元素的核电荷数
C.原子的核外电子数 D.原子的最外层电子数
7、在化学反应前后,以下各项一定不会发生变化的是(▲)
① 原子种类 ② 元素种类 ③ 分子种类 ④ 物质种类
A.①② B.①③ C.②③ D.②④
8、下列叙述正确的是(▲)
A.化学反应过程中都会放热 B.只有产生燃烧的化学反应才会放热
C.化学反应都伴随着能量变化 D.能量都是由化学反应产生的
9、将X、Y、Z三种金属单质分别放入盐酸中,仅Y的表面有气泡产生;再将它们分别
放入XCl 溶液中,又仅Y的表面有X单质析出。则这三种金属的活动性顺序是(▲)
m
A.X﹥Y﹥Z B.Y﹥X﹥Z C.Y﹥Z﹥X D.Z﹥Y﹥X
10、小明设计了下列四组物质,要求在一定条件下都能一步转化,其中错误的是(▲)
A.NaCO→NaCl→NaNO→NaOH B.C→CO→CO→NaCO
2 3 3 2 2 3
C.Cu→CuO→CuSO→Cu(OH) D.CaCO→CaO→Ca(OH) →NaOH
4 2 3 2
11、为了除去粗盐中的Ca2+、Mg2+、SO2-等离子,可将粗盐溶于水后进行如下操作:
4
① 加入适量盐酸, ② 加过量NaOH溶液, ③ 加过量NaCO 溶液,
2 3
④ 加过量BaCl 溶液, ⑤ 过滤。下列操作顺序合理的是(▲)
2
A.②③④⑤① B.②④③⑤① C.④②③①⑤ D.④③②①⑤
12、如图所示,处于连线两端的物质,在一定的条件下都能发生化学反应的物质组别是(▲)
甲 乙 丙 丁
甲 乙
A C O HSO CuO
2 2 4
B Fe HSO CuCl NaOH
2 4 2
C NaOH CO KOH CuCl
2 2 丙 丁
1D NaSO Ba(OH) HCl Ba(NO)
2 4 2 3 2
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案
五、填空题(本大题包括4个小题,共18分)
37、(4分)请根据题意和要求回答下列问题。
(1)实验室可用排水法收集氢气的原因是 。
(2)糖类、 、油脂、维生素、无机盐和水,常被称为人体的六大基本营养素。
(3)生石灰常用作食品干燥剂,其原理用化学方程式表示为 。
(4)在NHNO、KSO、KHPO、Ca(HPO) 四种化肥中,属于复合肥料的是 。
4 3 2 4 2 4 2 4 2
38、(4分)某粒子的结构示意图为 (其中n≠0),请回答下列问题。
+m 2 8 n
(1)n的最大值为 。
(2)若该粒子带两个单位的负电 荷,则其对应的化学符号为 ;由+6价
的该元素
形成的常见酸的化学式为 。
(3)若m – n =10,则该粒子对应的常见金属元素有 (写元素符号)。
39、(5分)有一种固体混合物质M,其中只可能含有Na CO 、NaNO 、Na SO 、
2 3 3 2 4
CuCl 、 BaCl 中的一种或几种。请根据以下实验操作回答下列问题。
2 2
操作① 取少量M放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤。
操作② 向滤出的沉淀中加入足量稀盐酸,沉淀全部溶解,此时所得溶液仍为无色。
(1)M中一定不含的物质是 ,不能确定是否含有的物质是 。
(2)上述实验过程中,发生反应的化学方程式为 、
。
(3)向操作①后所得的无色溶液中滴加溶液AgNO 溶液,一定能发生的反应的化学
3
方程式为 。
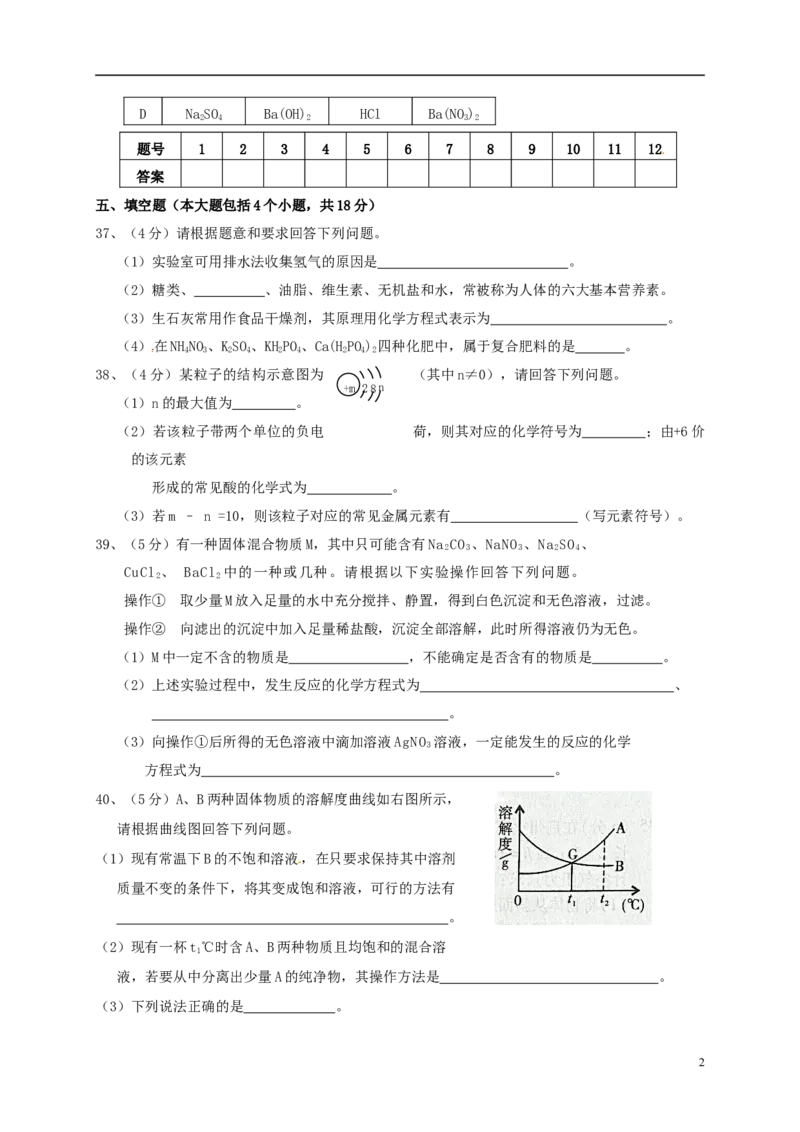
40、(5分)A、B两种固体物质的溶解度曲线如右图所示,
请根据曲线图回答下列问题。
(1)现有常温下B的不饱和溶液,在只要求保持其中溶剂
质量不变的条件下,将其变成饱和溶液,可行的方法有
。
(2)现有一杯t℃时含A、B两种物质且均饱和的混合溶
1
液,若要从中分离出少量A的纯净物,其操作方法是 。
(3)下列说法正确的是 。
2① t℃时,A的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
2
② 将t℃,A、B的饱和溶液分别降温至t℃,此时两溶液中的质量分数相等;
2 1
③ 在t℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等;
1
④ 在t℃时,用等量的A、B分别配制成两种饱和溶液,测得其质量依次为m g
2 1
和mg,则m < m。
2 1 2
六、实验题(本大题包括2个小题,共12分)
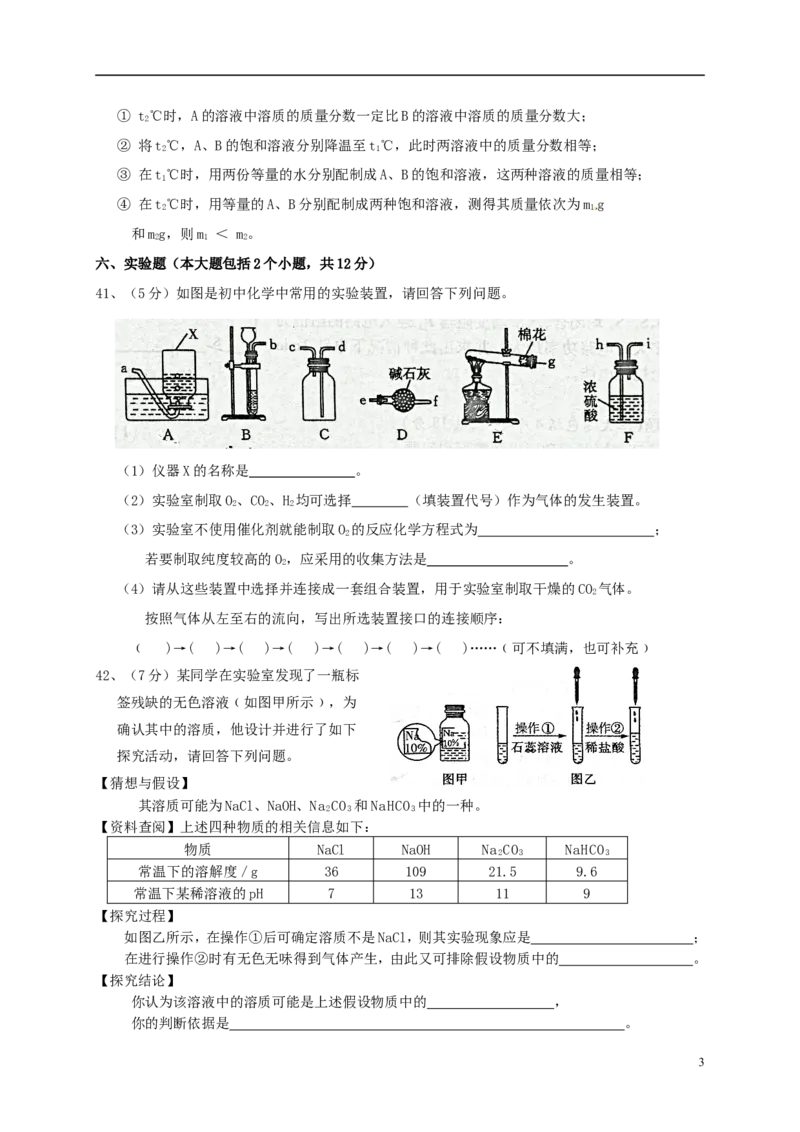
41、(5分)如图是初中化学中常用的实验装置,请回答下列问题。
(1)仪器X的名称是 。
(2)实验室制取O、CO、H 均可选择 (填装置代号)作为气体的发生装置。
2 2 2
(3)实验室不使用催化剂就能制取O 的反应化学方程式为 ;
2
若要制取纯度较高的O,应采用的收集方法是 。
2
(4)请从这些装置中选择并连接成一套组合装置,用于实验室制取干燥的CO 气体。
2
按照气体从左至右的流向,写出所选装置接口的连接顺序:
﹙ )→( )→( )→( )→( )→( )→( )……﹙可不填满,也可补充﹚
42、(7分)某同学在实验室发现了一瓶标
签残缺的无色溶液﹙如图甲所示﹚,为
确认其中的溶质,他设计并进行了如下
探究活动,请回答下列问题。
【猜想与假设】
其溶质可能为NaCl、NaOH、Na CO 和NaHCO 中的一种。
2 3 3
【资料查阅】上述四种物质的相关信息如下:
物质 NaCl NaOH Na CO NaHCO
2 3 3
常温下的溶解度/g 36 109 21.5 9.6
常温下某稀溶液的pH 7 13 11 9
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,
你的判断依据是 。
3【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),
实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na SO ,但又没有Na SO 的上述表列信息。
2 4 2 4
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na SO ,并叙述理由:
2 4
七、实验题(本大题包括1个小题,共6分)
43、(6分)如图是某胃药标签的部分内容。小明同学 胃舒乐
测定该药品中NaHCO 含量的过程如下:取10粒
3 主要成分: 碳酸氢钠
该药剂研碎后放入烧杯中,加入50克水后充分搅拌,
主 治: 胃酸过多
再向其中滴加稀盐酸至溶液的pH=7时(已知药品
每瓶50粒 每粒0.5克
中的其它成分既不溶于水,也不与稀盐酸反应),
形成NaCl的不饱和溶液,共消耗稀盐酸11.5克。
称得反应后烧杯内物质的总质量为64.3克。
请计算:(1)反应完成后生成气体的质量为 g。
(2)反应后烧杯中溶液的质量和胃药中NaHCO 的质量分数。
3
湖北省荆州市2015年中考化学答案
一、选择题(共12小题,每小题2分,满分24分)
1.B
2.D
3.D
4.B
5.C
6.D
7.A
8、C
9.B
10.A
11.B
12.C
二、填空题(本大题包括4个小题,共18分)
37.请根据题意和要求回答下列问题.
(1)实验室可用排水法收集氢气的原因是 氢气难溶于水 .
(2)糖类、 蛋白质 、油脂、维生素、无机盐和水,常被称为人体的六大基本营养素.
(3)生石灰常用作食品干燥剂,其原理用化学方程式表示为 CaO+ H O═C a ( O H ) .
2 2
(4)在NHNO、KSO、KHPO、Ca(HPO) 四种化肥中,属于复合肥料的是 K HPO .
4 3 2 4 2 4 2 4 2 2 4
38.某粒子的结构示意图为 (其中n≠0),请回答下列问题.
(1)n的最大值为 8 .
4(2)若该粒子带两个单位的负电荷,则其对应的化学符号为 S 2﹣ ;由+6价的该元素形成的常见酸
的化学式为 HSO .
2 4
(3)若m﹣n=10,则该粒子对应的常见金属元素有 N a 、 M g 、 A l (写元素符号).
39.有一种固体混合物质M,其中只可能含有NaCO、NaNO、NaSO、CuCl、BaCl 中的一种或几种.请根
2 3 3 2 4 2 2
据以下实验操作回答下列问题.
操作①取少量M放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤.操作②向滤出的
沉淀中加入足量稀盐酸,沉淀全部溶解,此时所得溶液仍为无色.
(1)M中一定不含的物质是 氯化铜、硫酸钠 ,不能确定是否含有的物质是 硝酸钠 .
(2)上述实验过程中,发生反应的化学方程式为 N aCO+BaCl=BaCO ↓+2NaC l 、
2 3 2 3
BaCO+2HCl=BaCl+HO+CO ↑ .
3 2 2 2
(3)向操作①后所得的无色溶液中滴加溶液AgNO 溶液,一定能发生的反应的化学方程式为
3
NaCl+AgNO=NaNO +AgCl↓ .
3 3
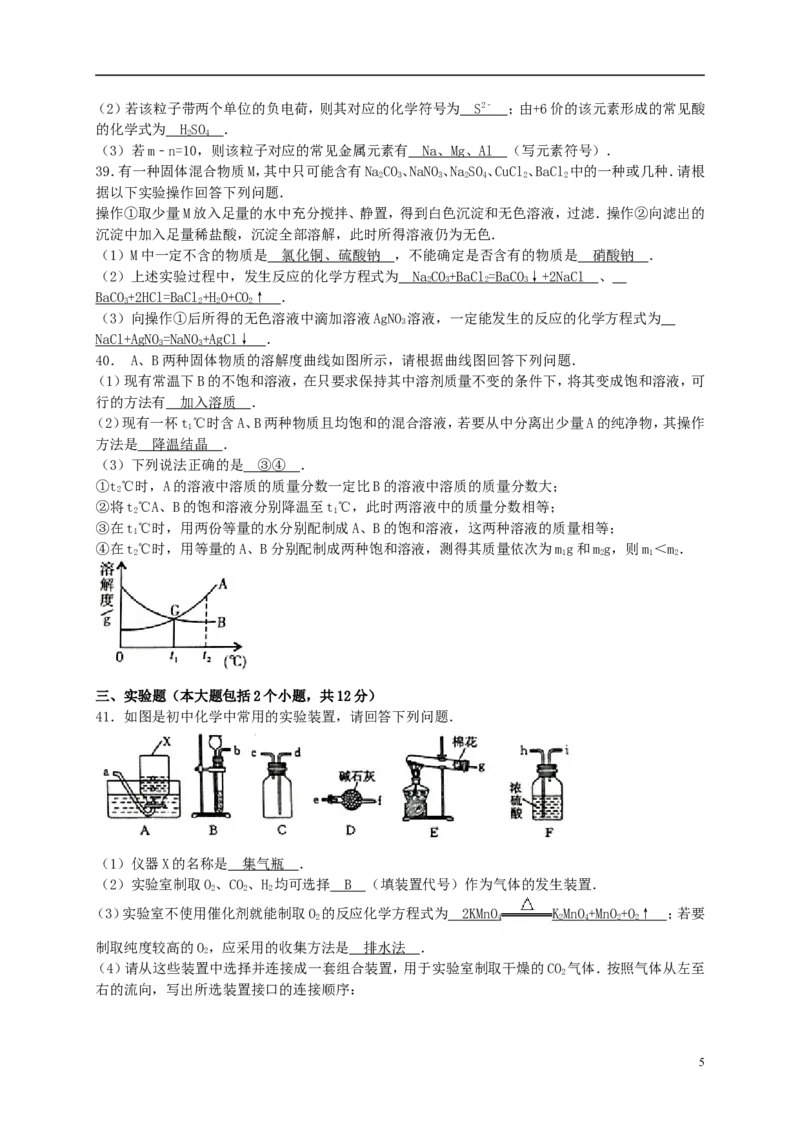
40. A、B两种固体物质的溶解度曲线如图所示,请根据曲线图回答下列问题.
(1)现有常温下B的不饱和溶液,在只要求保持其中溶剂质量不变的条件下,将其变成饱和溶液,可
行的方法有 加入溶质 .
(2)现有一杯t℃时含A、B两种物质且均饱和的混合溶液,若要从中分离出少量A的纯净物,其操作
1
方法是 降温结晶 .
(3)下列说法正确的是 ③④ .
①t℃时,A的溶液中溶质的质量分数一定比B的溶液中溶质的质量分数大;
2
②将t℃A、B的饱和溶液分别降温至t℃,此时两溶液中的质量分数相等;
2 1
③在t℃时,用两份等量的水分别配制成A、B的饱和溶液,这两种溶液的质量相等;
1
④在t℃时,用等量的A、B分别配制成两种饱和溶液,测得其质量依次为mg和mg,则m<m.
2 1 2 1 2
三、实验题(本大题包括2个小题,共12分)
41.如图是初中化学中常用的实验装置,请回答下列问题.
(1)仪器X的名称是 集气瓶 .
(2)实验室制取O、CO、H 均可选择 B (填装置代号)作为气体的发生装置.
2 2 2
(3)实验室不使用催化剂就能制取O 的反应化学方程式为 2KMn O KMnO+MnO+O ↑ ;若要
2 4 2 4 2 2
制取纯度较高的O,应采用的收集方法是 排水法 .
2
(4)请从这些装置中选择并连接成一套组合装置,用于实验室制取干燥的CO 气体.按照气体从左至
2
右的流向,写出所选装置接口的连接顺序:
5﹙ b ﹚→﹙ h ﹚→﹙ i ﹚→﹙ d ﹚→﹙ c ﹚→﹙ 0 ﹚→﹙ 0 ﹚…﹙可不填
满,也可补充﹚
42.某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并
进行了如下
探究活动,请回答下列问题.
【猜想与假设】溶质可能为NaCl、NaOH、NaCO 和NaHCO 中的一种.
2 3 3
【资料查阅】上述四种物质的相关信息如下:
物质 NaCl NaOH NaCO NaHCO
2 3 3
常温下的溶解度/g 36 109 21.5 9.6
常温下某稀溶液的pH 7 13 11 9
【探究过程】如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 石蕊试液变成蓝色
;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的 氢氧化钠 .
【探究结论】你认为该溶液中的溶质可能是上述假设物质中的 碳酸钠 ,你的判断依据是 碳酸氢
钠饱和溶液的质量分数不可能达到 10 % ,而碳酸钠溶液可以 .
【探究反思】(1)若上述探究结论是正确的,操作②产生的气体应是 C O (写化学式),实验室检验
2
该气体的实验操作及现象是 将气体通入石灰水,石灰水变浑浊 .
(2)另有同学猜想其中的溶质还可能是NaSO,但又没有NaSO 的上述表列信息.请你根据以上实验
2 4 2 4
操作的相关现象,判断该溶液中的溶质是否是NaSO,并叙述理由: 若滴加石蕊试液变成蓝色,则不
2 4
含有硫酸钠 .
四、计算题(共1小题,共6分)
43.(6分)(2015•荆州)如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO 含量的过程如
3
下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7
时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐
酸11.5克.称得反应后烧杯内物质的总质量为64.3克.
请计算:
(1)反应完成后生成气体的质量为 2.2 g .
(2)反应后烧杯中溶液的质量和胃药中NaHCO 的质量分数.
3
解:(1)每粒0.5g,10粒该药剂的质量为0.5g×10=5g.
由质量守恒定律,生成二氧化碳气体的质量为5g+50g+11.5g﹣64.3g=2.2g.
(2)设参加反应的碳酸氢钠的质量为x,
NaHCO+HCl=NaCl+HO+CO↑
3 2 2
84 44
6x 2.2g
x=4.2g
反应后烧杯中溶液的质量为4.2g+50g+11.5g﹣2.2g=63.5g.
胃药中NaHCO 的质量分数为 ×100%=84%.
3
答:(1)2.2g;(2)反应后烧杯中溶液的质量为63.5g;胃药中NaHCO 的质量分数为84%.
3
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧
化碳的质量是正确解答本题的前提和关键.
7