文档内容
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 P-31 S-32 Ca-40 Ba-137
一、选择题(本大题包括14小题,每小题2分,共28分)
1. 根据日常经验和你所学的化学知识,判断下列变化不属于化学变化的是( )
A.酿制甜酒 B.煤炭燃烧 C.瓷器破碎 D.钢铁生锈
【答案】C
考点:化学变化和物理变化的判断
2.一些食物的近似pH如下,其中显碱性的是( )
A.鸡蛋清7.6~8.0 B.牛奶 6.3~6.6
C.葡萄汁 3.5~4.5 D.苹果汁 2.9~3.3
【答案】A
【解析】
试题分析:溶液PH>7,呈碱性;PH<7,呈酸性;PH=7,呈中性。故选A。
考点:酸碱度
3.在化学实验室内外一般不会张贴的标志是( )
A.禁止烟火 B.当心爆炸 C.剧毒 D.禁止拍照
【答案】D
【解析】
试题分析:ABC中均与化学有关。故选D。
考点:常见标识的识别
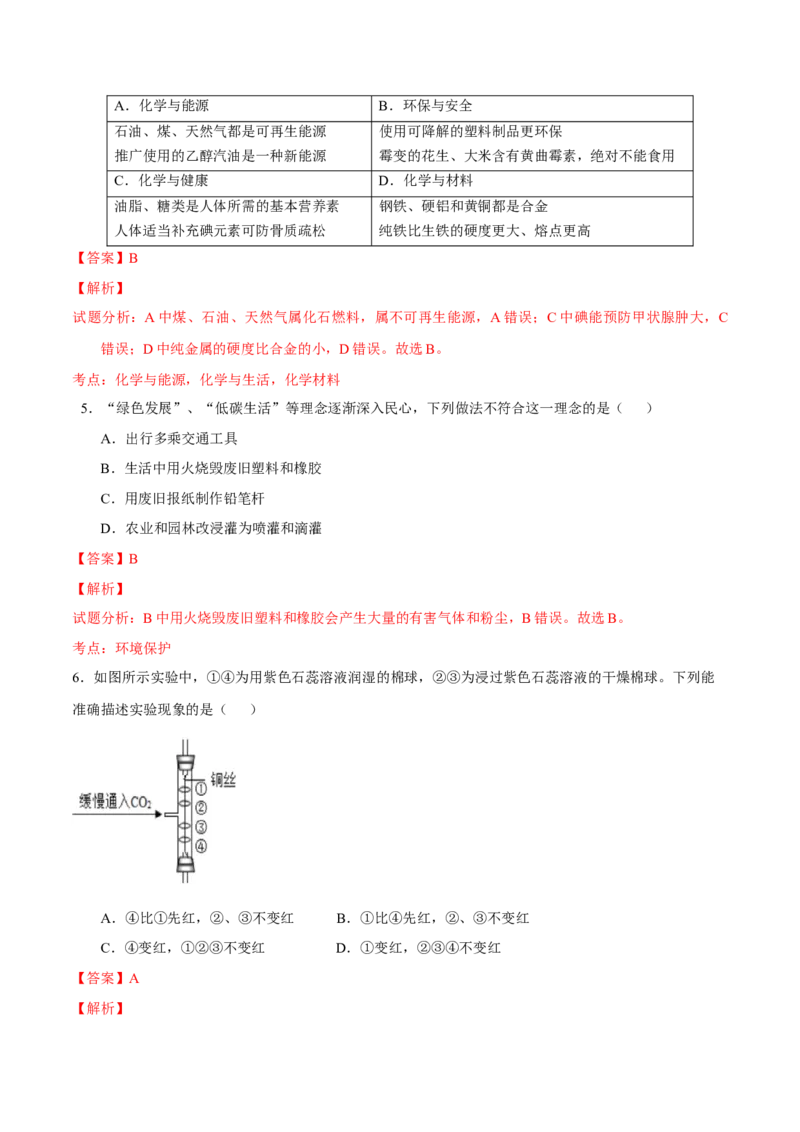
4. 下表中对部分知识的归纳正确的一组是( )A.化学与能源 B.环保与安全
石油、煤、天然气都是可再生能源 使用可降解的塑料制品更环保
推广使用的乙醇汽油是一种新能源 霉变的花生、大米含有黄曲霉素,绝对不能食用
C.化学与健康 D.化学与材料
油脂、糖类是人体所需的基本营养素 钢铁、硬铝和黄铜都是合金
人体适当补充碘元素可防骨质疏松 纯铁比生铁的硬度更大、熔点更高
【答案】B
【解析】
试题分析:A中煤、石油、天然气属化石燃料,属不可再生能源,A错误;C中碘能预防甲状腺肿大,C
错误;D中纯金属的硬度比合金的小,D错误。故选B。
考点:化学与能源,化学与生活,化学材料
[5.“绿色发展”、“低碳生活”等理念逐渐深入民心,下列做法不符合这一理念的是( )
A.出行多乘交通工具
B.生活中用火烧毁废旧塑料和橡胶
C.用废旧报纸制作铅笔杆
D.农业和园林改浸灌为喷灌和滴灌
【答案】B
【解析】
试题分析:B中用火烧毁废旧塑料和橡胶会产生大量的有害气体和粉尘,B错误。故选B。
考点:环境保护
6.如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能
准确描述实验现象的是( )
A.④比①先红,②、③不变红 B.①比④先红,②、③不变红
C.④变红,①②③不变红 D.①变红,②③④不变红
【答案】A
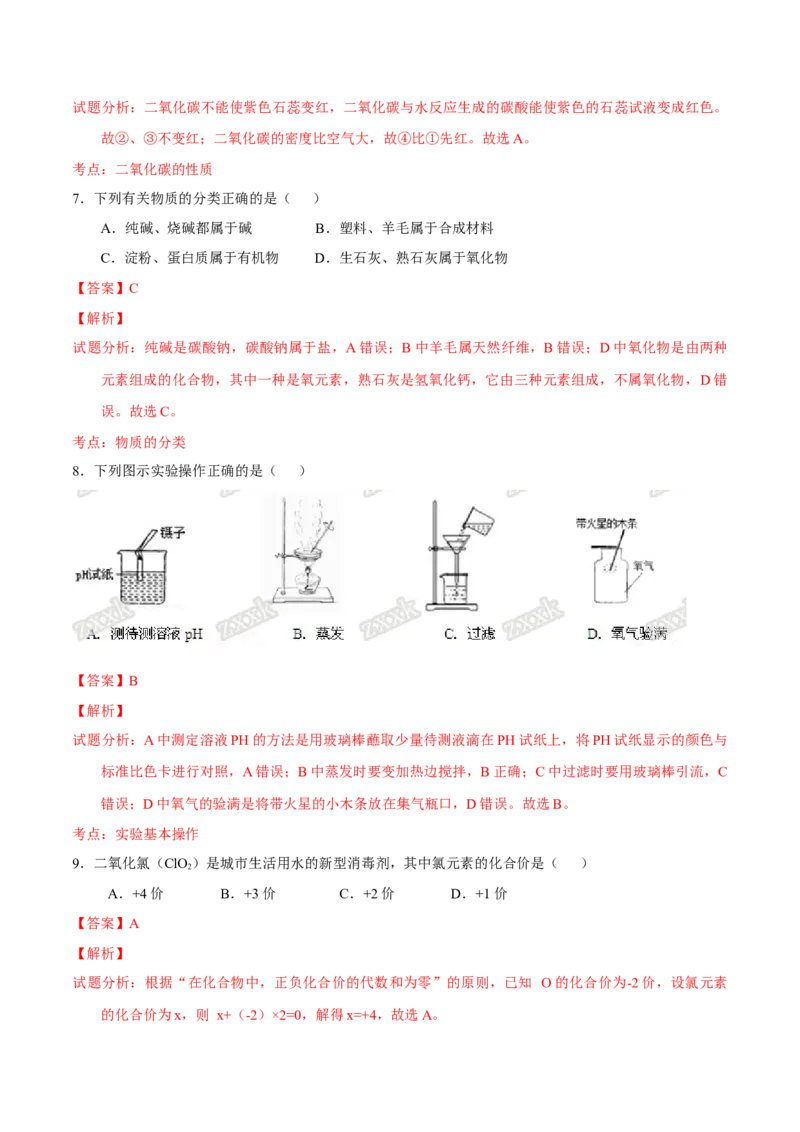
【解析】试题分析:二氧化碳不能使紫色石蕊变红,二氧化碳与水反应生成的碳酸能使紫色的石蕊试液变成红色。
故②、③不变红;二氧化碳的密度比空气大,故④比①先红。故选A。
考点:二氧化碳的性质
7.下列有关物质的分类正确的是( )
A.纯碱、烧碱都属于碱 B.塑料、羊毛属于合成材料
C.淀粉、蛋白质属于有机物 D.生石灰、熟石灰属于氧化物
【答案】C
【解析】
试题分析:纯碱是碳酸钠,碳酸钠属于盐,A错误;B中羊毛属天然纤维,B错误;D中氧化物是由两种
元素组成的化合物,其中一种是氧元素,熟石灰是氢氧化钙,它由三种元素组成,不属氧化物,D错
误。故选C。
考点:物质的分类
8.下列图示实验操作正确的是( )
【答案】B
【解析】
试题分析:A中测定溶液PH的方法是用玻璃棒蘸取少量待测液滴在PH试纸上,将PH试纸显示的颜色与
标准比色卡进行对照,A错误;B中蒸发时要变加热边搅拌,B正确;C中过滤时要用玻璃棒引流,C
错误;D中氧气的验满是将带火星的小木条放在集气瓶口,D错误。故选B。
考点:实验基本操作
9.二氧化氯(ClO )是城市生活用水的新型消毒剂,其中氯元素的化合价是( )
2
A.+4价 B.+3价 C.+2价 D.+1价
【答案】A
【解析】
试题分析:根据“在化合物中,正负化合价的代数和为零”的原则,已知 O的化合价为-2价,设氯元素
的化合价为x,则 x+(-2)×2=0,解得x=+4,故选A。考点:有关元素化合价的计算
10.下表除去物质中所含少量杂质的方法错误的是( )
物质 杂质 除去杂质的方法
A. NaCl 泥沙 溶解、过滤、蒸发
B. N O 通过灼热的铜网
2 2
C. NaOH溶液 NaCO 加入稀盐酸至不再产生气泡
2 3
D. CO CO 先通过足量的氢氧化钠溶液,在通过浓硫酸
2
【答案】C
考点:除杂质
11.水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )
A.水通电分解时产生的氢气和氧气质量比为2:1
B.活性炭吸附水中的色素和异味是化学变化
C.可用肥皂水区分硬水和软水
D.用过滤的方法可以使硬水软化
【答案】C
【解析】
试题分析:电解水实验中与正极产生的是氧气,用带火星的小木条检验,负极产生的是氢气,可用燃烧法
检验,正负两极气体的体积比为1:2 ,质量比为8:1,A错误;活性炭具有疏松多孔的结构,能吸附颜
色和异味,具有吸附性,属物理性质,B错误;鉴别硬水和软水用到的是肥皂水,产生大量泡沫的是
软水,泡沫较少的是硬水,C正确;D中过滤只能除去难溶性杂质,硬水软化的方法有蒸馏和煮沸,
D错误。故选C。
考点:水
12.下图为三种物质的溶解度曲线。下列说法错误的是( )A.约在64℃时KCl和NaSO 的溶解度相等
2 4
B.在室温至100℃区间,随温度升高,NaSO 的溶解度先增大后减小,醋酸钙则相反
2 4
C.分离含少量KCl的溶液,采用先蒸发浓缩,后降温结晶的方法
D.在40℃时,40gKCl固体溶于60g水得到40%KCl溶液
【答案】D
D错误。故选D。
考点:溶解度曲线
13.公园里部分植物的枝叶枯黄,茎也比较纤细。建议工作人员最好给这些植物施用的一种化肥是(
)
A.NH HCO B.KNO C.Ca(HPO ) D.(NH )PO
4 3 3 2 4 2 4 3 4
【答案】B
【解析】
试题分析:植物所需大量的N、P、K三种元素,其中氮元素作用与植物的叶,P作用于植物的根,K作用
于植物的茎。植物的枝叶枯黄,茎也比较纤细,故要施用含有N和K的复合肥。故选B。
考点:化学肥料
14.下图是表示在9.8g 10%的稀HSO 中逐滴滴入10%的Ba(OH) 溶液的变化过程。下列说法正确的是(
2 4 2
)A.X是时间,Y是pH
B.X是水的总质量,Y是HSO 的质量
2 4
C.X是加入Ba(OH) 溶液的质量,Y是沉淀物质的质量
2
D.X是加入Ba(OH) 溶液的质量,Y是溶液中溶质的质量
2
【答案】D
【解析】
试题分析:稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水。反应的过程中溶液的酸性逐渐减弱,PH变大,
恰
考点:化学反应与图像
二、填空题(本大题包括5小题,共21分)
15.(4分)钒被誉为“合金中的维生素”。钒元素的部分信息如图所示。请回答下列问题:
(1)钒原子的质子数为___________,x=___________。
(2)钒属于___________(填“金属”或“非金属”)元素;钒的相对原子质量为___________。
【答案】(1)23 , 2 (2) 金属 , 50.94
【解析】试题分析:(1)在原子中,质子数=核电荷数=核外电子数=原子序数,故钒原子的质子数为 23,x=23-
21=2;
(2)由元素的名称可知,钒属于金属元素;元素名称下面的数字表示的是相对原子质量,故钒的相对原
子质量为50.94 。
考点:原子的结构,元素周期表的应用
16.(4分)下图是某反应的微观示意图。
请回答:
(1)B框中的物质属于___________(填序号:①化合物、②单质、③纯净物、④混合物)。
(2)此反应的化学方程式为_____________________________,此图说明化学反应前后发生改变的微
粒是_________。
【答案】(1)② (2)2HS+3O 2SO +2H O ,分子
2 2 2 2
考点:化学反应的微观过程
17.(4分)查阅资料可知,米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C HOH)和氧气发生反
2 5
应生成了醋酸(CHCOOH)和另一种常见的液体。回答下列问题:
3
(1)食物变质是一种___________氧化反应(填“剧烈”、“缓慢”)。
(2)米酒味道变酸的化学反应方程式为______________________;可用___________验证米酒味道变
酸却是生成了醋酸。
【答案】(1)缓慢 (2) C HOH+O CHCOOH+H O 加入石蕊溶液变红
2 5 2 3 2
【解析】试题分析:(1)食物变质发生的是缓慢氧化,缓慢氧化发生的很慢,不易被察觉;
(2)米酒变酸发生的是缓慢氧化,即是与氧气发生反应。反应的化学方程式表示为:C HOH+O
2 5 2
CHCOOH+H O;醋酸属于酸,酸能使紫色的石蕊试液变成红色。
3 2
考点:缓慢氧化,化学方程式的书写
18.(5分)请根据下图回答问题:
① 关闭阀门 ② 浇水 ③加水 ④火焰飞溅
(1)图①和②两种灭火方式的原理分别是:①___________,②___________。
(2)图③是往燃烧的油锅里加水,结果不但没有熄灭锅里的水,还造成图④的后果,其原因是:
______________________,______________________,使燃烧更猛烈;正确熄灭油锅里火焰的方法是
___________。
【答案】(1)①(阻断)隔离可燃物 ② 使温度降低到着火点以下
(2)水的密度比油大下沉 ,水的沸点比油低导致暴沸,油滴飞溅出来在空气中剧烈燃烧; 盖上锅
盖(加大量青菜)
【解析】
考点:灭火的方法
19.(4分)实验室根据工业炼铁的原理设计了如图所示装置进行实验。请回答:(1)主要成分为氧化铁的矿石名称为___________;
图中还原氧化铁的化学方程式为:______________________
(2)“加热”和“通气”(通入CO)的操作顺序是______________________。
【答案】(1)赤铁矿 ;3CO+Fe O 2Fe+3CO
2 3 2
(2)通气 加热
考点:实验室炼铁
三、(本大题包括2小题,共15分)
20.(6分)初中化学常见物质A-I分别是下列物质中的一种:锌、氢氧化钠、硫酸铜溶液、稀盐酸、碳
酸钠溶液、石灰水、生石灰、石灰石和水。他们之间相互的反应(每种物质只能用一次)恰好包含了化合
反应(A+B)、分解反应(C)、置换反应(D+E)、中和反应(F+G)、复分解反应(H+I)等反应类型。
试回答下列问题:
(1)A+B的反应化学方程式是______________________
(2)C的化学式为___________;硫酸铜溶液参加___________反应(填反应类型)。
(3)H+I的反应方程式是_________________________________
【答案】(1)CaO+H O =Ca(OH)
2 2
(2)CaCO ;置换
3
(3)NaCO+Ca(OH) =CaCO +2NaOH
2 3 2 3
【解析】
试题分析:根据给出的物质可知氧化钙与水反应生成氢氧化钙,该反应属化合反应;碳酸钙在高温条件发
生分解反应生成氧化钙和二氧化碳;锌与硫酸铜反应生成铜和硫酸锌,发生的是置换反应;稀盐酸与
氢氧化钠反应生成氯化钠和水,属中和反应;碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,属复分解反应。
考点:化学反应类型,物质的推断
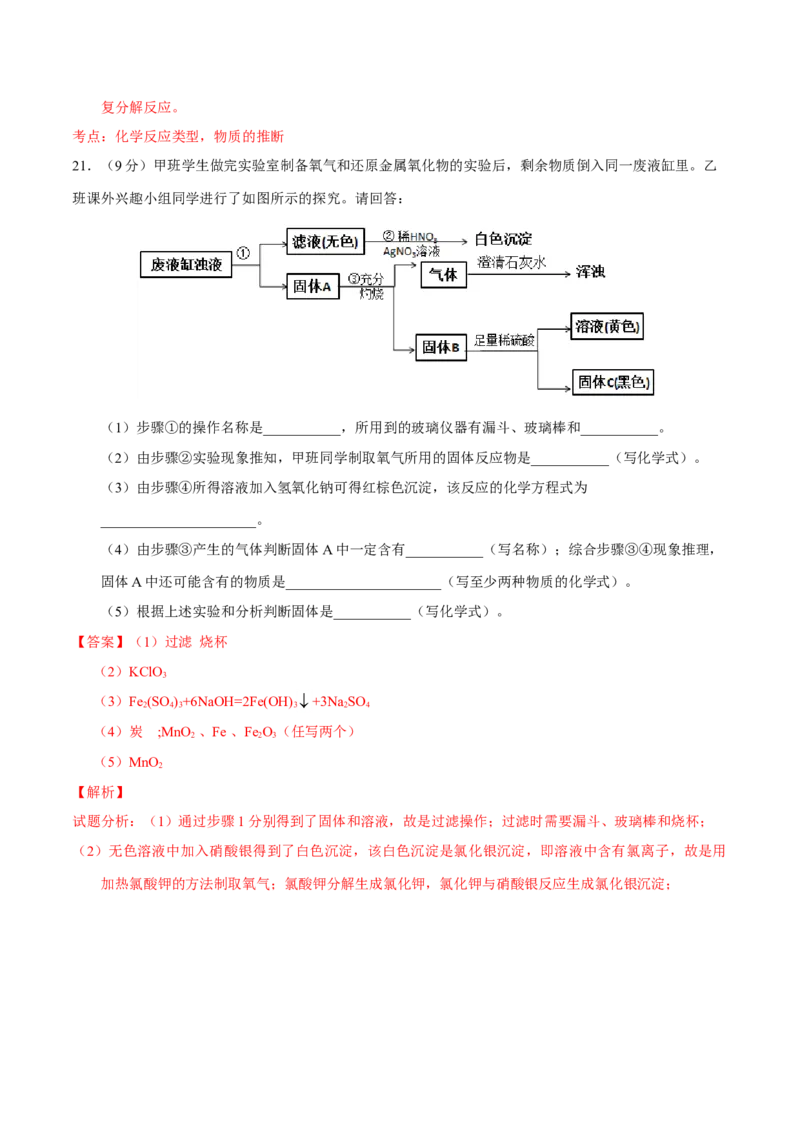
21.(9分)甲班学生做完实验室制备氧气和还原金属氧化物的实验后,剩余物质倒入同一废液缸里。乙
班课外兴趣小组同学进行了如图所示的探究。请回答:
(1)步骤①的操作名称是___________,所用到的玻璃仪器有漏斗、玻璃棒和___________。
(2)由步骤②实验现象推知,甲班同学制取氧气所用的固体反应物是___________(写化学式)。
(3)由步骤④所得溶液加入氢氧化钠可得红棕色沉淀,该反应的化学方程式为
______________________。
(4)由步骤③产生的气体判断固体A中一定含有___________(写名称);综合步骤③④现象推理,
固体A中还可能含有的物质是______________________(写至少两种物质的化学式)。
(5)根据上述实验和分析判断固体是___________(写化学式)。
【答案】(1)过滤 烧杯
(2)KClO
3
(3)Fe (SO )+6NaOH=2Fe(OH) +3Na SO
2 4 3 3 2 4
(4)炭 ;MnO 、Fe 、Fe O(任写两个)
2 2 3
(5)MnO
2
【解析】
试题分析:(1)通过步骤1分别得到了固体和溶液,故是过滤操作;过滤时需要漏斗、玻璃棒和烧杯;
(2)无色溶液中加入硝酸银得到了白色沉淀,该白色沉淀是氯化银沉淀,即溶液中含有氯离子,故是用
加热氯酸钾的方法制取氧气;氯酸钾分解生成氯化钾,氯化钾与硝酸银反应生成氯化银沉淀;(5)固体C是黑色的,碳会与氧气反应掉,铁会与稀硫酸反应,故是二氧化锰。
考点:化学反应流程
四、(本大题包括2小题,共22分)
22.(10分)小明在课外阅读中得知:氢氧化铜受热会分解生成氧化铜【Cu(OH) ==CuO+X】,于是用
2
CuSO 溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
4
(1)生成物X的化学式为___________。
(2)制取氢氧化铜的化学方程式为______________________。
(3)小明在加热氢氧化铜时,发现蓝色固体先变成黑色;继续高温灼烧黑色固体变成红色,同时有
气体产生。为弄清这种红色固体的成份,进行了如下的探究:
【查阅资料】Cu和Cu2O均为红色固体,且Cu O+HSO =Cu+CuSO +H O。
2 2 4 4 2
【提出猜想】红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.______________________。
【进行实验】
操作 现象 结论
①取灼烧后的红色固体1.44g于试管中,加 溶液由无色变蓝色,固体减 1.44g红色固体一定有:
入足量稀硫酸,加热并充分震荡,静置。 少。 ______________________
②过滤、洗涤、干燥。 得红色固体
【答案】(1)HO
2
(2)CuSO +2KOH=Cu(OH) +K SO
4 2 2 4
(3)Cu 和Cu O ;Cu O(结论表格中填写);
2 2
①II;②4CuO 2Cu O+O ;③对操作最后红色固体称量;计算
2 2考点:实验探究
23.(12分)根据下图回答有关问题。
(1)仪器E的名称为___________。
(2)图A~C是常见实验基本操作。其中正确的是___________(填序号);请选择一个有错误的操作
写出改正方法:
___________________________________________________________________________。
(3)选择仪器D~I完成下列实验操作:
①用KMnO 制备O,应选仪器___________(填序号),其化学反应方程式为
4 2
_______________________;
②用大理石与稀盐酸反应制备CO 并使反应随时发生或停止,应选仪器___________,
2
其反应方程式为______________________。
(4)下图是以锌粒和稀硫酸反应制备H,并用排水法收集。请把图补画完整。
2【答案】(1)试管
(2)B ; A ,先挤压出胶头中空气,再插入吸取液体(或C,液体加入量不能超过试管容积的1/3)
(3)DEFG ; 2KMnO KMnO +MnO+O ; E I ;
4 2 4 2 2
CaCO +2HCl=CaCl +H O+CO
3 2 2 2
(4)
【解析】
试题分析:(2)中取用液体药品时要先挤压出胶头中空气,再插入吸取液体;B正确;C中液体加入量不
能超过试管容积的1/3;
考点:常用气体的发生装置和收集装置与选取方法, 实验室制取氧气的反应原理,实验室制取二氧化碳
的反应原理
五、(本大题包括2小题,共14分)
24.(5分)某复合肥的部分说明书如图所示。请回答:(1)从肥效的角度看,共有种有效元素___________。
(2)该复合肥的有效成分之一是尿素[CO(NH)],则尿素中碳、氧、氮、氢的原子个数比为
2 2
___________。
(3)一袋该化肥至少含PO___________kg。
2 5
(4)从“注意事项”看,该复合肥料的物理性质是___________,
化学性质是___________(写一种)。
【答案】(1)3;(2)1:1:2:4 ;(3)2.5 ;
(4)易潮解 ;受热易分解
【解析】
试题分析:(1)植物需要大量的N、P、K三种元素,故由标签信息可知,该复合肥中含有的营养元素是
N、P、K三种;
(2)由尿素的化学式可知,尿素中碳、氧、氮、氢的原子个数比为1:1:2:4 ;
(3)由标签信息可知,三种物质的比例为15:5:5 。该袋化肥的总质量为50kg,总养分为25%,即为
50kg×25%=12.5kg;25x=12.5kg,X=0.5kg;含PO 的质量=0.5kg×5=2.5kg;
2 5
(4)由主要事项可知,该复合肥易潮解,受热易分解。
考点:化学肥料
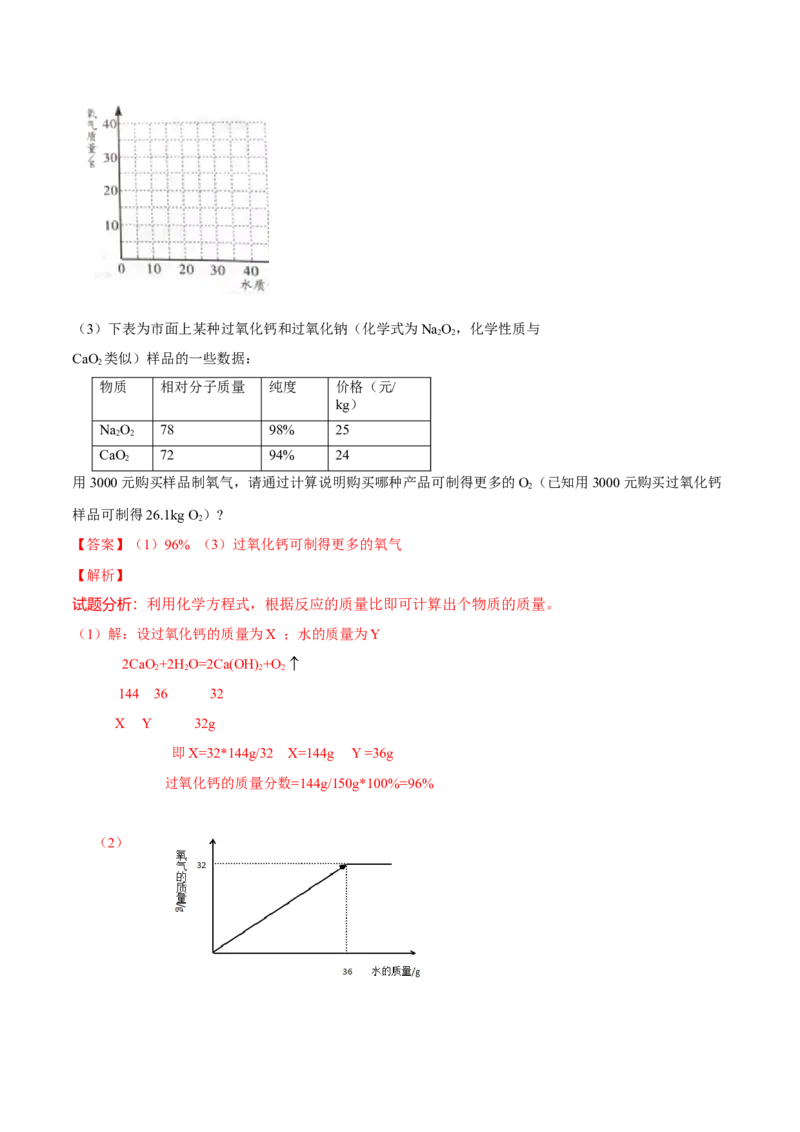
25.(9分)过氧化钙(CaO)是一种环境友好的化工原料,工农业生产中用作漂白剂、种子消毒剂以及
2
鱼类运输时的制氧剂等。过氧化钙与水反应方程式为:2CaO+2H O=2Ca(OH) +O 。
2 2 2 2
(1)若用150g某过氧化钙工业样品可制得氧气32g,请计算该过氧化钙样品的纯度(样品中CaO 的质量
2
分数)是多少?
(2)往150g上述过氧化钙工业样品中逐渐加入水至过量,在下图中画出产生氧气的曲线图。(3)下表为市面上某种过氧化钙和过氧化钠(化学式为NaO,化学性质与
2 2
CaO 类似)样品的一些数据:
2
物质 相对分子质量 纯度 价格(元/
kg)
NaO 78 98% 25
2 2
CaO 72 94% 24
2
用3000元购买样品制氧气,请通过计算说明购买哪种产品可制得更多的O(已知用3000元购买过氧化钙
2
样品可制得26.1kg O)?
2
【答案】(1)96% (3)过氧化钙可制得更多的氧气
【解析】
试题分析:利用化学方程式,根据反应的质量比即可计算出个物质的质量。
(1)解:设过氧化钙的质量为X ;水的质量为Y
2CaO+2H O=2Ca(OH) +O
2 2 2 2
144 36 32
X Y 32g
即X=32*144g/32 X=144g Y =36g
过氧化钙的质量分数=144g/150g*100%=96%
(2)考点:利用化学方程式的计算