文档内容
人教版(2019)必修第二册第七章第二节乙烯与有机高分子材料
课时训练三
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.有机高分子化合物是由千百个原子彼此以共价键结合形成相对分子质量特别大、具
有重复结构单元的有机化合物。下列物质不属于有机高分子化合物的是
A.聚四氟乙烯 B.油脂 C.纤维素 D.蛋白质
2.下列对合成材料的认识正确的是
A.高分子链之间靠分子间作用力结合,分子间作用力弱,因此高分子材料的强度较
小
B.乙烯合成聚乙烯的化学方程式是:nCH=CH
2 2
C.聚乙烯是由乙烯加聚生成的纯净物
D.高分子材料只能靠人工合成
3.学习化学要正确认识物质的组成结构和变化。下列说法正确的是
A.钢铁制品锈蚀、CO 制汽水的过程都没有包含化学变化
2
B.陶瓷、有机玻璃都是用途非常广泛的无机非金属材料
C.金刚石和石墨这两种物质中碳原子的排列方式是不同的
D.如图所示,从蜡烛火焰中引出的“白烟”属于纯净物
4.中美学者携手发现了全硼富勒烯团簇- 。 团簇的结构酷似中国的红灯笼(如图)。
该材料可用于组装分子器件,在储氢储锂、半导体、超导、绿色催化等领域具有重要
的应用前景。下列有关说法正确的是
A. 与石墨烯的结构相同,二者互为同素异形体B.44g该物质含有 个原子
C. 中含有离子键和共价键
D.全硼富勒烯团簇是一种新型的高分子材料
5.下列说法不正确的是
A.硅酸钠溶液浸泡过的木材、纺织品既耐腐蚀又不易着火
B. 胶体具有很强的杀菌消毒作用,因此可以用作净水剂
C.过氧化钠可用作漂白剂和呼吸面具中的供氧剂
D.利用二氧化碳等原料合成的可降解塑料替代聚乙烯塑料,可减少“白色污染”
6.神舟十三号载人飞船刷新了中国载人航天技术的新高度。下列说法正确的是
A.飞船表面结构的铝合金具有高强、高韧的优点
B.逃逸系统复合材料中的酚醛树脂属于天然高分子材料
C.计算机系统使用的国产CPU芯片主要成分为SiO
2
D.储能系统的锂离子蓄电池组在放电时将电能转化为化学能
7.11月12日天舟五号货运飞船与中国空间站天和核心舱后向端口成功交会对接。下
列有关空间站说法不正确的是
A.太阳能电池中的砷化镓——半导体材料 B.外层的热控保温材料石墨烯——无机
材料
C.外表面的高温结构陶瓷碳化硅——硅酸盐材料 D.外壳的烧蚀材料之一酚醛树脂
——高分子材料
8.下列化学用语表示正确的是
A.S2-的结构示意图: B.CO 的结构式: O-C-O
2
C.氯化氢分子的电子式: D.CH 的分子结构模型:
4
9.下列化学用语表述正确的是
A.金刚石的晶胞: B.甲基的电子式:
试卷第2页,共3页C.次氯酸的结构式: D.葡萄糖的实验式:
10.一次性医用口罩在防止新冠病毒的传播中发挥了重要的作用,生产医用口罩的主
要材料是聚丙烯材料。下列说法错误的是
A.医用口罩的随意丢弃会造成白色污染
B.聚丙烯是合成高分子材料
C.由丙烯合成聚丙烯的反应是加成聚合反应
D.聚丙烯的结构简式是
11.下列我国科研成果所涉材料中,主要成分为同主族元素组成的无机非金属材料的
是
A.“玉兔二号”钛合金筛选网轮 B.2022年冬奥会聚氨酯速滑服
C.能屏蔽电磁波的碳包覆银纳米线 D.4.03米大口径碳化硅反射镜
12.超级电容器是介于普通电容器与电池之间的储能装置。石墨烯/聚3,4-乙烯二氧
噻吩(PEDOP)可用于制备超级电容器。下列有关说法正确的是
A.石墨烯/聚3,4-乙烯二氧噻吩是一种新型化合物
B.聚3,4-乙烯二氧噻吩是人工合成高分子化合物
C.石墨与C 互为同分异构体
60
D.聚3,4-乙烯二氧噻吩是纯净物
13.化学与当今科技、生产、生活密不可分,下列说法正确的是
A.中国天眼FAST建造中用到的高性能碳化硅是一种新型的有机高分子材料
B.“冰丝带”冬奥馆采用二氧化碳跨临界制冰技术,利用了二氧化碳分解吸热原理
C.航天服使用的棉针织品、羊毛、氯丁尼龙橡胶等都属于天然高分子材料
D.新冠疫苗需要冷藏运输主要是防止蛋白质升温变性
14.关于化学与生活、化学与生产,下列说法不正确的是
A.冬奥会火炬“飞扬”以碳纤维复合材料为外壳,碳纤维是一种新型的无机非金属
材料
B.用浸泡过高锰酸钾溶液的硅藻土吸收水果中的乙烯,可实现水果保鲜
C.N95型口罩的核心材料聚丙烯能使酸性高锰酸钾溶液褪色
D.天然橡胶硫化前后,橡胶由链状分子变成网状分子
15.人类文明的发展和社会的进步与信息的传递关系密切,信息传递的载体随时代发
展不断变化,下列信息传递的载体的主要成分属于纤维素的是B.90年代寻呼机
A.古代的竹简 C.手机芯片 D.光导纤维
外壳
A.A B.B C.C D.D
二、填空题
16.阅读科技材料,回答下列问题
2022年2月20日,第二十四届冬奥会在北京胜利闭幕,本届冬奥会大量使用了高科技。
材料1:国家速滑馆“冰丝带”中神奇的二氧化碳跨临界直接制冰。该技术就是将气
态二氧化碳通过加温加压形成超临界二氧化碳流体(超临界二氧化碳流体是 形成气
态与液态交融在一起的流体),再对超临界二氧化碳进行降温降压达到-20℃至-15℃,
再相变蒸发吸热完成制冷和制冰的过程。该技术碳排放趋近于零,且对大气臭氧层没
有影响,是目前世界上最环保的制冰技术。
材料2:冬奥会服装中的“黑科技”。本次冬奥会颁奖礼仪服装的衣服内胆里特意添
加了第二代石墨烯发热材料,石墨烯是从石墨中分离出来的一层或几层碳原子构成的
石墨片,是目前世界上最薄、最坚硬的纳米材料,石墨烯导热系数非常高。穿着礼仪
服装前进行充电,充电完成后,石墨烯发热服会产生一种由内而外的温暖。此外,比
赛服装中的科技含量更高,例如速滑竞赛服中,含有弹性超强的橡胶材料,可以最大
程度减少体力消耗。
(1)文中涉及的有机合成材料是_______。
(2)第二代石墨烯作为一种新材料,它_______(选填“是”或“不是”)优良的导体,画
出构成石墨烯的原子结构示意图_______。
(3)下列说法正确的是_______。
A.石墨烯在常温下化学性质非常稳定
B.超临界:二氧化碳流体与普通二氧化碳化学性质不同
C.超临界二氧化碳流体中分子之间没有间隔
D.在一定条件下石墨烯可以还原氧化铜
(4)二氧化碳跨临界直接制冰的优点_______。
试卷第4页,共3页17.按要求填写:
(1)可用于催熟水果的是(填电子式) _______
(2)注射时常用于皮肤杀菌、消毒的有机物的主要成分是(填结构简式) _______
(3)甲烷与氯气混合光照一段时间后, 生成产物最多的是(填分子式) _______。
(4)聚合物: 的单体是(填结构简式) _______
18.聚四氟乙烯的耐热性和化学稳定性都超过其他塑料,甚至在“王水”中也不发生
变化,故号称“塑料王”,在工业上有着广泛的用途。
(1)按照下列所示的合成路线,试在方框中填入合适的化合物的结构简式:
A________B________C________D________
(2)写出下列化学方程式:B→C:___________,C→D:___________。
(3)聚四氟乙烯的链节为___________,单体为___________,四氟乙烯生成聚四氟乙烯
的反应类型为___________。
19.将下列物质及其结构简式与对应的小分子有机化合物连起来______。
物质及其结构简
小分子有机化合物
式
聚乙烯
聚氯乙烯
聚丙烯
聚四氟乙烯
20.乙烯是石油化工的重要基本原料。通过一系列化学反应,可以由乙烯得到有机高
分子材料、药物等成千上万种有用的物质。根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:试管①中装有溴的四氯化碳溶液,试管①可能出现的实验现象是___________。
试管②中装有溴水,则试管②可能出现的实验现象为___________。
(2)试管③中装有的是酸性高锰酸钾溶液,则试管③发生反应的类型为___________。
(3)写出试管①中发生反应的化学方程式:___________,反应类型为___________。
(4)做乙烯燃烧实验之前必须进行的操作是___________,乙烯燃烧可能观察到的现象是
___________。
(5)下列属于有机高分子化合物的是___________(填标号)。
①聚乙烯(PE) ②光导纤维 ③聚四氟乙烯(PTFE)
④聚丙烯(PP) ⑤聚氯乙烯(PVC) ⑥石墨纤维
A.①②③④ B.①③④⑤ C.③④⑤⑥ D.②③④⑥
三、实验题
21.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)预测:A装置中的现象是 _______,B装置中的现象是 _______ 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为 _______ 。
(3)写出A装置中发生反应的化学方程式 _______ ,反应类型为 _______ 。E装置的
作用是 _______ 。
(4)丙烯( )与乙烯具有相似的化学性质(写结构简式)。
试卷第6页,共3页①丙烯与溴的加成反应产物为 _______ 。
②在一定条件下丙烯与 的加成产物可能为_______ 。
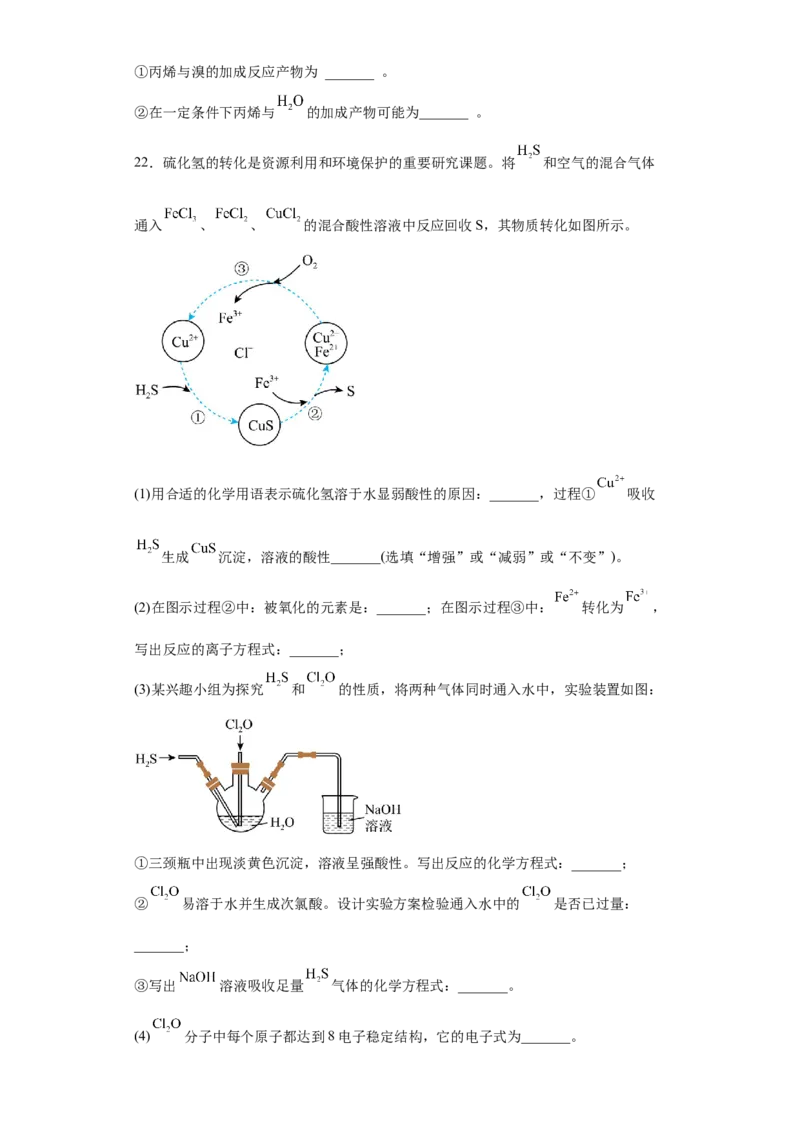
22.硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体
通入 、 、 的混合酸性溶液中反应回收S,其物质转化如图所示。
(1)用合适的化学用语表示硫化氢溶于水显弱酸性的原因:_______,过程① 吸收
生成 沉淀,溶液的酸性_______(选填“增强”或“减弱”或“不变”)。
(2)在图示过程②中:被氧化的元素是:_______;在图示过程③中: 转化为 ,
写出反应的离子方程式:_______;
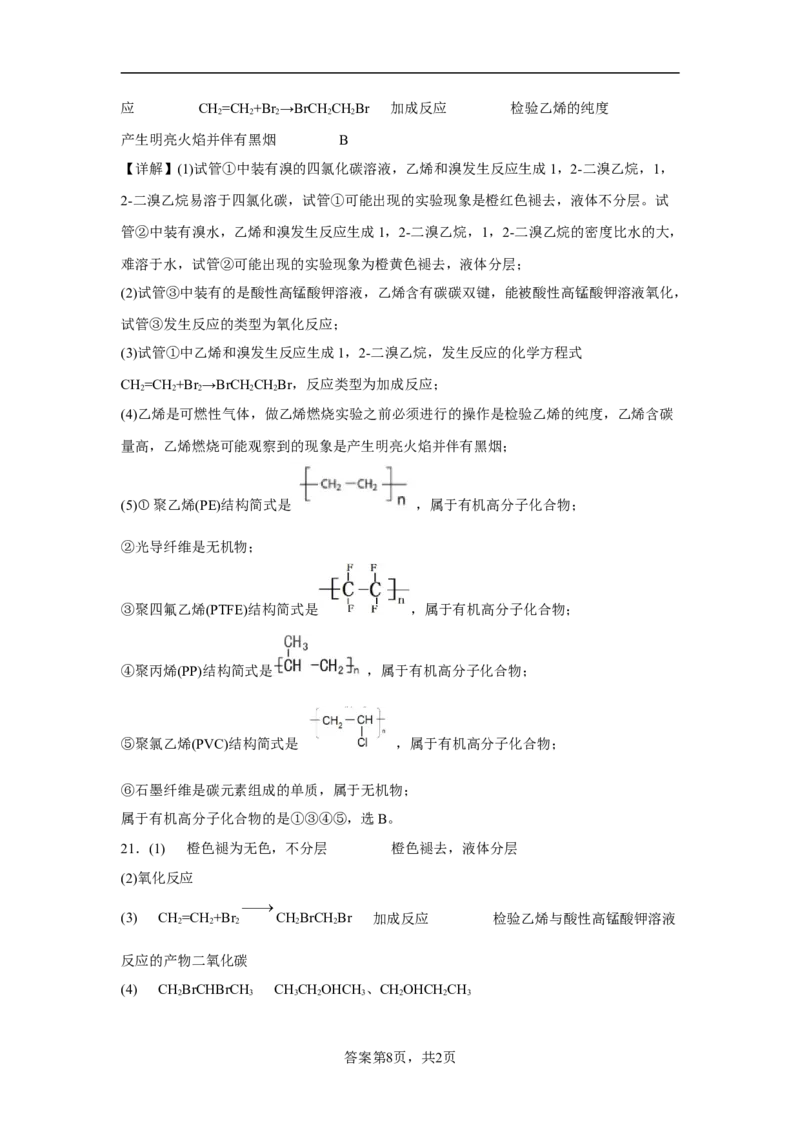
(3)某兴趣小组为探究 和 的性质,将两种气体同时通入水中,实验装置如图:
①三颈瓶中出现淡黄色沉淀,溶液呈强酸性。写出反应的化学方程式:_______;
② 易溶于水并生成次氯酸。设计实验方案检验通入水中的 是否已过量:
_______;
③写出 溶液吸收足量 气体的化学方程式:_______。
(4) 分子中每个原子都达到8电子稳定结构,它的电子式为_______。参考答案:
1.B
【详解】A.聚四氟乙烯是由四氟乙烯发生加聚反应得到高分子聚合物,故A不选;
B.油脂是高级脂肪酸和甘油形成的酯类,高级脂肪酸中的碳原子数是已知且通常在20个
左右,相对分子质量不是很大, 不属于高分子化合物,故B选;
C.纤维素是由单糖聚合而成的高分子聚合物,属于有机高分子化合物,故C不选;
D.蛋白质是由氨基酸发生缩聚反应得到的高分子聚合物,属于有机高分子化合物,故D
不选;
故选:B。
2.B
【详解】A.虽然高分子链之间靠分子间作用力结合,分子间作用力弱,但高分子长链是
由共价键结合的,结合较牢固,所以高分子材料的强度一般都较大,A项错误;
B.乙烯合成聚乙烯的化学方程式是:nCH=CH ,B项正
2 2
确;
C.聚乙烯可由乙烯加聚生成,聚乙烯中聚合度n不确定,则属于混合物,C项错误;
D.高分子材料可分为天然高分子材料和合成高分子材料两大类,故高分子材料不都是人
工合成的,D项错误;
答案选B。
3.C
【详解】A.有新物质生成的变化是化学变化,无新物质生成的变化是物理变化。钢铁制
品锈蚀有新物质生成,属于化学变化,CO 制汽水的过程中发生化学反应:
2
CO+H O=HCO,属于化学变化,此选项错误;
2 2 2 3
B.无机非金属材料包括陶瓷和混凝土等,而有机玻璃是化学合成的一种塑料,外观似玻
璃,属于合成材料,此选项错误;
C.金刚石和石墨都是由碳元素组成的单质,这两种物质中碳原子的排列方式是不同的,
所以金刚石与石墨的物理性质差别很大,此选项正确;
D.如图所示,从蜡烛火焰中引出的“白烟”是石蜡蒸汽冷凝后的固体物质,属于混合物,
此选项错误;
故选C。
4.B
【详解】A.B 与石墨烯是不同元素生成的单质,二者不互为同素异形体,故A错误;
40B.44gB 的物质的量为0.1mol,该物质含有4molB原子,即2.408×1024个原子,故B正确;
40
C.B 中只有只含有共价键、且B与B之间的共价键均为非极性键,故C错误;
40
D.全硼富勒烯团簇是一种单质,且相对分子质量不是很大,不是高分子化合物,故D错
误;
答案选B。
5.B
【详解】A.水玻璃为硅酸钠水溶液具有防腐作用和阻燃作用,人们经常把具有特殊用途
的木材、纺织品等用水玻璃浸泡,这样加工的产品既耐腐蚀又不易着火,故A正确;
B.Al(OH) 胶体,可以吸附水中的杂质,起到净水的目的,但没有杀菌消毒作用,故B错
3
误;
C.过氧化钠具有强氧化性,可用作漂白剂,可与二氧化碳反应生成氧气,用作供氧剂,
即2NaO+2CO =2Na CO+O ,故C正确;
2 2 2 2 3 2
D.利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代不能降解的聚乙烯塑料,可减
少白色污染,故D正确;
答案为B。
6.A
【详解】A.飞船表面结构的铝合金具有高强、高韧的优点,从而满足外太空中恶劣的环
境,A正确;
B.酚醛树脂为人工合成的高分子材料,B错误;
C.CPU的芯片主要是半导体材料硅单质,C错误;
D.蓄电池放电时为原电池,将化学能转化为电能,D错误;
综上所述答案为A。
7.C
【详解】A. 太阳能电池中的砷化镓导电性介于导体和半导体之间,属于半导体材料,故
A正确;
B. 外层的热控保温材料石墨烯主要成分是碳单质,属于无机材料,故B正确;
C. 外表面的高温结构陶瓷碳化硅属于无机非金属材料,故C错误;
D. 外壳的烧蚀材料之一酚醛树脂是高聚物,属于高分子材料,故D正确;
故选C。
8.D
答案第2页,共2页【详解】A.已知S是16号元素,则S2-的结构示意图为: ,A错误;
B.结构式是指用一跟“-”表示一对共用电子的式子,CO 中每个O与C形成双键,则CO
2 2
的结构式为: O=C=O,B错误;
C.HCl是共价化合物,故氯化氢分子的电子式为: ,C错误;
D.已知CH 是正四面体结构,故CH 的分子结构模型: ,D正确;
4 4
故答案为:D。
9.B
【详解】A.金刚石的晶胞结构如图所示: ,根据图可知由共价键形成的最小碳
环上有6个碳原子,选项A错误;
B.甲基不带电荷,甲基中碳原子的外层有7个电子,甲基的电子式为: ,选项B正
确;
C.HClO中O原子分别和H原子、Cl原子形成共价键,故其结构式为H-O-Cl,选项 C错
误;
D.葡萄糖的分子式为:C H O,葡萄糖的实验式为:CHO,选项D错误;
6 12 6 2
答案选B。
10.D
【详解】A.医用口罩的主要材料是聚丙烯,随意丢弃会造成白色污染,故A正确;
B.丙烯发生加聚反应生成聚丙烯,聚丙烯是合成高分子材料,故B正确;
C.丙烯发生加聚反应生成聚丙烯,反应类型是加成聚合反应,故C正确;
D.聚丙烯的结构简式是 ,故D错误;
选D。11.D
【详解】A.钛合金为含有金属钛元素的合金,其属于金属材料,不属于无机非金属材料,
故A不符合题意;
B.聚氨酯为有机高分子化合物,不属于无机非金属材料,故B不符合题意;
C.碳包覆银纳米材料属于复合材料,不属于无机非金属材料,且银不是主族元素,故C
不符合题意;
D.碳化硅(SiC)是由碳元素和硅元素组成的无机非金属材料,且碳元素与硅元素均位于元
素周期表第IVA族,故D符合题意;
故选D。
12.B
【详解】A.石墨烯/聚3,4-乙烯二氧噻吩是混合物,A项错误;
B.聚3,4-乙烯二氧噻吩是聚合物、是人工合成高分子化合物,B项正确;
C.石墨与C 都是碳元素的不同单质,故互为同素异形体,C项错误;
60
D.高分子化合物都是混合物,聚3,4-乙烯二氧噻吩是聚合物,是混合物,D项错误;
答案选B。
13.D
【详解】A.碳化硅化学式为SiC,属于无机非金属材料,故A错误;
B.冰丝带利用的是固态二氧化碳(干冰)汽化吸收大量热的原理,B项错误;
C.航天服使用的棉针织品、羊毛等都属于天然高分子材料,氯丁尼龙橡胶是人工合成的,
故C错误;
D.蛋白质高温会变性,新冠疫苗需要冷藏运输主要是防止蛋白质升温变性,故D正确;
故选D。
14.C
【详解】A.碳纤维为非金属单质,以碳纤维复合材料为外壳,碳纤维是一种新型的无机
非金属材料,故A正确;
B.乙烯是催熟剂,能被酸性高锰酸钾溶液吸收,所以用浸泡过高锰酸钾溶液的硅藻土吸
收水果中的乙烯,可实现水果保鲜,故B正确;
C.N95型口罩的核心材料聚丙烯中不含有碳碳双键,不能使酸性高锰酸钾溶液褪色,故C
错误;
D.天然橡胶硫化前后,橡胶由链状分子变成网状分子,具有较高的弹性、耐热性、拉伸
强度和在有机溶剂中的不溶解性等,故D正确;
答案第4页,共2页故选C。
15.A
【详解】A.竹简是用竹子做成,其主要成分属于纤维素,A符合题意;
B.寻呼机外壳是由塑料做成的,属于合成高分子材料,B不符合题意;
C.手机芯片的主要成分是硅单质,属于无机非金属材料,C不符合题意;
D.光导纤维的主要成分是二氧化硅,属于无机非金属材料,D不符合题意;
故选A。
16.(1)橡胶
(2) 是
(3)AD
(4)碳排放趋近于零,大气臭氧层没有影响,环保
【详解】(1)橡胶中的合成橡胶属于有机合成材料,故答案为橡胶。
(2)石墨烯是从石墨中分离出来的一层或几层碳原子构成的石墨片,石墨是优良的导体,
石墨烯是碳元素的一种单质,故其原子结构示意图为 。
(3)A.石墨烯是石墨的单质,石墨在常温下化学性质非常稳定,故A正确;
B.二氧化碳流体与普通二氧化碳都是由二氧化碳分子构成的,分子相同,化学性质相同,
故B错误;
C.超临界二氧化碳流体是 形成气态与液态交融在一起的流体,气态或液态,分子间
都是有间隔的,故C错误;
D.石墨烯是碳元素的一种单质,碳具有还原性,则在一定条件下石墨烯可以还原氧化铜,
故D正确;
答案AD。
(4)从第一段最后一句文字可以看出,二氧化碳跨临界直接制冰的优点碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保的制冰技术。故答案为碳排放趋近于零,
大气臭氧层没有影响,环保。
17.(1)
(2)CH CHOH
3 2
(3)HCl
(4)
【解析】(1)
可用于催熟水果的是乙烯, 乙烯结构简式为CH=CH ,电子式为 ;
2 2
(2)
注射时常用医用酒精对皮肤杀菌、消毒,医用酒精的主要成分是乙醇,结构简式为
CHCHOH;
3 2
(3)
甲烷与氯气混合光照条件下发生取代反应生成氯代甲烷和氯化氢,生成的氯化氢最多,化
学式为HCl;
(4)
发生加聚反应生成 ,所以 的单体是
。
18. CHCl CHClF CF=CF 2CHClF CF=CF +
3 2 2 2 2 2 2
答案第6页,共2页2HCl nCF=CF —CF—CF— CF=CF 加聚反应
2 2 2 2 2 2
【分析】氯仿为三氯甲烷,和HF反应生成二氟一氯甲烷,二氟一氯甲烷受热分解生成四
氟乙烯,四氟乙烯加聚生成聚四氟乙烯。
【详解】(1)A为氯仿,即三氯甲烷,结构简式为CHCl ,B为二氟一氯甲烷,即甲烷中的2
3
个H被2个F代替,1个H被1个Cl代替,结构简式为CHClF,C为四氟乙烯,即乙烯中
2
的4个H被4个F代替,结构简式为CF=CF ,D为聚四氟乙烯,结构简式为
2 2
。
(2)B→C是二氟一氯甲烷加热分解为四氟乙烯,根据原子守恒,可知还有HCl生成,化学
方程式为:2CHClF CF=CF +2HCl ;C→D是四氟乙烯聚合为聚四氟乙烯,化学方程
2 2 2
式为:nCF=CF 。
2 2
(3)链节为高聚物中的重复的结构单元,聚四氟乙烯的链节为—CF—CF—,单体是聚合成
2 2
高聚物的小分子,聚四氟乙烯的单体为四氟乙烯CF=CF ,四氟乙烯生成聚四氟乙烯的反
2 2
应类型为加聚反应。
19.
【详解】聚乙烯由乙烯加聚反应生成,对应小分子为 ,聚氯乙烯由氯乙烯加聚
反应生成,对应小分子为 ,聚丙烯由丙烯加聚反应生成,对应小分子为
,聚四氟乙烯由四氟乙烯加聚反应生成,对应小分子为 。
20. 橙红色褪去,液体不分层 橙黄色褪去,液体分层 氧化反应 CH=CH +Br →BrCHCHBr 加成反应 检验乙烯的纯度
2 2 2 2 2
产生明亮火焰并伴有黑烟 B
【详解】(1)试管①中装有溴的四氯化碳溶液,乙烯和溴发生反应生成1,2-二溴乙烷,1,
2-二溴乙烷易溶于四氯化碳,试管①可能出现的实验现象是橙红色褪去,液体不分层。试
管②中装有溴水,乙烯和溴发生反应生成1,2-二溴乙烷,1,2-二溴乙烷的密度比水的大,
难溶于水,试管②可能出现的实验现象为橙黄色褪去,液体分层;
(2)试管③中装有的是酸性高锰酸钾溶液,乙烯含有碳碳双键,能被酸性高锰酸钾溶液氧化,
试管③发生反应的类型为氧化反应;
(3)试管①中乙烯和溴发生反应生成1,2-二溴乙烷,发生反应的化学方程式
CH=CH +Br →BrCHCHBr,反应类型为加成反应;
2 2 2 2 2
(4)乙烯是可燃性气体,做乙烯燃烧实验之前必须进行的操作是检验乙烯的纯度,乙烯含碳
量高,乙烯燃烧可能观察到的现象是产生明亮火焰并伴有黑烟;
(5)①聚乙烯(PE)结构简式是 ,属于有机高分子化合物;
②光导纤维是无机物;
③聚四氟乙烯(PTFE)结构简式是 ,属于有机高分子化合物;
④聚丙烯(PP)结构简式是 ,属于有机高分子化合物;
⑤聚氯乙烯(PVC)结构简式是 ,属于有机高分子化合物;
⑥石墨纤维是碳元素组成的单质,属于无机物;
属于有机高分子化合物的是①③④⑤,选B。
21.(1) 橙色褪为无色,不分层 橙色褪去,液体分层
(2)氧化反应
(3) CH=CH +Br CHBrCHBr 加成反应 检验乙烯与酸性高锰酸钾溶液
2 2 2 2 2
反应的产物二氧化碳
(4) CHBrCHBrCH CHCHOHCH 、CHOHCH CH
2 3 3 2 3 2 2 3
答案第8页,共2页【分析】由实验装置可知,A中乙烯与溴发生加成反应,溴的四氯化碳溶液褪色;B中乙
烯与溴水发生加成反应,溴水褪色;C中乙烯与硝酸银溶液不反应,但C可检验挥发的溴;
D中乙烯被高锰酸钾氧化,溶液褪色;E中石灰水变浑浊,可知乙烯被高锰酸钾氧化生成
二氧化碳;
【详解】(1)AB装置中乙烯与溴发生加成反应均生成有机物CHBrCHBr,CHBrCHBr
2 2 2 2
能溶于四氯化碳、不溶于水,故现象分别为:溴的四氯化碳溶液褪色液体不分层;溴水褪
色液体分层;
(2)D装置中溶液由紫色变无色,是D装置中高锰酸钾被乙烯还原,乙烯被氧化,发生反
应的类型为氧化反应;
(3)A装置中乙烯与溴发生加成反应生成CHBrCHBr,反应为CH=CH +Br
2 2 2 2 2
CHBrCHBr;D中乙烯被高锰酸钾氧化生成二氧化碳气体,二氧化碳能使澄清石灰水变浑
2 2
浊,E装置的作用是检验乙烯与酸性高锰酸钾溶液反应的产物二氧化碳;
(4)①丙烯中含碳碳双键,与溴的加成反应的化学方程式为
CH=CHCH+Br →CHBrCHBrCH ,故与溴的加成产物为CHBrCHBrCH 。
2 3 2 2 3 2 3
②在一定条件下丙烯与HO的加成反应可能为CH=CHCH+H O→CH CH(OH)CH 或
2 2 3 2 3 3
CH=CHCH+H O→CH (OH)CHCH,产物为:CHCH(OH)CH 或CH(OH)CHCH。
2 3 2 2 2 3 3 3 2 2 3
22.(1) HS HS- + H+、HS- H+ + S2- 增强
2
(2) S 4Fe2+⇌ + 4H+ + O
2
= 4F⇌e3+ + 2H
2
O
(3) 2HS + ClO =2S↓+2HCl+ H O 用玻璃棒蘸取三颈瓶中的液体点到淀粉-KI试纸上,
2 2 2
将看到的现象是试纸变蓝 2NaOH + H S= Na S + 2HO
2 2 2
(4)
【分析】硫化氢具有还原性, 具有氧化性,两者在三颈瓶中反应会生成硫单质和氯化
氢;
(1)
硫化氢溶于水显弱酸性的原因为硫化氢在溶液中电离出氢离子,HS HS- + H+、HS-
2
H+ + S2-;过程①Cu2+吸收HS生成CuS沉淀,反应为Cu2+ + H S= CuS⇌↓+2H+,溶液的氢⇌离
2 2
子浓度变大,酸性增强。
(2)在图示过程②中铁离子和CuS反应生成铜离子、亚铁离子、S单质,化合价升高的元素被
氧化,S由- 2价变为0价,则被氧化的元素是S。在图示过程③中: 在氧气作用下转
化为 ,反应的离子方程式4Fe2+ + 4H+ + O = 4Fe3+ + 2H O。
2 2
(3)
①三颈瓶中出现淡黄色沉淀,应生成硫,溶液呈强酸性,说明二者发生氧化还原反应,
ClO被还原生成盐酸,硫化氢转化为硫单质,反应的方程式为2HS + ClO =2S↓+2HCl+
2 2 2
HO。
2
② 和 发生反应2HS + ClO =2S↓+2HCl+ H O,若通入水中的ClO过量,溶液中会
2 2 2 2
有HClO生成,HClO具有强氧化性,将碘离子氧化为碘单质,碘能使淀粉变蓝色,故方案
可以为:用玻璃棒蘸取三颈瓶中的液体点到淀粉-KI试纸上,将看到的现象是试纸变蓝。
③足量的NaOH溶液吸收H S气体生成硫化钠和水:2NaOH + H S= Na S + 2HO。
2 2 2 2
(4)
分子中每个原子都达到8电子稳定结构,它的电子式为 。
答案第10页,共2页