文档内容
第七章第二节乙烯与有机高分子材料跟踪训练--人教版
(2019)必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1. 和 都是温室气体。可通过如下反应实现转化和利用:
(未配平)。下列说法正确的是
A.该反应中, 作氧化剂,被氧化 B. 、 均为弱电解质
C. 的电子式: D. 分子是正四面体结构
2.下列有关化学用语表述正确的是
A.NaClO的电子式: B. 与 互为同位素
C.葡萄糖的结构简式:C H O D.钾原子的原子结构示意图:
6 12 6
3.潮阳区拥有丰富的旅游资源与饮食文化。下列有关代表物主要由纤维素组成的是
选项 A B C D
文化(代
表物)
潮阳博物馆陶 大峰风景区大峰 海门莲花峰摩崖 潮阳剪纸
瓷 祖师石像 石刻
A.A B.B C.C D.D
4.科技发展迅猛离不开材料的不断更新和优化。下列说法正确的是
A.制作火箭所使用的材料均为钢铁
B.新型电池的电极材料石墨烯属于有机高分子化合物
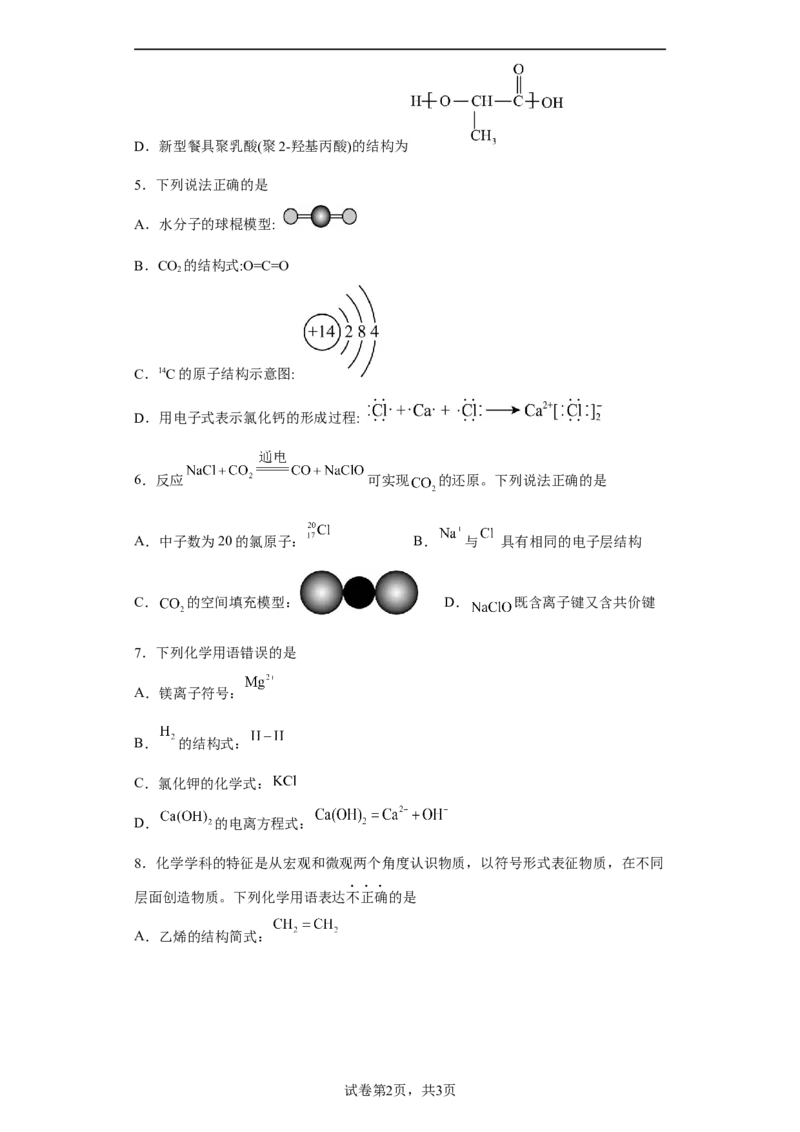
C.天宫二号卫星所使用的高性能计算机芯片含有硅单质D.新型餐具聚乳酸(聚2-羟基丙酸)的结构为
5.下列说法正确的是
A.水分子的球棍模型:
B.CO 的结构式:O=C=O
2
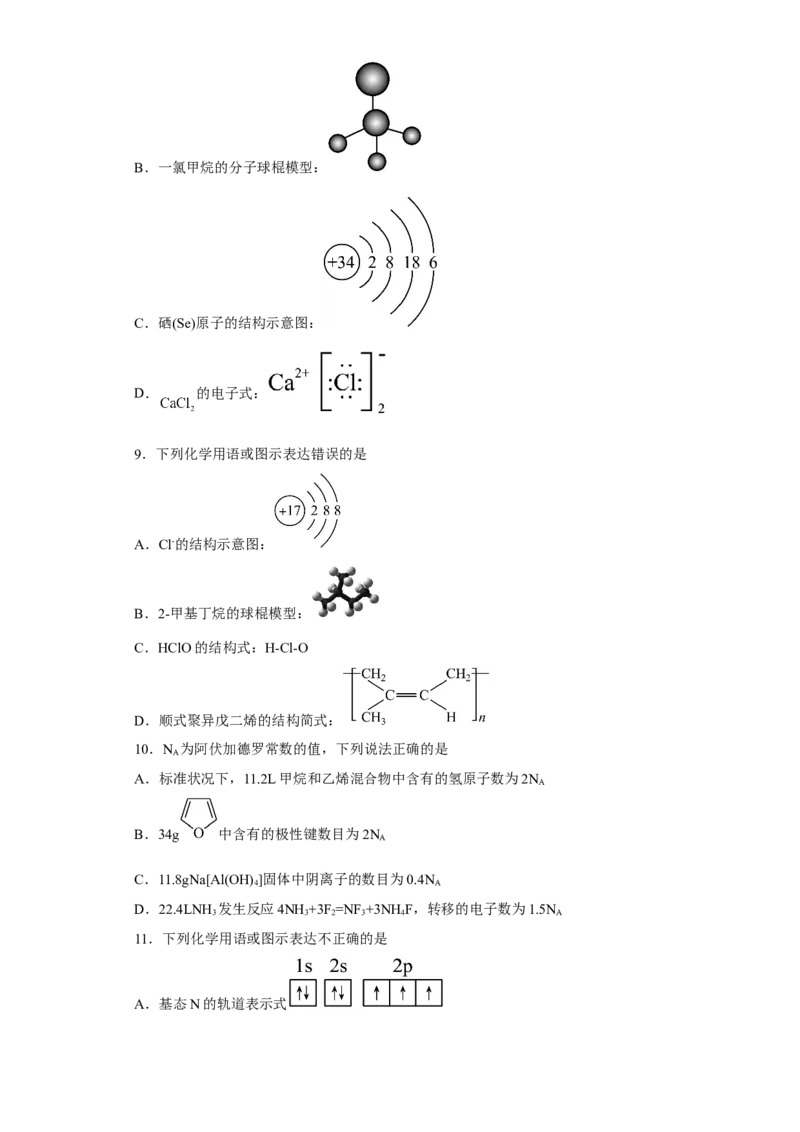
C.14C的原子结构示意图:
D.用电子式表示氯化钙的形成过程:
6.反应 可实现 的还原。下列说法正确的是
A.中子数为20的氯原子: B. 与 具有相同的电子层结构
C. 的空间填充模型: D. 既含离子键又含共价键
7.下列化学用语错误的是
A.镁离子符号:
B. 的结构式:
C.氯化钾的化学式:
D. 的电离方程式:
8.化学学科的特征是从宏观和微观两个角度认识物质,以符号形式表征物质,在不同
层面创造物质。下列化学用语表达不正确的是
A.乙烯的结构简式:
试卷第2页,共3页B.一氯甲烷的分子球棍模型:
C.硒(Se)原子的结构示意图:
D. 的电子式:
9.下列化学用语或图示表达错误的是
A.Cl-的结构示意图:
B.2-甲基丁烷的球棍模型:
C.HClO的结构式:H-Cl-O
D.顺式聚异戊二烯的结构简式:
10.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,11.2L甲烷和乙烯混合物中含有的氢原子数为2N
A
B.34g 中含有的极性键数目为2N
A
C.11.8gNa[Al(OH) ]固体中阴离子的数目为0.4N
4 A
D.22.4LNH 发生反应4NH +3F =NF+3NHF,转移的电子数为1.5N
3 3 2 3 4 A
11.下列化学用语或图示表达不正确的是
A.基态N的轨道表示式B.Cl-的结构示意图
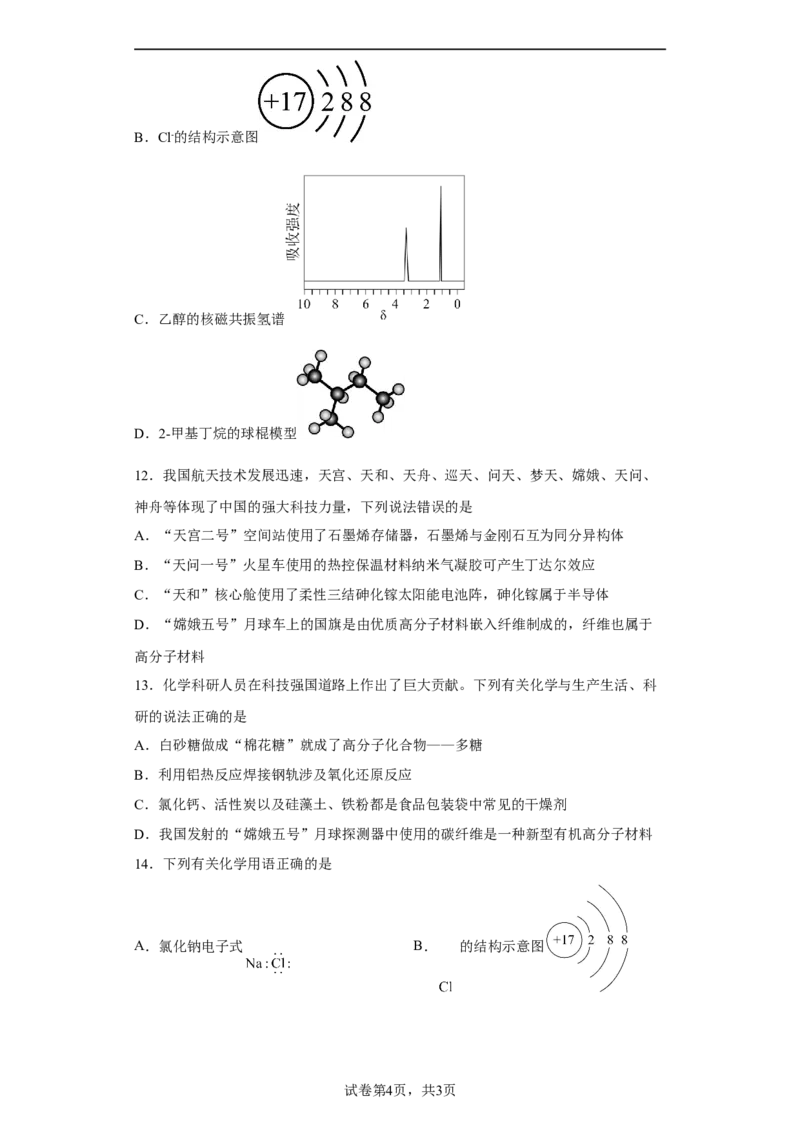
C.乙醇的核磁共振氢谱
D.2-甲基丁烷的球棍模型
12.我国航天技术发展迅速,天宫、天和、天舟、巡天、问天、梦天、嫦娥、天问、
神舟等体现了中国的强大科技力量,下列说法错误的是
A.“天宫二号”空间站使用了石墨烯存储器,石墨烯与金刚石互为同分异构体
B.“天问一号”火星车使用的热控保温材料纳米气凝胶可产生丁达尔效应
C.“天和”核心舱使用了柔性三结砷化镓太阳能电池阵,砷化镓属于半导体
D.“嫦娥五号”月球车上的国旗是由优质高分子材料嵌入纤维制成的,纤维也属于
高分子材料
13.化学科研人员在科技强国道路上作出了巨大贡献。下列有关化学与生产生活、科
研的说法正确的是
A.白砂糖做成“棉花糖”就成了高分子化合物——多糖
B.利用铝热反应焊接钢轨涉及氧化还原反应
C.氯化钙、活性炭以及硅藻土、铁粉都是食品包装袋中常见的干燥剂
D.我国发射的“嫦娥五号”月球探测器中使用的碳纤维是一种新型有机高分子材料
14.下列有关化学用语正确的是
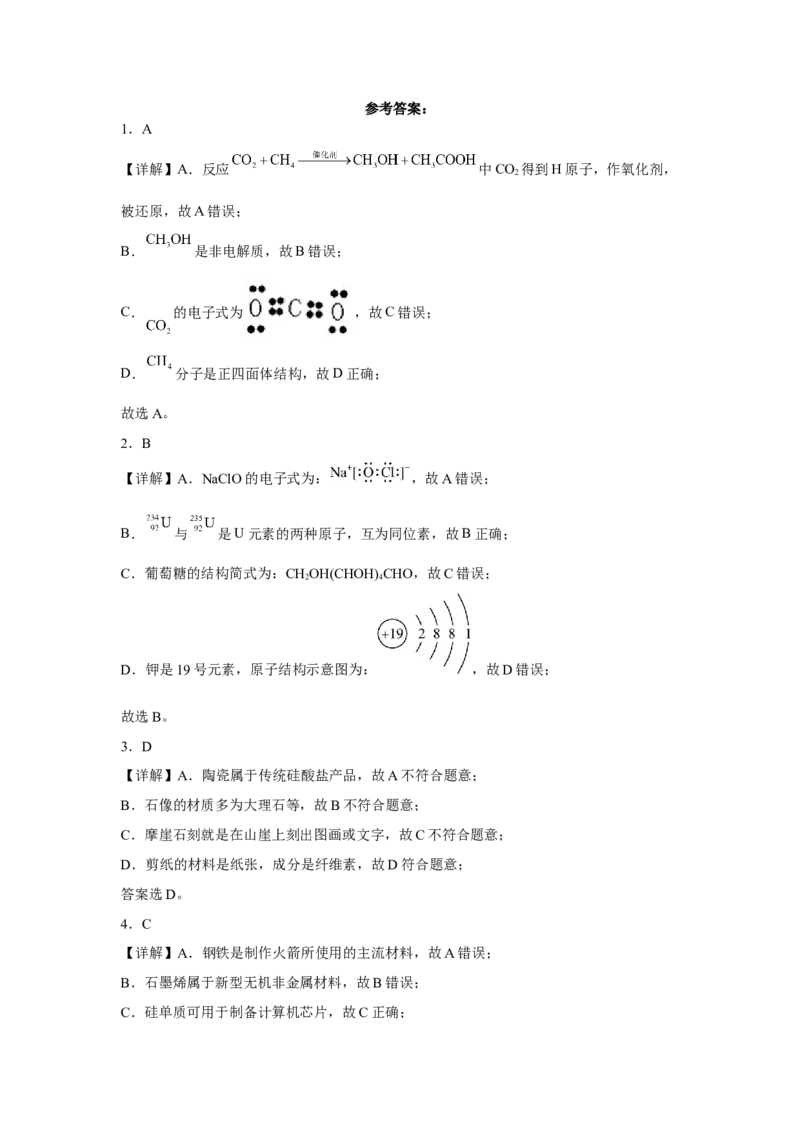
A.氯化钠电子式 B. 的结构示意图
试卷第4页,共3页C. 的电子式 D. 的结构式
15.下列化学用语书写正确的是
A.中子数为148的铀原子: B.氨基( )的电子式:
C. 分子的空间填充模型: D.聚氯乙烯的链节:
二、计算题
16.计算:
(1)已知有机物A的相对分子质量为90。将9.0 g A在足量纯 中充分燃烧,并使其产
物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g,则有机物A的分
子式为_______。
(2)将60 g由甲烷和乙烯组成的混合气体通入盛有足量溴水的容器,充分反应后容器的
总质量增加28 g,则原混合气中甲烷和乙烯的物质的量之比为_______。
17.将11.2L(标准状况)乙烯和乙烷的混合气体通入足量的溴水中,充分反应后,溴水
的质量增加了5.6g。请通过计算分析:
(1)求原混合气体中乙烯与乙烷的物质的量之比_______;
(2)该混合气体完全燃烧,生成二氧化碳和水的质量各是多少_______?参考答案:
1.A
【详解】A.反应 中CO 得到H原子,作氧化剂,
2
被还原,故A错误;
B. 是非电解质,故B错误;
C. 的电子式为 ,故C错误;
D. 分子是正四面体结构,故D正确;
故选A。
2.B
【详解】A.NaClO的电子式为: ,故A错误;
B. 与 是U元素的两种原子,互为同位素,故B正确;
C.葡萄糖的结构简式为:CHOH(CHOH) CHO,故C错误;
2 4
D.钾是19号元素,原子结构示意图为: ,故D错误;
故选B。
3.D
【详解】A.陶瓷属于传统硅酸盐产品,故A不符合题意;
B.石像的材质多为大理石等,故B不符合题意;
C.摩崖石刻就是在山崖上刻出图画或文字,故C不符合题意;
D.剪纸的材料是纸张,成分是纤维素,故D符合题意;
答案选D。
4.C
【详解】A.钢铁是制作火箭所使用的主流材料,故A错误;
B.石墨烯属于新型无机非金属材料,故B错误;
C.硅单质可用于制备计算机芯片,故C正确;D.聚2-羟基丙酸的结构为 ,故D错误;
故答案选C。
5.B
【详解】A.水分子的球棍模型为 ,A错误;
B.CO 的结构式为O=C=O ,B正确;
2
C.14C 的原子结构示意图为 ,C错误;
D.用电子式表示氯化钙的形成过程为 ,D错
误;
故选B。
6.D
【详解】A.中子数为20的氯原子质量数为:20+17=37,表示为: ,故A错误;
B. 有2个电子层, 有3个电子层,故B错误;
C. 是直线形结构,氧原子半径小于碳原子,空间填充模型为: ,故
C错误;
D. 是离子化合物,既含离子键又含共价键,故D正确;
故选D。
7.D
【详解】A.镁离子是镁原子失去最外层2个电子形成的,故镁离子符号: ,A正确;
B. 分子中氢原子之间形成了非极性键,故 的结构式: ,B正确;
C.氯化钾是由氯离子和钾离子构成的,故氯化钾的化学式: ,C正确;
答案第2页,共2页D. 中含有2个氢氧根离子, 的电离方程式: ,D
错误;
故本题选D。
8.D
【详解】A.乙烯的分子式为C H,分子中含有碳碳双键,故其结构简式为:CH=CH ,A
2 4 2 2
正确;
B.一氯甲烷分子呈四面体结构,且原子半径Cl>C>H,故其分子球棍模型为:
,B正确;
C.Se是34号元素,与O元素同一主族,位于第4周期第ⅥA族,故硒(Se)原子的结构示
意图为: ,C正确;
D.CaCl 是离子化合物,故其电子式为: ,D错误;
2
故答案为:D。
9.C
【详解】A.Cl-的核电荷数为17,核外电子数为18,故为 ,故A正确;B.2-甲基丁烷的球棍模型为 ,故B正确;
C.HClO的结构式为H -O-Cl,故C错误;
D.顺式聚异戊二烯的结构简式为 ,故D正确;
故选C。
10.A
【详解】A.标准状况下,11.2L甲烷和乙烯混合气体的物质的量是0.5mol,甲烷和乙烯分
子均含有4个氢原子,则混合物中含有的氢原子数为2N ,A正确;
A
B.1个 中含有6个极性键,分别是4个碳氢键和2个碳氧键,则34g 的物质
的量为0.5mol,则其中含有的极性键数目为3N ,B错误;
A
C.11.8gNa[Al(OH) ]的物质的量是11.8g÷118g/mol=0.1mol,该物质含有的阴离子是Al(OH)
4
,则固体中阴离子的数目为0.1N ,C错误;
A
D.温度和压强未知,则22.4LNH 的物质的量无法计算,因此不能计算反应中转移的电子
3
数,D错误;
答案选A。
11.C
【详解】A.N原子基态时的电子排布式为1s22s22p3,其原子的轨道表示式为:
,选项A正确;
B.Cl-离子质子数为17,核外电子数为18,有3个电子层,各层电子数为2、8、8,氯离
子结构示意图为 ,选项B正确;
C.乙醇结构简式为CHCHOH,共有三种氢,所以核磁共振氢谱有三组吸收峰,选项C
3 2
不正确;
D.线代表化学键,可连结以球型表示的原子中心,能正确表示2-甲基丁烷的球棍模型,
答案第4页,共2页选项D正确;
答案选C。
12.A
【详解】A.石墨烯、金刚石均是碳的单质,它们结构不同,因此互为同素异形体,故A
说法错误;
B.纳米气凝胶属于胶体,具有丁达尔效应,故B说法正确;
C.砷化镓作太阳能电池阵,说明砷化镓属于半导体,故C说法正确;
D.纤维属于高分子,故D说法正确;
答案为A。
13.B
【详解】A.白砂糖的主要成分是蔗糖,做成“棉花糖”只是分子状态的变化,组成成分
仍然是蔗糖,A错误;
B.铝热反应的原理是铝和氧化铁在高温下反应生成氧化铝和铁, 、 化合价均发生变
化,涉及氧化还原反应,B正确;
C.铁粉具有还原性,可用作食品抗氧化剂,不能用作干燥剂,C错误;
D.碳纤维是一种新型无机材料,不是高分子材料,D错误;
故答案为:B。
14.B
【详解】A.氯化钠属于离子化合物,其电子式中需要标出阴阳离子所带电荷,氯化钠正
确的电子式为: ,故A错误;
B. 的核电荷数、核外电子总数分别为17和18,氯原子结构示意图为: ,
故B正确;
C.CO 的电子式为 ,故C错误;
2
D. 的结构式为: ,故D错误;
故选B。15.B
【详解】A.质量数标注于元素符号的左上角,质子数标注于左下角,中子数为148的铀
原子的质量数=质子数+中子数 ,选项A错误;
B.氮原子的最外层电子数为5,氨基中N上除两个成键电子对外还有1个孤电子对和1个
单电子,选项B正确;
C.碳原子的半径比氧原子的大,故 分子的空间填充模型为 ,选项C错误;
D.CH=CHCl是聚氯乙烯的单体,而聚氯乙烯的链节应为—CH—CHCl—,选项D错误;
2 2
答案选B。
16.(1)C HO
3 6 3
(2)2:1
【解析】(1)浓硫酸增重5.4g,则生成水的质量是5.4g,生成n(H O)= =0.3mol,
2
所含有H原子的物质的量n(H)=0.3mol×2=0.6mol,碱石灰增重13.2g,生成m(CO)是
2
13.2g,n(CO)= =0.3mol,则n(C)=0.3mol,9.0gA中m(O)=9g-0.6g-12g/
2
mol×0.3mol=4.8g,n(O)= =0.3mol,所以n(C):n(H):n(O)=0.3mol:0.6mol:
0.3mol=1:2:1,即有机物A的实验式为CHO,设其分子式为(CHO) ,A相对分子质量
2 2 x
为90,则30x=90,故x=3,则A的分子式为C HO。
3 6 3
(2)将60 g由甲烷和乙烯组成的混合气体通入盛有足量溴水的容器,充分反应后容器的
总质量增加28 g,这说明乙烯的质量是28g、物质的量是1mol,甲烷的质量是60g—28g=
32g、物质的量是2mol,则原混合气体中甲烷和乙烯的物质的量之比为2:1。
17.(1)2:3
(2)m(CO)=44g,m(HO)=23.4g
2 2
【解析】(1)
混合气体物质的量为 =0.5mol,乙烯与溴水发生加成反应CH=CH +Br →CHBr-
2 2 2 2
答案第6页,共2页CHBr,溴水增加的质量则为乙烯的质量,即乙烯物质的量为 =0.2mol,则乙烷的
2
物质的量为(0.5-0.2)mol=0.3mol,原混合气体乙烯与乙烷的物质的量之比为0.2∶0.3=2∶3;故
答案为2∶3;
(2)
根据(1)分析以及原子守恒,混合气体燃烧后产生CO 的物质的量为(0.2×2+0.3×2)=1mol,
2
即二氧化碳的质量为44g,同理产生水的质量为 =23.4g;故
答案为m(CO )=44g,m(HO)=23.4g。
2 2答案第8页,共2页