文档内容
2010 年普通高等学校招生全国统一考试(安徽卷)
理科综合能力测试
第Ⅰ卷
(选择题 共120分)
7.亚氨基锂(LiNH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:
2
LiNH+H LiNH+LiH,下列有关说法正确的是
2 2 2
A. LiNH中N的化合价是 B.该反应中H 既是氧化剂又是还原剂
2 2
C. 和 的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
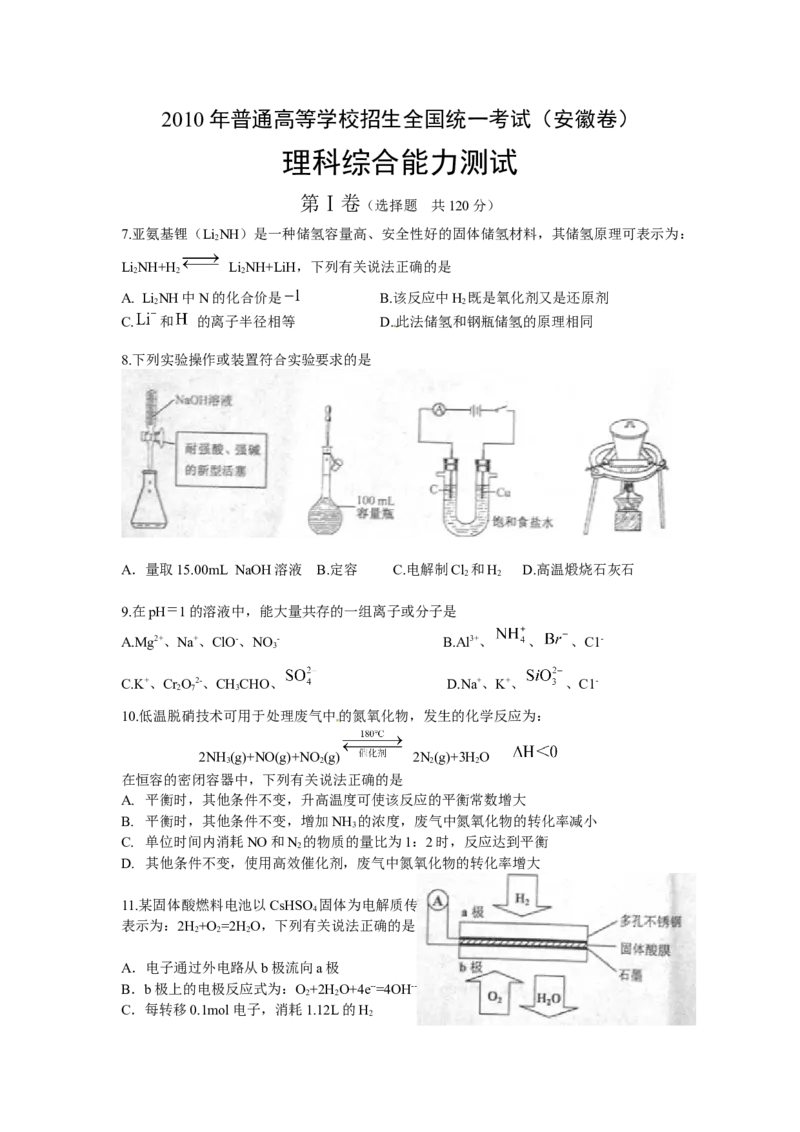
8.下列实验操作或装置符合实验要求的是
A.量取15.00mL NaOH溶液 B.定容 C.电解制Cl 和H D.高温煅烧石灰石
2 2
9.在pH 1的溶液中,能大量共存的一组离子或分子是
A.Mg2+、Na+、ClO-、NO - B.Al3+、 、 、C1-
3
C.K+、Cr O2-、CHCHO、 D.Na+、K+、 、C1-
2 7 3
10.低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH (g)+NO(g)+NO (g) 2N(g)+3HO
3 2 2 2
在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
[来源:学科网ZXXK]
B. 平衡时,其他条件不变,增加NH 的浓度,废气中氮氧化物的转化率减小
3
C. 单位时间内消耗NO和N 的物质的量比为1:2时,反应达到平衡
2
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
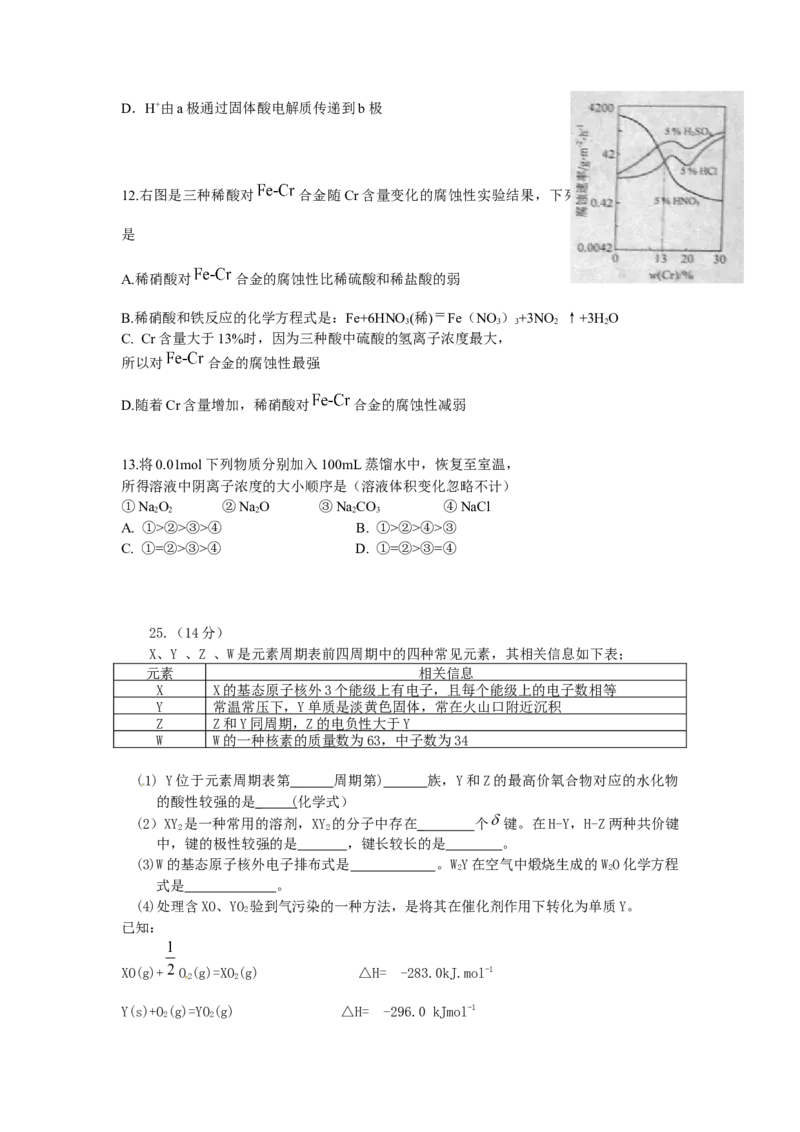
11.某固体酸燃料电池以CsHSO 固体为电解质传递H+,其基本结构见下图,电池总反应可
4
表示为:2H+O =2H O,下列有关说法正确的是
2 2 2
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O+2H O+4e--=4OH--
2 2
C.每转移0.1mol电子,消耗1.12L的H
2D.H+由a极通过固体酸电解质传递到b极
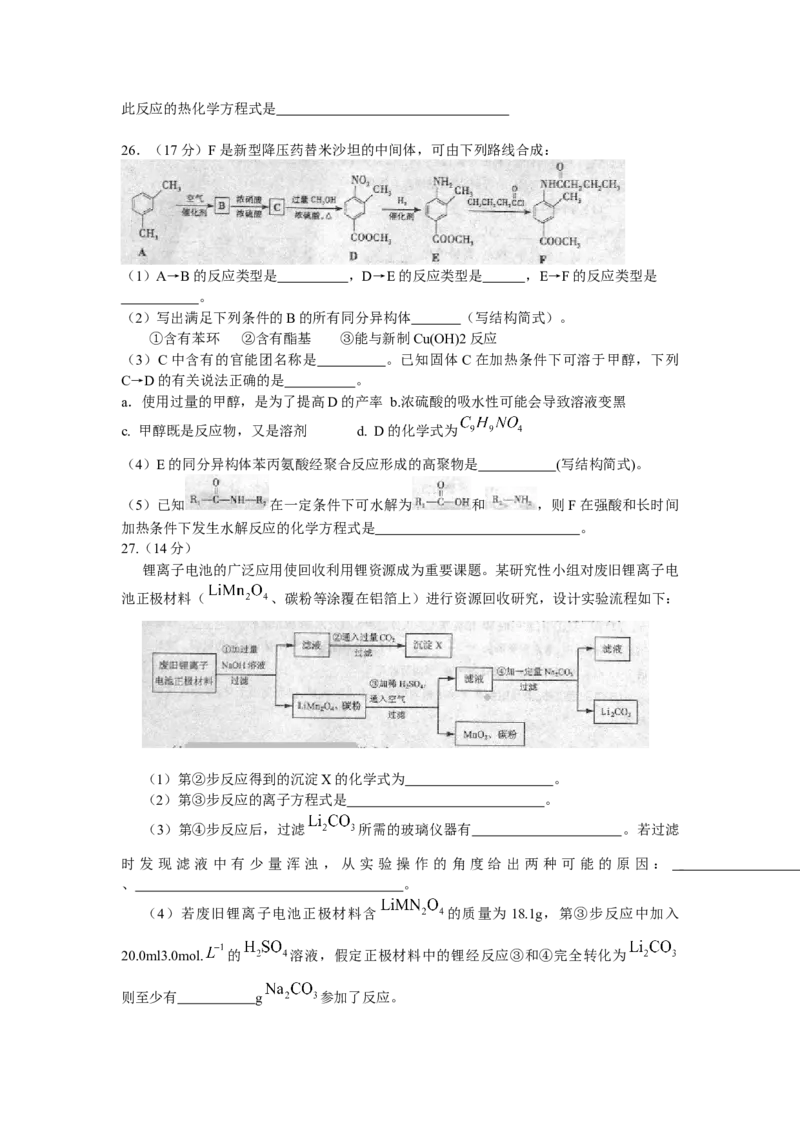
12.右图是三种稀酸对 合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的
是
A.稀硝酸对 合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是:Fe+6HNO (稀) Fe(NO )+3NO ↑+3H O
3 3 3 2 2
C. Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,
所以对 合金的腐蚀性最强
D.随着Cr含量增加,稀硝酸对 合金的腐蚀性减弱
13.将0.01mol下列物质分别加入100mL蒸馏水中,恢复至室温,
所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①NaO ②NaO ③NaCO ④NaCl
2 2 2 2 3
A. ①>②>③>④ B. ①>②>④>③
C. ①=②>③>④ D. ①=②>③=④
25.(14分)
X、Y 、Z 、W是元素周期表前四周期中的四种常见元素,其相关信息如下表;
元素 相关信息
X X的基态原子核外3个能级上有电子,且每个能级上的电子数相等
Y 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积
Z Z和Y同周期,Z的电负性大于Y
W W的一种核素的质量数为63,中子数为34
(1) Y位于元素周期表第 _ 周期第) 族,Y和Z的最高价氧合物对应的水化物
的酸性较强的是 _ (化学式)
(2)XY 是一种常用的溶剂,XY 的分子中存在 _ 个键。在H-Y,H-Z两种共价键
2 2
中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是 。WY在空气中煅烧生成的WO化学方程
2 2
式是 。
(4)处理含XO、YO 验到气污染的一种方法,是将其在催化剂作用下转化为单质Y。
2
已知:
1
XO(g)+2 O (g)=XO(g) △H= -283.0kJ.mol-1
2 2
Y(s)+O(g)=YO(g) △H= -296.0 kJmol-1
2 2此反应的热化学方程式是
[来源:学科网ZXXK]
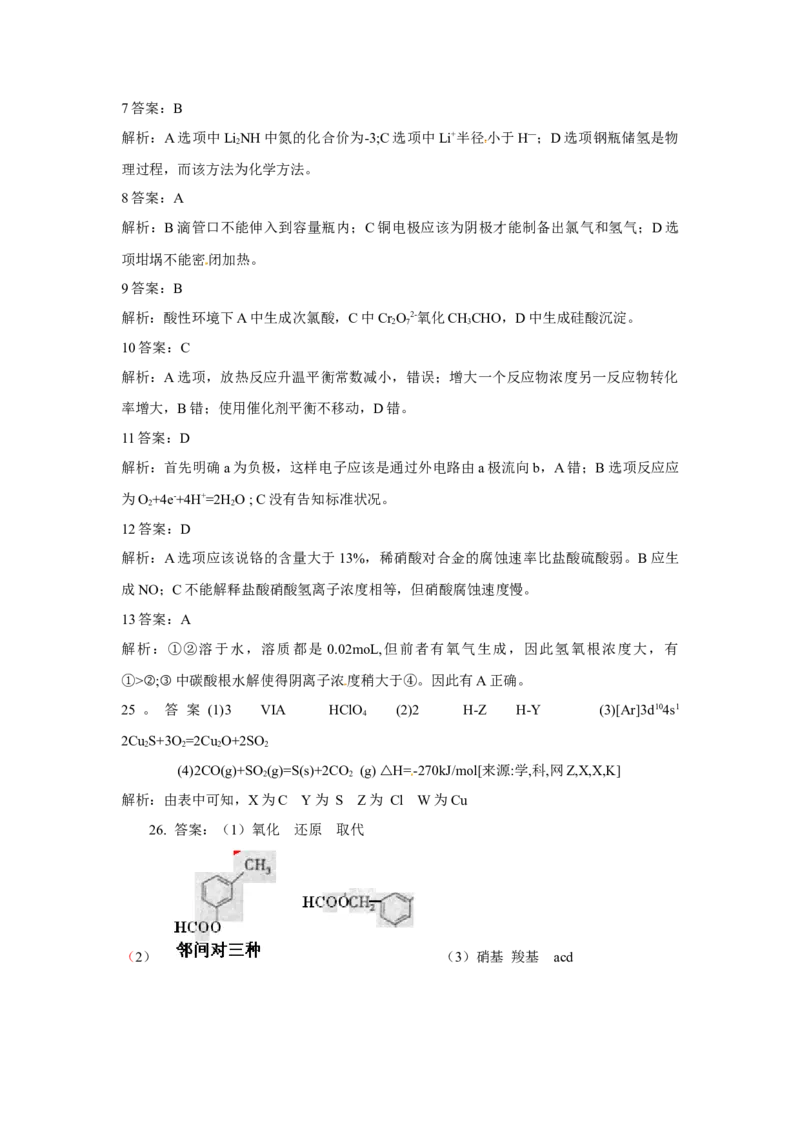
26.(17分)F是新型降压药替米沙坦的中间体,可由下列路线合成:
(1)A→B的反应类型是 ,D→E的反应类型是 ,E→F的反应类型是
。
(2)写出满足下列条件的B的所有同分异构体 (写结构简式)。
①含有苯环 ②含有酯基 ③能与新制Cu(OH)2反应
(3)C中含有的官能团名称是 。已知固体C在加热条件下可溶于甲醇,下列
C→D的有关说法正确的是 。
a.使用过量的甲醇,是为了提高D的产率 b.浓硫酸的吸水性可能会导致溶液变黑
c. 甲醇既是反应物,又是溶剂 d. D的化学式为
(4)E的同分异构体苯丙氨酸经聚合反应形成的高聚物是 (写结构简式)。
[来源:Z*xx*k.Com]
(5)已知 在一定条件下可水解为 和 ,则F在强酸和长时间
加热条件下发生水解反应的化学方程式是 。
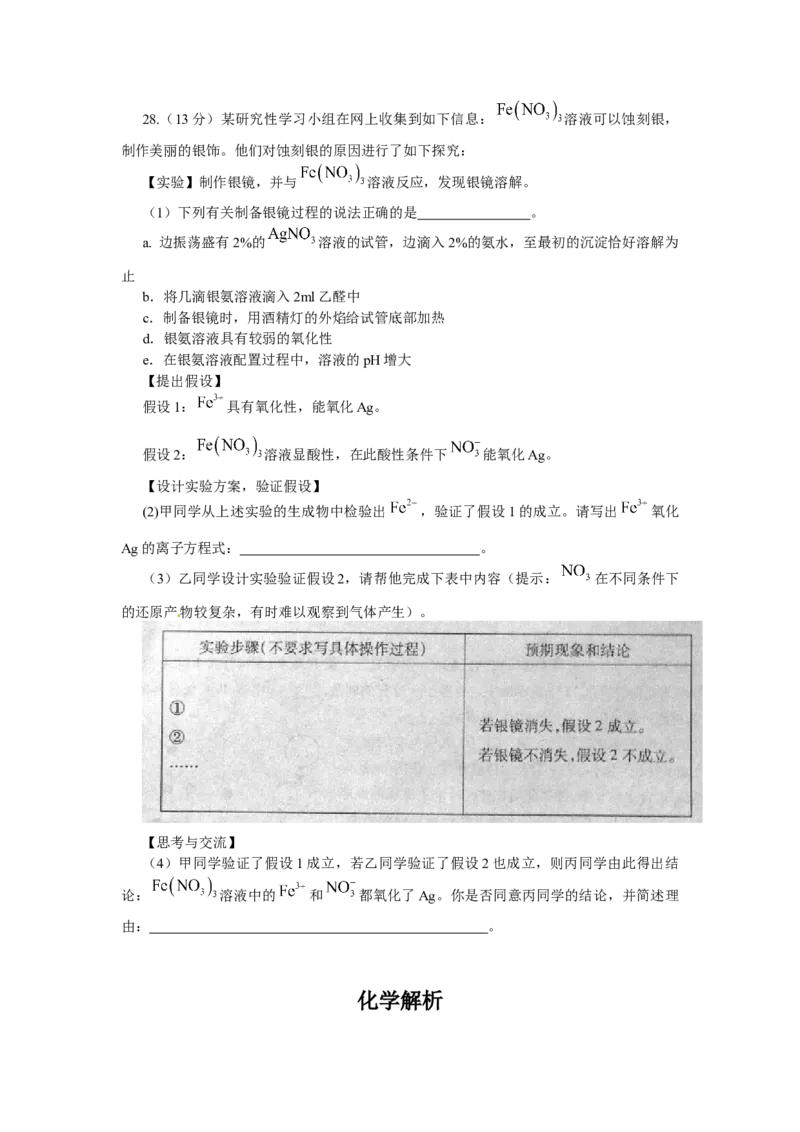
27.(14分)
锂离子电池的广泛应用使回收利用锂资源成为重要课题。某研究性小组对废旧锂离子电
池正极材料( 、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下:
(1)第②步反应得到的沉淀X的化学式为 。
(2)第③步反应的离子方程式是 。
(3)第④步反应后,过滤 所需的玻璃仪器有 。若过滤
时 发 现 滤 液 中 有 少 量 浑 浊 , 从 实 验 操 作 的 角 度 给 出 两 种 可 能 的 原 因 :
、 。
(4)若废旧锂离子电池正极材料含 的质量为18.1g,第③步反应中加入
20.0ml3.0mol. 的 溶液,假定正极材料中的锂经反应③和④完全转化为
则至少有 g 参加了反应。28.(13分)某研究性学习小组在网上收集到如下信息: 溶液可以蚀刻银,
制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】制作银镜,并与 溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是 。
a. 边振荡盛有2%的 溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为
止
b.将几滴银氨溶液滴入2ml乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配置过程中,溶液的pH增大
【提出假设】
假设1: 具有氧化性,能氧化Ag。
假设2: 溶液显酸性,在此酸性条件下 能氧化Ag。
【设计实验方案,验证假设】
(2)甲同学从上述实验的生成物中检验出 ,验证了假设1的成立。请写出 氧化
Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: 在不同条件下
的还原产物较复杂,有时难以观察到气体产生)。
【思考与交流】
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结
论: 溶液中的 和 都氧化了Ag。你是否同意丙同学的结论,并简述理
由: 。
化学解析7答案:B
解析:A选项中LiNH中氮的化合价为-3;C选项中Li+半径小于H—;D选项钢瓶储氢是物
2
理过程,而该方法为化学方法。
8答案:A
解析:B滴管口不能伸入到容量瓶内;C铜电极应该为阴极才能制备出氯气和氢气;D选
项坩埚不能密闭加热。
9答案:B
解析:酸性环境下A中生成次氯酸,C中Cr O2-氧化CHCHO,D中生成硅酸沉淀。
2 7 3
10答案:C
解析:A选项,放热反应升温平衡常数减小,错误;增大一个反应物浓度另一反应物转化
率增大,B错;使用催化剂平衡不移动,D错。
11答案:D
解析:首先明确a为负极,这样电子应该是通过外电路由a极流向b,A错;B选项反应应
为O+4e-+4H+=2H O ; C没有告知标准状况。
2 2
12答案:D
解析:A选项应该说铬的含量大于13%,稀硝酸对合金的腐蚀速率比盐酸硫酸弱。B应生
成NO;C不能解释盐酸硝酸氢离子浓度相等,但硝酸腐蚀速度慢。
13答案:A
解析:①②溶于水,溶质都是 0.02moL,但前者有氧气生成,因此氢氧根浓度大,有
①>②;③中碳酸根水解使得阴离子浓度稍大于④。因此有A正确。
25 。 答 案 (1)3 VIA HClO (2)2 H-Z H-Y (3)[Ar]3d104s1
4
2Cu S+3O=2Cu O+2SO
2 2 2 2
(4)2CO(g)+SO (g)=S(s)+2CO (g) △H=-270kJ/mol[来源:学,科,网Z,X,X,K]
2 2
解析:由表中可知,X为C Y为 S Z为 Cl W为Cu
26. 答案:(1)氧化 还原 取代
(2) (3)硝基 羧基 acd(4)
(5)略。
27答案:(1)Al(OH)3
(2)4 LiMn O+O +4H+=4Li++8MnO+2H O
2 4 2 2 2
(3) 漏斗 玻璃棒 烧杯 ; 滤纸破损、滤液超过滤纸边缘等
(4)5.3
解析:第一步就是铝溶解在氢氧化钠溶液中 第二步就是偏铝酸钠与二氧化碳生成氢氧化铝
第三步是氧化还原反应,注意根据第一步反应LiMn O 不溶于水。
2 4
第(4)小题计算时要通过计算判断出硫酸过量。
28。答案(1)ade
(2)Fe3++Ag= Fe2++Ag+ [来源:学。科。网]
(3)①将银镜在硝酸铜溶液中
(4)同意 4Fe3++6H O+9Ag+3NO -=4Fe(OH)+9Ag++3NO
2 3 3
解析:本题第(1)小题是考查学生实验,最后2小题具有较大的开放度。