文档内容
2012年全国统一高考化学试卷(大纲版)
一、选择题
1.下列关于化学键的叙述,正确的一项是( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.含有极性键的分子一定是极性分子
D.含有共价键的化合物一定是共价化合物
2.能正确表示下列反应的离子方程式是( )
A.硫酸铝溶液中加入过量氨水 Al3++3OH﹣=Al(OH) ↓
3
B.碳酸钠溶液中加入澄清石灰水 Ca(OH) +CO 2﹣=CaCO ↓+2OH﹣
2 3 3
C.冷的氢氧化钠溶液中通入氯气 Cl +2OH﹣=ClO﹣+Cl﹣+H O
2 2
D.稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H ↑
2
3.合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:
CO(g)+H O(g) CO (g)+H (g)△H<0反应达到平衡后,为提
2 2 2
高CO的转化率,下列措施中正确的是( )
A.增加压强 B.降低温度 C.增大CO的浓度 D.更换催化
剂
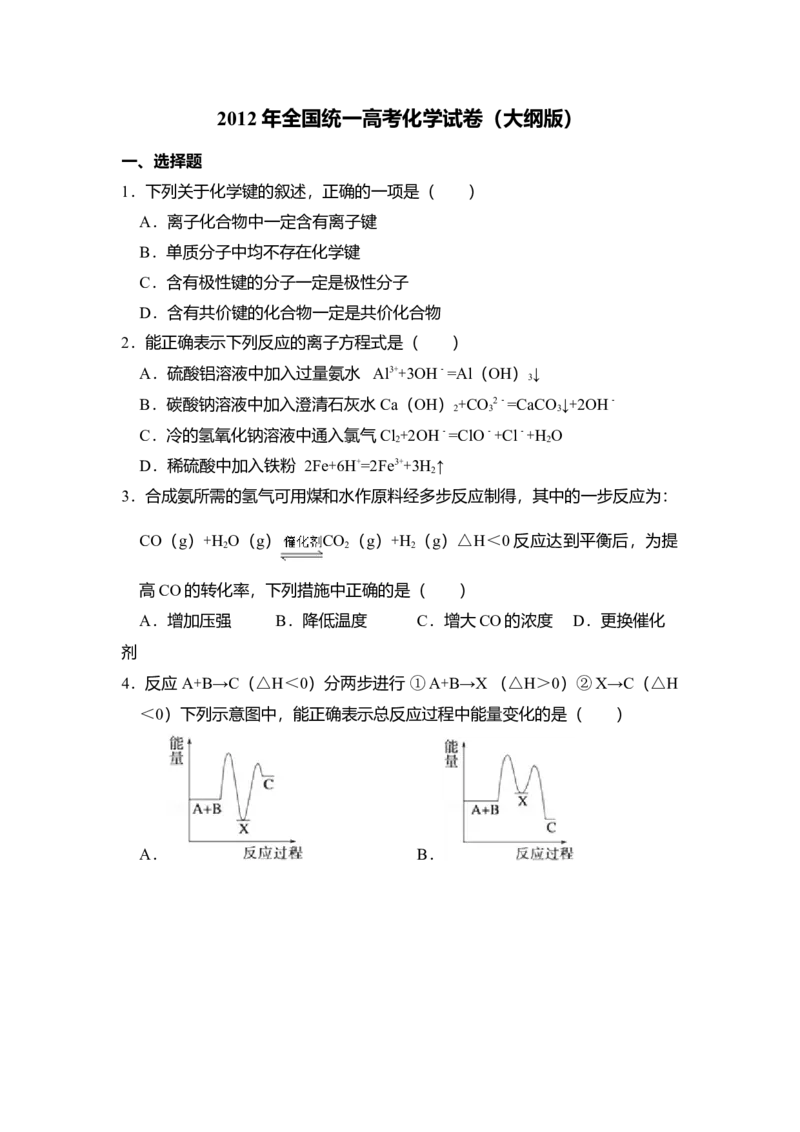
4.反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H
<0)下列示意图中,能正确表示总反应过程中能量变化的是( )
A. B.C. D.
5.元素X形成的离子与钙离子的核外电子排布相同,且 X的离子半径小于负
二价硫离子的半径.X元素为( )
A.Al B.P C.Ar D.K
6.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,
外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡
逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的
顺序是( )
A.①③②④ B.①③④② C.③④②① D.③①②④
7.在常压和 500℃条件下,等物质的量的 Ag O、Fe(OH) 、NH HCO 、
2 3 4 3
NaHCO 完全分解,所得气体体积依次为 V 、V 、V 、V ,体积大小顺序正
3 1 2 3 4
确的是( )
A.V >V >V >V B.V >V >V >V
3 2 4 1 3 4 2 1
C.V >V >V >V D.V >V >V >V
3 2 1 4 2 3 1 4
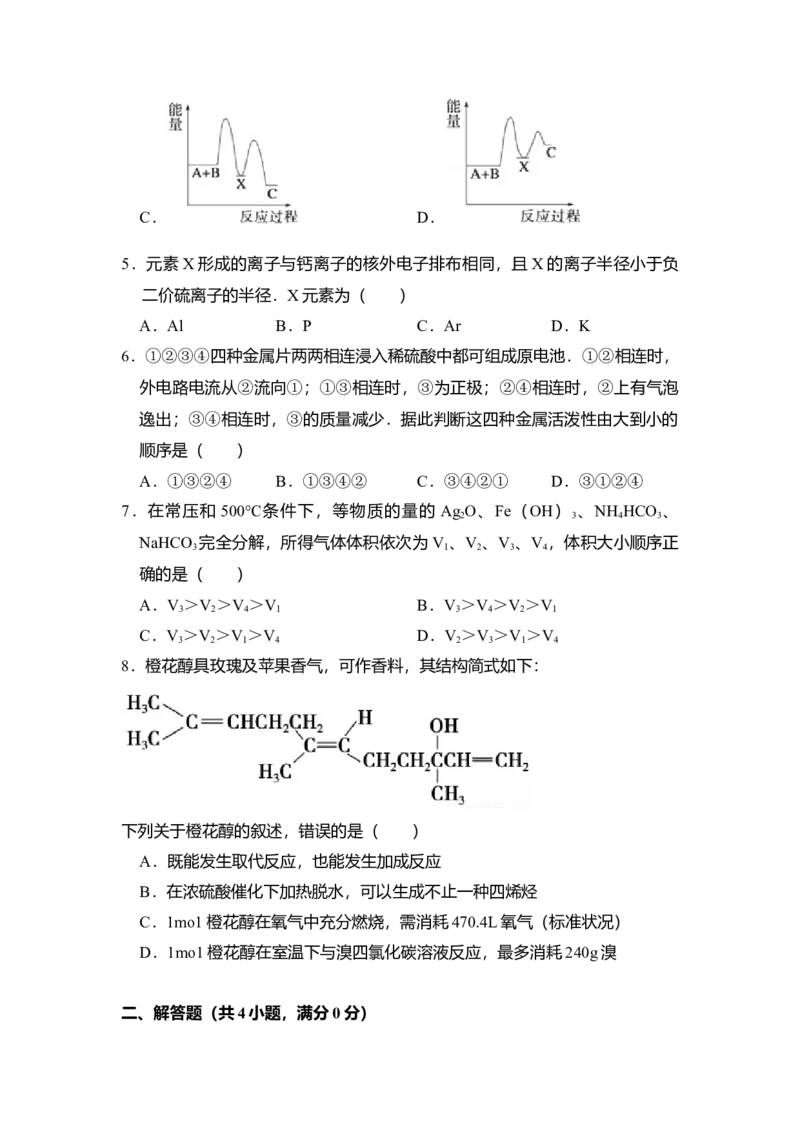
8.橙花醇具玫瑰及苹果香气,可作香料,其结构简式如下:
下列关于橙花醇的叙述,错误的是( )
A.既能发生取代反应,也能发生加成反应
B.在浓硫酸催化下加热脱水,可以生成不止一种四烯烃
C.1mo1橙花醇在氧气中充分燃烧,需消耗470.4L氧气(标准状况)
D.1mo1橙花醇在室温下与溴四氯化碳溶液反应,最多消耗240g溴
二、解答题(共4小题,满分0分)9.原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其
周期数的二倍;b和d的A B型氢化物均为 V型分子,c的+1价离子比e的
2
﹣1价离子少8个电子.
回答下列问题:
(1)元素a为 ,c为 ;
(2)由这些元素形成的双原子分子为 ;
(3)由这些元素形成的三原子分子中,分子的空间结构属于直线型的是 ,
非直线型的是 (写两种);
(4)这些元素的单质或由它们形成的AB型化合物中,其晶体类型属于原子晶
体的是 ,离子晶体的是 ,金属晶体的是 ,分子晶体的是
;(每空填一种)
(5)元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用
于防毒面具,该反应的化学方程式为 .
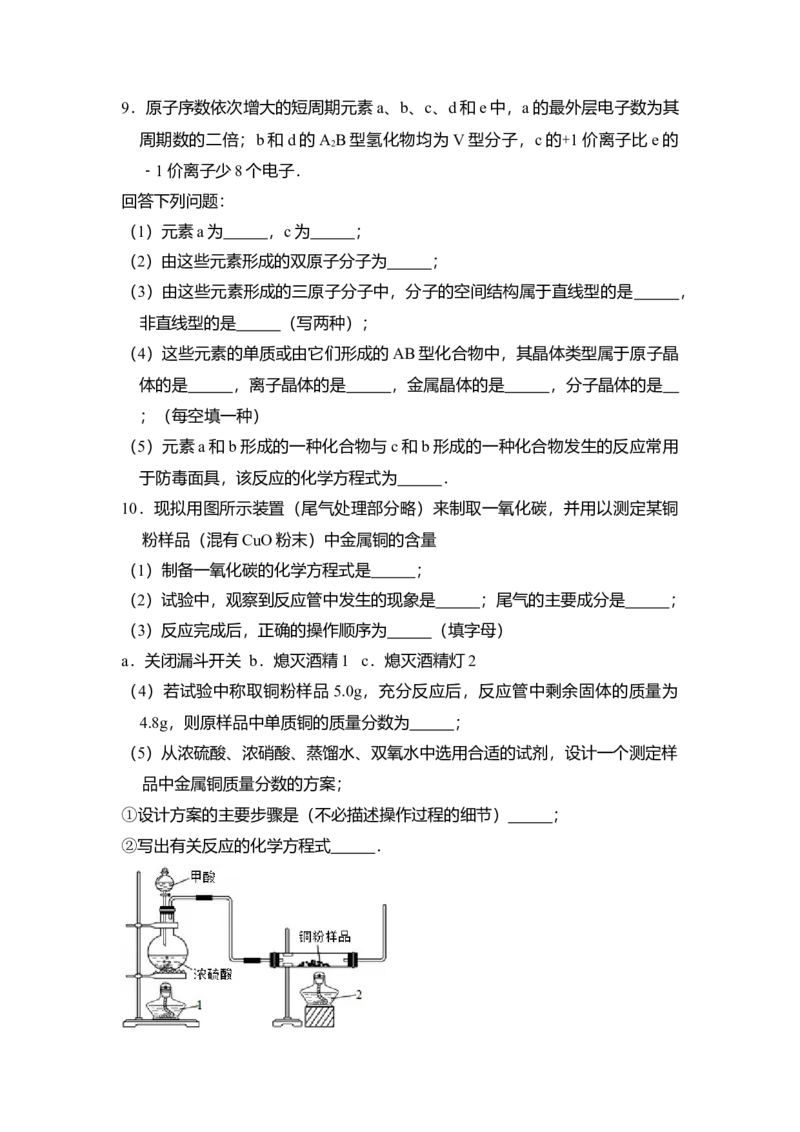
10.现拟用图所示装置(尾气处理部分略)来制取一氧化碳,并用以测定某铜
粉样品(混有CuO粉末)中金属铜的含量
(1)制备一氧化碳的化学方程式是 ;
(2)试验中,观察到反应管中发生的现象是 ;尾气的主要成分是 ;
(3)反应完成后,正确的操作顺序为 (填字母)
a.关闭漏斗开关 b.熄灭酒精1 c.熄灭酒精灯2
(4)若试验中称取铜粉样品 5.0g,充分反应后,反应管中剩余固体的质量为
4.8g,则原样品中单质铜的质量分数为 ;
(5)从浓硫酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,设计一个测定样
品中金属铜质量分数的方案;
①设计方案的主要步骤是(不必描述操作过程的细节) ;
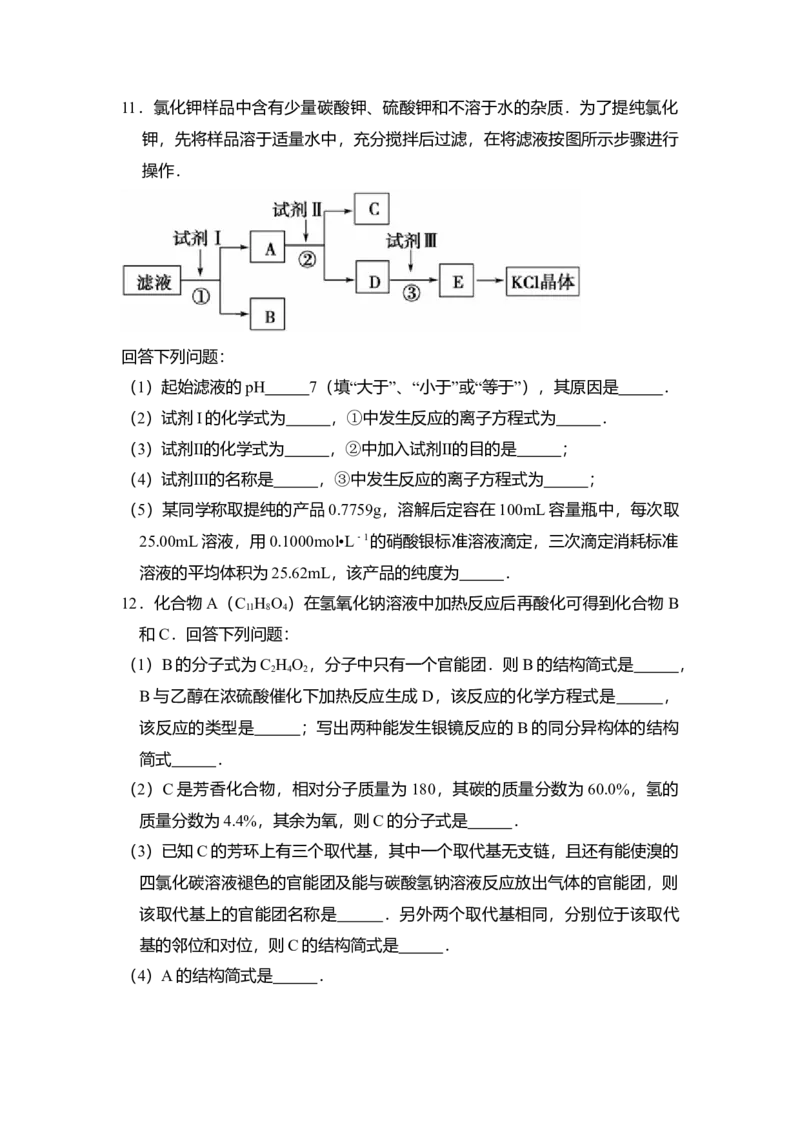
②写出有关反应的化学方程式 .11.氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质.为了提纯氯化
钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按图所示步骤进行
操作.
回答下列问题:
(1)起始滤液的pH 7(填“大于”、“小于”或“等于”),其原因是 .
(2)试剂I的化学式为 ,①中发生反应的离子方程式为 .
(3)试剂Ⅱ的化学式为 ,②中加入试剂Ⅱ的目的是 ;
(4)试剂Ⅲ的名称是 ,③中发生反应的离子方程式为 ;
(5)某同学称取提纯的产品0.7759g,溶解后定容在100mL容量瓶中,每次取
25.00mL溶液,用0.1000mol•L﹣1的硝酸银标准溶液滴定,三次滴定消耗标准
溶液的平均体积为25.62mL,该产品的纯度为 .
12.化合物A(C H O )在氢氧化钠溶液中加热反应后再酸化可得到化合物 B
11 8 4
和C.回答下列问题:
(1)B的分子式为C H O ,分子中只有一个官能团.则B的结构简式是 ,
2 4 2
B与乙醇在浓硫酸催化下加热反应生成 D,该反应的化学方程式是 ,
该反应的类型是 ;写出两种能发生银镜反应的 B的同分异构体的结构
简式 .
(2)C是芳香化合物,相对分子质量为 180,其碳的质量分数为 60.0%,氢的
质量分数为4.4%,其余为氧,则C的分子式是 .
(3)已知C的芳环上有三个取代基,其中一个取代基无支链,且还有能使溴的
四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则
该取代基上的官能团名称是 .另外两个取代基相同,分别位于该取代
基的邻位和对位,则C的结构简式是 .
(4)A的结构简式是 .