文档内容
2012年安徽高考理综化学
7.科学家最近研究出一种安全、环保的储氢方法,其原理可表示为:
储氢
释氢
NaHCO +H HCOONa+HO 下列有关说法正确的是
3 2 2
A.储氢、释氢过程均无能量变化
B. NaHCO 、 HCOONa均含有离子键和共价键
3
C. 储氢过程中NaHCO 被氧化
3
D. 释氢过程中,每消耗0.1molHO放出2.24L的H
2 2
8.下列离子或分子在溶液中能大量共存,通入CO 后仍能大量共存的一组是
2
A.K+、Ca2+、Cl-、NO - B. K+、Na+、Br-、SiO2-
3 3
C. H+、Fe2+、SO 2-、Cl D. K+、Ag+、NH ·HO、NO-
4 2 3 2 3
9.一定条件下,通过下列反应可实现燃煤烟气中硫的回收
催化剂
SO (g) +2CO(g) 2CO (g) +S(l) △H<0
2 2
若反应在恒容得密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡前,其它条件不变,分离出硫,正反应速率加快
C.平衡前,其它条件不变,升高温度可提高SO 的转化率
2
D.其它条件不变,使用不同催化剂,该反应的平衡常数不变
10.仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是
选项 实验目的 玻璃仪器
A 分离乙醇和乙酸乙酯的混合物 分液漏斗、烧杯
B 用PH=1的盐酸配置100mL PH=2 100mL容量瓶、烧杯、玻璃棒、胶头滴管
的盐酸
C 用溴水、淀粉-KI溶液比较Br 与I 试管、胶头滴管
2 2
的氧化性强弱
D 用NH Cl固体和Ca(OH) 固体制备并 酒精灯、烧杯、导管、集气瓶
4 2
收集NH
3
11.某兴趣小组设计如下微型实验装置。实验时,先断开
K ,闭合K ,两极均有气泡产生;一段时间后,断开
2 1
K,闭合K,发现电流表A指针偏转。
1 2
下列有关描述正确的是
A.断开K,闭合K 时,总反应的离子方程式为:
2 1
通电
2H++2Cl- H↑+Cl↑
2 2
B. 断开K,闭合K 时,石墨电极附近溶液变红
2 1
C. 断开K,闭合K 时,铜电极上的电极反应式为:
1 2
Cl+2e-=2Cl-
2
D. 断开K,闭合K 时,石墨电极作正极
1 212.氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
① HF(aq)+OH-(aq)= F-(aq)+ HO(l) △H=-67.7kJ·mol-1
2
② H+(aq)+OH-(aq) =HO(l) △H=-57.3kJ·mol-1
2
在20mL0.1mol·L-1的氢氟酸中加入VmL0.1mol·L-1的NaOH溶液。下列有关说法正确
的是
A.氢氟酸的电离方程式及热效应可表示为
HF(aq) F-(aq) + H+ (aq) △H=+10.4kJ·mol-1
B.当V=20时,溶液中: c (OH-)= c (HF)+c (F-)
C. 当V=20时,溶液中: c (F-)< c (Na+)=0.1mol·L-1
D. 当V>0时,溶液中一定存在: c (Na+)> c (F-) >c (OH-)>c (H+)
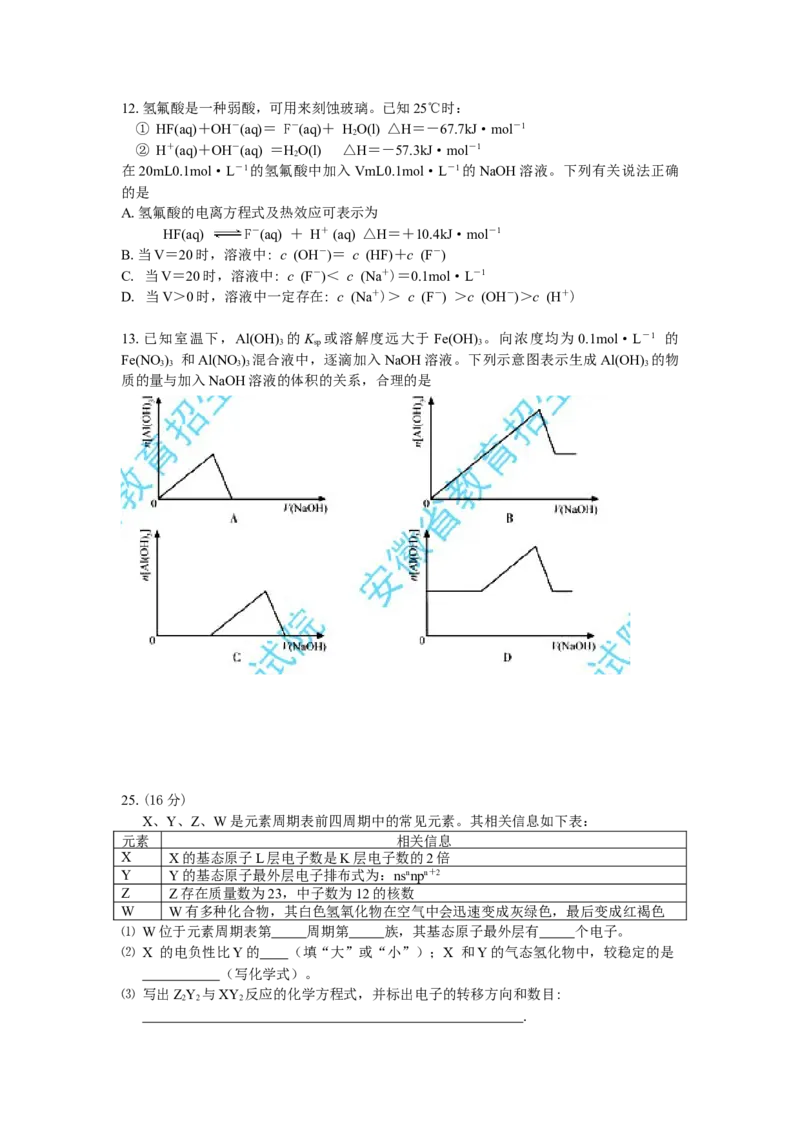
13.已知室温下,Al(OH) 的K 或溶解度远大于 Fe(OH) 。向浓度均为 0.1mol·L-1 的
3 sp 3
Fe(NO ) 和Al(NO ) 混合液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH) 的物
3 3 3 3 3
质的量与加入NaOH溶液的体积的关系,合理的是
25.(16分)
X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
元素 相关信息
X X的基态原子L层电子数是K层电子数的2倍
Y Y的基态原子最外层电子排布式为:nsnnpn+2
Z Z存在质量数为23,中子数为12的核数
W W有多种化合物,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色
⑴ W位于元素周期表第 周期第 族,其基态原子最外层有 个电子。
⑵ X 的电负性比Y的 (填“大”或“小”);X 和Y的气态氢化物中,较稳定的是
(写化学式)。
⑶ 写出ZY 与XY 反应的化学方程式,并标出电子的转移方向和数目:
2 2 2
.⑷ 在X的原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写
出其中一种分子的名称: 。氢元素、X、Y的原子也可共同形成多种分子和某种
常见的无机阴离子,写出其中一种分子和该无机阴离子反应的离子方程式:
。
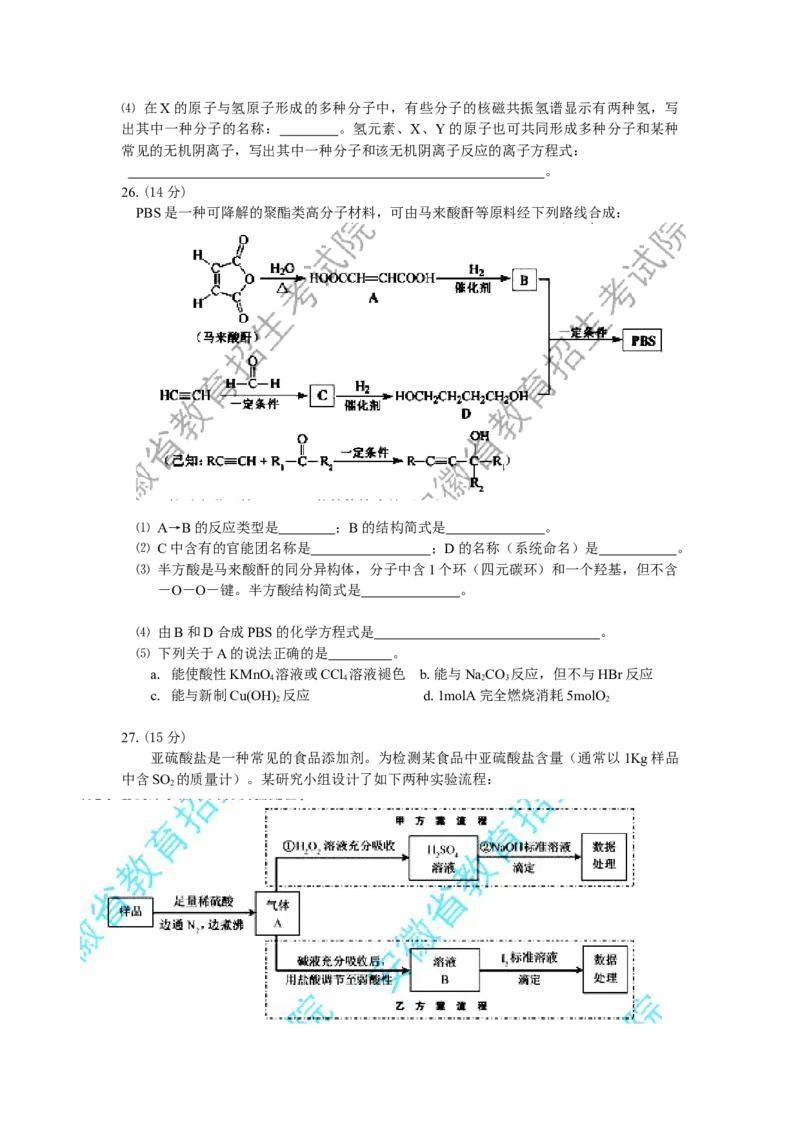
26.(14分)
PBS是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:
⑴ A→B的反应类型是 ;B的结构简式是 。
⑵ C中含有的官能团名称是 ;D的名称(系统命名)是 。
⑶ 半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和一个羟基,但不含
-O-O-键。半方酸结构简式是 。
⑷ 由B和D合成PBS的化学方程式是 。
⑸ 下列关于A的说法正确的是 。
a. 能使酸性KMnO 溶液或CCl 溶液褪色 b.能与NaCO 反应,但不与HBr反应
4 4 2 3
c. 能与新制Cu(OH) 反应 d.1molA完全燃烧消耗5molO
2 2
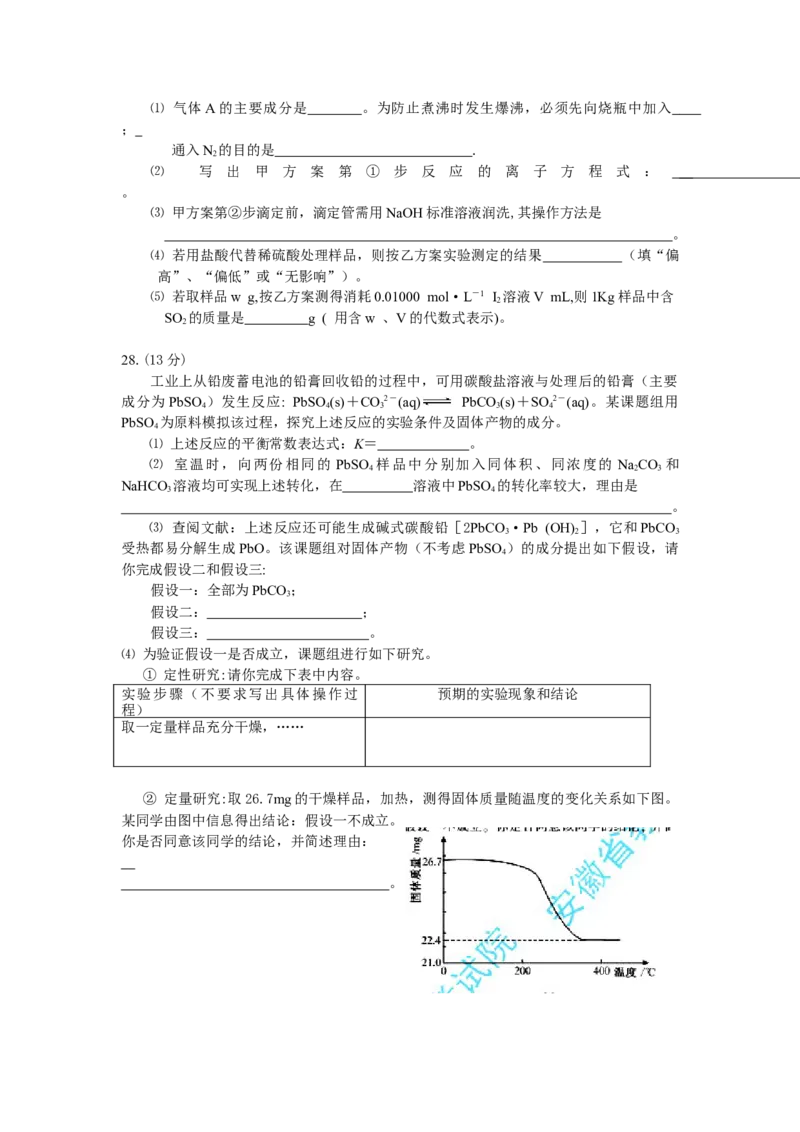
27.(15分)
亚硫酸盐是一种常见的食品添加剂。为检测某食品中亚硫酸盐含量(通常以1Kg样品
中含SO 的质量计)。某研究小组设计了如下两种实验流程:
2⑴ 气体A的主要成分是 。为防止煮沸时发生爆沸,必须先向烧瓶中加入
;
通入N 的目的是 .
2
⑵ 写 出 甲 方 案 第 ① 步 反 应 的 离 子 方 程 式 :
。
⑶ 甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是
。
⑷ 若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果 (填“偏
高”、“偏低”或“无影响”)。
⑸ 若取样品w g,按乙方案测得消耗0.01000 mol·L-1 I 溶液V mL,则1Kg样品中含
2
SO 的质量是 g ( 用含w 、V的代数式表示)。
2
28.(13分)
工业上从铅废蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要
成分为PbSO )发生反应: PbSO (s)+CO2-(aq) PbCO (s)+SO 2-(aq)。某课题组用
4 4 3 3 4
PbSO 为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
4
⑴ 上述反应的平衡常数表达式:K= 。
⑵ 室温时,向两份相同的 PbSO 样品中分别加入同体积、同浓度的 NaCO 和
4 2 3
NaHCO 溶液均可实现上述转化,在 溶液中PbSO 的转化率较大,理由是
3 4
。
⑶ 查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO ·Pb (OH) ],它和PbCO
3 2 3
受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO )的成分提出如下假设,请
4
你完成假设二和假设三:
假设一:全部为PbCO ;
3
假设二: ;
假设三: 。
⑷ 为验证假设一是否成立,课题组进行如下研究。
① 定性研究:请你完成下表中内容。
实验步骤(不要求写出具体操作过 预期的实验现象和结论
程)
取一定量样品充分干燥,……
② 定量研究:取26.7mg的干燥样品,加热,测得固体质量随温度的变化关系如下图。
某同学由图中信息得出结论:假设一不成立。
你是否同意该同学的结论,并简述理由:
。2012年安徽省高考理综化学答案
7. B 8.A 9.D 10.C 11.D 12.B 13.C