文档内容
2016 年全国统一考试(新课标 I 卷)
一、选择题:
7. 化学与生活密切相关。下列有关说法错误的是( )
A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度为95%
8. 设 为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 乙烯和丙烯混合气体中的氢原子数为
B.1 与4 反应生成的 分子数为
C.1 溶于过量硝酸,电子转移数为
D.标准状况下, 含有的共价键数为
9. 下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称为异丁烷 B.由乙烯生成乙醇属于加成反应
C. 有3种同分异构体 D. 油脂和蛋白质都属于高分子化合物
10.下列实验操作能达到实验目的的是( )
A.用长颈漏斗分离出乙酸与乙醇反应的产物
B.用向上排空气法收集铜粉与稀硝酸反应产生的
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释
D.将 与 混合气体通过饱和食盐水可得到纯净的
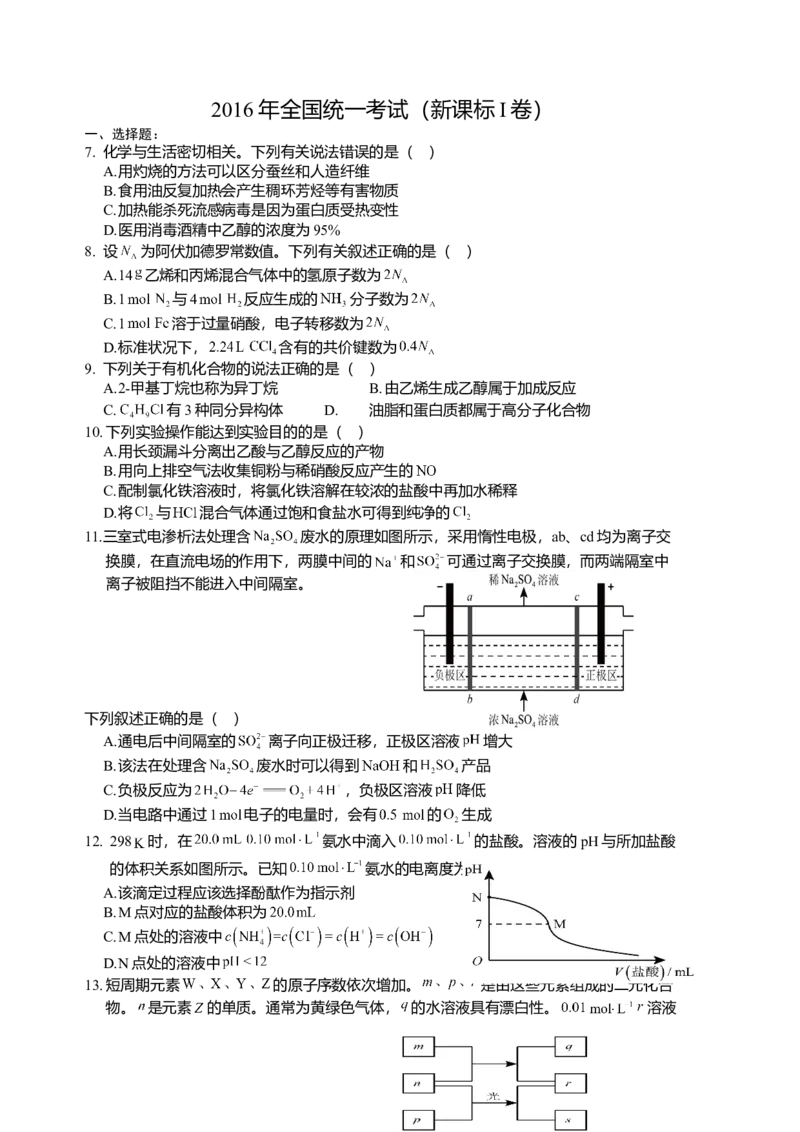
11.三室式电渗析法处理含 废水的原理如图所示,采用惰性电极,ab、cd均为离子交
换膜,在直流电场的作用下,两膜中间的 和 可通过离子交换膜,而两端隔室中
离子被阻挡不能进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的 离子向正极迁移,正极区溶液 增大
B.该法在处理含 废水时可以得到 和 产品
C.负极反应为 ,负极区溶液 降低
D.当电路中通过1 电子的电量时,会有 的 生成
12. 298 时,在 氨水中滴入 的盐酸。溶液的pH与所加盐酸
的体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为
C.M点处的溶液中
D.N点处的溶液中
13.短周期元素 的原子序数依次增加。 是由这些元素组成的二元化合
物。 是元素 的单质。通常为黄绿色气体, 的水溶液具有漂白性。 溶液的 为2, 通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确
的是( )
A. 原子半径的大小
B.元素的非金属性
C. 的氢化物常温常压下为液态
D. 的最高价氧化物的水化物为强酸
26. 氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用 将
还原生成 。某同学在实验室中对 与 反应进行了探究。回答下列问题:
(1)氨气的制备
①氨气的发生装置可以选择上图中的________,反应的化学方程式为 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置
(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
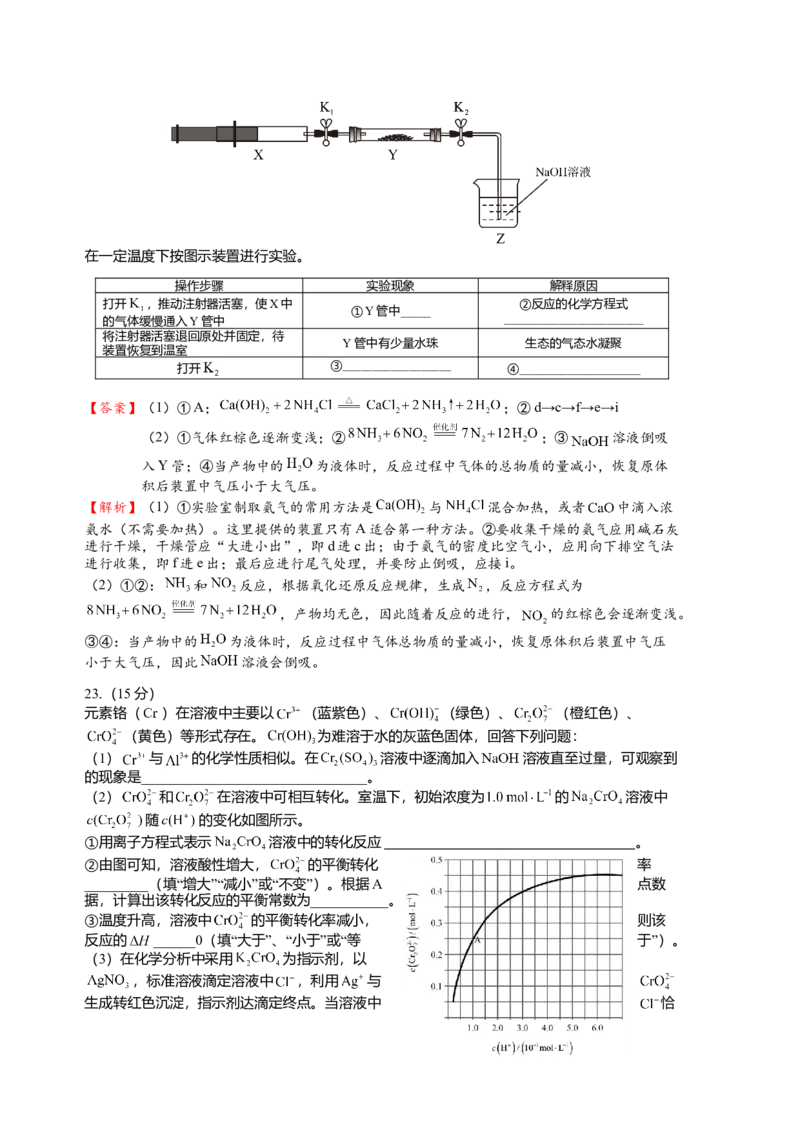
将上述收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端
用夹子 夹好)。
在一定温度下按图示装置进行实验。
操作步骤 实验现象 解释原因
打开 ,推动注射器活塞,
②反应的化学方程式
使X中的气体缓慢通入Y管 ①Y管中_____
_______________________
中
将注射器活塞退回原处并固
Y管中有少量水珠 生态的气态水凝聚
定,待装置恢复到温室
打开 ③__________________ ④____________________
14. (15分)
元素铬( )在溶液中主要以 (蓝紫色)、 (绿色)、 (橙红色)、
(黄色)等形式存在。 为难溶于水的灰蓝色固体,回答下列问题:
(1) 与 的化学性质相似。在 溶液中逐滴加入 溶液直至过量,可观
察到的现象是________________________________。
(2) 和 在溶液中可相互转化。室温下,初始浓度为 的 溶液
中 随 的变化如图所示。
①用离子方程式表示 溶液中的转化反应 。②由图可知,溶液酸性增大, 的平衡转化率_________
(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化
反应的平衡常数为___________。
③温度升高,溶液中 的平衡转化率减小,则该反应的
______0(填“大于”、“小于”或“等于”)。
(3)在化学分析中采用 为指示剂,以 ,标准溶
液滴定溶液中 ,利用 与 生成转红色沉淀,指示剂
达滴定终点。当溶液中 恰好沉淀完全(浓度等于
)时,溶液中 为__________ ,此
时溶液中 等于__________ 。(已知 的 分别为 和
)。
(4) 价铬的化合物毒性较大,常用 将废液中的 还原成 ,该反应的离
子方程式为______________________________________________________________。
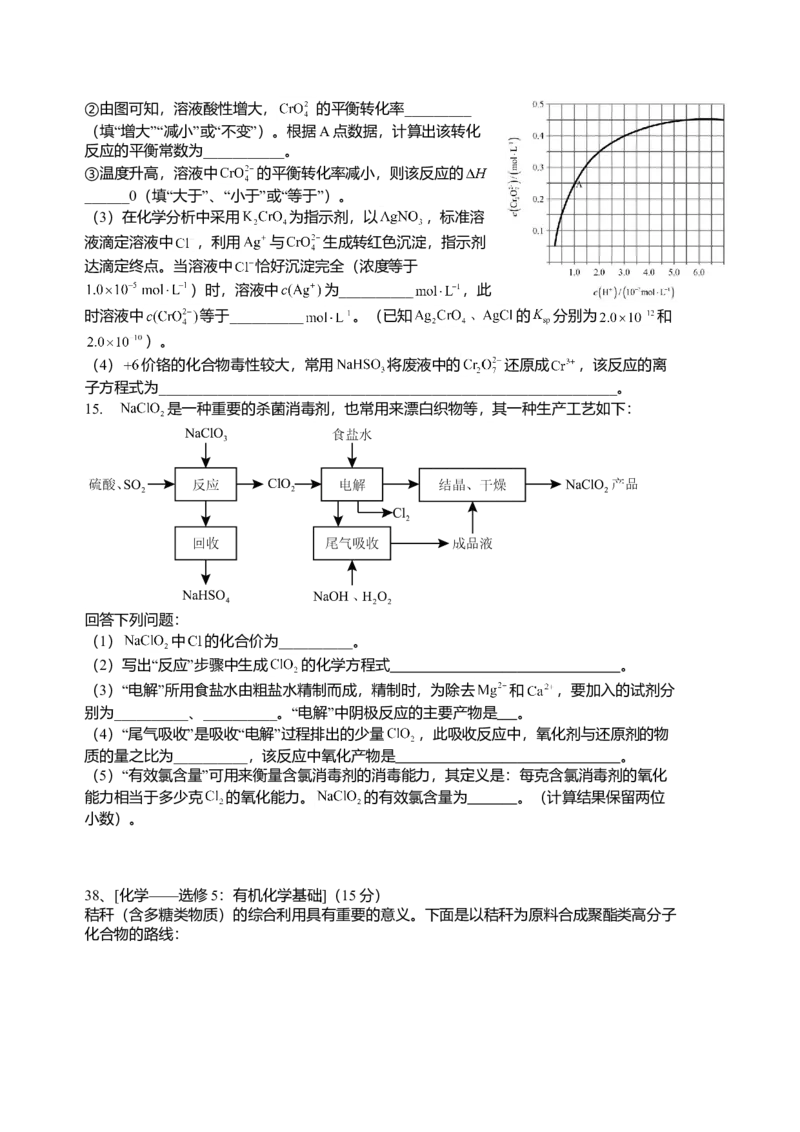
15. 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1) 中 的化合价为__________。
(2)写出“反应”步骤中生成 的化学方程式 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和 ,要加入的试剂分
别为__________、__________。“电解”中阴极反应的主要产物是 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物
质的量之比为__________,该反应中氧化产物是 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化
能力相当于多少克 的氧化能力。 的有效氯含量为 。(计算结果保留两位
小数)。
38、[化学——选修5:有机化学基础](15分)
秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子
化合物的路线:回答下列问题:
(1)下列关于糖类的说法正确的是__________。(填标号)
a.糖类都有甜味,具有 的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为__________。
(3)D中的官能团名称为__________,D生成E的反应类型为__________。
(4)F的化学名称是__________,由F生成G的化学方程式为__________。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体, W与足量碳酸氢钠
溶液反应生成 ,W共有__________种(不含立体异构),其中核磁共振氢谱为三组
峰的结构简式为__________。
(6)参照上述合成路线,以 , 和 为原料(无机试剂任选),设计
制备对苯二甲酸的合成路线__________。
一、选择题:
16.化学与生活密切相关。下列有关说法错误的是( )
A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度为95%【答案】D
【解析】A、蚕丝的主要成分为蛋白质,灼烧时会有烧焦羽毛的气味,而人造纤维由纤维素改性
得到,灼烧时有刺激性气味,可由此区分二者,故A正确。
B、食用油反复加热,碳链会变成环状,产生稠环芳烃等有害物质,故B正确。
C、加热、强酸碱、重金属盐均可以使蛋白质变性,因此加热可杀死流感病毒,故C正确。
D、医用酒精中乙醇的浓度为75%,工业酒精中乙醇的浓度为95%,故D错误。
因此,本题选D。
17.设 为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 乙烯和丙烯混合气体中的氢原子数为
B.1 与4 反应生成的 分子数为
C.1 溶于过量硝酸,电子转移数为
D.标准状况下, 含有的共价键数为
【答案】A
【解析】A、乙烯和丙烯最简式均为为 , 混合气体中含有的原子团 的物质的量为
,含有的氢原子数为 ,故A正确。
B、若 的 与 的 完全反应则生成 ,但此反应是可逆反应,反应不完全,
所以 分子数小于 ,故B错误。
C、 溶于过量硝酸,由于硝酸具有强氧化性,最终氧化产物是 ,因此 与过量硝酸
反应转移 电子,故C错误。
D、标准状况下, 呈液态, 不能由气体摩尔体积得出其物质的量为 ,故
其含有的共价键数也不为 ,故D错误。
因此,本题选A。
18.下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称为异丁烷
B.由乙烯生成乙醇属于加成反应
C. 有3种同分异构体
D.油脂和蛋白质都属于高分子化合物
【答案】B
【解析】A、2-甲基丁烷,其结构简式为 ,共5个碳,习惯命名法应该为异戊烷,
故A错误。
B、乙烯生成乙醇的反应方程式为: ,符合加成反应的定
义,故B正确。
C、 有4种同分异构体,分别为 、 、 、
,故C错误。
D、高分子化合物要求分子量在10000以上,油脂是高级脂肪酸甘油酯,不属于高分子化合物,
故D错误。
因此,本题选B。
19.下列实验操作能达到实验目的的是( )A.用长颈漏斗分离出乙酸与乙醇反应的产物
B.用向上排空气法收集铜粉与稀硝酸反应产生的
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释
D.将 与 混合气体通过饱和食盐水可得到纯净的
【答案】C
【解析】A、乙酸和乙醇反应的产物为乙酸乙酯,分离乙酸乙酯应该用分液漏斗,长颈漏斗不带
有活塞,无法用于分离操作,故A错误。
B、 会与空气中的氧气反应生成 ,且NO密度与空气相近,故不能用排空气法收集,故
B错误。
C、氯化铁易发生水解,所以配制时应在较浓的盐酸中溶解,抑制其水解,防止生成沉淀,再加
水稀释,故C正确。
D、将 与 的混合气体通过饱和食盐水可除去其中的 ,但是得到的 未干燥,会含有
水蒸气,故D错误。
因此,本题选C。
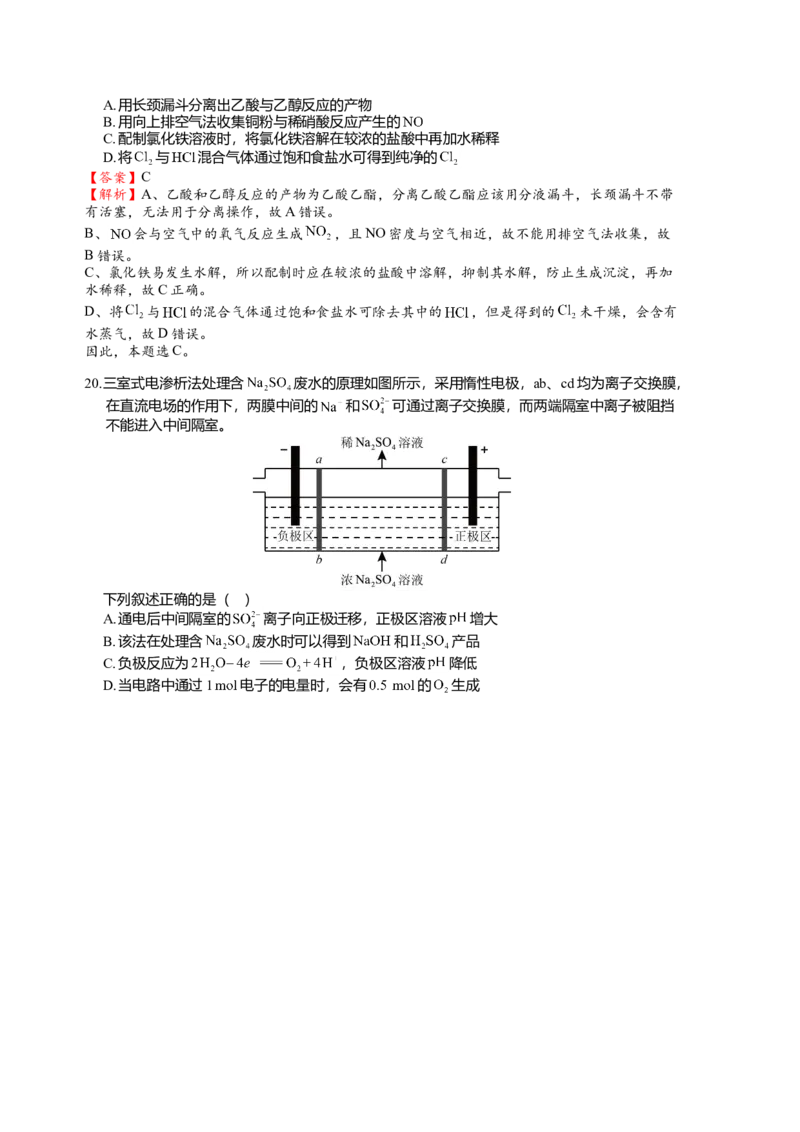
20.三室式电渗析法处理含 废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,
在直流电场的作用下,两膜中间的 和 可通过离子交换膜,而两端隔室中离子被阻挡
不能进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的 离子向正极迁移,正极区溶液 增大
B.该法在处理含 废水时可以得到 和 产品
C.负极反应为 ,负极区溶液 降低
D.当电路中通过1 电子的电量时,会有 的 生成【答案】B
【解析】直流电作用下电解硫酸钠溶液,由于钠离子与硫酸根在水溶液中均不放电,因此其本质
为电解水。
A、电流从正极流出,负极流入, 为阴离子,其移动方向应与电流相反,因此 向正极
区(阳极)移动。正极区发生氧化反应,电极反应为 ,则正极附近酸
性增强,pH下降。故A项错误。
B、负极区(阴极)的电极反应为 ,剩余 ,中间区域的 迁移
到负极区,得到 ;正极区的电极反应为 ,余下 ,中间区域的
迁移到正极区,得到 ,故B项正确。
C、负极区发生还原反应: ,负极附近碱性增强,pH升高,故C错误。
D、由正极区的电极反应可知,转移电子与产生氧气的物质的量之比为4:1,因此转移 电子
时会有 氧气生成,故D项错误。
因此,本题选B。
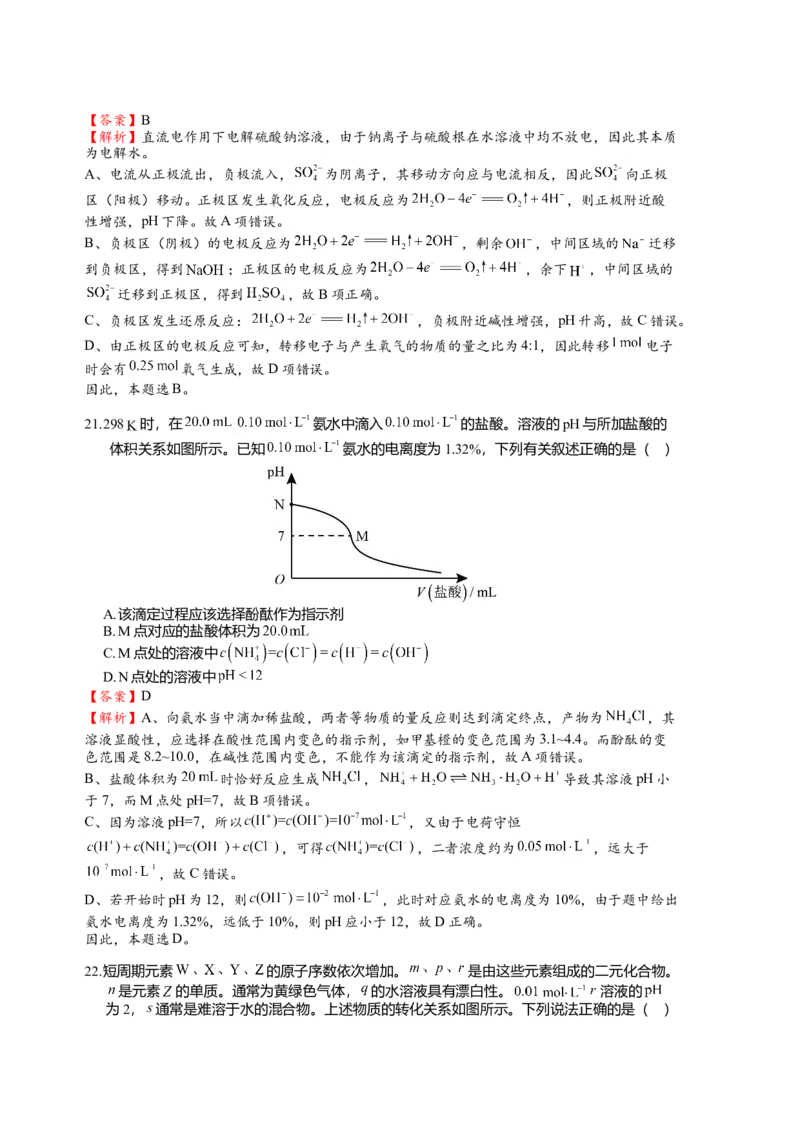
21.298 时,在 氨水中滴入 的盐酸。溶液的pH与所加盐酸的
体积关系如图所示。已知 氨水的电离度为1.32%,下列有关叙述正确的是( )
A.该滴定过程应该选择酚酞作为指示剂
B.M点对应的盐酸体积为
C.M点处的溶液中
D.N点处的溶液中
【答案】D
【解析】A、向氨水当中滴加稀盐酸,两者等物质的量反应则达到滴定终点,产物为 ,其
溶液显酸性,应选择在酸性范围内变色的指示剂,如甲基橙的变色范围为3.1~4.4。而酚酞的变
色范围是8.2~10.0,在碱性范围内变色,不能作为该滴定的指示剂,故A项错误。
B、盐酸体积为 时恰好反应生成 , 导致其溶液pH小
于7,而M点处pH=7,故B项错误。
C、因为溶液pH=7,所以 ,又由于电荷守恒
,可得 ,二者浓度约为 ,远大于
,故C错误。
D、若开始时pH为12,则 ,此时对应氨水的电离度为10%,由于题中给出
氨水电离度为1.32%,远低于10%,则pH应小于12,故D正确。
因此,本题选D。
22.短周期元素 的原子序数依次增加。 是由这些元素组成的二元化合物。
是元素 的单质。通常为黄绿色气体, 的水溶液具有漂白性。 溶液的
为2, 通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )A.原子半径的大小
B.元素的非金属性
C. 的氢化物常温常压下为液态
D. 的最高价氧化物的水化物为强酸
【答案】C
【解析】Z的单质 为黄绿色气体, 为 ,因此Z为氯元素。 的水溶液pH值为
2,说明 为一元强酸。 与 在光的条件下反应得到 以及难溶于水的混合物 ,因此 为烷
烃(如 ), 为 , 为发生取代反应后的有机混合物。 与 反应可得 以及具有
漂白性的 ,可知 为 , 为 。综上,W、X、Y、Z分别为 、 、 、 。
A、原子半径大小排序为 ,即WX,故B错误。
C、Y为氧元素,其氢化物为 或 ,常温下均为液态,故C正确。
D、X为碳元素,其最高价氧化物的水化物为碳酸,是弱酸,故D错误。
因此,本题选C。
26.(14分)
氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用 将 还原
生成 。某同学在实验室中对 与 反应进行了探究。回答下列问题:
(1)氨气的制备
①氨气的发生装置可以选择上图中的________,反应的化学方程式为 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置
(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两端用夹
子 夹好)。在一定温度下按图示装置进行实验。
操作步骤 实验现象 解释原因
打开 ,推动注射器活塞,使X中 ②反应的化学方程式
①Y管中_____
的气体缓慢通入Y管中 _______________________
将注射器活塞退回原处并固定,待
Y管中有少量水珠 生态的气态水凝聚
装置恢复到温室
打开 ③__________________ ④____________________
【答案】(1)①A; ;②d→c→f→e→i
(2)①气体红棕色逐渐变浅;② ;③ 溶液倒吸
入Y管;④当产物中的 为液体时,反应过程中气体的总物质的量减小,恢复原体
积后装置中气压小于大气压。
【解析】(1)①实验室制取氨气的常用方法是 与 混合加热,或者 中滴入浓
氨水(不需要加热)。这里提供的装置只有A适合第一种方法。②要收集干燥的氨气应用碱石灰
进行干燥,干燥管应“大进小出”,即d进c出;由于氨气的密度比空气小,应用向下排空气法
进行收集,即f进e出;最后应进行尾气处理,并要防止倒吸,应接i。
(2)①②: 和 反应,根据氧化还原反应规律,生成 ,反应方程式为
,产物均无色,因此随着反应的进行, 的红棕色会逐渐变浅。
③④:当产物中的 为液体时,反应过程中气体总物质的量减小,恢复原体积后装置中气压
小于大气压,因此 溶液会倒吸。
23.(15分)
元素铬( )在溶液中主要以 (蓝紫色)、 (绿色)、 (橙红色)、
(黄色)等形式存在。 为难溶于水的灰蓝色固体,回答下列问题:
(1) 与 的化学性质相似。在 溶液中逐滴加入 溶液直至过量,可观察到
的现象是________________________________。
(2) 和 在溶液中可相互转化。室温下,初始浓度为 的 溶液中
随 的变化如图所示。
①用离子方程式表示 溶液中的转化反应 。
②由图可知,溶液酸性增大, 的平衡转化 率
_________(填“增大”“减小”或“不变”)。根据A 点数
据,计算出该转化反应的平衡常数为___________。
③温度升高,溶液中 的平衡转化率减小, 则该
反应的 ______0(填“大于”、“小于”或“等 于”)。
(3)在化学分析中采用 为指示剂,以
,标准溶液滴定溶液中 ,利用 与
生成转红色沉淀,指示剂达滴定终点。当溶液中 恰好沉淀完全(浓度等于 )时,溶液中 为__________ ,此时溶液
中 等于__________ 。(已知 的 分别为 和
)。
(4) 价铬的化合物毒性较大,常用 将废液中的 还原成 ,该反应的离子方
程式为______________________________________________________________。
【答案】(1)蓝紫色溶液变浅,同时生成灰蓝色沉淀,继续滴加NaOH溶液,沉淀溶解,最终
溶液变绿色
(2)① ②增大; ;③小于
(3) ;
(4)
或:
【解析】(1)类比 与 反应的性质,但需注意反应过程中伴有颜色变化。 为蓝紫
色,滴加 后蓝紫色变浅同时产生灰蓝色沉淀 ,继续滴加,沉淀溶解, 变
为 ,溶液最终变为绿色。
(2)①选修四26页的方程式, 在酸性条件会转化为 。②从图上可以看出,
浓度升高, 浓度上升,说明反应向右进行的更多, 的平衡转化率增大;根据A
点数据,列三段式计算平衡常数:
③升高温度,溶液中 平衡转化率减小,说明反应逆向移动,故该反应为放热反应,
。
(3)已知 , , ,当根据沉
淀溶解平衡可得:
,
。
(4) 盐溶液为酸性,因此配平时应在方程式左边添加 或 。
24. 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:回答下列问题:
(1) 中 的化合价为__________。
(2)写出“反应”步骤中生成 的化学方程式 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和 ,要加入的试剂分别为
__________、__________。“电解”中阴极反应的主要产物是 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的
量之比为__________,该反应中氧化产物是 。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力
相当于多少克 的氧化能力。 的有效氯含量为 。(计
算结果保留两位小数)。
【答案】(1)+3
(2)
(3) ; ;
(4) ,
(5)
【解析】(1) 中Na为+1价,O为-2价,计算可得 的化合价为 。
(2)由流程图可知反应物为 、 和 ,产物为 和 ,根据氧化还原
化合价升降守恒进行配平,可得方程式为:
(3)粗盐提纯过程,主要考虑除去杂质离子,且不引入新的杂质,故加入 除去 、加
入 除去 ;电解食盐水并加入 ,产物中有 生成,由于阴极发生还原反应,
所以应该是 在阴极被还原生成 。
(4)根据尾气吸收过程中加入的反应物和生成物,写出氧化还原反应方程式并配平,可得:
。其中氧化剂为 ,还原剂为 ,氧化
剂与还原剂的比值为 ,该反应的氧化产物为 。
(5)“有效氯含量”的定义是每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。其实就
是求相同质量的 和 在还原为 时,转移的电子数之比。 还原为 时
转移 电子, 还原为 时转移 电子,也就是说每摩尔 相当于
。即 相当于 ,即“有效氯含量”= (保留两位小数)。
36.[化学——选修2:化学与技术](15分)
高锰酸钾( )是一种常见氧化剂。主要用于化工、防腐及制药工业等。以软锰矿(主要
成分为 )为原料生产高锰酸钾的工艺路线如下:
回答下列问题:
(1)原料软锰矿与氢氧化钾按 的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是
______________。
(2)“平炉”中发生反应的化学方程式为 。
(3)“平炉”中需要加压,其目的是 。(4)将 转化为 的生产有两种工艺。
①“ 歧化法”是传统工艺,即在 溶液中通入 气体,使体系呈中性或弱酸性,
发生歧化反应。反应中生成 和__________(写化学式)。
②“电解法”为现代工艺,即电解 水溶液。电解槽中阳极发生的电极反应为__________,
阴极逸出的气体是__________。
③“电解法”和“ 歧化法”中, 的理论利用率之比为__________。
(5)高锰酸钾纯度的测定:称取 样品,溶解后定容于 容量瓶中,摇匀。取浓度
为 的 标准溶液 ,加入稀硫酸酸化,用 溶液平行滴定三次,
平均消耗的体积为 。该样品的纯度为__________(列出计算式即可,已知
)。
【答案】(1)增大接触面积,提高反应速率。
(2) 。
(3)增大压强,提高反应速率。
(4)① ;② ; ;③
(5)
【解析】(1)影响固体反应速率的因素之一是接触面积,粉碎矿石可增大其接触面积,提高反
应速率。
(2)由题目可知 转化为 , 作还原剂,氧化剂应为空气中的 ,反应物还
有 ,根据氧化还原基本原理配平方程式即可。
(3)反应不是可逆反应,加压应从反应速率的方面来考虑。由于此反应有气体参加,增大压强,
氧气的浓度提高,反应速率提高。
(4)①由于反应体系为中性或弱酸性, 没有变价,产物应为 ,故反应的方程式为:
②阳极反应为氧化反应, 被氧化为 ,电极反应为 ;阴极反应
为还原反应,电极反应为 ,故阴极产生的气体为 ;总反应为
③电解中所有的 都转化成了 ,而歧化反应中只有 的 转化为了 ,
因此利用率之比为 ,即 。
(5)由题中反应方程式得到 与 反应的比例为 ,列式计算:
即:
代入数据得:
37.[化学——选修3:物质结构与性质](15分)
锗( )是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:(1)基态 原子的核外电子排布式为 __________,有__________个未成对电子。
(2) 与 是同族元素, 原子之间可以形成双键、叁键,但 原子之间难以形成双键或叁
键,从原子结构角度分析,原因是 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因 。
熔点/℃ 26 146
沸点/℃ 186 约400
(4)光催化还原 制备 反应中,带状纳米 是该反应的良好催化剂, 、 、
电负性由大至小的顺序是____________________。
(5) 单晶具有金刚石型结构,其中 原子的杂化方式为__________,微粒之间存在的作用
力是__________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数
A为 ;B为 ;C为 。则D原子的坐标参数为 。
②晶胞参数,描述晶胞的大小和形状。已知 单晶的晶胞参数 ,其密度为
__________ (列出计算式即可)。
【答案】(1) ;2。
(2) 原子半径较大,难以形成稳定的 键,不易形成双键或叁键。
(3) 、 、 的熔沸点依次上升。因为其组成和结构相似的物质,随分
子量增大,范德华力增大,熔沸点上升。
(4) 。
(5) ,共价键。
(6)① ;② 。
【解析】(1)锗位于硅的正下方,是 号元素,核外电子排布为 。
(2)双键、叁键与单键中均有 键,但只有双键和叁键中存在 键。锗难以形成双键或叁键,
说明锗难以形成稳定的 键。这是因为 原子半径较大,4p形成肩并肩重叠较难。
(3)由表中数据可知,三种物质熔沸点均不高,均为分子晶体,并且不存在氢键,因此熔沸点
由范德华作用力的强弱决定。即熔沸点依次升高,是范德华力依次增强的结果,而对于组成和结
构相似的物质而言,范德华力主要受分子量决定。分子量越大,范德华力越大,熔沸点越高。
(4)由三种元素在周期表的相对位置可知电负性相对强弱。
(5)锗与金刚石结构相似,金刚石中碳原子是 杂化,锗晶体中锗也是相同的杂化,原子间以
共价键结合。
(6)①将晶胞切成8个相同的小正方体后,D是左下角小正方体的体心,因此原子坐标是
;②每个晶胞中含有8个锗原子,根据密度公式进行计算,注意换算单位:
25.[化学——选修5:有机化学基础](15分)
秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合
物的路线:
回答下列问题:
(1)下列关于糖类的说法正确的是__________。(填标号)
a.糖类都有甜味,具有 的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为__________。
(3)D中的官能团名称为__________,D生成E的反应类型为__________。
(4)F的化学名称是__________,由F生成G的化学方程式为__________。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体, W与足量碳酸氢钠溶
液反应生成 ,W共有__________种(不含立体异构),其中核磁共振氢谱为三组峰的
结构简式为__________。
(6)参照上述合成路线,以 , 和 为原料(无机试剂任选),设计制
备对苯二甲酸的合成路线__________。
【答案】(1)cd
(2)取代反应(酯化反应)
(3)酯基、碳碳双键;氧化反应
(4)1,6-己二酸(己二酸);
(5)12;
(6)
【解析】(1)糖类不一定都有甜味,比如淀粉和纤维素;糖类也不一定具有 的通式,
比如脱氧核糖( )、鼠李糖( )等,故a错误;一分子麦芽糖水解得到两分子
葡萄糖,蔗糖水解得到葡萄糖和果糖,故b错误;淀粉水解得到葡萄糖,银镜反应能用于检验含有醛基的葡萄糖,只能检验淀粉是否发生水解,不能检验是否水解完全,故c正确;淀粉和纤维
素属于多糖,也属于天然高分子化合物(选修五课本p83),故d正确。
(2)C分子式为 ,不饱和度为4,相比B增加了2个C,结合D中的酯基,说明C是由
B与2分子 发生酯化反应,从反应类型说,酯化反应也可认为是取代反应,故答案为取
代反应或酯化反应。
(3)D生成E为失氢的过程,为氧化反应。
(4)F的系统名称为1,6-己二酸;F和1,4-丁二烯生成聚酯G为羧基和羟基的缩聚反应(注意不
要漏掉端基原子和小分子 )。
(5)0.5 W与足量 生成1 ,说明W中含有两个羧基。E不饱和度为6,除
苯环和2个羧基以外的碳原子均饱和。又已知W为二取代芳香化合物,对两个取代基进行分类:
、 、 、 ,共4种情况,分
别有邻、间、对三种位置异构,故共有 种。核磁共振氢谱为三组峰,说明对称性较好,应
为对位的对称二取代物,其结构简式为
(6)根据推断可知,C为 ,C与 反应可以成环生成D(
),D在 催化下加热,可得E(
)。仿照上述反应进行过程,可得(反,反)-2,4-己二烯(
)可与 反应生成 (该反应2014年新课标II卷和2011年全
国卷也有出现),在 催化下加热,可得 。仿照课本甲苯被 酸性溶
液氧化的过程,可得 可被 酸性溶液氧化为对苯二甲酸(
)。