文档内容
一、选择题(本题包括 13小题.每小题只有一个选项符合题意)
7.化学与生产和生活密切相关,下列说法正确的是
A.聚乙烯塑料的老化是因为发生了加成反应
B.煤经过气化和液化等物理变化可转化为清洁燃料
C.合成纤维、人造纤维及碳纤维都属于有机高分子材料
D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
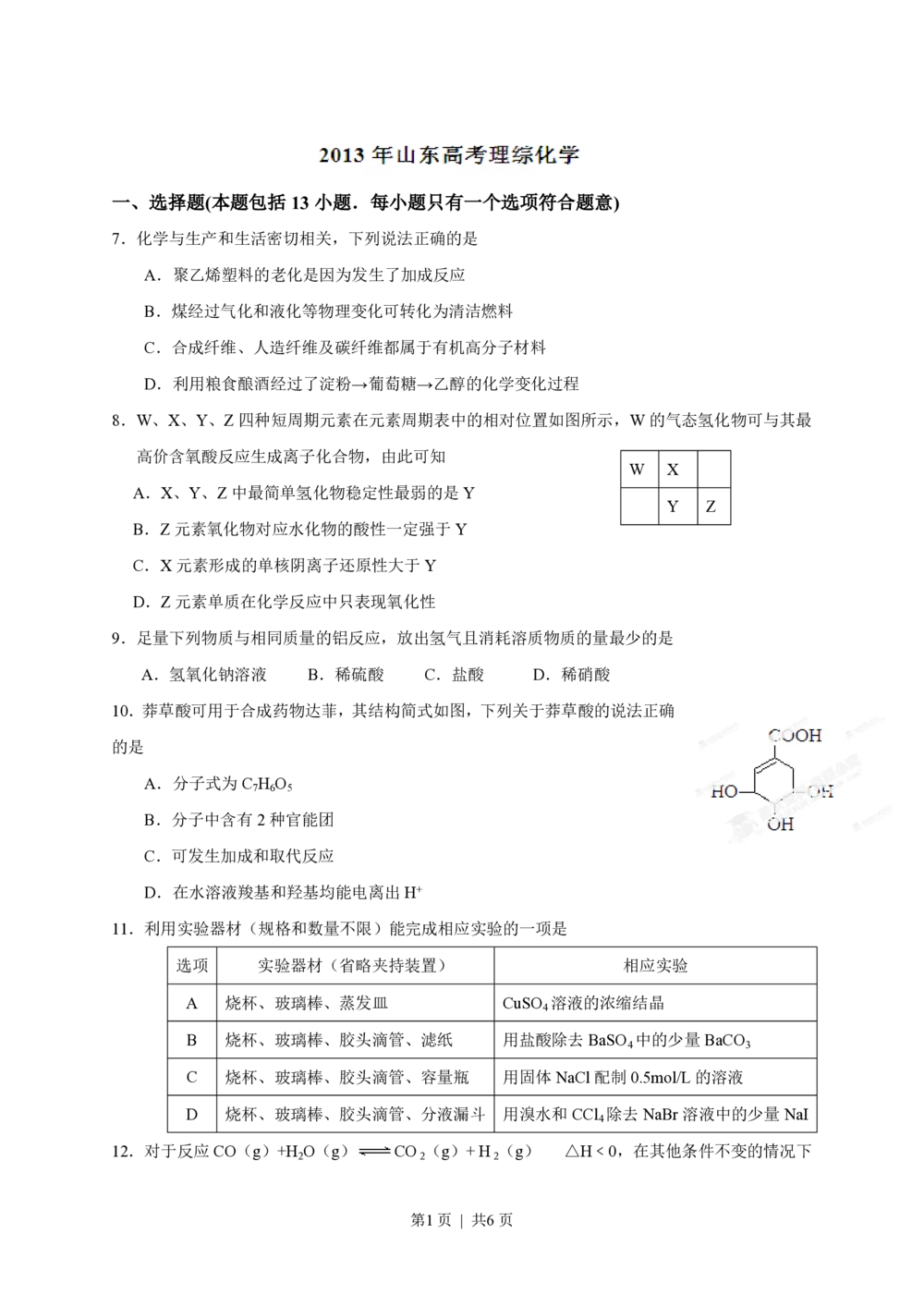
8.W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最
高价含氧酸反应生成离子化合物,由此可知
W X
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
Y Z
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
9.足量下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是
A.氢氧化钠溶液 B.稀硫酸 C.盐酸 D.稀硝酸
10.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确
的是
A.分子式为C H O
7 6 5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
11.利用实验器材(规格和数量不限)能完成相应实验的一项是
选项 实验器材(省略夹持装置) 相应实验
A 烧杯、玻璃棒、蒸发皿 CuSO 溶液的浓缩结晶
4
B 烧杯、玻璃棒、胶头滴管、滤纸 用盐酸除去BaSO 中的少量BaCO
4 3
C 烧杯、玻璃棒、胶头滴管、容量瓶 用固体NaCl配制0.5mol/L的溶液
D 烧杯、玻璃棒、胶头滴管、分液漏斗 用溴水和CCl 除去NaBr溶液中的少量NaI
4
12.对于反应CO(g)+H O(g) CO (g)+ H (g) △H﹤0,在其他条件不变的情况下
2 2 2
第1页 | 共6页A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
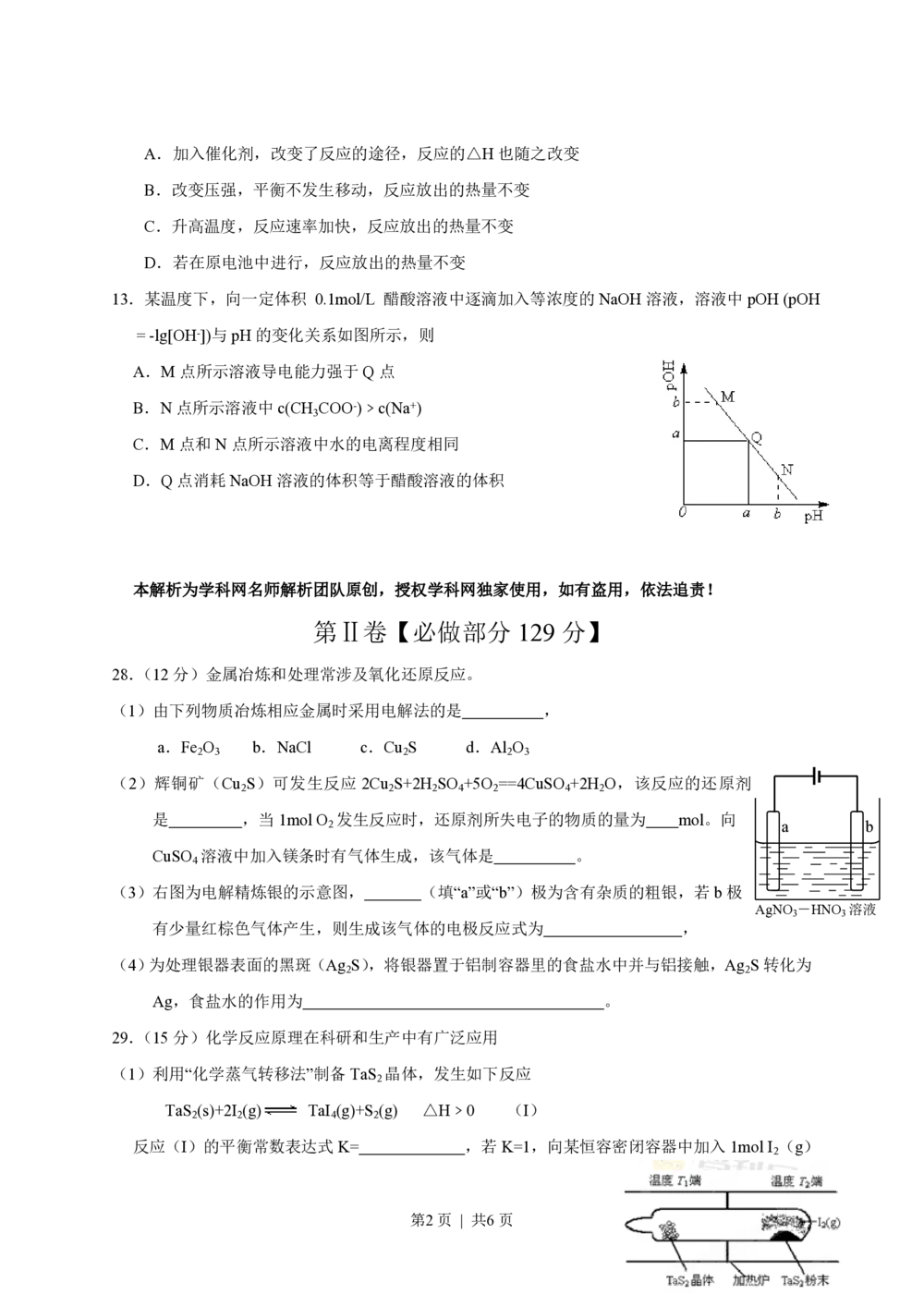
13.某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH (pOH
= -lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH COO-)﹥c(Na+)
3
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
本解析为学科网名师解析团队原创,授权学科网独家使用,如有盗用,依法追责!
第Ⅱ卷【必做部分 129 分】
28.(12分)金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是 ,
a.Fe O b.NaCl c.Cu S d.Al O
2 3 2 2 3
(2)辉铜矿(Cu S)可发生反应 2Cu S+2H SO +5O ==4CuSO +2H O,该反应的还原剂
2 2 2 4 2 4 2
是 ,当1mol O 发生反应时,还原剂所失电子的物质的量为 mol。向
2 a b
CuSO 溶液中加入镁条时有气体生成,该气体是 。
4
(3)右图为电解精炼银的示意图, (填“a”或“b”)极为含有杂质的粗银,若b极
AgNO -HNO 溶液
3 3
有少量红棕色气体产生,则生成该气体的电极反应式为 ,
(4)为处理银器表面的黑斑(Ag S),将银器置于铝制容器里的食盐水中并与铝接触,Ag S转化为
2 2
Ag,食盐水的作用为 。
29.(15分)化学反应原理在科研和生产中有广泛应用
(1)利用“化学蒸气转移法”制备TaS 晶体,发生如下反应
2
TaS (s)+2I (g) TaI (g)+S (g) △H﹥0 (I)
2 2 4 2
反应(I)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I (g)
2
第2页 | 共6页和足量TaS (s),I (g)的平衡转化率为 ,
2 2
(2)如图所示,反应(I)在石英真空管中进行,先在温度为T 的一端放入未提纯的TaS 粉末和
2 2
少量I (g),一段时间后,在温度为T 的一端得到了纯净的TaS 晶体,则温度T T (填
2 1 2 1 2
“﹥”“﹤”或“=”)。上述反应体系中循环使用的物质是 。
(3)利用I 的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为 H SO ,然后用一定浓
2 2 3
度的I 溶液进行滴定,所用指示剂为 ,滴定反应的离子方程式为 ,
2
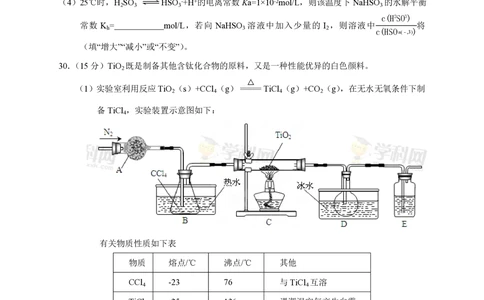
(4)25℃时,H SO HSO -+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO 的水解平衡
2 3 3 3
c(H2SO3)
常数 K = mol/L,若向 NaHSO 溶液中加入少量的 I ,则溶液中 将
h 3 2 c(HSO\s(-,3))
(填“增大”“减小”或“不变”)。
30.(15分)TiO 既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
2
△
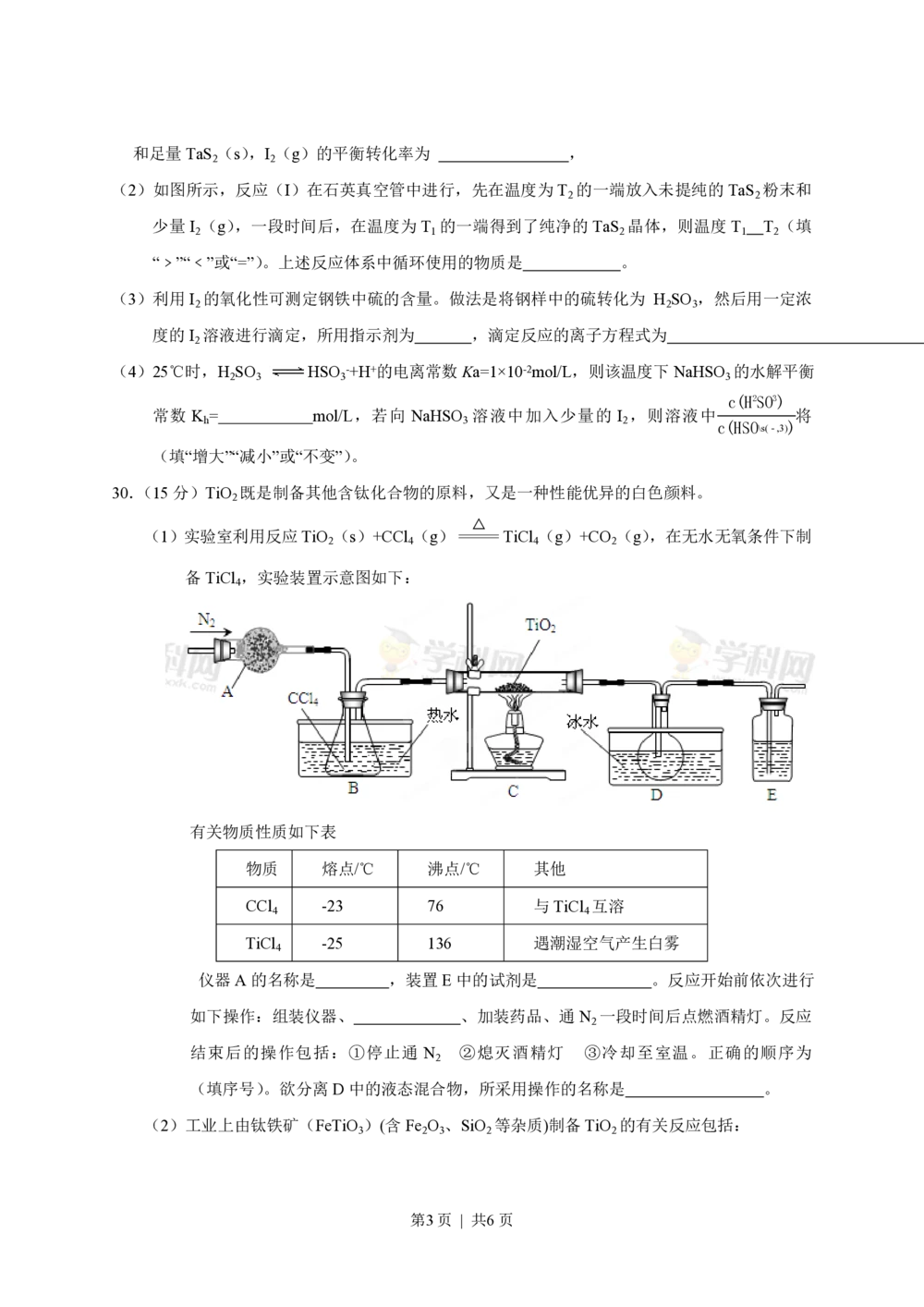
(1)实验室利用反应TiO (s)+CCl (g)=====TiCl (g)+CO (g),在无水无氧条件下制
2 4 4 2
备TiCl ,实验装置示意图如下:
4
有关物质性质如下表
物质 熔点/℃ 沸点/℃ 其他
CCl -23 76 与TiCl 互溶
4 4
TiCl -25 136 遇潮湿空气产生白雾
4
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行
如下操作:组装仪器、 、加装药品、通N 一段时间后点燃酒精灯。反应
2
结束后的操作包括:①停止通 N ②熄灭酒精灯 ③冷却至室温。正确的顺序为
2
(填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
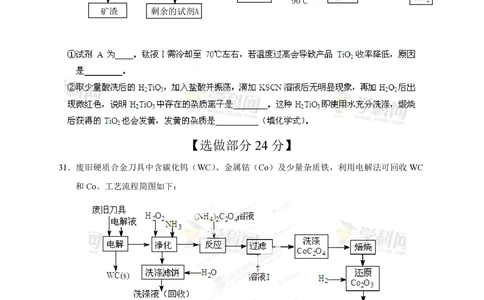
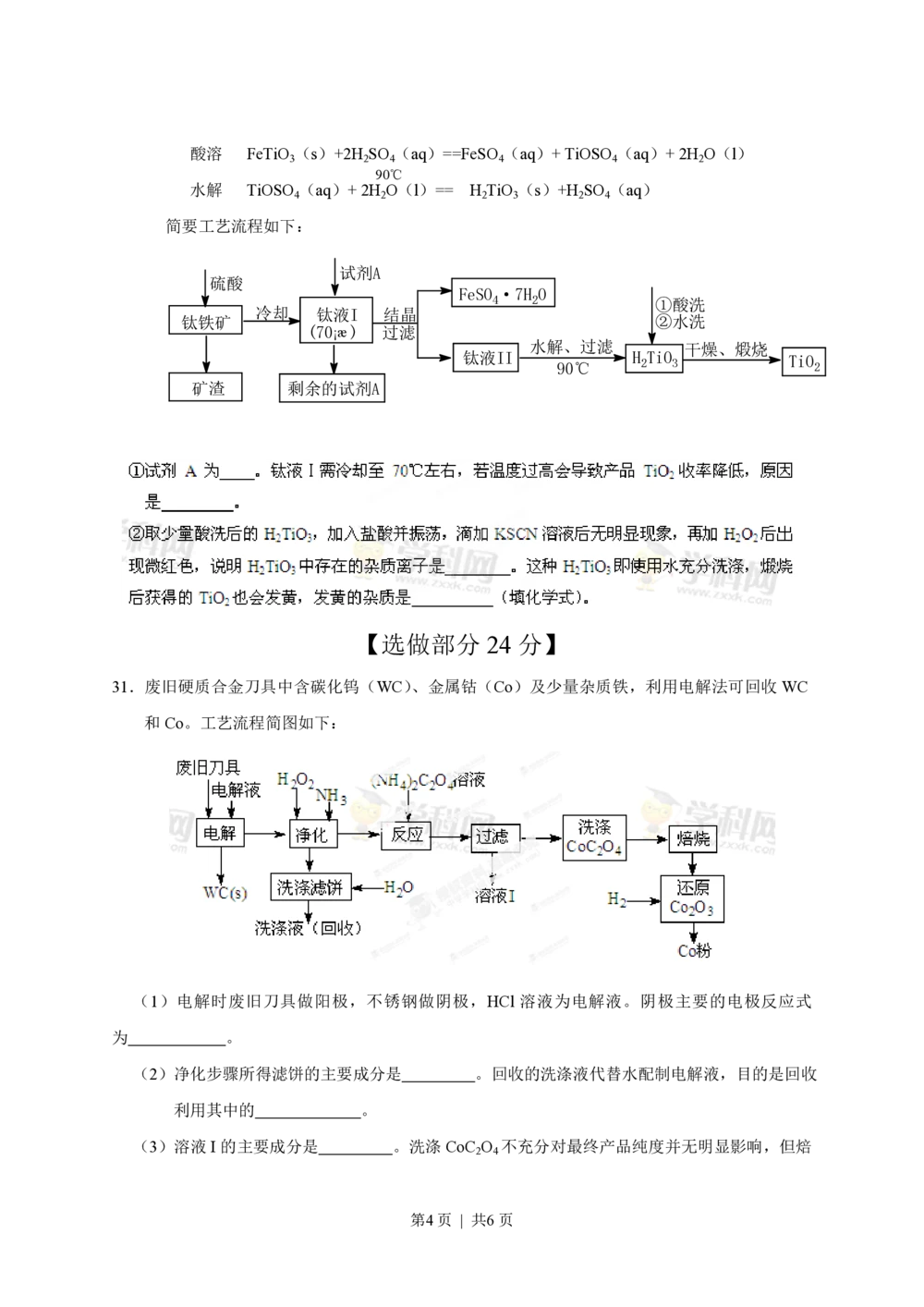
(2)工业上由钛铁矿(FeTiO )(含Fe O 、SiO 等杂质)制备TiO 的有关反应包括:
3 2 3 2 2
第3页 | 共6页酸溶 FeTiO (s)+2H SO (aq)==FeSO (aq)+ TiOSO (aq)+ 2H O(l)
3 2 4 4 4 2
90℃
水解 TiOSO (aq)+ 2H O(l)== H TiO (s)+H SO (aq)
4 2 2 3 2 4
简要工艺流程如下:
试剂A
硫酸
FeSO ·7H O
4 2 ①酸洗
冷却 钛液I 结晶
钛铁矿 ②水洗
(70¡æ) 过滤
水解、过滤 干燥、煅烧
钛液II 90℃ H 2 TiO 3 TiO 2
矿渣 剩余的试剂A
【选做部分 24 分】
31.废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC
和Co。工艺流程简图如下:
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl 溶液为电解液。阴极主要的电极反应式
为 。
(2)净化步骤所得滤饼的主要成分是 。回收的洗涤液代替水配制电解液,目的是回收
利用其中的 。
(3)溶液I的主要成分是 。洗涤CoC O 不充分对最终产品纯度并无明显影响,但焙
2 4
第4页 | 共6页烧时会造成环境污染,原因是 。
(4)将Co O 还原成Co粉的化学反应方程式为 。
2 3
32.卤族元素包括F、Cl、Br等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 。
.
HBr
电 . F 最 . . . 沸 H . Cl 熔 . F 2 .
负 性 . 高 正 F Cl Br 点 . HF 点 Cl 2
Cl .Br
价
.
Br
2
核电荷数 核电荷数 核电荷数 核电荷数
a b c d
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,右图为其晶胞结
构示意图,则每个晶胞中含有B原子的个数为 ,该功能陶瓷
的化学式为 。
(3)BCl 和NCl 中心原子的杂化方式分别为 和 。第一电
3 3
离能介于B、N之间的第二周期元素有 种。
(4)若BCl 与XY 通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对
3 n
电子的原子是 。
33.(8分)【化学——有机化学基础】
聚酰胺—66常用于生产帐篷、渔网、降落伞及弹力丝袜等织物,可利用下列路线合成:
O H 2 O HCl CH 2 CH 2 CH 2 CH 2 HCl D 2NaCN
¢Ù
Ni
Cl OH
A B C
H O¡¢H+
2
F
CH CH CH CH
2 2 2 2
聚合
H£¨¾Ûõ£°·-66£©
CN CN
H ¡¢Ni
E 2 G
H O H
已知反应: R¡ª CN H 2 + R¡ª COOH R¡ª CN N 2 i R¡ª CH 2 NH 2
第5页 | 共6页第6页 | 共6页