文档内容
绝密★启用前
2019 年全国统一高考化学试卷(新课标Ⅲ)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I
127
一、选择题:本题共 13个小题,每小题 6分。共 78分,在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与生活密切相关。下列叙述错误的是
A. 高纯硅可用于制作光感电池
B. 铝合金大量用于高铁建设
A. 经过阳离子交换树脂后,水中阳离子的总数不变
C. 活性炭具有除异味和杀菌作用
B. 水中的NO 、SO2、Cl−通过阳离子树脂后被除去
3 4
D. 碘酒可用于皮肤外用消毒 C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH− H O
2.下列化合物的分子中,所有原子可能共平面的是 2
A. 甲苯 B. 乙烷 C. 丙炔 D. 1,3−丁二烯
5.设N
A
为阿伏加德罗常数值。关于常温下pH=2的H
3
PO
4
溶液,下列说法正确的是
A. 每升溶液中的H+数目为0.02N
3.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和我10,X与Z同族,Y最外层电子数等于X次 A
B. c(H+)= c(H PO)+2c(HPO)+3c(PO3)+ c(OH−)
外层电子数,且Y原子半径大于Z。下列叙述正确的是
2 4 4 4
A. 熔点:X的氧化物比Y的氧化物高 C. 加水稀释使电离度增大,溶液pH减小
B. 热稳定性:X的氢化物大于Z的氢化物 D. 加入NaH PO 固体,溶液酸性增强
2 4
C. X与Z可形成离子化合物ZX
6.下列实验不能达到目的的是
D. Y的单质与Z的单质均能溶于浓硫酸
选项 目的 实验
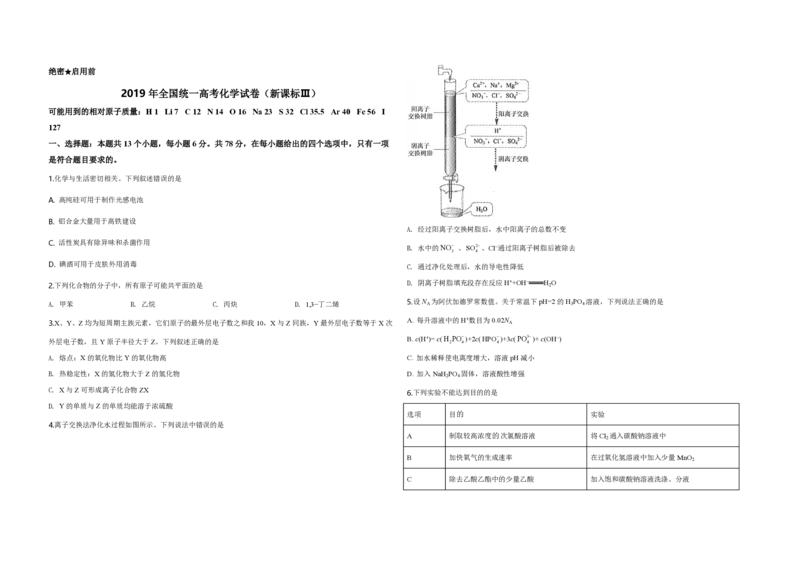
4.离子交换法净化水过程如图所示。下列说法中错误的是
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸 6 2
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 . 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
A. A B. B C. C D. D
7.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设
计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H O(l)
2
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式
充电 ZnO(s)+2Ni(OH) (s)。
充 电 2
____________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是将________________________。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
_____________________________________________________________________。
B. 充电时阳极反应为Ni(OH) (s)+OH−(aq)−e− NiOOH(s)+H O(l)
2 2
(6)写出“沉锰”的离子方程式___________________________________________________。
C. 放电时负极反应为Zn(s)+2OH−(aq)−2e− ZnO(s)+H O(l)
2
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNi Co MnO ,其中Ni、Co、Mn的化合
x y z 2
D. 放电过程中OH−通过隔膜从负极区移向正极区
1
价分别为+2、+3、+4。当x=y= 时,z=___________。
三、非选择题:共 174分,第 22~32 题为必考题,每个试题考生都必须作答。第 33~38 题为选考 3
题,考生根据要求作答。 9.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如
(一)必考题:共 129分。 下:
8.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、
Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相关金属离子[c (Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下: 相对密度/(g·cm﹣3) 1.44 1.10 1.35
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+ 相对分子质量 138 102 180实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL
浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。 可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c ,根据进料
0
回答下列问题: 浓度比c(HCl)∶c(O )=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料可以保持
2
(1)该合成反应中应采用__________加热。(填标号) 反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O )过低、过高的不利影响分别是
2
A.热水浴 B.酒精灯 C.煤气灯 D.电炉 ____________。
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名 (2)Deacon直接氧化法可按下列催化过程进行:
1
称)。
CuCl (s)=CuCl(s)+ Cl (g) ΔH =83 kJ·mol-1
2 2 1
2
1 1
CuCl(s)+ O (g)=CuO(s)+ Cl (g) ΔH =-20 kJ·mol-1
2 2 2
2 2
CuO(s)+2HCl(g)=CuCl (s)+H O(g) ΔH =-121 kJ·mol-1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2H O(g)的ΔH=_________ kJ·mol-1。
2 2 2
(3)在一定温度的条件下,进一步提高HCI的转化率的方法是______________。(写出2种)
(3)①中需使用冷水,目的是______________________________________。 (4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。 要包括电化学过程和化学过程,如下图所示:
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。
10.
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为
氯气的技术成为科学研究的热点。回答下列问题: 负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气
(1)Deacon发明的直接氧化法为:4HCl(g)+O (g)=2Cl (g)+2H O(g)。下图为刚性容器中,进料浓度比 __________L(标准状况)
2 2 2
c(HCl) ∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系: (二)选考题:共 45分。请考生从 2道物理题、2道化学题、2道生物题中每科任选一题作答。
2如果多做,则每科按所做的第一题计分。 (1)A的化学名称为___________。
[化学——选修 3:物质结构与性质]
(2) 中的官能团名称是___________。
11.磷酸亚铁锂(LiFePO
4
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,
(3)反应③的类型为___________,W的分子式为___________。
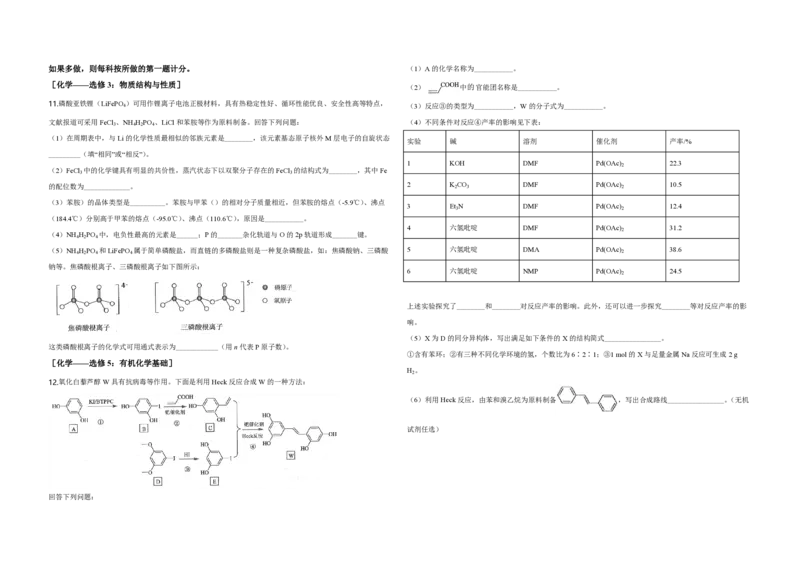
文献报道可采用FeCl 、NH H PO 、LiCl和苯胺等作为原料制备。回答下列问题: (4)不同条件对反应④产率的影响见下表:
3 4 2 4
(1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态
实验 碱 溶剂 催化剂 产率/%
_________(填“相同”或“相反”)。
1 KOH DMF Pd(OAc) 22.3
2
(2)FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl 的结构式为________,其中Fe
3 3
的配位数为_____________。 2 K 2 CO 3 DMF Pd(OAc) 2 10.5
(3)苯胺)的晶体类型是__________。苯胺与甲苯()的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点
3 Et N DMF Pd(OAc) 12.4
3 2
(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________。
4 六氢吡啶 DMF Pd(OAc) 31.2
2
(4)NH H PO 中,电负性最高的元素是______;P的_______杂化轨道与O的2p轨道形成_______键。
4 2 4
(5)NH 4 H 2 PO 4 和LiFePO 4 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸 5 六氢吡啶 DMA Pd(OAc) 2 38.6
钠等。焦磷酸根离子、三磷酸根离子如下图所示:
6 六氢吡啶 NMP Pd(OAc) 24.5
2
上述实验探究了________和________对反应产率的影响。此外,还可以进一步探究________等对反应产率的影
响。
(5)X为D的同分异构体,写出满足如下条件的X的结构简式________________。
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
①含有苯环;②有三种不同化学环境的氢,个数比为6∶2∶1;③1 mol的X与足量金属Na反应可生成2 g
[化学——选修 5:有机化学基础]
H 。
2
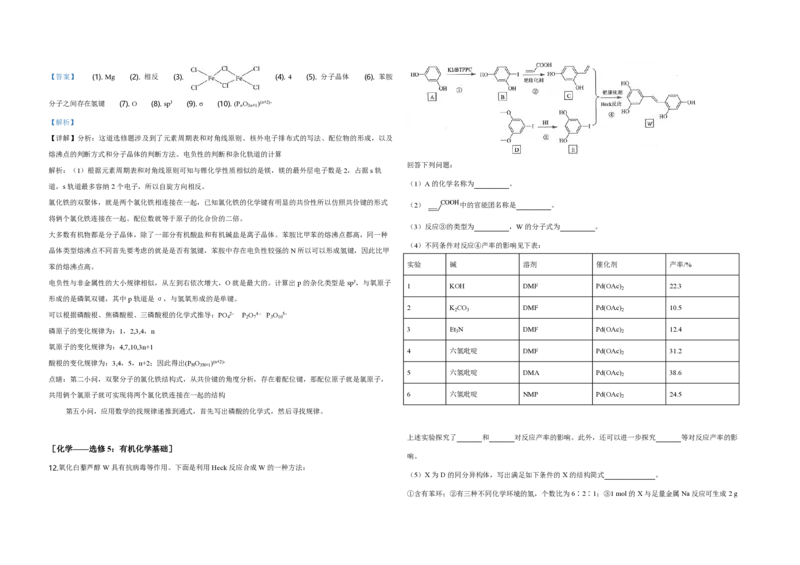
12.氧化白藜芦醇W具有抗病毒等作用。下面是利用Heck反应合成W的一种方法:
(6)利用Heck反应,由苯和溴乙烷为原料制备 ,写出合成路线________________。(无机
试剂任选)
回答下列问题:绝密★启用前
【解析】
【详解】A、甲苯中含有饱和碳原子,所有原子不可能共平面,A不选;
2019 年全国统一高考化学试卷(新课标Ⅲ)
B、乙烷是烷烃,所有原子不可能共平面,B不选;
答案解析版
C、丙炔中含有饱和碳原子,所有原子不可能共平面,C不选;
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I D、碳碳双键是平面形结构,因此1,3-丁二烯分子中所有原子共平面,D选。
127 答案选D。
一、选择题:本题共 13个小题,每小题 6分。共 78分,在每小题给出的四个选项中,只有一项
是符合题目要求的。
3.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和我10,X与Z同族,Y最外层电子数等于X次
1.化学与生活密切相关。下列叙述错误的是
外层电子数,且Y原子半径大于Z。下列叙述正确的是
A. 高纯硅可用于制作光感电池
A. 熔点:X的氧化物比Y的氧化物高
B. 铝合金大量用于高铁建设
B. 热稳定性:X的氢化物大于Z的氢化物
C. 活性炭具有除异味和杀菌作用
C. X与Z可形成离子化合物ZX
D. 碘酒可用于皮肤外用消毒
D. Y的单质与Z的单质均能溶于浓硫酸
【答案】C
【答案】B
【解析】
【解析】
【详解】A、硅是半导体,高纯硅可用于制作光感电池,A正确;
【详解】Y的最外层电子数等于X次外层电子数,由于均是主族元素,所以Y的最外层电子数不可能是8个,
B、铝合金硬度大,可用于高铁建设,B正确;
则X只能是第二周期元素,因此Y的最外层电子数是2个,又因为Y的原子半径大于Z,则Y只能是第三周
C、活性炭具有吸附性,可用于除异味,但不能杀菌消毒,C错误;
期的Mg,因此X与Z的最外层电子数是(10-2)/2=4,则X是C,Z是Si。
D、碘酒能使蛋白质变性,可用于皮肤外用消毒,D正确;
A、碳的氧化物形成的分子晶体,Y的氧化物是离子化合物氧化镁,则氧化镁的熔点高于碳的氧化物熔点,A
答案选C。
错误;
B、碳元素的非金属性强于硅元素,非金属性越强,氢化物越稳定,则碳的氢化物稳定性强于硅的氢化物稳定
性,B正确;
2.下列化合物的分子中,所有原子可能共平面的是
C、C与Si形成的是共价化合物SiC,C错误;
A. 甲苯 B. 乙烷 C. 丙炔 D. 1,3−丁二烯
D、单质镁能溶于浓硝酸,单质硅不溶于浓硝酸,D错误;
【答案】D
答案选B。D、根据以上分析可知阴离子交换树脂填充段存在反应H++OH-=H O,D正确;
2
答案选A。
4.离子交换法净化水过程如图所示。下列说法中错误的是
5.设N 为阿伏加德罗常数值。关于常温下pH=2的H PO 溶液,下列说法正确的是
A 3 4
A. 每升溶液中的H+数目为0.02N
A
B. c(H+)= c(H PO)+2c(HPO)+3c(PO3)+ c(OH−)
2 4 4 4
C. 加水稀释使电离度增大,溶液pH减小
D. 加入NaH PO 固体,溶液酸性增强
2 4
【答案】B
【解析】
【详解】A、常温下pH=2,则溶液中氢离子浓度是0.01mol/L,因此每升溶液中H+数目为0.01N ,A错误;
A
A. 经过阳离子交换树脂后,水中阳离子的总数不变
B、根据电荷守恒可知选项B正确;
B. 水中的NO 3 、SO2 4 、Cl−通过阳离子树脂后被除去 C、加水稀释促进电离,电离度增大,但氢离子浓度减小,pH增大,C错误;
D、加入NaH PO 固体,H PO -浓度增大,抑制磷酸的电离,溶液的酸性减弱,D错误;
C. 通过净化处理后,水的导电性降低 2 4 2 4
答案选B。
D. 阴离子树脂填充段存在反应H++OH− H O
2
【答案】A
6.下列实验不能达到目的的是
【解析】
选项 目的 实验
【详解】离子交换树脂净化水的原理是:当含有Na+、Ca2+、Mg2+等阳离子及SO 2-、Cl-、NO -等阴离子的原
4 3
水通过阳离子交换树脂时,水中的阳离子为树脂所吸附,而树脂上可交换的阳离子H+则被交换到水中,并和水
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
中的阴离子组成相应的无机酸;当含有无机酸的水再通过阴离子交换树脂时,水中的阴离子也为树脂所吸附,
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
树脂上可交换的阴离子OH-也被交换到水中,同时与水中的H+离子结合成水,则
A、根据电荷守恒可知经过阳离子交换树脂后,水中阳离子总数增加,A错误; C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
B、根据以上分析可知水中的SO 2-、Cl-、NO -等阴离子通过阴离子交换树脂被除去,B正确;
4 3 D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸
C、通过净化处理后,溶液中离子的浓度降低,导电性降低,C正确;D. 放电过程中OH−通过隔膜从负极区移向正极区
【答案】D
A. A B. B C. C D. D
【解析】
【详解】A、三维多孔海绵状Zn具有较高的表面积,吸附能力强,所沉积的ZnO分散度高,A正确;
【答案】A
B、充电相当于是电解池,阳极发生失去电子的氧化反应,根据总反应式可知阳极是Ni(OH) 失去电子转化为
2
【解析】
NiOOH,电极反应式为Ni(OH) (s)+OH-(aq)-e-=NiOOH(s)+H O(l),B正确;
2 2
【详解】A、氯气与碳酸钠溶液反应生成氯化钠、次氯酸钠和碳酸氢钠,不能制备次氯酸,不能达到实验目
C、放电时相当于是原电池,负极发生失去电子的氧化反应,根据总反应式可知负极反应式为Zn(s)+2OH-(aq)
的,A选;
-2e-=ZnO(s)+H O(l),C正确;
2
B、过氧化氢溶液中加入少量二氧化锰作催化剂,加快双氧水的分解,因此可以加快氧气的生成速率,能达到实
D、原电池中阳离子向正极移动,阴离子向负极移动,则放电过程中OH-通过隔膜从正极区移向负极区,D错
验目的,B不选;
误
。
C、碳酸钠溶液与乙酸反应,与乙酸乙酯不反应,可以除去乙酸乙酯中的乙酸,能达到实验目的,C不选;
答案选D。
D、根据较强酸制备较弱酸可知向饱和亚硫酸钠溶液中滴加浓硫酸可以制备二氧化硫,能达到实验目的,D不
选;
答案选A。 三、非选择题:共 174分,第 22~32 题为必考题,每个试题考生都必须作答。第 33~38 题为选考
题,考生根据要求作答。
(一)必考题:共 129分。
7.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设
8.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、
计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H O(l)
2
Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
充电 ZnO(s)+2Ni(OH) (s)。
充 电 2
相关金属离子[c (Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
B. 充电时阳极反应为Ni(OH) (s)+OH−(aq)−e− NiOOH(s)+H O(l)
2 2
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
C. 放电时负极反应为Zn(s)+2OH−(aq)−2e− ZnO(s)+H O(l)
2(5)由HF H++F-知,酸度过大,F-浓度减低,使得MgF 2 Mg2++2F-平衡向沉淀溶解方向移动,
Mg2+沉淀不完全;
(6)根据题干信息沉锰的过程是生成了MnCO 沉淀,所以反应离子方程式为:Mn2++2HCO -
3 3
=MnCO ↓+CO ↑+H O;
3 2 2
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式
(7)根据化合物中各元素化合价代数和为0的规律得:1+2x+3y+4z=6,已知,x=y=1/3,带入计算得:z=1/3
____________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是将________________________。 9.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如
2
下:
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂2”的目的是生成MgF 沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
_____________________________________________________________________。
水杨酸 醋酸酐 乙酰水杨酸
(6)写出“沉锰”的离子方程式___________________________________________________。
熔点/℃ 157~159 -72~-74 135~138
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNi Co MnO ,其中Ni、Co、Mn的化合
x y z 2
相对密度/(g·cm﹣3) 1.44 1.10 1.35
1
价分别为+2、+3、+4。当x=y= 时,z=___________。
3
相对分子质量 138 102 180
【答案】 (1). SiO (不溶性硅酸盐) (2). MnO +MnS+2H SO =2MnSO +S+2H O (3). 将Fe2+氧化为
2 2 2 4 4 2
Fe3+ (4). 4.7 (5). NiS和ZnS (6). F−与H+结合形成弱电解质HF,MgF Mg2++2F−平衡向右移动
2
1
(7). Mn2++2HCO=MnCO ↓+CO ↑+H O (8).
3 3 2 2 3
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL
【解析】
浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作.
【详解】(1)Si元素以SiO 或不溶性硅盐存在,SiO 与硫酸不反应,所以滤渣I中除了S还有SiO ;在硫酸的
2 2 2
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
溶浸过程中,二氧化锰和硫化锰发生了氧化还原反应,二氧化锰作氧化剂,硫化锰作还原剂,方程式为:
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
MnO +MnS+2H SO =2MnSO +S+2H O;
2 2 4 4 2
③滤液用浓盐酸酸化后冷却、过滤得固体。
(2)二氧化锰作为氧化剂,使得MnS反应完全,且将溶液中Fe2+氧化为Fe3+;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
(3)由表中数据知pH在4.7时,Fe3+和Al3+沉淀完全,所以应该控制pH在4.7~6之间;
回答下列问题:
(4)根据题干信息,加入Na S除杂为了出去锌离子和镍离子,所以滤渣3是生成的沉淀ZnS和NiS;
26.9g m
(1)该合成反应中应采用__________加热。(填标号)
9g
A.热水浴 B.酒精灯 C.煤气灯 D.电炉 m( C H O )=(6.9g×180)/138=9g,则产率为 100%=60% 。
9 8 4 5.4g
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名称)。
10.
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为
氯气的技术成为科学研究的热点。回答下列问题:
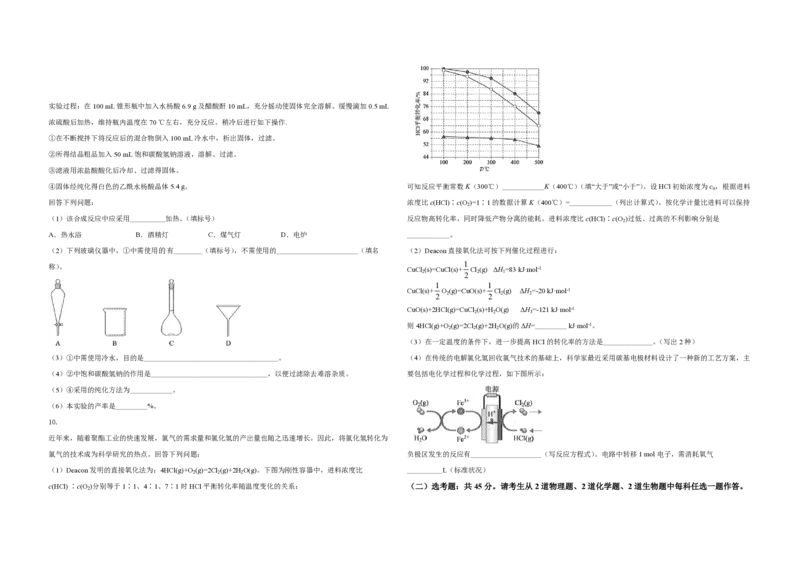
(1)Deacon发明的直接氧化法为:4HCl(g)+O (g)=2Cl (g)+2H O(g)。下图为刚性容器中,进料浓度比
2 2 2
(3)①中需使用冷水,目的是______________________________________。
c(HCl) ∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。
【答案】 (1). A (2). BD (3). 分液漏斗、容量瓶 (4). 充分析出乙酰水杨酸固体(结晶) (5).
生成可溶的乙酰水杨酸钠 (6). 重结晶 (7). 60
可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c ,根据进料
0
【解析】
【详解】(1)因为反应温度在70℃,低于水的沸点,且需维温度不变,故采用热水浴的方法加热;
浓度比c(HCl)∶c(O
2
)=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料可以保持
(2)操作①需将反应物倒入冷水,需要用烧杯量取和存放冷水,过滤的操作中还需要漏斗,则答案为:B、 反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O )过低、过高的不利影响分别是
2
D;分液漏斗主要用于分离互不相容的液体混合物,容量瓶用于配制一定浓度的溶液,这两个仪器用不到。
____________。
(3)反应时温度较高,所以用冷水的目的是使得乙酰水杨酸晶体充分析出;
(2)Deacon直接氧化法可按下列催化过程进行:
(4)乙酰水杨酸难溶于水,为了除去其中的杂质,可将生成的乙酰水杨酸与碳酸氢钠反应生成可溶性的乙酰水
1
CuCl (s)=CuCl(s)+ Cl (g) ΔH =83 kJ·mol-1
2 2 1
2
杨酸钠,以便过滤除去杂质;
1 1
CuCl(s)+ O (g)=CuO(s)+ Cl (g) ΔH =-20 kJ·mol-1
(5)每次结晶过程中会有少量杂质一起析出,可以通过多次结晶的方法进行纯化,也就是重结晶; 2 2 2
2 2
(6)水杨酸分子式为C H O ,乙酰水杨酸分子式为C H O ,根据关系式法计算得: CuO(s)+2HCl(g)=CuCl (s)+H O(g) ΔH =-121 kJ·mol-1
7 6 3 9 8 4 2 2 3
C H O ~ C H O
7 6 3 9 8 4 则4HCl(g)+O (g)=2Cl (g)+2H O(g)的ΔH=_________ kJ·mol-1。
2 2 2
138 180以增大压强,使平衡正向移动;也可以及时除去产物,较小产物浓度,使平衡正向移动;
(3)在一定温度的条件下,进一步提高HCI的转化率的方法是______________。(写出2种)
(4)电解过程中,负极上发生的是得电子反应,元素化合价降低,属于还原反应,则图中左侧为负极反应,根
(4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主
据图示信息知电极反应为:Fe3++e-=Fe2+和4=Fe2++O +4H+=4Fe3++2H O;
要包括电化学过程和化学过程,如下图所示: 2 2
(二)选考题:共 45分。请考生从 2道物理题、2道化学题、2道生物题中每科任选一题作答。
如果多做,则每科按所做的第一题计分。
[化学——选修 3:物质结构与性质]
负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气__________L 11.磷酸亚铁锂(LiFePO )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,
4
(标准状况) 文献报道可采用FeCl 、NH H PO 、LiCl和苯胺等作为原料制备。回答下列问题:
3 4 2 4
(0.42)2(0.42)2 (1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态
【答案】 (1). 大于 (2). (3). O 和 Cl 分离能耗较高、HCl转化率较低
(10.84)4(10.21)c 2 2
0
_________(填“相同”或“相反”)。
(4). ﹣116 (5). 增加反应体系压强、及时除去产物 (6). Fe3++e−=Fe2+,4Fe2++O +4H+=4Fe3++2H O (7).
2 2
(2)FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl 的结构式为________,其中Fe
3 3
5.6
【解析】
的配位数为_____________。
【详解】(1)根据反应方程式知,HCl平衡转化率越大,平衡常数K越大,结合图像知K(300℃)>K(400℃);
(3)苯胺)的晶体类型是__________。苯胺与甲苯()的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点
由图像知,400℃时,HCl平衡转化率为84%,用三段式法对数据进行处理得:
(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________。
4HCl(g)O (g)2Cl (g)2H O(g)
2 2 2
(4)NH H PO 中,电负性最高的元素是______;P的_______杂化轨道与O的2p轨道形成_______键。
4 2 4
起始(浓度) c c
0 0 0 0
(5)NH H PO 和LiFePO 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸
变化(浓度) 0.84c 0.21c 0.42c 0.42c 4 2 4 4
0 0 0 0
钠等。焦磷酸根离子、三磷酸根离子如下图所示:
平衡(浓度)(1-0.84)c (1-0.21)c 0.42c 0.42c
0 0 0 0
(0.42)2(0.42)2
则K= ;根据题干信息知,进料浓度比过低,氧气大量剩余,导致分离产物氯气和氧气的
(10.84)4(10.21)c
0
能耗较高;进料浓度比过高,HCl不能充分反应,导致HCl转化率较低;
(2)根据盖斯定律知,(反应I+反应II+反应III)×2得4HCl(g)O (g)2Cl (g)2H O(g) ∆H=
2 2 2
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
(∆H +∆H +∆H )×2=-116kJ∙mol-1;
1 2 3
(3)若想提高HCl的转化率,应该促使平衡正向移动,该反应为气体体积减小的反应,根据勒夏特列原理,可【答案】 (1). Mg (2). 相反 (3). (4). 4 (5). 分子晶体 (6). 苯胺
分子之间存在氢键 (7). O (8). sp3 (9). σ (10). (P O )(n+2)-
n 3n+1
【解析】
【详解】分析:这道选修题涉及到了元素周期表和对角线原则、核外电子排布式的写法、配位物的形成,以及
熔沸点的判断方式和分子晶体的判断方法。电负性的判断和杂化轨道的计算
回答下列问题:
解析:(1)根据元素周期表和对角线原则可知与锂化学性质相似的是镁,镁的最外层电子数是2,占据s轨
道,s轨道最多容纳2个电子,所以自旋方向相反。
(1)A的化学名称为___________。
氯化铁的双聚体,就是两个氯化铁相连接在一起,已知氯化铁的化学键有明显的共价性所以仿照共价键的形式
(2) 中的官能团名称是___________。
将俩个氯化铁连接在一起。配位数就等于原子的化合价的二倍。
(3)反应③的类型为___________,W的分子式为___________。
大多数有机物都是分子晶体,除了一部分有机酸盐和有机碱盐是离子晶体。苯胺比甲苯的熔沸点都高,同一种
(4)不同条件对反应④产率的影响见下表:
晶体类型熔沸点不同首先要考虑的就是是否有氢键,苯胺中存在电负性较强的N所以可以形成氢键,因此比甲
苯的熔沸点高。
实验 碱 溶剂 催化剂 产率/%
电负性与非金属性的大小规律相似,从左到右依次增大,O就是最大的。计算出p的杂化类型是sp3,与氧原子
1 KOH DMF Pd(OAc) 22.3
2
形成的是磷氧双键,其中p轨道是σ,与氢氧形成的是单键。
2 K CO DMF Pd(OAc) 10.5
2 3 2
可以根据磷酸根、焦磷酸根、三磷酸根的化学式推导:PO 2- P O 4 - P O 5-
4 2 7 3 10
磷原子的变化规律为:1,2,3,4,n 3 Et 3 N DMF Pd(OAc) 2 12.4
氧原子的变化规律为:4,7,10,3n+1
4 六氢吡啶 DMF Pd(OAc) 31.2
2
酸根的变化规律为:3,4,5,n+2;因此得出(P O )(n+2)-
N 3N+1
5 六氢吡啶 DMA Pd(OAc) 38.6
2
点睛:第二小问,双聚分子的氯化铁结构式,从共价键的角度分析,存在着配位键,那配位原子就是氯原子,
共用俩个氯原子就可实现将两个氯化铁连接在一起的结构 6 六氢吡啶 NMP Pd(OAc) 24.5
2
第五小问,应用数学的找规律递推到通式,首先写出磷酸的化学式,然后寻找规律。
上述实验探究了________和________对反应产率的影响。此外,还可以进一步探究________等对反应产率的影
[化学——选修 5:有机化学基础]
响。
12.氧化白藜芦醇W具有抗病毒等作用。下面是利用Heck反应合成W的一种方法:
(5)X为D的同分异构体,写出满足如下条件的X的结构简式________________。
①含有苯环;②有三种不同化学环境的氢,个数比为6∶2∶1;③1 mol的X与足量金属Na反应可生成2 gH 。 证明有两个酚羟基或醇羟基,又有三种不同环境的氢6:2:1,那一定是有两个甲基和两个酚羟基,因为醇羟基没
2
有6个相同环境的氢。
(6)利用Heck反应,由苯和溴乙烷为原料制备 ,写出合成路线________________。(无机试
由题意中的heck反应可知需要一个反应物中含双建,一个反应物中含I;
从苯出发可以经过溴乙烷和溴化铁的反应制得乙苯,乙苯在乙基上通过烷烃的取代反应生成氯乙苯,氯乙苯在
剂任选)
氢氧化钠醇溶液下发生卤代烃的水解从而生成双键,得到苯乙烯;可以仿照反应1通过相同条件在苯环上上一
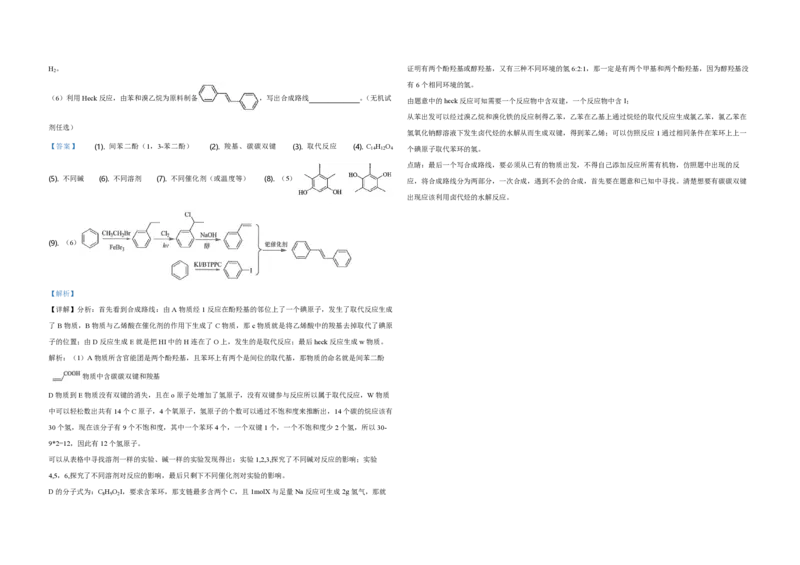
【答案】 (1). 间苯二酚(1,3-苯二酚) (2). 羧基、碳碳双键 (3). 取代反应 (4). C 14 H 12 O 4 个碘原子取代苯环的氢。
点睛:最后一个写合成路线,要必须从已有的物质出发,不得自己添加反应所需有机物,仿照题中出现的反
(5). 不同碱 (6). 不同溶剂 (7). 不同催化剂(或温度等) (8). (5) 应,将合成路线分为两部分,一次合成,遇到不会的合成,首先要在题意和已知中寻找。清楚想要有碳碳双键
出现应该利用卤代烃的水解反应。
(9). (6)
【解析】
【详解】分析:首先看到合成路线:由A物质经1反应在酚羟基的邻位上了一个碘原子,发生了取代反应生成
了B物质,B物质与乙烯酸在催化剂的作用下生成了C物质,那c物质就是将乙烯酸中的羧基去掉取代了碘原
子的位置;由D反应生成E就是把HI中的H连在了O上,发生的是取代反应;最后heck反应生成w物质。
解析:(1)A物质所含官能团是两个酚羟基,且苯环上有两个是间位的取代基,那物质的命名就是间苯二酚
物质中含碳碳双键和羧基
D物质到E物质没有双键的消失,且在o原子处增加了氢原子,没有双键参与反应所以属于取代反应,W物质
中可以轻松数出共有14个C原子,4个氧原子,氢原子的个数可以通过不饱和度来推断出,14个碳的烷应该有
30个氢,现在该分子有9个不饱和度,其中一个苯环4个,一个双键1个,一个不饱和度少2个氢,所以30-
9*2=12,因此有12个氢原子。
可以从表格中寻找溶剂一样的实验、碱一样的实验发现得出:实验1,2,3,探究了不同碱对反应的影响;实验
4,5,6,探究了不同溶剂对反应的影响,最后只剩下不同催化剂对实验的影响。
D的分子式为:C H O I,要求含苯环,那支链最多含两个C,且1molX与足量Na反应可生成2g氢气,那就
8 9 2