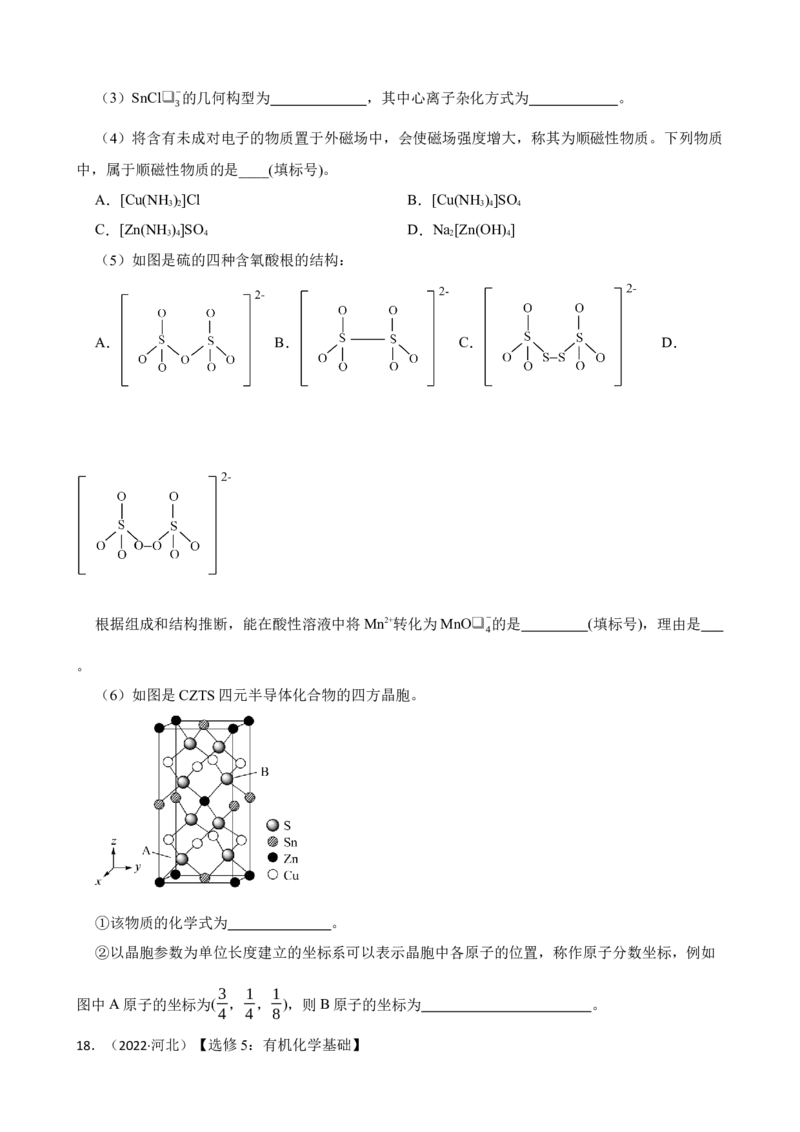文档内容
【高考真题】2022年河北省高考真题化学试题
一、单项选择题
1.(2022·河北)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
2.(2022·河北)茯苓新酸DM是从中药茯苓中提取的一种化学物质,具有一定生理活性,其结构简
式如图。关于该化合物下列说法错误的是( )
A.可使酸性KMnO 溶液褪色 B.可发生取代反应和加成反应
4
C.可与金属钠反应放出H D.分子中含有3种官能团
2
3.(2022·河北)化学是材料科学的基础。下列说法错误的是( )
A.制造5G芯片的氮化铝晶圆属于无机非金属材料
B.制造阻燃或防火线缆的橡胶不能由加聚反应合成
C.制造特种防护服的芳纶纤维属于有机高分子材料
D.可降解聚乳酸塑料的推广应用可减少“白色污染”
4.(2022·河北)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和Mg N,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO❑ 2−的个数为0.1N
2 3 A
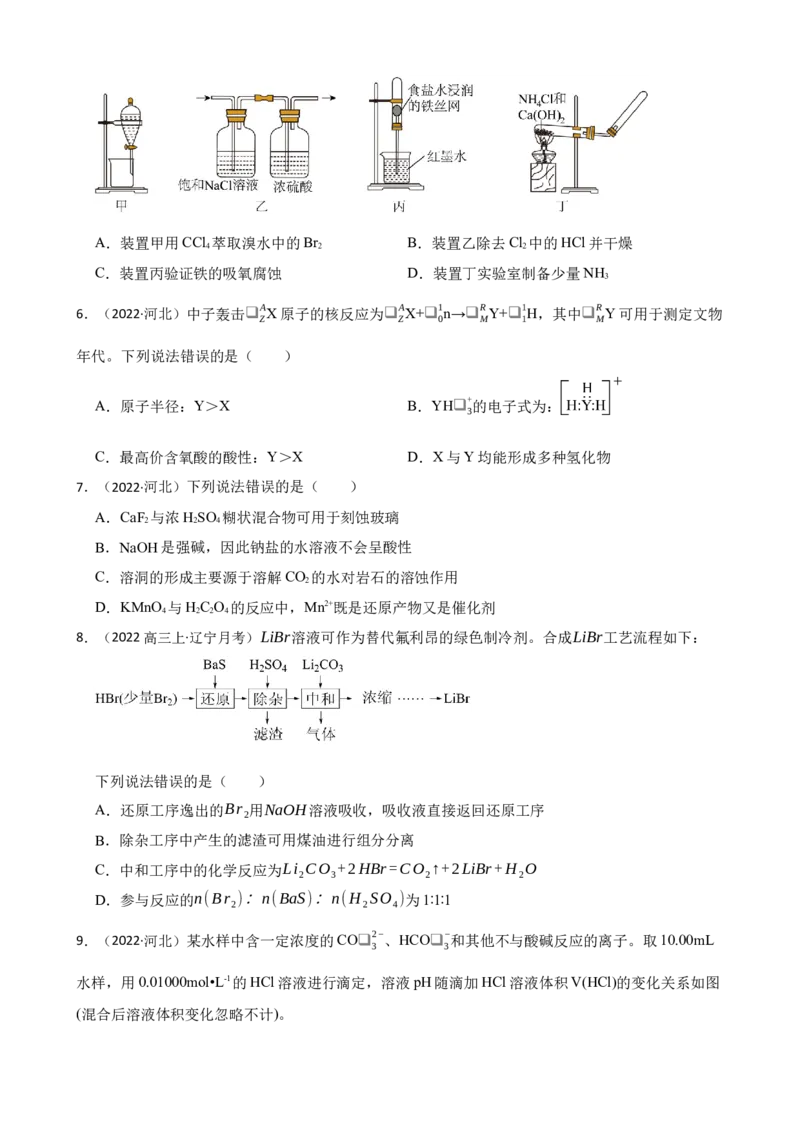
5.(2022·河北)下列图示装置不能达到实验目的的是( )A.装置甲用CCl 萃取溴水中的Br B.装置乙除去Cl 中的HCl并干燥
4 2 2
C.装置丙验证铁的吸氧腐蚀 D.装置丁实验室制备少量NH
3
6.(2022·河北)中子轰击❑ AX原子的核反应为❑ AX+❑ 1n→❑ RY+❑ 1H,其中❑ RY可用于测定文物
Z Z 0 M 1 M
年代。下列说法错误的是( )
+
A.原子半径:Y>X B.YH❑ 的电子式为:
3
C.最高价含氧酸的酸性:Y>X D.X与Y均能形成多种氢化物
7.(2022·河北)下列说法错误的是( )
A.CaF 与浓HSO 糊状混合物可用于刻蚀玻璃
2 2 4
B.NaOH是强碱,因此钠盐的水溶液不会呈酸性
C.溶洞的形成主要源于溶解CO 的水对岩石的溶蚀作用
2
D.KMnO 与HCO 的反应中,Mn2+既是还原产物又是催化剂
4 2 2 4
8.(2022高三上·辽宁月考)LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为Li CO +2HBr=CO ↑+2LiBr+H O
2 3 2 2
D.参与反应的n(Br ):n(BaS):n(H SO )为1∶1∶1
2 2 4
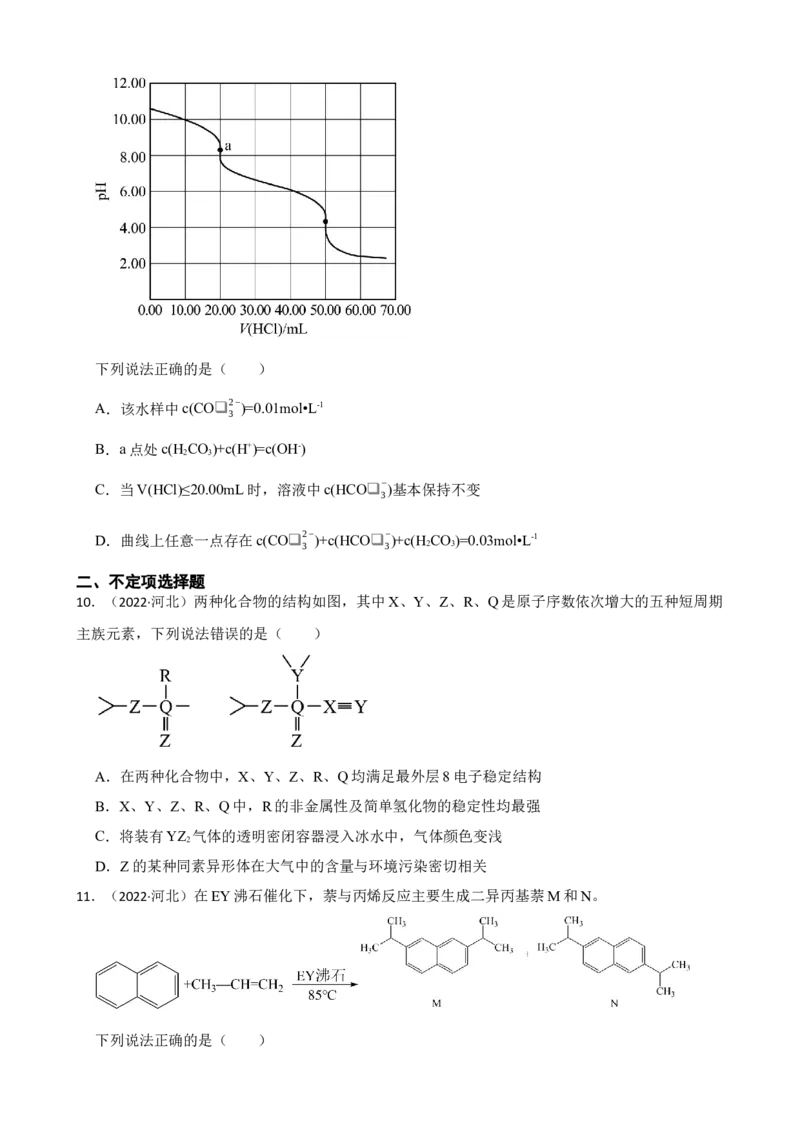
9.(2022·河北)某水样中含一定浓度的CO❑ 2−、HCO❑ −和其他不与酸碱反应的离子。取10.00mL
3 3
水样,用0.01000mol•L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积V(HCl)的变化关系如图
(混合后溶液体积变化忽略不计)。下列说法正确的是( )
A.该水样中c(CO❑ 2−)=0.01mol•L-1
3
B.a点处c(H CO )+c(H+)=c(OH-)
2 3
C.当V(HCl)≤20.00mL时,溶液中c(HCO❑ −)基本保持不变
3
D.曲线上任意一点存在c(CO❑ 2−)+c(HCO❑ −)+c(H CO )=0.03mol•L-1
3 3 2 3
二、不定项选择题
10.(2022·河北)两种化合物的结构如图,其中X、Y、Z、R、Q是原子序数依次增大的五种短周期
主族元素,下列说法错误的是( )
A.在两种化合物中,X、Y、Z、R、Q均满足最外层8电子稳定结构
B.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强
C.将装有YZ 气体的透明密闭容器浸入冰水中,气体颜色变浅
2
D.Z的某种同素异形体在大气中的含量与环境污染密切相关
11.(2022·河北)在EY沸石催化下,萘与丙烯反应主要生成二异丙基萘M和N。
下列说法正确的是( )A.M和N互为同系物
B.M分子中最多有12个碳原子共平面
C.N的一溴代物有5种
D.萘的二溴代物有10种
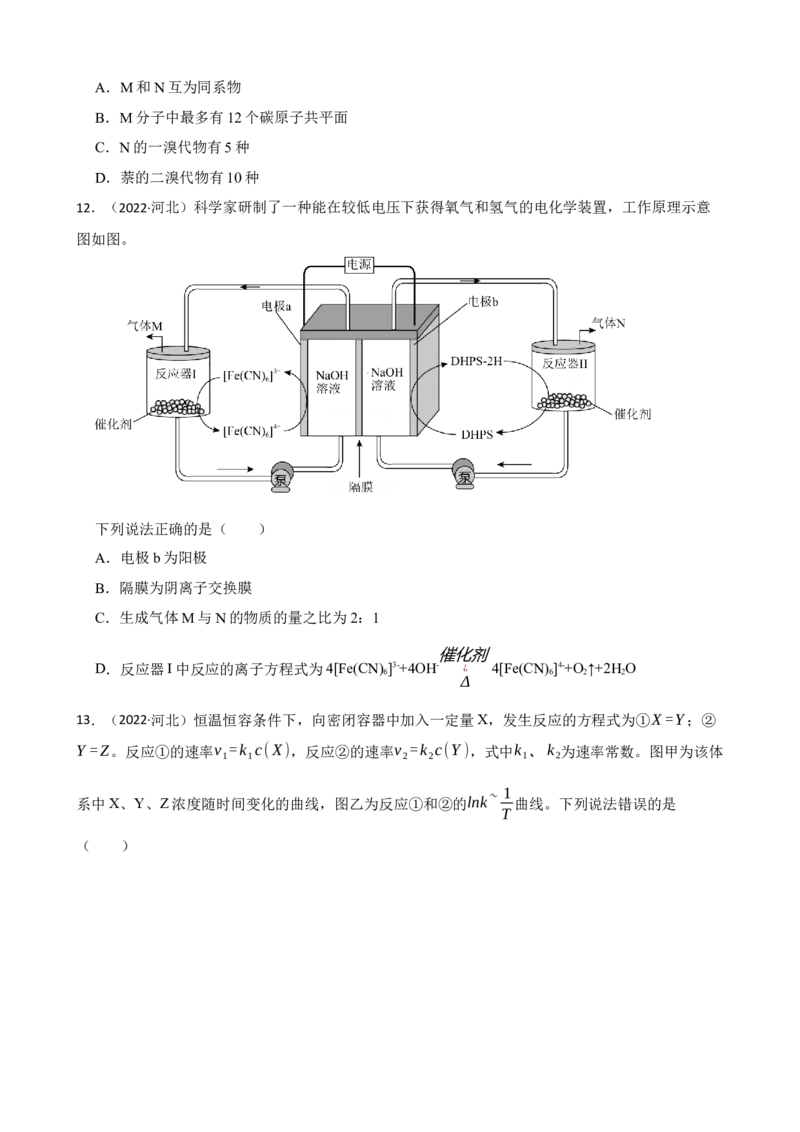
12.(2022·河北)科学家研制了一种能在较低电压下获得氧气和氢气的电化学装置,工作原理示意
图如图。
下列说法正确的是( )
A.电极b为阳极
B.隔膜为阴离子交换膜
C.生成气体M与N的物质的量之比为2:1
催化剂
D.反应器I中反应的离子方程式为4[Fe(CN) 6 ]3-+4OH- ¿ 4[Fe(CN) 6 ]4-+O 2 ↑+2H 2 O
Δ
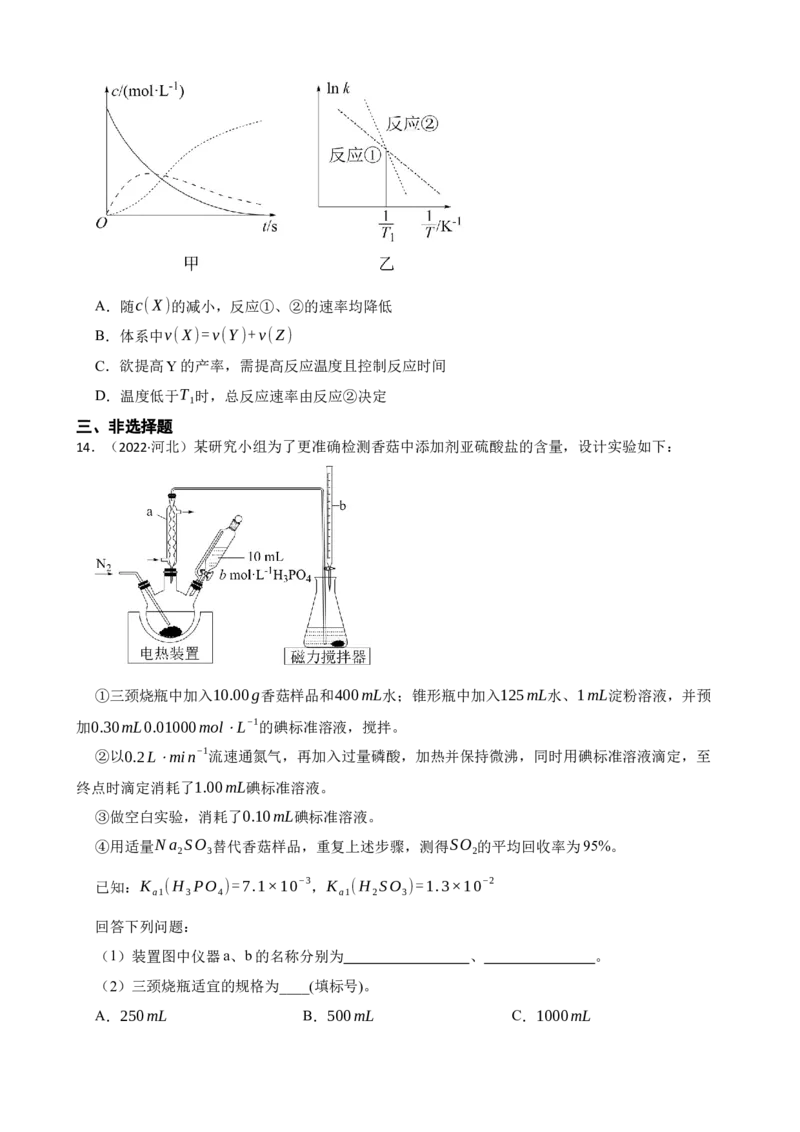
13.(2022·河北)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①X=Y;②
Y =Z。反应①的速率v =k c(X),反应②的速率v =k c(Y),式中k 、k 为速率常数。图甲为该体
1 1 2 2 1 2
1
系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的lnk~ 曲线。下列说法错误的是
T
( )A.随c(X)的减小,反应①、②的速率均降低
B.体系中v(X)=v(Y)+v(Z)
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
三、非选择题
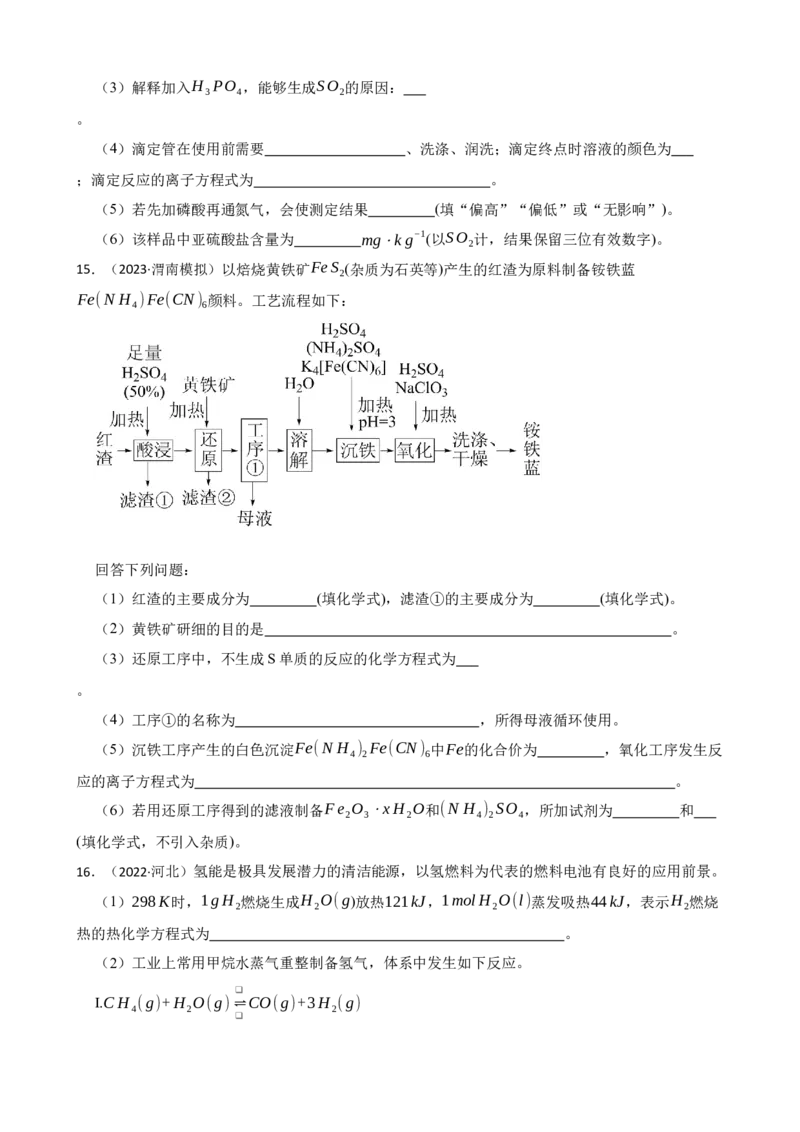
14.(2022·河北)某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下:
①三颈烧瓶中加入10.00g香菇样品和400mL水;锥形瓶中加入125mL水、1mL淀粉溶液,并预
加0.30mL0.01000mol⋅L−1的碘标准溶液,搅拌。
②以0.2L⋅min−1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至
终点时滴定消耗了1.00mL碘标准溶液。
③做空白实验,消耗了0.10mL碘标准溶液。
④用适量Na SO 替代香菇样品,重复上述步骤,测得SO 的平均回收率为95%。
2 3 2
已知:K (H PO )=7.1×10−3,K (H SO )=1.3×10−2
a1 3 4 a1 2 3
回答下列问题:
(1)装置图中仪器a、b的名称分别为 、 。
(2)三颈烧瓶适宜的规格为____(填标号)。
A.250mL B.500mL C.1000mL(3)解释加入H PO ,能够生成SO 的原因:
3 4 2
。
(4)滴定管在使用前需要 、洗涤、润洗;滴定终点时溶液的颜色为
;滴定反应的离子方程式为 。
(5)若先加磷酸再通氮气,会使测定结果 (填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为 mg⋅kg−1(以SO 计,结果保留三位有效数字)。
2
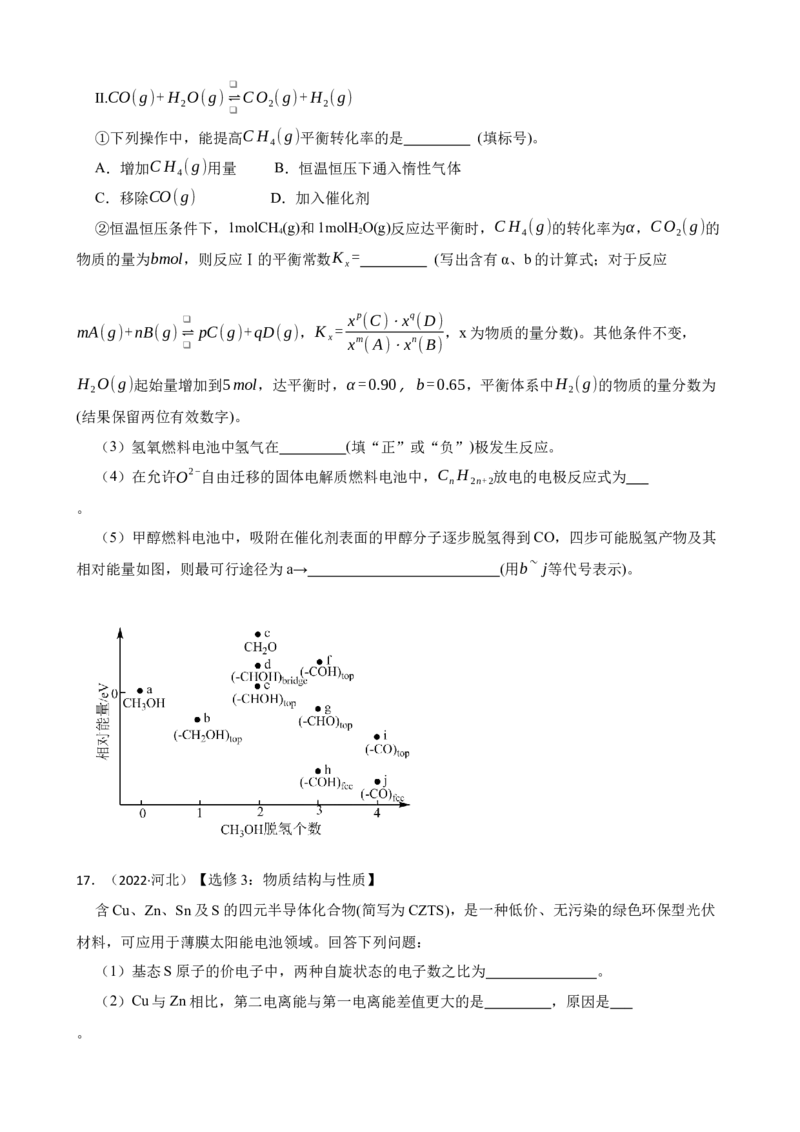
15.(2023·渭南模拟)以焙烧黄铁矿FeS (杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(N H )Fe(CN) 颜料。工艺流程如下:
4 6
回答下列问题:
(1)红渣的主要成分为 (填化学式),滤渣①的主要成分为 (填化学式)。
(2)黄铁矿研细的目的是 。
(3)还原工序中,不生成S单质的反应的化学方程式为
。
(4)工序①的名称为 ,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(N H ) Fe(CN) 中Fe的化合价为 ,氧化工序发生反
4 2 6
应的离子方程式为 。
(6)若用还原工序得到的滤液制备Fe O ⋅xH O和(N H ) SO ,所加试剂为 和
2 3 2 4 2 4
(填化学式,不引入杂质)。
16.(2022·河北)氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(1)298K时,1gH 燃烧生成H O(g)放热121kJ,1molH O(l)蒸发吸热44kJ,表示H 燃烧
2 2 2 2
热的热化学方程式为 。
(2)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
❑
Ⅰ.CH (g)+H O(g)⇌CO(g)+3H (g)
4 2 2
❑❑
Ⅱ.CO(g)+H O(g)⇌CO (g)+H (g)
2 2 2
❑
①下列操作中,能提高CH (g)平衡转化率的是 (填标号)。
4
A.增加CH (g)用量 B.恒温恒压下通入惰性气体
4
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1molCH (g)和1molH O(g)反应达平衡时,CH (g)的转化率为α,CO (g)的
4 2 4 2
物质的量为bmol,则反应Ⅰ的平衡常数K = (写出含有α、b的计算式;对于反应
x
❑ xp (C)⋅xq (D)
mA(g)+nB(g)⇌pC(g)+qD(g),K = ,x为物质的量分数)。其他条件不变,
❑
x xm (A)⋅xn (B)
H O(g)起始量增加到5mol,达平衡时,α=0.90,b=0.65,平衡体系中H (g)的物质的量分数为
2 2
(结果保留两位有效数字)。
(3)氢氧燃料电池中氢气在 (填“正”或“负”)极发生反应。
(4)在允许O2−自由迁移的固体电解质燃料电池中,C H 放电的电极反应式为
n 2n+2
。
(5)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其
相对能量如图,则最可行途径为a→ (用b~ j等代号表示)。
17.(2022·河北)【选修3:物质结构与性质】
含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏
材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为 。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是 ,原因是
。(3)SnCl❑ −的几何构型为 ,其中心离子杂化方式为 。
3
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质
中,属于顺磁性物质的是____(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO
3 2 3 4 4
C.[Zn(NH )]SO D.Na [Zn(OH)]
3 4 4 2 4
(5)如图是硫的四种含氧酸根的结构:
A. B. C. D.
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO❑ −的是 (填标号),理由是
4
。
(6)如图是CZTS四元半导体化合物的四方晶胞。
①该物质的化学式为 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如
3 1 1
图中A原子的坐标为( , , ),则B原子的坐标为 。
4 4 8
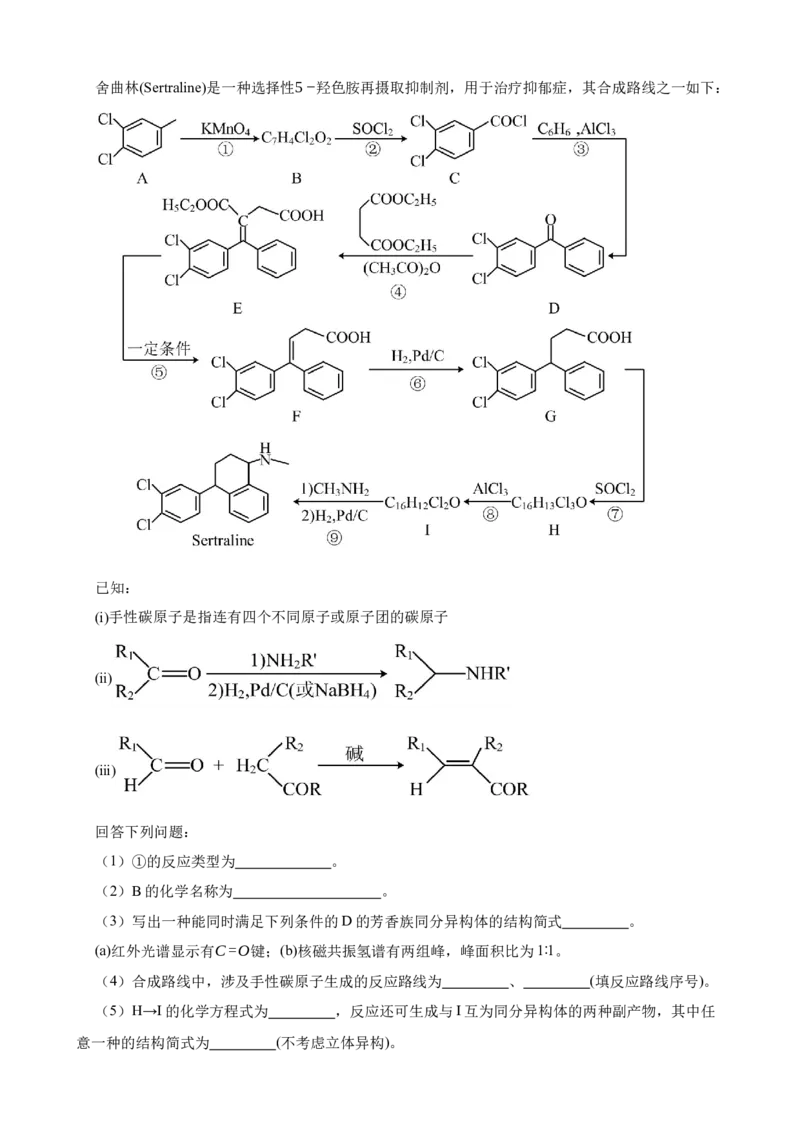
18.(2022·河北)【选修5:有机化学基础】舍曲林(Sertraline)是一种选择性5−羟色胺再摄取抑制剂,用于治疗抑郁症,其合成路线之一如下:
已知:
(ⅰ)手性碳原子是指连有四个不同原子或原子团的碳原子
(ⅱ)
(ⅲ)
回答下列问题:
(1)①的反应类型为 。
(2)B的化学名称为 。
(3)写出一种能同时满足下列条件的D的芳香族同分异构体的结构简式 。
(a)红外光谱显示有C=O键;(b)核磁共振氢谱有两组峰,峰面积比为1∶1。
(4)合成路线中,涉及手性碳原子生成的反应路线为 、 (填反应路线序号)。
(5)H→I的化学方程式为 ,反应还可生成与I互为同分异构体的两种副产物,其中任
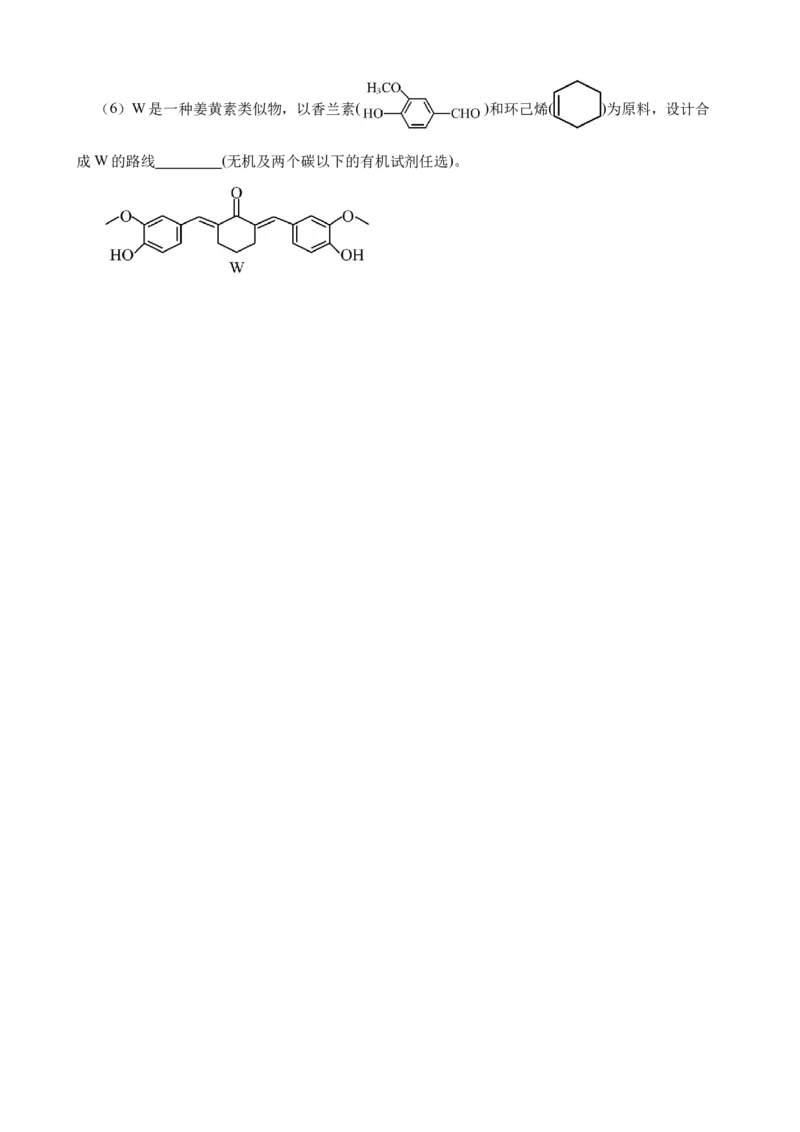
意一种的结构简式为 (不考虑立体异构)。(6)W是一种姜黄素类似物,以香兰素( )和环己烯( )为原料,设计合
成W的路线 (无机及两个碳以下的有机试剂任选)。