文档内容
酸和碱单元测试附参考答案
一、选择题
1.(宿迁市)小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关
系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示
出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
2.(2006年济宁市)按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组
物质中,符合“氧化物—酸—碱—盐” 顺序排列的是( )
A.HClO HCl Mg(OH) MgCl
2 2
B.CO HCO CaCO Ca(HCO )
2 2 3 3 3 2
C.H O HNO NH·H O NH NO
2 3 3 2 4 3
D.SO NaHSO NaOH Na SO
3 4 2 4
3.(连云港)下列设计方案可行,且化学方程式书写正确的是( )
A.用NaOH溶液治疗胃酸过多症:NaOH+HCl=NaCl+H O
2
B.实验室用稀硫酸与大理石反应制取CO:HSO +CaCO =CaSO +CO ↑+H O
2 2 4 3 4 2 2
C.用适量的稀盐酸除去铁表面的锈迹:Fe O+6HCl=2FeCl +3H O
2 3 3 2
D.用点燃的方法除去二氧化碳气体中混有的少量一氧化碳:2CO+O 点=== 2CO
2 2
4.(2006年烟台市)欲除去下列物质中的杂质,所需药品(括号中的物质)选择不正确的是( )
A.NaCl溶液中含有少量的NaSO (硝酸钡溶液)
2 4
B.CO 中含有少量的水蒸气(浓硫酸)
2
C.NaOH溶液中含有少量的NaCO(石灰水)
2 3
D.铜粉中含有少量的氧化铜(稀盐酸)
5.(2006年滨州市)Cu 0与硫酸反应的化学方程式为Cu O+HSO =Cu+ Cu SO +H O。氧化铜与氢气
2 2 2 4 4 2
反应 后得到的Cu中常常混有少量Cu O。现将10 g Cu和Cu O的混合物放入足量的稀硫酸中充分反应,
2 2
过滤得到9.5g固体,则原混合物中含Cu O的质量为( )
2
A.0.9 g B.9.5 g C.0.5 g D. 0.45 g
6.(2006·北京市)北京市正在实施“人文奥运文物保护计划”,其中修缮长城使用了大量的氢氧化钙,
氢氧化钙的俗称是( )
A、火碱 B、烧碱 C、熟石灰 D、小苏打
7.(2006·北京市)下列药品不需要密闭保存的是( )
A、浓盐酸 B、浓硫酸 C、烧碱 D、食盐
8.(韶关)化学中常常出现“1+1≠2”的有趣现象,但也有例外。下列符合“1+1=2”的事实是( )
1A. 20℃,1 L水与1 L酒精混合后的体积等于2 L
B. 20℃,1 g镁与1 g稀硫酸充分反应后所得的溶液质量为2 g
C. 20℃,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫
D. 20℃,1 g硝酸钾饱和溶液中加入1 g硝酸钾固体能得到2 g硝酸钾溶液
9.(深圳)日常生活中遇到的下列污垢,不宜用盐酸清洗的是( )。
A、保温瓶内的水垢 B、玻璃水槽内的黄色铁锈斑
C、不锈钢茶杯内的茶垢 D、盛石灰水的试剂内壁的白色固体
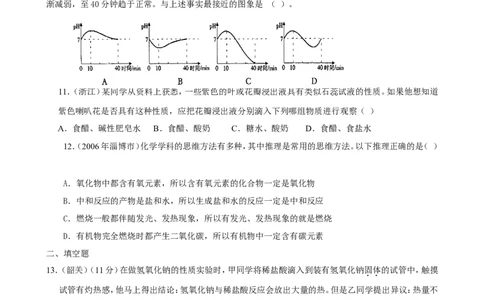
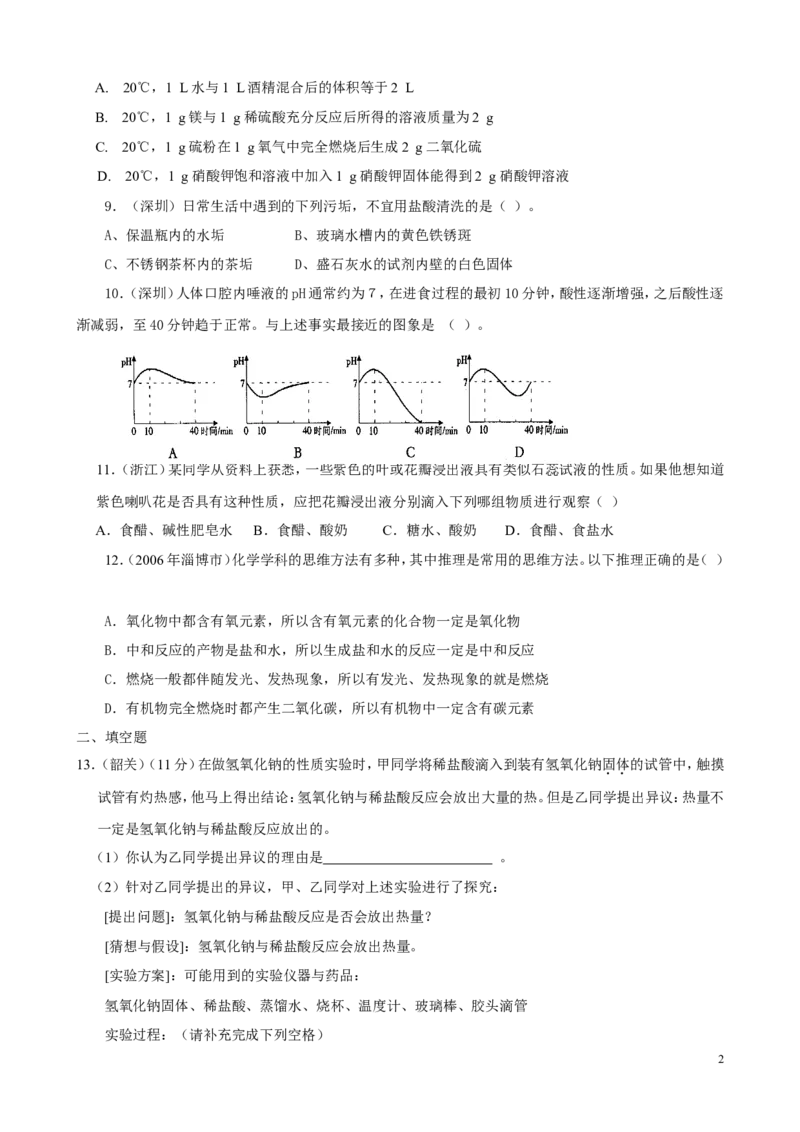
10.(深圳)人体口腔内唾液的pH通常约为7,在进食过程的最初10分钟,酸性逐渐增强,之后酸性逐
渐减弱,至40分钟趋于正常。与上述事实最接近的图象是 ( )。
11.(浙江)某同学从资料上获悉,一些紫色的叶或花瓣浸出液具有类似石蕊试液的性质。如果他想知道
紫色喇叭花是否具有这种性质,应把花瓣浸出液分别滴入下列哪组物质进行观察( )
A.食醋、碱性肥皂水 B.食醋、酸奶 C.糖水、酸奶 D.食醋、食盐水
12.(2006年淄博市)化学学科的思维方法有多种,其中推理是常用的思维方法。以下推理正确的是( )
A.氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物
B.中和反应的产物是盐和水,所以生成盐和水的反应一定是中和反应
C.燃烧一般都伴随发光、发热现象,所以有发光、发热现象的就是燃烧
D.有机物完全燃烧时都产生二氧化碳,所以有机物中一定含有碳元素
二、填空题
13.(韶关)(11分)在做氢氧化钠的性质实验时,甲同学将稀盐酸滴入到装有氢氧化钠固体的试管中,触摸
试管有灼热感,他马上得出结论:氢氧化钠与稀盐酸反应会放出大量的热。但是乙同学提出异议:热量不
一定是氢氧化钠与稀盐酸反应放出的。
(1)你认为乙同学提出异议的理由是 。
(2)针对乙同学提出的异议,甲、乙同学对上述实验进行了探究:
[提出问题]:氢氧化钠与稀盐酸反应是否会放出热量?
[猜想与假设]:氢氧化钠与稀盐酸反应会放出热量。
[实验方案]:可能用到的实验仪器与药品:
氢氧化钠固体、稀盐酸、蒸馏水、烧杯、温度计、玻璃棒、胶头滴管
实验过程:(请补充完成下列空格)
2实 验 结
实 验 步 骤 实 验 现 象
论
取适量NaOH固体放入
步
烧杯中,加入适量的水,
骤j 。
。
, 氢氧化钠
用胶头滴管将稀盐酸滴入到 与稀盐酸反应
步 。
步骤j所得的溶液中。 会放出热量。
骤k
(3)丙同学取步骤k反应后所得的溶液,继续进行探究。他向溶液中滴入无色酚酞试液,发现酚酞试液不
变色。因此他得出溶液呈中性的结论。你认为他的结论是否正确?
(填“是”或“否”),理由是 。
14. (2006·济南市) (4分)选择H、O、S、K四种元素中的适当元素,组成符合下列要求的物质,将化学
式填在空格中:
(1)最常用的溶剂 (2)能够供给呼吸的气体单质
(3)常用做干燥剂的一种酸 (4)常做化肥的一种盐
15.(长春)请对以下方案及现象做出合理补充或解释:
(1)将NaOH溶液滴在 上,再与标准比色卡比较,便可粗略测定氢氧化钠溶液的酸碱度。
(2)用一种试剂分别与食盐水、氢氧化钠溶液、稀硫酸作用,就能把它们直接鉴别出来,这种试剂是
。
(3)不能服用NaOH治疗胃酸过多,原因是NaOH具有 性。
(4)用NaCO 和KOH在溶液中进行反应制取NaOH,无法达到目的的原因是 。
2 3
16.(长春)根据信息回答下列问题:
(1)右图中三种酸溶于水时生成的阳离子全部是 ;
(2)由右图中可推测出,它们具有相似的化学性质。请写出氢溴酸(HBr)与
Ca(OH) 溶液反应的化学方程式为 ;
2
(3)依据一定的分类标准,可将这三种酸划分为两组:一组是HCl和HBr,另
一组只有HSO 。分类依据可以是①从组成方面看,HCl和HBr不含氧元素,HSO 含氧元素;
2 4 2 4
②从物理性质方面看 。
15.(2006·江西)(4分)请用化学方程式表示下列化工生产中的变化:
(1)生石灰制熟石灰 ; (2)一氧化碳还原氧化铁 ;
(3)用烧碱溶液吸收二氧化硫 ;
(4)铝和二氧化锰在高温条件下反应制造金属锰,同时生成另一种氧化物 。
17.(武汉)从熟石灰、一氧化碳、汽油、浓硫酸、硫磺、合成纤维中选择符合下列用途的物质,将其名称
或化学式填入相应的空格内。
3(1)干燥剂 ; (2)冶炼金属 ;
(3)有机溶剂 ; (4)处理酸性污水 。
(锦州)化学与人类的生活和生产有着密切的关系。
(1)请你用化学方程式表示生活或生产中的下列事实:
①在通风不畅的室内使用煤炉时,会产生有毒气体:
____________________________;
②胃酸过多的病人常服用含氢氧化铝的药物:
____________________________;
③工业上常用一氧化碳从赤铁矿(主要成分为FeO)中把铁还原出来:
2 3
____________________________。
(2)以上反应属于复分解反应的是(填序号)____。
三、实验题
18.(2006·沈阳市)(3分)中考前,沈阳市对初中毕业生进行了实验操作考查,小翔抽到的题签是:检验
溶液的酸碱性。他选择紫色石蕊试液完成了这个实验。一直喜欢科学探究的他在得知成绩合格后,立即向老
师询问,知道了样品1为稀氯化钠溶液,样品2为稀盐酸,样品3是稀碳酸钠溶液。细心的小翔还发现自己
废液缸里的废液呈现红色。请你帮他分析:
(1)废液里一定含有的物质是 、 (石蕊试液和水不填)。
(2)废液呈现红色的可能原因是 (从实验前配制样品或小翔实
验操作的角度分析,答一点即可)。
19.(深圳)某化学活动小组以“酸碱盐的性质”为主题,进行探究学习,请你做为该小组成员来解决
下列问题:
(1)小刚同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”。你认为这种推理
(填“正确”或“不正确”),你的例证是 。
(2)小丽同学从某一欠收农田里取回一份土壤样品,请你用两种不同的方法帮小丽测出该土壤样品浸
出液的酸碱性(只写出所用物品的名称即可):
① ;② 。
4如果检测的结果呈酸性,那么要改良此土壤,应该向农田里施加 。
(3)请你设计一个实验,能通过清晰可见的现象,除去氯化钙溶液中的少量稀盐酸。你的实验方案是
(写出实验操作、现象和结论):
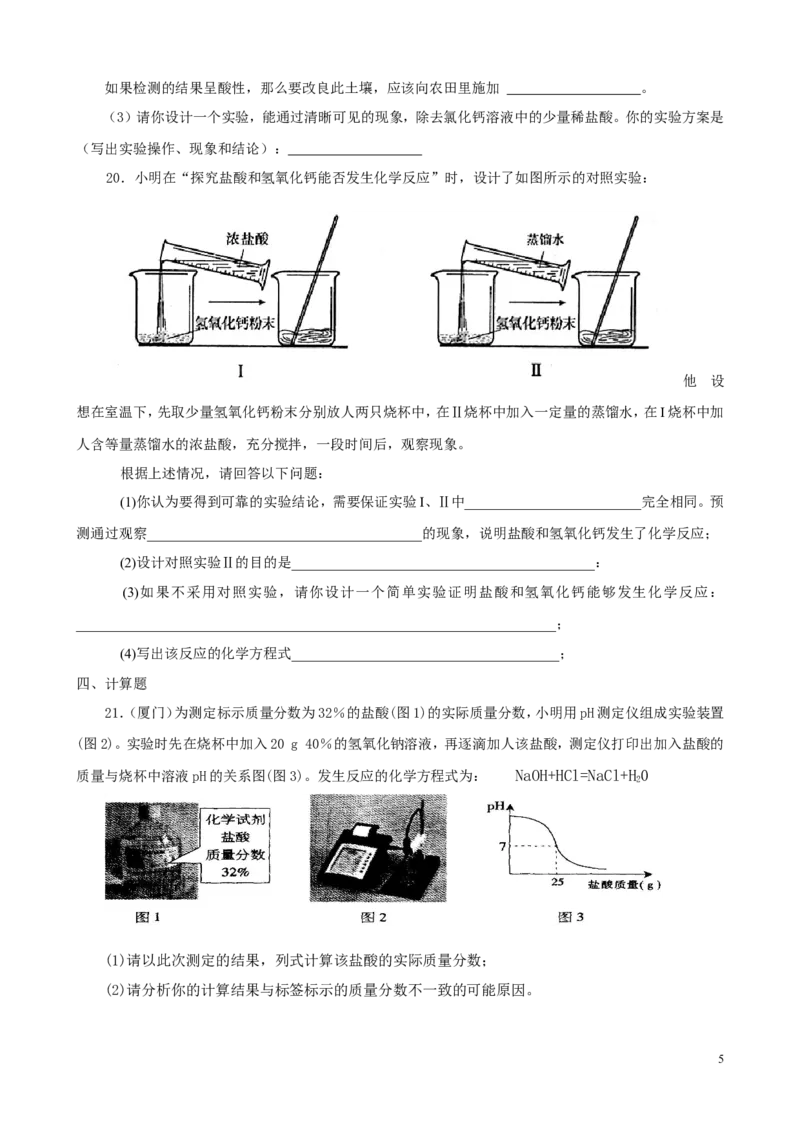
20.小明在“探究盐酸和氢氧化钙能否发生化学反应”时,设计了如图所示的对照实验:
他 设
想在室温下,先取少量氢氧化钙粉末分别放人两只烧杯中,在Ⅱ烧杯中加入一定量的蒸馏水,在I烧杯中加
人含等量蒸馏水的浓盐酸,充分搅拌,一段时间后,观察现象。
根据上述情况,请回答以下问题:
(1)你认为要得到可靠的实验结论,需要保证实验I、Ⅱ中_________________________完全相同。预
测通过观察_______________________________________的现象,说明盐酸和氢氧化钙发生了化学反应;
(2)设计对照实验Ⅱ的目的是___________________________________________:
(3)如果不采用对照实验,请你设计一个简单实验证明盐酸和氢氧化钙能够发生化学反应:
____________________________________________________________________;
(4)写出该反应的化学方程式______________________________________;
四、计算题
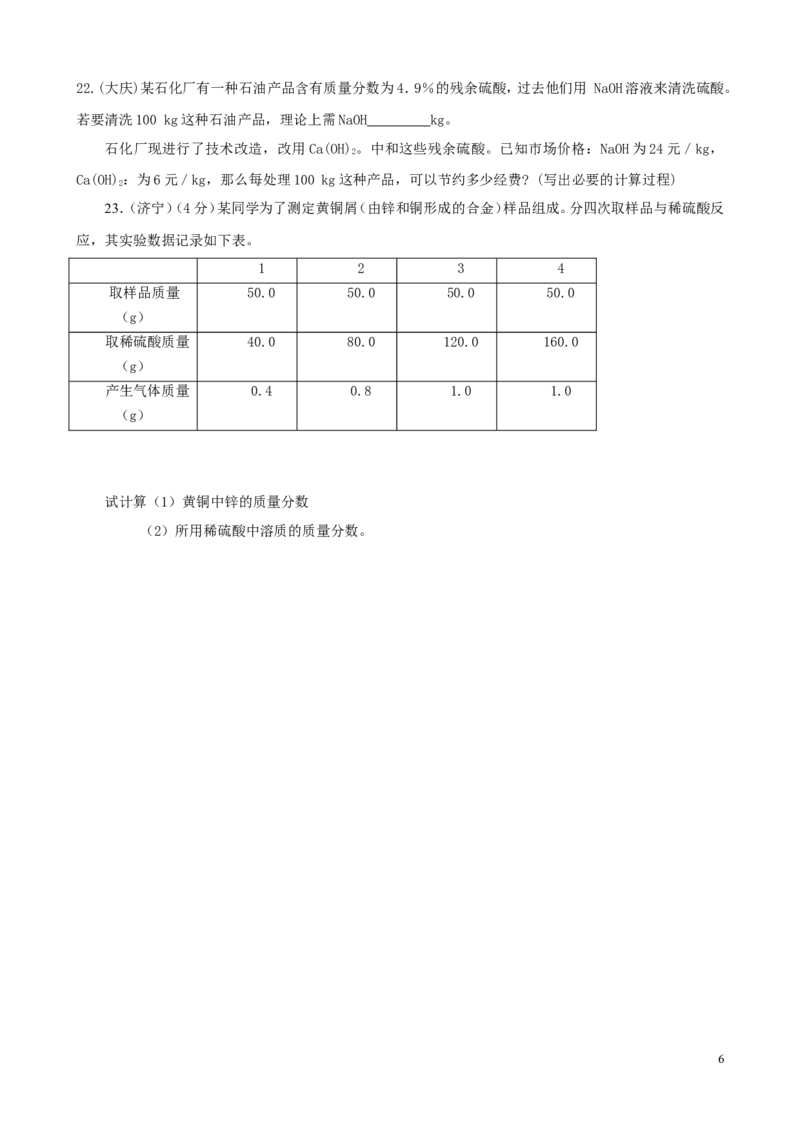
21.(厦门)为测定标示质量分数为32%的盐酸(图1)的实际质量分数,小明用pH测定仪组成实验装置
(图2)。实验时先在烧杯中加入20 g 40%的氢氧化钠溶液,再逐滴加人该盐酸,测定仪打印出加入盐酸的
质量与烧杯中溶液pH的关系图(图3)。发生反应的化学方程式为: NaOH+HCl=NaCl+H 0
2
(1)请以此次测定的结果,列式计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因。
522.(大庆)某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们用 NaOH溶液来清洗硫酸。
若要清洗100 kg这种石油产品,理论上需NaOH kg。
石化厂现进行了技术改造,改用Ca(OH) 。中和这些残余硫酸。已知市场价格:NaOH为24元/kg,
2
Ca(OH):为6元/kg,那么每处理100 kg这种产品,可以节约多少经费? (写出必要的计算过程)
2
23.(济宁)(4分)某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反
应,其实验数据记录如下表。
1 2 3 4
取样品质量 50.0 50.0 50.0 50.0
(g)
取稀硫酸质量 40.0 80.0 120.0 160.0
(g)
产生气体质量 0.4 0.8 1.0 1.0
(g)
试计算(1)黄铜中锌的质量分数
(2)所用稀硫酸中溶质的质量分数。
61 2 3 4 5 6
A C C A A C
7 8 9 10 11 12
D C C B A D
13(1)理由是: 氢氧化钠溶于水也会放热 (2分)。
(2)实验过程:(请补充完成下列空格)
(3) 否 (1分), 理由是: 若溶液呈酸性,酚酞试液也不变色 (2分) 。
14(1)HO (2)O (3)HSO (4)KSO
2 2 2 4 2 4
15 (1)PH试纸 (2)石蕊试液(或NH HCO 等) (3)腐蚀
4 3
(4)不符合复分解反应条件(或没有沉淀生成、不反应)
16(1)氢离子(或H+) (2)2HBr+Ca(OH) =CaBr +2H O
2 2 2
(3)HCI、HBr有挥发性,HSO 没有挥发性(或HCI, HBr有刺激性气味HSO 没有)
2 4 2 4
16(1)CaO+HO=Ca(OH) (2)3CO+Fe O 高温 2Fe+3CO
2 2 2 3 2
(3)2NaOH+SO ===Na SO +H O (4)4Al+3MnO 高温 3Mn+2Al O
2 2 3 2 2 2 3
17⑴浓硫酸 ⑵一氧化碳 ⑶汽油 ⑷熟石灰 (每空1分,写化学式或名称均可)
18 (4分,每空1分)(1)① ② ③
(2)②
19(1)HCl NaCl (2)盐酸溶液的溶质质量分数大(或盐酸加多了)
20(1)不正确 碳酸钠是盐,但水溶液呈碱性
(2)PH试纸 紫色石蕊试液 熟石灰
(3)往溶液中加过量的碳酸钙,会产生气泡。CaCO+2HCl=CaCl+HO+CO↑,当不再产生气泡时,将溶液过
3 2 2 2
滤,滤液中就不含有稀盐酸了。
21 (1)氢氧化钙粉末的质量(1分)
实验I中白色粉末消失成为无色溶液或实验I中的浑浊程度比实验Ⅱ中小(1分)
(2)排除氢氧化钙粉末溶于水的因素,以证实氢氧化钙粉末与盐酸发生化学反应(1分)
(3)在一定量的氢氧化钙粉末中加入适量的水,再滴加2--3滴酚酞试液,浑浊液变红,然后加入适量盐酸至
红色消失,变为无色液体,说明盐酸与氢氧化钙能够发生化学反应 (1分)
(4)Ca(OH) +2HCI=CaCl +2H 0(1分)
2 2 2
722(1)设此盐酸的质量分数为x (1分)
答 : (1)此待测盐酸质量分数为
29.2% (1分)
(2)盐酸具有挥发性(或需要进行重复实验等反思实验方案的答案) (2分)
23解:设改进后需要Ca(OH) 的质量为y
2
Ca(OH) +H S0 ==CaSO +2H O
2 2 4 4 2
74 98
y 100 kg x4.9%
y=4 kg
(1分)
可以节约经费:(4 kg x 24元/kg)—(3.7 kg×6元/kg)=73.8元(1分) 。
答:略
24(4分)(1)65% (2)49%
8