文档内容
辽宁省滨海实验中学 2019-2020 学年高一上学期期末化学试题
(2019 新人教版)
一、单选题(本大题共28小题,共56分)
1.下列物质与常用危险化学品的分类不对应的是( )
A. NaOH——腐蚀品 B. Na——遇湿易燃物品
C. 浓硫酸——易爆品 D. KMnO ——氧化剂
4
【答案】C
【解析】
【详解】A. NaOH具有腐蚀性,属于腐蚀品,A正确;
B. Na极易与水反应生成氢气和氢氧化钠,属于遇湿易燃物品,B正确;
C. 浓硫酸具有腐蚀性,不是易爆品,C错误;
D. KMnO 具有强氧化性,属于氧化剂,D正确;
4
答案选C。
2.“以人为本,安全至上”,下列化学实验操作方法不正确的是( )
A. 用坩埚或蒸发皿加热的实验完成后,不要直接用手拿回,应用坩埚钳夹取
B. 不慎将酸液溅到眼里,应立即用水冲洗,边洗边眨眼睛
C. 不得用燃着的酒精灯去点燃另一只酒精灯;酒精灯熄灭时不得用嘴去吹
D. 氢氧化钡固体洒落到地板上,立即用水冲洗
【答案】D
【解析】
【详解】A.用坩埚钳夹取灼热的坩埚或蒸发皿,不能直接用手拿回坩埚或蒸发皿,以免烫伤,故A正确;
B.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛,以最大程度减小对眼睛的危害,故B正确;
C.用燃着的火柴或木条点燃酒精灯,禁止用燃着的酒精灯引燃另一只酒精灯,用完酒精灯后,必须用灯帽
盖灭,不可用嘴去吹,否则可能将火焰沿灯颈压入灯内,引燃灯内的酒精蒸汽及酒精,可能会导致爆炸的
现象发生,故C正确;
D.氢氧化钡固体洒落到地板上时,应先收集固体药品,然后用大量水冲洗,故D错误;
故选D。
3.分类法在化学学习中具有重要意义,下列关于物质分类的正确组合是( )
碱 电解质 非电解质 碱性氧化物 酸性氧化物A NaCO HSO NaHCO MgO SO
2 3 2 4 3 2
B NaOH Cu NaCl NaO CO
2 2
C Ba(OH) CHCOOH Cl NaO NO
2 3 2 2
D KOH HNO SO CaO SO
3 2 3
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A. Na CO 属于盐类;NaHCO 属于电解质,A项错误;
2 3 3
B.Cu是金属单质,不属于电解质,也不属于非电解质;NaCl属于电解质;NaO 与酸反应除了盐和水之外,
2 2
还有氧气,不属于碱性氧化物;CO不与碱反应,不属于酸性氧化物,B项错误;
C. Cl 是非金属单质,不属于电解质,也不属于非电解质;NO不与碱反应,不属于酸性氧化物,C项错误;
2
D.所有物质分类均正确,D项正确;
答案选D。
【点睛】电解质和非电解质均属于化合物,单质和混合物,既不是电解质也不是非电解质。电解质包括酸、
碱、盐、活泼金属氧化物、水等;非电解质包括非金属氧化物、大多数有机物。
酸性氧化物和碱性氧化物分别与碱、酸反应生成盐和水,且化合物不发生改变。
4.在某无色、透明的强酸性溶液中,能大量共存的离子组是( )
A. NH +、NO -、Al3+、Cl- B. Na+、SO 2-、Ba2+、NO -
4 3 4 3
C. MnO -、K+、SO 2-、Na+ D. H+、SO 2-、HCO -、Na+
4 4 4 3
【答案】A
【解析】
【详解】A、NH +、NO -、Al3+、Cl-中无有色离子,在强酸性条件下不会发生化学反应,能够大量共存,
4 3
故A符合题意;
B、SO 2-与Ba2+会生成难溶物BaSO,不能大量共存,故B不符合题意;
4 4
C、MnO -溶液为紫红色,不符合题干无色溶液要求,故C不符合题意;
4
D、H+与HCO -会发生化学反应,不能大量共存,故D不符合题意。
3
【点睛】离子之间若不发生任何反应,则可以大量共存,若发生反应,则不能大量共存。离子之间发生的
反应类型有复分解反应、氧化还原反应、络合反应、盐的双水解反应,还要掌握常见的有色离子有哪些、这些离子的颜色是什么颜色等。
5.ClO 是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO :
2 2
,下列说法不正确的是( )
A. 1mol 参加反应,转移2mol电子
B. 在反应中被氧化
C. 的还原性强于ClO
2
D. CO 是 被氧化后得到的产物
2
【答案】A
【解析】
【分析】
中 元素从+5价降低到+4价, C元
素的化合价由+3价升高到+4价,据此分析;
【详解】A. 中 元素从+5价降低到+4价,1mol 参加反应,转移1mol电子,故A错误;
B. 中C元素化合价升高,作还原剂,在反应中被氧化,故B正确;
C.该反应中草酸是还原剂,二氧化氯是还原产物,所以草酸的还原性强于 ,故C正确;
D.该反应中C元素的化合价由+3价升高到+4价,所以草酸是还原剂, 是 被氧化后得到的产物,
故D正确。
故选A。
6.下列离子方程式,书写正确的是( )
.
A 盐酸与石灰石反应:CO2-+H+=CO ↑+H O
3 2 2
B. 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO2-=BaSO ↓
4 4
C. 氢氧化镁和盐酸反应:H++OH-=H O
2
D. 氯化铝溶液中加入过量氨水:Al3++3NH·HO=Al(OH) ↓+3NH+
3 2 3 4
【答案】D【解析】
【详解】A.碳酸钙不溶于水,不能写成离子形式,故A错误;
B.二者反应生成硫酸钡沉淀和氢氧化铜沉淀,故B错误;
C.氢氧化镁不溶于水,故C错误;
D.氯化铝和过量的氨水反应生成氢氧化铝沉淀和氯化铵,故D正确;
故选D。
【点睛】掌握离子方程式的书写要求,注意强酸和强碱和可溶性盐写成离子形式,有些反应和物质的量的
关系。
7.已知2MO x-+5S2-+16H+=2M2++5S↓+8H O,则MO x-中的x的值为
y 2 y
A. 1 B. 2 C. 3 D. 4
【答案】A
【解析】
【详解】根据电子的得失守恒可知5×2=2×n,解得n=5,即MO x-在反应中得到5个电子,所以化合价是
y
+7价。根据原子守恒可知,y=4,所以x=1,答案A。
8.反应 中,被氧化的物质与被还原的物质的物质的量之比为
A. 1:1 B. 1:2 C. 2:1 D. 3:1
【答案】C
【解析】
【分析】
根据化合价的变化分析,找出被氧化、被还原的物质。
【详解】反应中只有氮元素的化合价有变化,2NO 失电子被氧化为2HNO ,1NO 得电子被还原为1NO。
2 3 2
即被氧化的NO 与被还原的NO 的物质的量之比为2:1 。
2 2
本题选C。
9.下列有关NaCO 和NaHCO 的说法错误的是
2 3 3
A. 等质量NaCO 和NaHCO 分别和足量盐酸反应,相同条件下前者生成CO 少
2 3 3 2
B. 将石灰水分别加入NaHCO 和NaCO 中,前者不生成沉淀
3 2 3
C. 相同条件下NaCO 比NaHCO 更易溶于水
2 3 3
D. Na CO 固体中含少量NaHCO ,可用加热法除去
2 3 3
【答案】B
【解析】【详解】A.等质量的NaCO 和NaHCO ,碳酸钠的摩尔质量大,其物质的量少,盐酸足量,碳元素守恒,
2 3 3
则与盐酸完全反应碳酸钠产生的气体少,故A正确;
B.NaCO 和NaHCO 都能与澄清的石灰水反应生成沉淀,反应为CO2﹣+Ca2+=CaCO ↓,2HCO ﹣+Ca2+
2 3 3 3 3 3
+2OH﹣=CaCO ↓+2HO+CO2﹣,故B错误;
3 2 3
C.向饱和碳酸钠溶液中通入二氧化碳析出碳酸氢钠晶体,则相同条件下,在水中的溶解性为NaHCO <
3
NaCO,故C正确;
2 3
D.NaHCO 不稳定,加热易分解:2NaHCO NaCO+CO↑+HO,碳酸钠受热稳定,可用加热法除去,
3 3 2 3 2 2
故D正确;
故选B。
10.下列关于钠的化合物的叙述不正确的是
A. 热稳定性:
B. 与 都能和水反应生成碱,它们都是碱性氧化物
C. 碳酸氢钠可用于治疗胃酸过多
D. 中阴、阳离子的个数比为1:2
【答案】B
【解析】
【详解】A.NaHCO 不稳定,加热易分解,发生2NaHCO NaCO+H O+CO↑,碳酸钠受热不分解,
3 3 2 3 2 2
正确;
B.NaO 与水反应生成氢氧化钠和氧气,不是碱性氧化物,错误;
2 2
C.碳酸氢钠可与盐酸反应,且碳酸氢钠的碱性较弱,对胃壁的刺激作用较小,可用于中和胃酸过多,正
确;
D.NaO 中阴离子为O2-,NaO 中阴、阳离子的个数比为1:2,正确;
2 2 2 2 2
故选B。
11.经氯气消毒的自来水,若用于配制以下溶液:
①KOH ②AgNO ③NaHCO ④FeCl ⑤NaI ⑥NaHS ⑦NaHSO 会使配制的溶液变质的是
3 3 2 3
A. 全部 B. ②④⑤⑥ C. ②⑤ D. ④⑥
【答案】A
【解析】【详解】氯水含有 、 、H+、 、 ;KOH与H+反应而变质;AgNO 与 反应生成氯化
3
银沉淀;NaHCO 与H+反应生成二氧化碳;FeCl 与 反应生成氯化铁;NaI与 反应生成硫化钠;
3 2
NaHS与 反应生成硫单质;NaHSO 被 氧化成硫酸钠;
3
故A正确。
12.将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是
X气体 Y溶液 预测的现象
① CO 饱和NaCO 溶液 白色沉淀析出
2 2 3
② SO Ba(NO) 溶液 白色沉淀析出
2 3 2
③ Cl AgNO 溶液 白色沉淀析出
2 3
④ NH AlCl 溶液 白色沉淀析出
3 3
A. 只有①②③ B. 只有①②④ C. 只有①③④ D. ①②③④
【答案】D
【解析】
【详解】①二氧化碳与饱和NaCO 溶液发生反应生成碳酸钠,由于碳酸氢钠的溶解度小于碳酸钠,则会析
2 3
出白色沉淀,①正确;
②SO 通入水中生成HSO ,溶液呈酸性,NO ﹣在酸性条件下具有强氧化性,可发生反应:
2 2 3 3
3SO +2HO+2NO ﹣+3Ba2+=3BaSO↓+4H++2NO,则会析出白色沉淀,②正确;
2 2 3 4
③氯气与水反应:Cl+HO=H++Cl﹣+HClO,氯离子和银离子发生反应:Ag++Cl﹣=AgCl↓,则会析出白色
2 2
沉淀,③正确;
④一水合氨是弱碱,不能溶解氢氧化铝,氯化铝溶液通入过量氨气的反应方程式为:AlCl +3NH +3HO=
3 3 2
Al(OH)↓+3NH Cl,则会析出白色沉淀,④正确;
3 4
答案选D。
13.将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向
所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正
确的是( )A. Mg和Al的总质量为8g
B. 硫酸的物质的量浓度为5 mol/L
C. 生成的H 在标准状况下的体积为11.2L
2
D. NaOH溶液的物质的量浓度为5mol/L
【答案】D
【解析】
【分析】
由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后硫酸有剩
余,此时发生的反应为:HSO +2NaOH=Na SO +2H O。当V(NaOH溶液)=200mL时,沉淀量最大,此
2 4 2 4 2
时为 Mg(OH) 和Al(OH) ,二者物质的量之和为 0.35mol,溶液中溶质为 NaSO ,从 200mL到
2 3 2 4
240mL,NaOH溶解Al(OH) :NaOH+Al(OH) =NaAlO +2H O,当V(NaOH溶液)=240mL时,沉
3 3 2 2
淀不再减少,此时全部为Mg(OH),物质的量为0.15mol,所以Al(OH) 为0.35mol-0.15mol=0.2mol。
2 3
【详解】A.由元素守恒可知n(Al)=n[Al(OH) ]=0.2mol,n(Mg)=n[Mg(OH) ]=0.15mol,所以镁
3 2
和铝的总质量为0.2mol×27g/mol+0.15mol×24g/mol=9g,A错误;
B.沉淀量最大时为Mg(OH) 和Al(OH),溶液中溶质为NaSO ,根据钠元素守恒可知此时n
2 3 2 4
(NaSO )等于240mL氢氧化钠溶液中含有的n(NaOH)的1/2倍,所以n(NaSO )=1/2×0.2L×5mol/
2 4 2 4
L=0.5mol,硫酸的浓度为0.5mol÷0.5L=1mol/L,B错误;
C.由A中分析可知n(Al)=0.2mol,n(Mg)=0.15mol,根据电子转移守恒可知2n(H)=3n(Al)+2n
2
(Mg)=3×0.2mol+2×0.15mol=0.9mol,所以n(H)=0.45mol,故氢气体积为0.45mol×22.4mol/L=10.08L,
2
C错误;
D.由200~240mL发生Al(OH)+NaOH=NaAlO +2H O,所以该阶段消耗n(NaOH)=n[Al(OH)
3 2 2
]=0.2mol,氢氧化钠的浓度为0.2mol÷(0.24L−0.2L)=5mol/L,D正确;
3
答案选D。
14.设N 是阿伏加德罗常数 的值,以下说法正确的是( )
A
A. 在常温、常压下,11.2 L N 含有的分子数为0.5 N
2 AB. 标准状况下,22.4 L H 和O 的混合气体所含分子数为N
2 2 A
C. 标准状况下,18 g HO的体积是22.4 L
2
D. 1 mol SO 的体积是22.4 L
2
【答案】B
【解析】
【详解】A. 在常温、常压下,气体摩尔体积不为22.4L/mol,则11.2 L N 含有 的分子数无法计算,与题意
2
不符,A错误;
B. 标准状况下,1mol任何气体的体积均为22.4L,则22.4 L H 和O 的混合气体的物质的量为1mol,所含
2 2
分子数为N ,符合题意,B正确;
A
C. 标准状况下,18 g H0为1mol,其为液体,则体积小于22.4 L,与题意不符,C错误;
2
D. 标准状况下,1 mol SO 的体积是22.4 L,与题意不符,D错误;
2
答案为B。
15.已知硝酸能将Fe2+氧化为Fe3+.下列物质反应后能使KSCN溶液变红的是( )
①过量的Fe与Cl 反应
2
②Fe和过量稀硫酸反应
③FeCl 溶液中通入少量Cl
2 2
④Fe和Fe O 的混合物溶于盐酸中
2 3
⑤向Fe(NO ) 溶液中加入过量稀硫酸.
3 2
.
A 只有① B. 只有①③⑤ C. 只有①②③ D. 全部
【答案】B
【解析】
【分析】
①过量的Fe与Cl 反应生成氯化铁;
2
②Fe和过量稀硫酸反应生成硫酸亚铁;
③FeCl 溶液中通入少量Cl,反应生成氯化铁;
2 2
④Fe和Fe O 的混合物溶于盐酸中,铁与盐酸反应生成氯化亚铁,三氧化二铁与盐酸反应生成氯化亚铁和
2 3
氯化铁,如果铁过量,铁与绿化铁反应生成氯化亚铁;
⑤向Fe(NO ) 溶液中加入过量稀硫酸,硝酸根离子在酸性环境下能够氧化二价铁离子生成三价铁离子。
3 2
能使KSCN溶液变红是三价铁离子,据此分析。
【详解】①过量的Fe与Cl 反应生成氯化铁,氯化铁中含有三价铁离子,能使KSCN溶液变红,故①正确;
2
②Fe和过量稀硫酸反应生成硫酸亚铁,不含三价铁离子,不能使KSCN溶液变红,故②错误;③FeCl 溶液中通入少量Cl,反应生成氯化铁,含有三价铁离子,能使KSCN溶液变红,故③正确;
2 2
④Fe和Fe O 的混合物溶于盐酸中,铁与盐酸反应生成氯化亚铁,三氧化二铁与盐酸反应生成氯化亚铁和
2 3
氯化铁,如果铁过量,铁与氯化铁反应生成氯化亚铁,不含三价铁离子,不能使KSCN溶液变红,故④错
误;
⑤向Fe(NO ) 溶液中加入过量稀硫酸,硝酸根离子在酸性环境下能够氧化二价铁离子生成三价铁离子,
3 2
能使KSCN溶液变红,故⑤正确;
答案选B。
16.某溶液中含有大量Fe2+、Al3+、Fe3+、Na+、Cl-、SO 2-离子,其中加入足量NaO 固体后,再加入足量的
4 2 2
盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
A. Na+、Fe2+ B. Al3+、SO 2- C. Fe3+、SO 2- D. Al3+、Cl-
4 4
【答案】B
【解析】
【详解】A.因为NaO 是强氧化剂,而且遇水生成NaOH,钠离子浓度增大,故A错误;
2 2
B.NaO 是强氧化剂,而且遇水生成NaOH,铝离子能和过量的氢氧化钠反应生成四羟基合铝酸根离子,
2 2
在盐酸作用下又会生成铝离子,根据铝元素守恒,则铝离子量不变,硫酸根离子自始至终不发生变化,故
B正确;
C.因为NaO 是强氧化剂,而且遇水生成NaOH,Fe2+氧化成Fe3+,并沉淀,再和盐酸反应生成三价铁离
2 2
子,所以三价铁离子浓度增大,故C错误;
D.加入足量的盐酸溶解沉淀,氯离子浓度增大,故D错误;
故选B。
【点晴】可以根据所学知识进行回答,难度不大,注意亚铁离子被氧化为三价铁离子是解题的易错点,溶
液中加入足量的NaO 固体,充分反应后,再加入过量的稀盐酸,Fe2+氧化成Fe3+,减少的是亚铁离子,增
2 2
加的是三价铁离子。
17.下列反应的离子方程式书写正确的是( )
A. 铝粉投入NaOH溶液中:2Al+2OH-===2AlO-+H↑
2 2
B. Na与CuSO 溶液反应:Cu2++2Na===2Na++Cu
4
C. 向AlCl 溶液中加入足量的氨水:Al3++3OH-===Al(OH)↓
3 3
D. Ba(OH) 溶液与稀硫酸反应:Ba2++2OH-+2H++SO2-===BaSO↓+2HO
2 4 4 2
【答案】D
【解析】
【详解】A. 题干中离子方程式得失电子不守恒,质量不守恒,应改为 2Al+2OH-+2HO=2AlO-+3H↑,
2 2 2故A错误;
B、钠放入硫酸铜溶液中是与水发生反应,离子方程式为2Na+2HO+Cu2+=2Na++H ↑+Cu(OH) ,故B错误;
2 2 2
C、一水合氨为弱碱,书写离子方程式时不能拆开,离子反应为:Al3++3NH ·H O=Al(OH) ↓+ NH +,故C
3 2 3 4
错误;
D、Ba(OH) 溶液与稀硫酸反应生成硫酸钡沉淀和水,离子方程式为:Ba2++2OH-+2H++SO
2
===BaSO ↓+2HO,故D正确;
4 2
综上所述,本题应选D。
【点睛】本题考查离子方程式正误的判断。判断离子方程式是否正确可从以下几个方面进行:①从反应原
理进行判断,如反应是否能发生、反应是否生成所给产物等(题中B项);②从物质存在形态进行判断,如
拆分是否正确、是否正确表示了难溶物和气体等(题中C项);③从守恒角度进行判断,如原子守恒、电荷
守恒、氧化还原反应中的电子守恒等(题中A项);④从反应的条件进行判断;⑤从反应物的组成以及反
应物之间的配比进行判断。
18.等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的物
质的量之比是( )
A. 1:1 B. 3:4 C. 2:3 D. 4:3
【答案】B
【解析】
【分析】
令Fe 的物质的量为1mol,根据方程式计算出生成氢气的物质的量,再根据相同条件下体积之比等于物质
的量之比确定两反应中生成氢气体积之比。
【详解】令Fe的物质的量为1mol,则:
Fe+2HCl=FeCl +H ↑
2 2
1mol 1mol
3Fe+4H O(g) Fe O+4H
2 3 4 2
1mol mol,相同条件下体积之比等于物质的量之比,则两反应中生成氢气体积之比为1mol: mol =3:4。
答案选B。
【点睛】本题考查根据方程式的计算,比较基础,清楚铁与水蒸气的反应是关键,注意基础知识的理解掌
握。
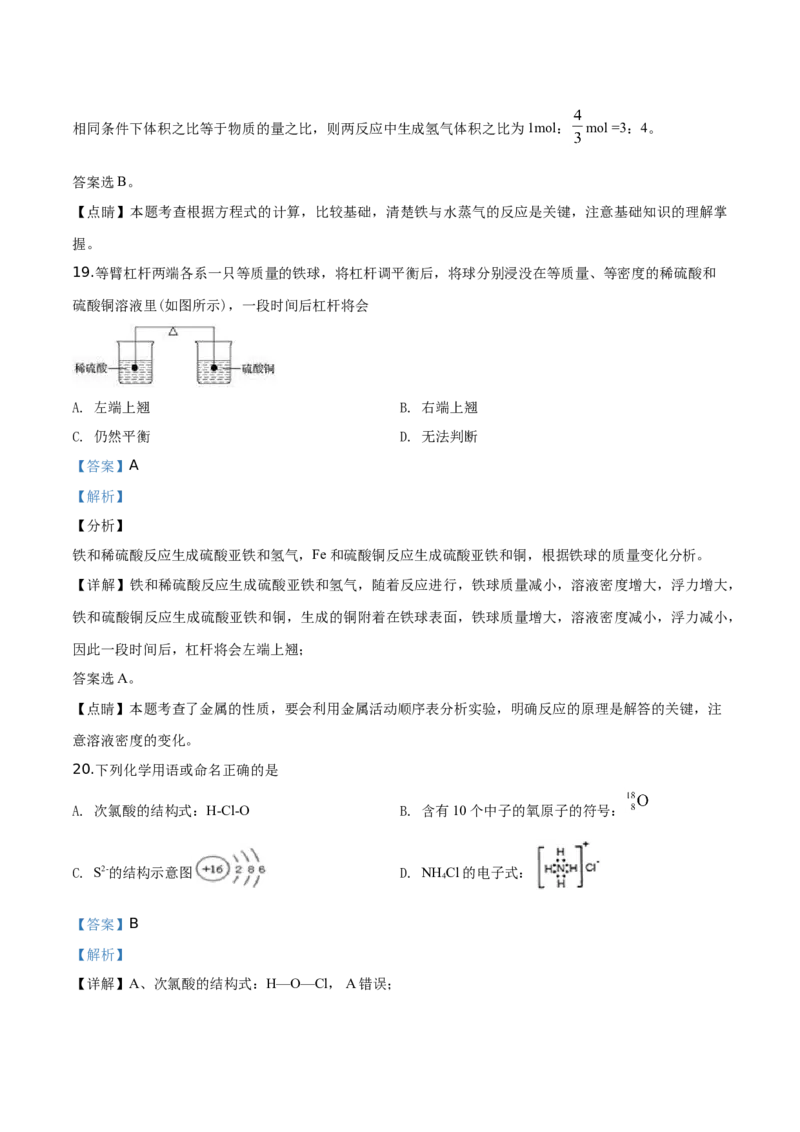
19.等臂杠杆两端各系一只等质量的铁球,将杠杆调平衡后,将球分别浸没在等质量、等密度的稀硫酸和
硫酸铜溶液里(如图所示),一段时间后杠杆将会
A. 左端上翘 B. 右端上翘
C. 仍然平衡 D. 无法判断
【答案】A
【解析】
【分析】
铁和稀硫酸反应生成硫酸亚铁和氢气,Fe和硫酸铜反应生成硫酸亚铁和铜,根据铁球的质量变化分析。
【详解】铁和稀硫酸反应生成硫酸亚铁和氢气,随着反应进行,铁球质量减小,溶液密度增大,浮力增大,
铁和硫酸铜反应生成硫酸亚铁和铜,生成的铜附着在铁球表面,铁球质量增大,溶液密度减小,浮力减小,
因此一段时间后,杠杆将会左端上翘;
答案选A。
【点睛】本题考查了金属的性质,要会利用金属活动顺序表分析实验,明确反应的原理是解答的关键,注
意溶液密度的变化。
20.下列化学用语或命名正确的是
A. 次氯酸的结构式:H-Cl-O B. 含有10个中子的氧原子的符号:
C. S2-的结构示意图 D. NH Cl的电子式:
4
【答案】B
【解析】
【详解】A、次氯酸的结构式:H—O—Cl, A 错误;B、氧的元素符号为O,该氧原子的质量数A=8+10=18,则该原子的化学符号为 ,B正确;
C、S2-最外层为8个电子,结构示意图为 ,C错误;
D、NH Cl的电子式: ,D错误;
4
答案选B。
21.已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,
不正确的是( )
A. 原子序数:Y>X>Z>W B. 离子半径:X+>Y2+>Z->W2-
C. 原子最外层电子数:Z>W>Y>X D. 还原性:X>Y,W2->Z-
【答案】B
【解析】
【分析】
四种离子均具有相同的电子层结构,阳离子原子序数=核外电子数 +电荷数,阴离子
原子序数=核外电子数-电荷数,
A.根据原子序数与核外电子数、电荷数之间的关系式确定原子序数;
B.电子层结构相同的离子,离子半径随着 原子序数增大而减小;
C.主族元素阳离子最外层电子数=其最高正化合价,阴离子最低负化合价=最外层电子数-8;
D.同一周期元素,元素的金属性越强,其还原性越强;同一周期非金属元素,元素的非金属性越强,其简
单阴离子的还原性越弱;
【详解】X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,由离子所带电荷可知,X、Y处于同一周期,
原子序数Y>X;Z、W处于同一周期,且处于X、Y所在周期上一周期,原子序数Z>W,所以原子序数
Y>X>Z>W,再根据元素周期律递变规律判断;
A.X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,由离子所带电荷可知,X、Y处于同一周期,原子
序数Y>X;Z、W处于同一周期,且处于X、Y所在周期上一周期,原子序数Z>W,所以原子序数Y>
X>Z>W,故A正确;
B.电子层结构相同核电荷数越大,离子半径越小,故离子半径:Y2+<X+<Z-<W2-,故B错误;
C.X、Y处于同一周期,原子序数Y>X,则原子最外层电子数Y>X;Z、W处于同一周期,原子序数Z>W,则原子最外层电子数Z>W,X、Y形成阳离子,Z、W形成阴离子,所以最外层电子数Z>W>Y>
X,故C正确;
D.X、Y处于同一周期,形成阳离子,原子序数Y>X,所以金属性:X>Y;Z、W处于同一周期,形成阴
离子,原子序数Z>W,所以非金属性Z>W,非金属性越强,阴离子还原性越弱,所以还原性:W2->
Z-,故D正确。
故选B。
22.下列各组性质比较中,正确的是()
①沸点:
②离子还原性:
③酸性:
④金属性:
⑤气态氢化物稳定性:
⑥半径:
A. ①②③ B. ③④⑤⑥ C. ②③④ D. ①③④⑤⑥
【答案】B
【解析】
【详解】①.HF 中含分子间氢键,沸点最高,其它氢化物中相对分子质量大的沸点高,则沸点为
,故错误;
②.元素的非金属性 ,对应离子还原性 ,故错误;
③.非金属性 ,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,即酸性:
,故正确;
④.同主族从上到下,金属性增强: ,同周期从左到右,金属性减弱,即 ,即金属
性: ,故正确;⑤.元素的非金属性 ,气态氢化物稳定性 ,故正确;
⑥.电子层越多,离子半径越大,核外电子排布相同时,核电荷数越多,半径越小,即
,故正确。
故选B。
23.下列物质中,既有离子键又有共价键的是( )
A. MgCl B. Ca(OH) C. HO D. N
2 2 2 2
【答案】B
【解析】
【详解】A.氯化镁中只含离子键,故A错误;
B.氢氧化钙中钙离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,故B正确;
C.水分子中只含共价键,故C错误;
D.氮气分子中只含共价键,故D错误。
故选B。
【点睛】既含离子键有含共价键的物质是离子化合物:①铵盐类,如NH Cl、NH NO 、(NH )CO 等;
4 4 3 4 2 3
②强碱类,如KOH、NaOH等;③含氧酸盐,如KSO 、NaHCO 等;④过氧化物,如NaO,超氧化物,
2 4 3 2 2
如KO 。
2
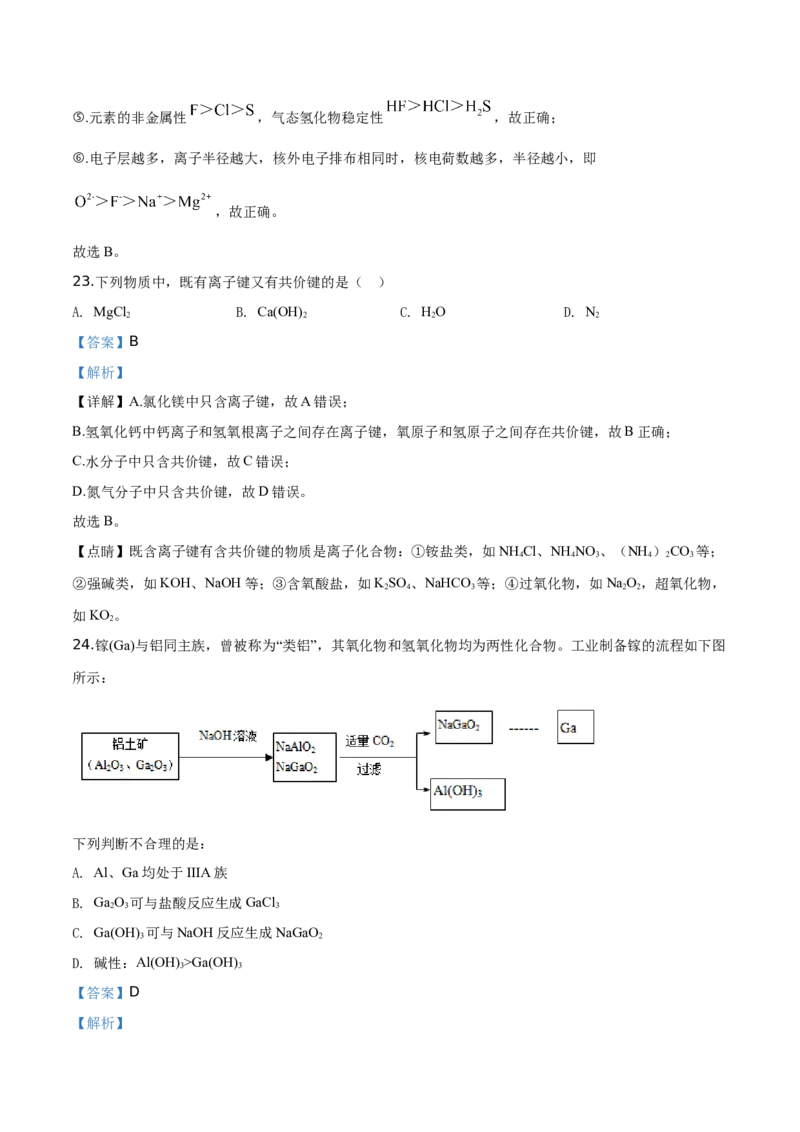
24.镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图
所示:
下列判断不合理的是:
A. Al、Ga均处于IIIA族
B. GaO 可与盐酸反应生成GaCl
2 3 3
C. Ga(OH) 可与NaOH反应生成NaGaO
3 2
D. 碱性:Al(OH) >Ga(OH)
3 3
【答案】D
【解析】【详解】A.镓(Ga)与铝同主族,均处于ⅢA族,故A正确;
B.GaO 与Al O 的性质具有相似性,可与盐酸反应生成GaCl ,故B正确;
2 3 2 3 3
C.Ga(OH) 属于两性氢氧化物,与Al(OH) 的性质相似,能与NaOH溶液生成NaGaO ,故C正确;
3 3 2
D.同主族元素从上到下金属性增强,则碱性:Al(OH) <Ga(OH) ,故D错误;
3 3
故选D。
25.实验室配制250 mL 0.200 mol/L NaCl溶液,下列操作导致所配溶液浓度偏高的是( )
A. 容量瓶洗净后未干燥 B. 移液后烧杯未洗涤
C. 定容时俯视读数 D. 摇匀后液面低于刻度线再滴加水至刻度线
【答案】C
【解析】
【分析】
依据 进行误差分析,凡是使n偏大或者使V偏小的操作,溶液浓度偏高,凡是使n偏小或者V偏大
的操作,溶液浓度偏低,据此进行判断;
【详解】A.容量瓶洗净后未干燥,在定容时要加入蒸馏水,不影响溶液浓度,故A错误;
B.移液后烧杯未洗涤,相当于损失了一部分的溶质,故溶液浓度会偏低,故B错误;
C.定容时俯视读数,溶液体积偏小,溶液浓度偏大,故C正确;
D.摇匀后液面低于刻度线再滴加水至刻度线,会使溶液浓度偏低,故D错误;
故选C。
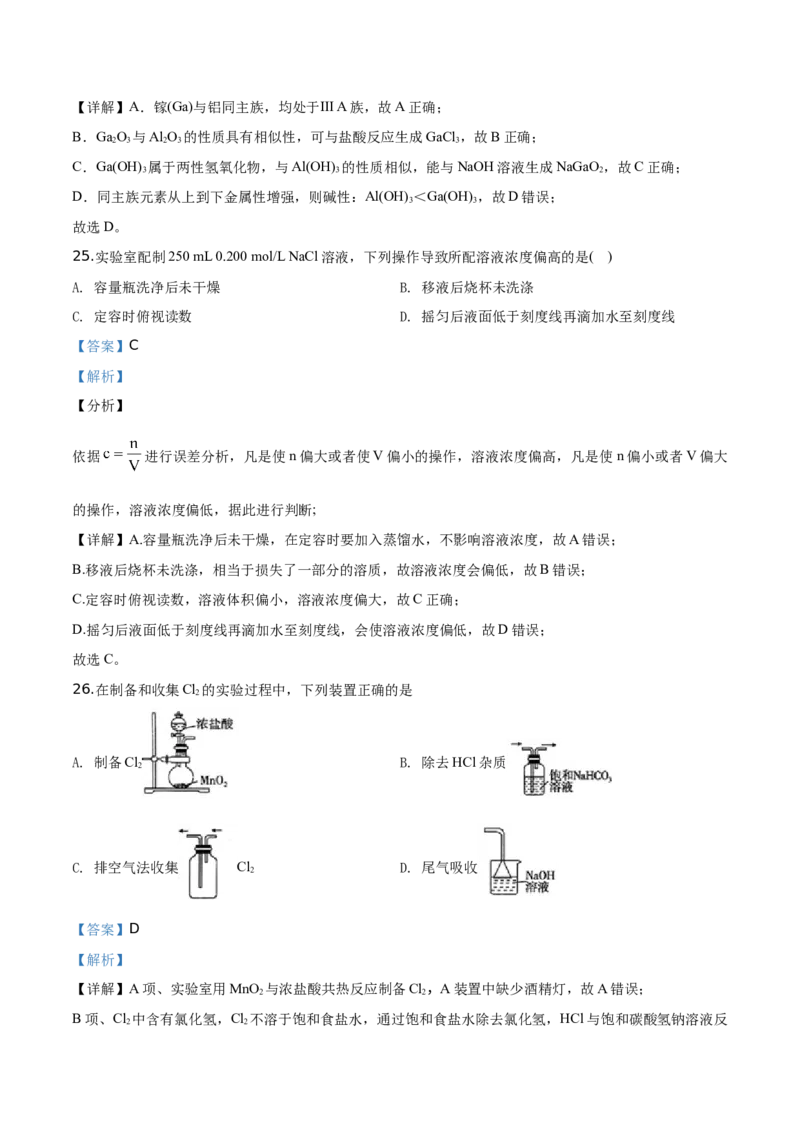
26.在制备和收集Cl 的实验过程中,下列装置正确的是
2
A. 制备Cl B. 除去HCl杂质
2
C. 排空气法收集 Cl D. 尾气吸收
2
【答案】D
【解析】
【详解】A项、实验室用MnO 与浓盐酸共热反应制备Cl,A装置中缺少酒精灯,故A错误;
2 2
B项、Cl 中含有氯化氢,Cl 不溶于饱和食盐水,通过饱和食盐水除去氯化氢,HCl与饱和碳酸氢钠溶液反
2 2应会生成CO 杂质,达不到除杂目的,故B错误;
2
C项、Cl 密度比空气大,用向上排空气法收集Cl,应从长管通入气体,故C错误;
2 2
D项、Cl 有毒需要用氢氧化钠溶液吸收,倒置的漏斗能够防止倒吸,故D正确。
2
故选D。
【点睛】本题考查氯气的实验室制法,B项为易错点,注意从氯气的制备原理和氯气的性质进行分析判断。
27.在制作印刷电路板的过程中常利用FeCl 溶液与Cu反应,其反应方程式为:
3
2FeCl +Cu=2FeCl +CuCl 。现向FeCl 溶液中加入a g Cu粉,完全溶解后,再加入b g Fe粉,充分反应后
3 2 2 3
尚有c g残余固体。若c<a,则下列说法正确的是
A. 残余固体全部是Cu
B. 残余固体可能为Fe和Cu的混合物
C. 最后得到的溶液可能含有Fe3+
D. 残余固体是Fe,溶液中一定不含Cu2+
【答案】A
【解析】
【分析】
此题中发生的化学反应有三个,方程式如下: 2FeCl +Cu=2FeCl +CuCl 、CuCl +Fe=FeCl +Cu、
3 2 2 2 2
2FeCl +Fe=3FeCl ,依元素守恒可知:
3 2
步骤一:ag铜完全溶解后,变为ag铜离子;
步骤二:若加入的铁足够多的话,可将溶液中的铜离子全部变回金属铜(ag)甚至还会有铁剩余,此时,
残余固体(cg)应大于或等于ag;
依题意:a>c可知,加入的铁是不足量的,此时溶液中还有部分铜未完全置换出来,
结论1:剩余固体为Cu,不可能有Fe剩余;
步骤三:根据方程式1、2、3可知,溶液中一定有Fe2+,由上述推导可知,溶液中还应有Cu2+剩余,由方
程式1可知,Cu与Fe3+是不能共存的,剩余固体中有Cu,则溶液中必无Fe3+,
结论2:充分反应后剩余固体为Cu,而溶液中含FeCl 和CuCl ;
2 2
【详解】A、由上述分析可知,残余固体全部是Cu,A正确;
B、由上述分析可知,残余固体全部是Cu,B错误;
C、因Cu可以和Fe3+反应,所以Cu与Fe3+是不能共存的,C错误;
D、残余固体是Cu,溶液中一定含有Cu2+,D错误;
答案选A。
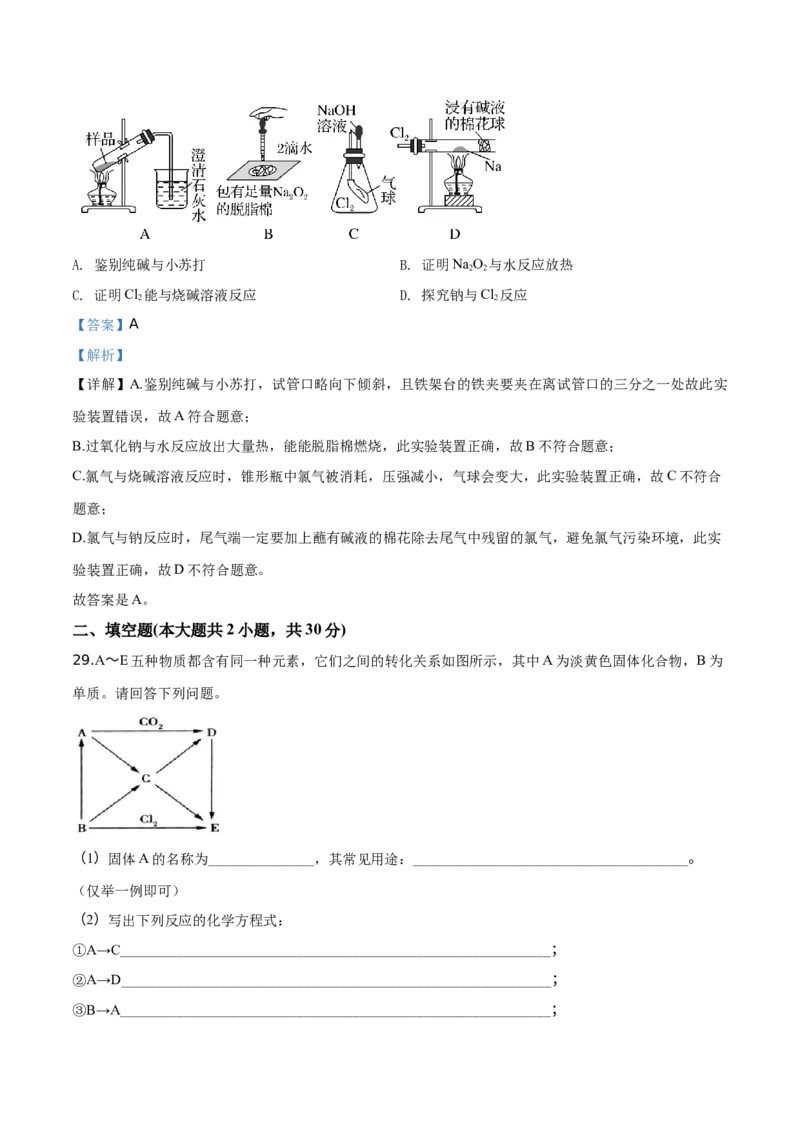
28.用如图所示实验装置进行相关实验探究,其中装置不合理的是( )A. 鉴别纯碱与小苏打 B. 证明NaO 与水反应放热
2 2
C. 证明Cl 能与烧碱溶液反应 D. 探究钠与Cl 反应
2 2
【答案】A
【解析】
【详解】A.鉴别纯碱与小苏打,试管口略向下倾斜,且铁架台的铁夹要夹在离试管口的三分之一处故此实
验装置错误,故A符合题意;
B.过氧化钠与水反应放出大量热,能能脱脂棉燃烧,此实验装置正确,故B不符合题意;
C.氯气与烧碱溶液反应时,锥形瓶中氯气被消耗,压强减小,气球会变大,此实验装置正确,故C不符合
题意;
D.氯气与钠反应时,尾气端一定要加上蘸有碱液的棉花除去尾气中残留的氯气,避免氯气污染环境,此实
验装置正确,故D不符合题意。
故答案是A。
二、填空题(本大题共2小题,共30分)
29.A~E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为
单质。请回答下列问题。
(1)固体A的名称为_______________,其常见用途:_______________________________________。
(仅举一例即可)
(2)写出下列反应的化学方程式:
①A→C_____________________________________________________________;
②A→D_____________________________________________________________;
③B→A_____________________________________________________________;④B→C_____________________________________________________________。
【答案】 (1). 过氧化钠 (2). 漂白剂、供氧剂等 (3). 2NaO +2HO ===4NaOH+O↑ (4).
2 2 2 2
2NaO+2CO===2Na CO+O (5). 2Na+O NaO (6). 2Na+2HO===2NaOH+H↑
2 2 2 2 3 2 2 2 2 2 2
【解析】
【分析】
A为淡黄色固体化合物,B为单质,则A为过氧化钠,B为钠单质,B在氧气中加热反应生成过氧化钠,
过氧化钠与二氧化碳反应生成D,D为碳酸钠,故此可推出C为氢氧化钠,E为氯化钠。据此分析可得结
论。
【详解】(1)由上述分析可知固体A为过氧化钠,通常可作漂白剂和供氧剂,故答案为过氧化钠;漂白
剂、供氧剂等;
(2)① A→C反应的化学方程式为:2NaO+2HO ===4NaOH+O↑;
2 2 2 2
②A→D反应的化学方程式为:2NaO+2CO===2Na CO+O;
2 2 2 2 3 2
③B→A反应的化学方程式为:2Na+O NaO;
2 2 2
④B→C反应的化学方程式为:2Na+2HO===2NaOH+H↑。
2 2
30.从古至今,铁及其化合物在人类的生产生活中都起了巨大的作用。
(1)实验室在配制 FeSO 溶液时为了防止 FeSO 溶液变质,经常向其中加入铁粉,其原因是
4 4
______________(用离子方程式表示)。
(2)向FeSO 溶液中滴加氨水的现象为 ______________________,请用化学用语解释出现此现象的原因
4
___________________;_____________________
(3)现有配制所得的 100mL 6mol/L FeSO 溶液,往其中滴入一定量稀硝酸,请回答下列问题:
4
①配平该反应的离子方程式:____Fe2+____NO -+____H+ = ___Fe3++____NO↑+_____HO(在横线上写
3 2
上化学计量数)
②要检验该反应后的溶液中是否还含有 Fe2+,可选用下列的一种试剂为_______
A.酸性 KMnO 溶液 B.KSCN 溶液 C. Cl
4 2
③写出上述②的具体实验方案(含操作、现象、结论):____________________。
④经检验,上述反应后的溶液中不存在 Fe2+,则该反应过程中产生的 NO 体积为(标准状况
下)____________________L。
【答案】 (1). Fe+2Fe3+=3Fe2+ (2). 产生白色沉淀,迅速变为灰绿色最后变为红褐色 (3). Fe2+
+2NH·H O=Fe(OH) ↓+2NH+ (4). 4Fe(OH) +O +2H O=4Fe(OH) (5). 3 (6). 1 (7). 4 (8). 3
3 2 2 4 2 2 2 3
(9). 1 (10). 2 (11). A (12). 取少量反应后溶液于试管,往其中滴加少量酸性高锰酸钾溶液,若溶
液颜色变浅或褪色,则溶液中含Fe2+,否则不含Fe2+ (13). 4.48【解析】
【分析】
(1). 变质时二价铁被氧化为三价铁,利用 ,可以在配制二价铁溶液时防止变质;
(2). 是弱碱盐,会和氨水发生反应生成弱碱 , 极易被氧化为 ;
(3). ①.氧化还原方程式配平找出反应中的氧化剂,还原剂,氧化产物,还原产物,分析价态变化利用元素
守恒和电荷守恒配平;
②. 具有还原性可以使有色氧化剂因发生氧化还原反应褪色,所以可以据此检验二价铁是否存在;
③.离子检验一般遵循步骤为:取样液于试管中,滴加检验试剂,描述现象结合现象得出结论;
④. ,依据反应中 与 以及转移电子之间的关系进行
求解;
【详解】(1)在试管中加入少量绿矾样品,加水溶解,配制成 溶液。在溶液中需加入少量铁屑,其
目的是防止 被氧化: ,故答案为: ;
(2)向 溶液滴加氨水生成白色沉淀氢氧化亚铁,迅速变为灰绿色,最后变为红褐色,发生的反应为:
, ,故答案为:产生白
色沉淀,迅速变为灰绿色最后变为红褐色; ;
;
(3)① 氧化为 ,失去1个电子,稀硝酸被还原为 ,N元素得到3个电子,根据得失电子守恒,
的计量数为3, 的计量数为1,结合电荷守恒可知H+的计量数为4,结合原子守恒
可知 的计量数为2,故答案为:3;1;4;3;1;2;② 具有还原性,可将酸性 溶液还原变色,所以可用酸性 溶液检验该反应后的溶液中
是否还含有 ,故答案为:A;
③ 具有还原性,可将酸性 溶液还原,使溶液颜色变浅或褪色,上述②的具体实验方案为:取
少量反应后溶液于试管,往其中滴加少量酸性高锰酸钾溶液,若溶液颜色变浅或褪色,则溶液中含 ,
否则不含 ,故答案为:取少量反应后溶液于试管,往其中滴加少量酸性高锰酸钾溶液,若溶液颜色变
浅或褪色,则溶液中含 ,否则不含 ;
④100mL6mol/L 溶液中, =0.1L×6mol/L=0.6mol, 溶与稀硝酸反应的离子方程式为:
,由方程式可知,3mol 完全反应生成标准状况下
22.4L,所以0.6mol完全反应生成标准状况下 4.48L,故答案为:4.48。
三、实验题(本大题共1小题,共14分)
31.某Al O 样品中含有一定量的Cu、Fe、Fe O 杂质。现通过下列生产过程,从该样品中回收铁红。流程如
2 3 2 3
下:
(1)操作a是________,在实验室进行该操作需要的玻璃仪器有烧杯、漏斗和_______。
(2) 试剂①是_______,固体II是_________(填化学式)。
(3)红褐色沉淀的成分是_________;写出白色沉淀转化为红褐色沉淀的化学方程式:______________。
(4)溶液II中铁元素的存在形式是_______(填离子符号),如何用实验证明:__________。【答案】 (1). 过滤 (2). 玻璃棒 (3). NaOH 溶液 (4). Cu (5). Fe(OH) (6).
3
4Fe(OH) +O +2H O=4Fe(OH) (7). Fe2+ (8). 取少量溶液Ⅱ于试管中,滴入几滴KSCN溶液,无明显现
2 2 2 3
象,再滴入适量氯水,溶液变红,则说明铁元素的存在形式是Fe2+
【解析】
试题分析:本题以从含有Cu、Fe、Fe O 杂质的Al O 样品中回收铁红为载体,考查流程的分析,物质的分
2 3 2 3
离和提纯,化学方程式的书写,Fe2+的检验,涉及Al O 、Fe、Fe O 、Fe(OH) 、Fe(OH) 等的化学性
2 3 2 3 2 3
质。流程中加入过量试剂①后得到的固体I最终可回收铁红,试剂①不溶解Fe、Fe O 、Cu,且在溶液II
2 3
中加入试剂①产生的白色沉淀能转化为红褐色沉淀,则试剂①为NaOH溶液,加入试剂①与样品发生的反
应为Al O+2NaOH=2NaAlO +H O,经过滤得到的固体I中含Cu、Fe、Fe O ;固体I中加入过量的盐酸发
2 3 2 2 2 3
生反应Fe+2HCl=FeCl +H ↑、Fe O+6HCl=2FeCl +3H O、Fe+2FeCl =3FeCl ,反应经过滤得到的固体II为
2 2 2 3 3 2 3 2
Cu,溶液II中含FeCl 和过量HCl;溶液II中加入NaOH溶液,FeCl 与NaOH反应生成白色Fe(OH) 沉
2 2 2
淀,Fe(OH) 在空气中久置转化为红褐色的Fe(OH),Fe(OH) 受热分解生成Fe O。
2 3 3 2 3
(1)操作a是将溶液和固体分离,操作a是过滤,过滤时需要的玻璃仪器有烧杯、漏斗和玻璃棒。
(2)根据上述分析,试剂①是NaOH溶液,固体II是Cu。
(3)红褐色沉淀的成分是Fe(OH)。白色沉淀转化为红褐色沉淀的化学方程式为4Fe(OH)
3
+O +2H O=4Fe(OH)。
2 2 2 3
(4)溶液II中含FeCl 和过量HCl,铁元素的存在形式是Fe2+。检验溶液II中含Fe2+的方法是:取少量溶
2
液Ⅱ于试管中,滴入几滴KSCN溶液,无明显现象,再滴入适量氯水,溶液变红,则说明铁元素的存在形
式是Fe2+。