文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 14 物质的检验、鉴别与除杂
目 录
2
3
考点一 物质的检验 4
【夯基·必备基础知识梳理】 4
一、原理 4
二、物质检验的一般步骤 4
三、检验方法 4
【提升·必考题型归纳】 6
考向01 气体的检验 6
考向02 混合气体的检验 6
考向03 混合物的成分确定 7
考点二 物质的鉴别 8
【夯基·必备基础知识梳理】 8
一、物质的鉴别原则 8
二、物质鉴别的方法 8
三、物质鉴别的形式 8
四、常见物质的鉴别 9
【提升·必考题型归纳】 9
考向01 物质的鉴别 9
考向02 生成物成分探究 10
考点三 物质的除杂 13
【夯基·必备基础知识梳理】 13
一、除杂的原则 13
二、除杂的方法 14
【提升·必考题型归纳】 16
考向01 气体的除杂 16
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考向02 液体的除杂 17
考向03 固体的除杂 17
考点要求 课标要求 命题预测
知道几种气体的检验方法
掌握氢离子和铵根离子的检验
方法
掌握氢氧离子、氯离子、硫酸
根离子、碳酸根离子、氢氧根离子的检
物质的检验和鉴别 物质的检验、鉴别和除杂等
验方法
知识点属于选考内容。
能根据物质的特性鉴别一些物
考查的内容:①常见的气体
质
检验;②离子的检验;③混合物
能根据实验现象确定混合物的
成分的缺点;④物质的除杂。
组成
考查的题型与方向:题型为
掌握不同气体干燥的方法,除
选择题、填空题和实验探究题。
去气体中水分
预计2024年中考考查物质的除杂
掌握能除去固体混合物中某种
可能性较大
杂质
物质的除杂
掌握能除去液体混合物中某种
杂质
能灵活使用理化方法除去气体
中杂质
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 物质的检验
一、原理
1. 检验的思路:根据物质的某一特性,用化学方法确定是不是该物质或者是否含有某种成分。
2. 检验的依据:任何具有明显实验现象差异的物理性质、化学性质都可作为物质检验的依据。如颜色
的变化、是否有气体产生、能否溶解、有无沉淀产生、有无吸热或放热等。
二、物质检验的一般步骤
三、检验方法
1. 物理方法:根据物质的特殊物理性质,如颜色、气味、水溶性等,通过观察、分析、判断、得出结论。
(1)常见有特殊颜色的物质(离子代表含有这种离子的溶液)
①固体物质:Cu:红(或紫红)色;CuSO ·5H O:蓝色;S:淡黄色。
4 2
②沉淀:Cu(OH) :蓝色;Fe(OH) :红褐色。
2 3
③溶液:Fe2+:浅绿色;Fe3+:黄色;Cu2+:蓝色;MnO -:紫红色。
4
(2)常见有特殊气味的物质
氨气:刺激性的氨味气体;SO :刺激性气味气体。
2
2. 化学方法:利用物质的特殊化学性质,反应时产生的特征现象,对所给物质进行检验。
(1)常见气体的检验
气体 检验方法 实验现象
O 将带火星的木条伸入集气瓶内 木条复燃
2
CO 将气体通入 水中 澄清石灰水变
2
H 点燃,在火焰上方罩一个干冷的烧杯 烧杯内壁有水雾(或水珠)生成
2
点燃,在火焰上方罩一个干 ;一
CH 4 烧杯内壁有 (或水珠)生成;澄清石
段时间后,迅速倒转烧杯,向烧杯中加入
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
,振荡 灰水变
点燃,在火焰上方罩一个涂有澄清石灰水的
CO 澄清石灰水变浑浊
烧杯
NH 将湿润的 放在试管口 红色石蕊试纸变为
3
HO 通过无水硫酸铜 无水硫酸铜由白色变成蓝色
2
HCl 先通入 溶液,再滴加稀HNO 有 生成,且沉淀不溶解
3
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)常见离子的检验
离子 检验方法 实验现象
①取少量试剂滴加紫色石蕊溶液 石蕊溶液变红
②用玻璃棒蘸取少量试剂滴在 pH 试纸 上 与标准比色卡对照pH<7
H+
③取少量试剂加入Zn 粒 有气泡产生
④取少量试剂加入碳酸钠 有气泡产生
①取少量试剂滴加 溶液 石蕊溶液
②取少量试剂滴加 溶液 酚酞溶液
OH-
③用玻璃棒蘸取少量试剂滴在 上 与标准比色卡对照
④取少量试剂加入可溶性 有 生成
Cl- 取少量试剂滴加少量AgNO 溶液和稀HNO 产生白色沉淀,且沉淀不消失
3 3
SO 2- 取少量试剂滴加少量 溶液和稀HNO 产生 ,且沉淀不消失
4 3
取少量试剂滴加稀盐酸,将产生的气体通入澄
CO2- 产生气泡,澄清石灰水变浑浊
3
清石灰水中
Cu2+ 取少量试剂滴加 有 生成
Fe3+ 取少量试剂滴加可溶性碱 有红褐色沉淀生成
取少量试剂滴加可溶性碱,加热,将湿润的红 产生有刺激性气味的气体,红色石蕊
NH +
4
色石蕊试纸放在试管口 试纸变蓝
Ag+ 取少量试剂滴加少量 溶液和稀HNO 产生 ,且沉淀不消失
3
Ba2+ 取少量试剂滴加少量 和稀HNO 产生白色沉淀,且沉淀不消失
3
Ca2+ 取少量试剂滴加 溶液 有 生成
考向01 气体的检验
【例1】一次性鉴别空气、氧气、二氧化碳三种气体,最简单可行的方法是
A.试验其溶解性
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.闻气味
C.用燃着的木条
D.用澄清石灰水
【变式1-1】要一次性区别一瓶无色气体为空气、氧气还是二氧化碳,最好的方法为
A.将燃着的木条分别伸入集气瓶中 B.将带火星的木条分别伸入集气瓶中
C.将气体分别通入澄清石灰水中 D.将气体分别通入水中
【变式1-2】区别氢气、氧气、空气和二氧化碳四瓶无色气体最简单的方法是
A.用带火星的木条伸到瓶中,观察现象 B.闻气味
C.倒入澄清石灰水观察 D.将燃着的木条分别放入瓶中,观察现象
考向02 混合气体的检验
【例2】(2023·东莞市一模)某气体由氢气、一氧化碳、甲烷中的一种或几种组成.点燃该气体后,在火
焰上方罩一冷而干燥的烧杯,烧杯内壁出现水雾;把烧杯迅速倒转过来,注入少量澄清石灰水,振荡,石
灰水变浑浊.下列对气体组成的推断正确的是
A.可能只有氢气一种气体
B.可能只有甲烷一种气体
C.三种气体一定都存在
D.一定是氢气和一氧化碳的混合气体
【变式2-1】某无色气体可能含有HO、CO、CO、H 中的一种或几种,若将该气体依次通过以下实验装
2 2 2
置(假设每步操作中,参加反应的气体均完全反应或吸收); 下列实验设计不能达到预期要求的是
A.气体依次通过E→D来验证是否含有CO 和HO
2 2
B.气体依次通过B→A→E来验证是否含有H
2
C.气体依次通过C→A→D来验证是否含有CO
D.气体依次通过E→D→C→B→A→D→E来验证是否含有HO、CO、CO、H
2 2 2
【变式2-2】某无色气体可能含有CO、H、CO、N 中的一种或几种。当混合气体通过紫色石蕊溶液时,
2 2 2
溶液没有变色;又通过灼热CuO时,有红色固体生成;再通过澄清石灰水时,石灰水不变浑浊。则下列有
关该气体的组成叙述正确的是
A.一定有H,一定不含CO 和氮气
2 2
B.一定含H 和CO中的其中一种
2
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.一定不含CO和CO,一定含H,可能含氮气
2 2
D.一定含有H 和N 两种气体
2 2
考向03 混合物的成分确定
【例3】一包由CuSO 、CaCO 、BaCl 、NaSO 、NaOH中的两种或两种以上的物质混合而成。取少量白
4 3 2 2 4
色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液X。在滤出的白色沉淀中加入
足量的盐酸,沉淀全部溶解,并产生无色气体。下列判断错误的是
A.原白色粉末的组成有3组可能
B.原白色粉末中一定含有CaCO
3
C.原白色粉末中一定不含有CuSO
4
D.若向无色滤液X中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl 、NaOH
2
【变式3-1】某实验室的废液中,可能含有FeCl 、NaCl、NaSO 、Ba(NO ) 中的一种或多种。某同学取该
3 2 4 3 2
废液样品观察为无色溶液,向其中滴加BaCl 溶液产生白色沉淀,继续加稀硝酸无明显现象。根据以上实
2
验现象分析,下列推断正确的是
A.可能存在NaCl B.可能存在NaSO C.一定存在FeCl D.一定存在Ba(NO )
2 4 3 3 2
【变式3-2】一包白色粉末,可能含有CuSO 、CaCO 、BaCl 、NaSO 、NaOH中的一种或几种。为探究其
4 3 2 2 4
组成进行如下实验:
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
②取实验①滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体;
③取实验①得到的滤液,向其中通入CO,产生白色沉淀;
2
根据以上实验现象,判断白色粉末。下列结论错误的是
A. 白色粉末中一定不含CuSO 、NaSO
4 2 4
B. 白色粉末中一定含有CaCO 、BaCl
3 2
C. 白色粉末中一定含有CaCO 、BaCl 、NaOH
3 2
D. 白色粉末中可能含有NaOH
考点二 物质的鉴别
一、物质的鉴别原则
操作简单、试剂种类少、现象明显。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
二、物质鉴别的方法
1. 物理方法:
依据物质特殊的物理性质(如颜色、状态、气味、溶解性、溶解时的吸放热现象)进行观察、分析、判断,
得出结论。
2. 化学方法:
依据物质间反应时所产生的特殊反应现象(如变色、放出气体、生成沉淀、放热等)进行鉴别。
三、物质鉴别的形式
1. 一种试剂鉴别:选择一种试剂,分别加入待测物质中,观察实验现象。
2. 多种试剂鉴别:选择多种试剂,依次加入待测物质中,会出现明显不同现象。
3. 无试剂鉴别:先利用物质物理性质不同或物质间的相互反应(包括与生成物反应)而产生不同现象把物质
鉴别出来。
四、常见物质的鉴别
常见物质 所选试剂或方法 现象
软水、硬水 肥皂水 泡沫较多、的是软水;泡沫较少、浮渣较多的是硬水
棉花 有 气味的是羊毛;
羊毛 有 气味、燃烧后有灰烬的是棉花;
有气味,灰烬为灰褐色玻璃球状,不易破碎的是合成纤
合成纤维
维
看外观或加水 灰白色或难溶于水或部分溶于水的是磷肥
常见化肥
加熟石灰研磨 有刺激性气味气体产生的是铵态氮肥(铵盐)
硝酸铵固体和 溶液温度 的是氢氧化钠固体
氢氧化钠固体 溶液温度 的是硝酸铵固体
黄铜和纯铜 相互刻画 有明显划痕的为纯铜,反之为黄铜
白醋和白酒 有 的是白醋,有醇香味的是白酒
热塑性塑料和 加热熔化,冷却凝固为热塑性塑料
加热
热固性塑料 加热时不能熔化,保持外部形状的为热固性塑料
的是真黄金, 的是假黄金。
真假黄金
加 或稀硫酸 的是假黄金,没有气泡产生的是真黄金
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考向01 物质的鉴别
【例1】下列除杂或鉴别方法不正确的是
A.用浓硫酸除去氧气中的水蒸气 B.用点燃的方法除去混在CO 中的CO
2
C.用饱和NaHCO 溶液除去CO 中的HCl D.用水鉴别NaCl、NH NO 和NaOH三种固体
3 2 4 3
【变式1-1】下列各组稀溶液,仅用组内物质及其反应产物就能鉴别出来的是
A.KCl H SO NaOH Ba(NO ) B.NaCl AgNO CaCl HNO
2 4 3 2 3 2 3
C.CuSO NaCl KNO BaC1 D.NaCl HCl NaOH MgCl
4 3 2 2
【变式1-2】下列各组溶液中,不用其它试剂就不能鉴别出来的是
A.FeCl NaOH HCl KCl B.BaCl Na SO Na CO HCl
3 2 2 4 2 3
C.CuSO NaOH KNO BaCl D.KCl AgNO HCl HNO
4 3 2 3 3
【变式1-3】用括号内试剂不能一次性将组内物质鉴别出来的是
A.固体:NaOH、NH NO 、NaCl(水)
4 3
B.液体:稀盐酸、HO、Ca(OH) 溶液(石蕊溶液)
2 2
C.固体:ZnSO、CaCO 、KCl(水)
4 3
D.液体:Ba(NO ) 溶液、MgCl 溶液、KCO 溶液(稀硫酸)
3 2 2 2 3
考向02 生成物成分探究
【例2】某化工厂排放的废水中含有硝酸镁、硝酸铜和硝酸银。我校化学兴趣小组的小华同学为了回收废
液中的贵重金属铜和银,将一定量锌粉加入样品中,充分反应后过滤,得到滤液A和固体B.请回答下列
有关问题:
(1)关于滤液A所含溶质的猜想中,合理的是_____ (填写序号)。
①猜想一:硝酸锌、硝酸镁
②猜想二:硝酸锌、硝酸铜
③猜想三:硝酸锌、硝酸镁、硝酸铜
④猜想四:硝酸锌、硝酸镁、硝酸银
⑤猜想五:硝酸锌、硝酸镁、硝酸铜、硝酸银。
(2)如果固体B含有两种金属,则滤液A的颜色为_____。
(3)反应后析出金属的质量_____(选填“一定”或“不一定”)比参加反应的金属质量大。
(4)对于滤液成分,如果猜想一成立,则固体B的成分是:_____。
(5)为了证明小华所加入的锌粉是否过量,你设计的简单方法是_____。
【变式2-1】已知某金属粉末由铁、铜、铝三种金属中的两种组成,兴趣小组的同学对此进行了如下探究。
(提出问题)该粉末由什么组成?
(查阅资料)铁和铜与氢氧化钠溶液都不反应,而铝与氢氧化钠溶液可反应生成溶于水的偏铝酸钠和氢气
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2Al+2NaOH+2H O═2NaAlO+3H ↑)。
2 2 2
(1)(提出猜想)
猜想Ⅰ:该粉末由铜、铁组成;
猜想Ⅱ:该粉末由铜、铝组成;
猜想Ⅲ:该粉末由________组成。
(2)(实验探究)
步骤 实验操作 实验现象 实验结论
取一个烧杯,加入适量粉末样品,再加入足 粉末一定含有
① 粉末部分溶解,有气泡产生
量的稀盐酸 ________
另取一个烧杯,加入适量粉末样品,再加入粉末部分溶解,________
② 粉末一定含有铝
足量NaOH溶液 气泡产生
综合上述实验,说明猜想________成立。
(3)(实验 反思)有同学认为能用浅绿色的FeSO 溶液代替NaOH溶液完成步骤②,你认为能________
4
(填“能”或“不能”),理由是________。
(4)(拓展应用)铝与稀盐酸反应的化学方程式是________。
【变式2-2】铁是世界上年产量最高的金属,铁及其合金也是应用最广泛的金属材料。请根据我们所学的
有关金属的知识回答问题:
(1)验证金属的活动性(实验装置如图1)
①若要证明Fe在金属活动性顺序中位于氢前,X溶液可选用________,其现象为________。
②若X溶液为少量硫酸铜溶液,该反应的化学方程式为________。待充分反应后,取出铁片,放入金属
R,观察到R表面有黑色固体析出。根据上述实验现象,得出Fe、Cu、R的金属活动性顺序为________。
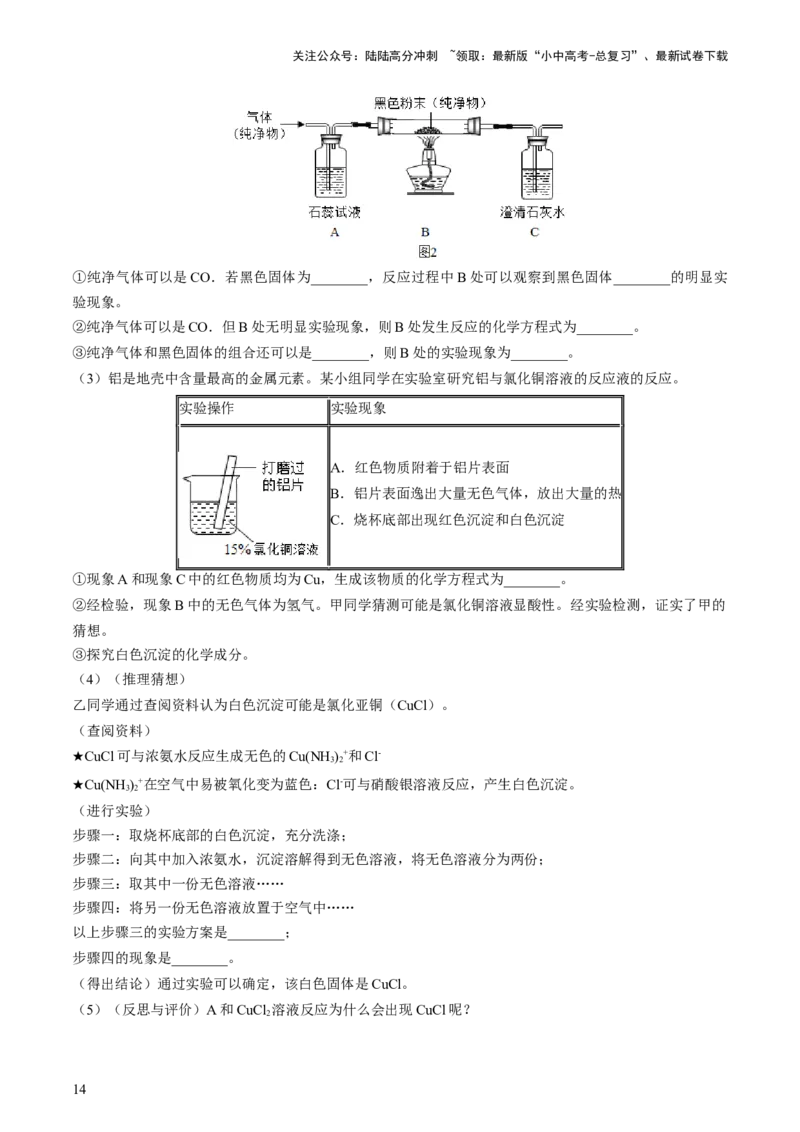
(2)某纯净气体通过如图2装置时,可观察到:A中紫色石蕊试液不变色,C中澄清石灰水变浑浊。请按
要求回答问题:
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①纯净气体可以是CO.若黑色固体为________,反应过程中B处可以观察到黑色固体________的明显实
验现象。
②纯净气体可以是CO.但B处无明显实验现象,则B处发生反应的化学方程式为________。
③纯净气体和黑色固体的组合还可以是________,则B处的实验现象为________。
(3)铝是地壳中含量最高的金属元素。某小组同学在实验室研究铝与氯化铜溶液的反应液的反应。
实验操作 实验现象
A.红色物质附着于铝片表面
B.铝片表面逸出大量无色气体,放出大量的热
C.烧杯底部出现红色沉淀和白色沉淀
①现象A和现象C中的红色物质均为Cu,生成该物质的化学方程式为________。
②经检验,现象B中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性。经实验检测,证实了甲的
猜想。
③探究白色沉淀的化学成分。
(4)(推理猜想)
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
(查阅资料)
★CuCl可与浓氨水反应生成无色的Cu(NH )+和Cl-
3 2
★Cu(NH )+在空气中易被氧化变为蓝色:Cl-可与硝酸银溶液反应,产生白色沉淀。
3 2
(进行实验)
步骤一:取烧杯底部的白色沉淀,充分洗涤;
步骤二:向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
步骤三:取其中一份无色溶液……
步骤四:将另一份无色溶液放置于空气中……
以上步骤三的实验方案是________;
步骤四的现象是________。
(得出结论)通过实验可以确定,该白色固体是CuCl。
(5)(反思与评价)A和CuCl 溶液反应为什么会出现CuCl呢?
2
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
丙同学猜测:可能是Cu与CuCl 溶液反应生成了CuCl。
2
丙同学为了验证猜想,取Cu粉与15%CuCl 溶液混合,无白色沉淀产生。
2
④丙通过分析Al与CuCl 溶液反应的实验现象,改进了实验,证明了Cu与CuCl 溶液反应生成了CuCl,
2 2
改进之处是________。
⑤丁同学认为丙同学的实验还不够严谨,还应考虑________对Cu与CuCl 溶液反应的影响。
2
考点三 物质的除杂
一、除杂的原则
1. 杂不增:
所选试剂不能与被提纯物质(主要成分)反应。
如除去NaCl溶液中少量的NaCO
2 3
错误方法:加入适量的硫酸或稀硝酸。
错误原因:会引入杂质硫酸钠(或硝酸钠)
正确方法:加入适量的稀盐酸或加入适量的氯化钙或氯化钡溶液
2. 主不减:
在除去杂质的同时,不能减少主体物质的总量。
如除去CO 气体中少量的HCl
2
错误方法:将气体先通过氢氧化钠溶液,再通过浓硫酸。
错误原因:在除去HCl的同时,也将CO 气体除去。
2
正确方法:现将气体通过饱和的NaHCO (CO 气体不溶于该溶液,也不与该溶液反应)溶液,再通
3 2
过浓硫酸。
3.易分离:
除杂后生成的产物的状态与被提纯物质的状态要不同,方便除去。也即尽量将杂质转化为气体或沉淀!
如上例除去NaCl溶液中少量的NaCO,可加入适量的稀盐酸至不再产生气泡,该方法是将NaCO 转
2 3 2 3
化为NaCl同时,生成CO 气体,这样CO 气体自行逸出。
2 2
再比如除去NaNO3溶液中的少量NaCl杂质时,可先滴加适量的硝酸银溶液至不再产生沉淀,再过滤
即可除去难溶性的AgCl。
4.易复原:
若混合物为固体时,除杂之后要考虑到容易将物质恢复至初始状态固态。
如:除去KCl固体中少量的MnO (难溶)时,应先加水溶解→过滤→,
2
对蒸发KCl溶液蒸发结晶的目的是:将KCl溶液转化成KCl固体,恢复原物质的状态!
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
二、除杂的方法
1. 气体的除杂
方法一:将杂质气体通过物质吸收、反应除去,如氧气中的水蒸气可通过浓硫酸吸收除去、一氧化碳
中的二氧化碳可通过氢氧化钠溶液吸收除去。
方法二:将杂质气体转化为主气体,如二氧化碳中的一氧化碳可通过灼热的氧化铜,使一氧化碳转化
成二氧化碳。
【常见气体除杂举例】
物质 杂质 除杂方法
CO CO 通过灼热的氧化铜
2
CO CO 溶液,再通过浓硫酸
2
H HCl气体 先通过氢氧化钠溶液,再通过浓硫酸或碱石灰
2
CO 水蒸气 通过
2
CO HCl 先通过饱和碳酸氢钠溶液,再通过浓硫酸
2
N CO 先通过氢氧化钠溶液,再通过
2 2
O CO 先通过氢氧化钠溶液,再通过浓硫酸
2 2
O 水蒸气 通过氧化钙、浓硫酸或
2
N O 通过灼热的铜网
2 2
H 水蒸气 通过 、浓硫酸或氢氧化钠固体
2
2. 固体的除杂
方法一:将杂质化为气体除去,如氧化铜中的炭粉通过在空气中灼烧除去。
方法二:将杂质转化为溶液除去,如铜中的铁可通过与盐酸反应除去。
【常见固体除杂举例】
物质 杂质 除杂方法
CuO Cu 在空气(或氧气)中灼烧
Cu Fe 加入足量的 /稀盐酸,
Cu CuO 加入足量的稀硫酸/稀盐酸,过滤
Cu Zn 加入足量的 /稀盐酸,过滤
CuO C 在氧气流中加热
C CuO 加入足量的稀硫酸/ ,过滤
CaO CaCO 高温煅烧
3
MnO KCl 、过滤
2
Fe Zn 加入足量硫酸亚铁溶液,过滤
Ag Cu 加入足量的 溶液,过滤
CaCO CaCl 加水溶解,过滤
3 2
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
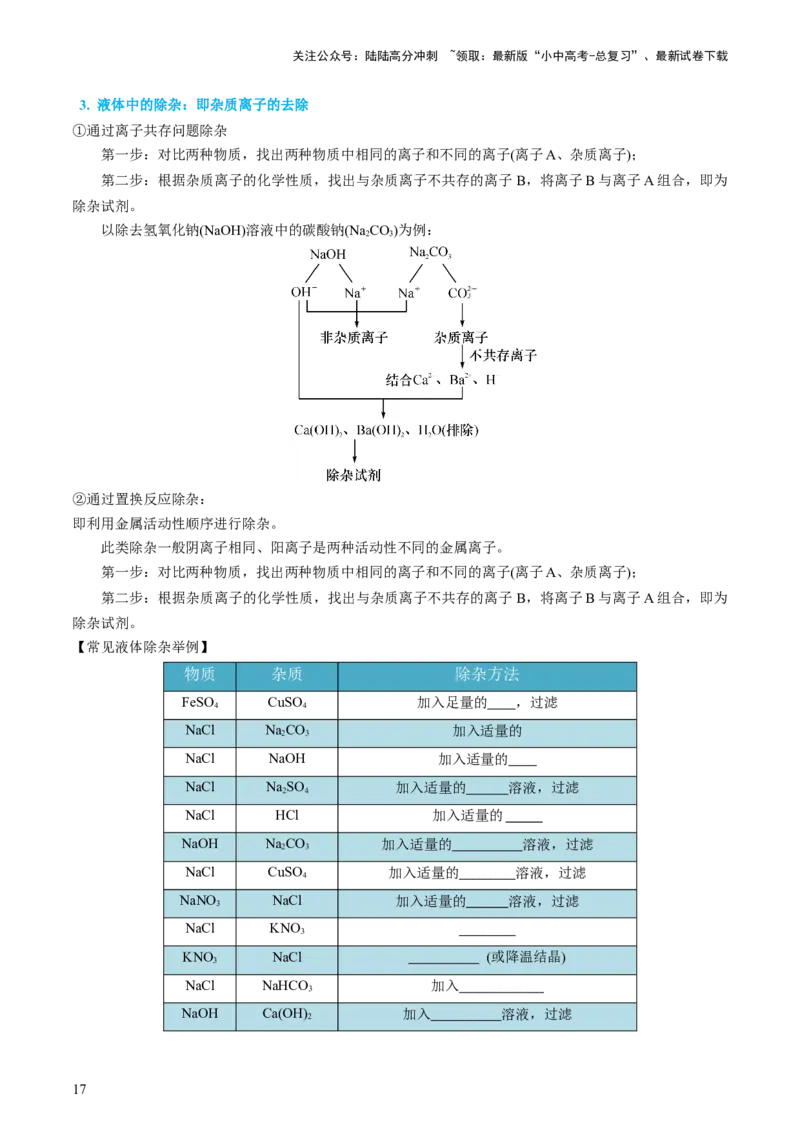
3. 液体中的除杂:即杂质离子的去除
①通过离子共存问题除杂
第一步:对比两种物质,找出两种物质中相同的离子和不同的离子(离子A、杂质离子);
第二步:根据杂质离子的化学性质,找出与杂质离子不共存的离子 B,将离子B与离子A组合,即为
除杂试剂。
以除去氢氧化钠(NaOH)溶液中的碳酸钠(Na CO)为例:
2 3
②通过置换反应除杂:
即利用金属活动性顺序进行除杂。
此类除杂一般阴离子相同、阳离子是两种活动性不同的金属离子。
第一步:对比两种物质,找出两种物质中相同的离子和不同的离子(离子A、杂质离子);
第二步:根据杂质离子的化学性质,找出与杂质离子不共存的离子 B,将离子B与离子A组合,即为
除杂试剂。
【常见液体除杂举例】
物质 杂质 除杂方法
FeSO CuSO 加入足量的铁粉,过滤
4 4
NaCl NaCO 加入适量的
2 3
NaCl NaOH 加入适量的盐酸
NaCl NaSO 加入适量的 溶液,过滤
2 4
NaCl HCl 加入适量的NaOH
NaOH NaCO 加入适量的 溶液,过滤
2 3
NaCl CuSO 加入适量的氢氧化钡溶液,过滤
4
NaNO NaCl 加入适量的 溶液,过滤
3
NaCl KNO 蒸发结晶
3
KNO NaCl (或降温结晶)
3
NaCl NaHCO 加入适量的稀盐酸
3
NaOH Ca(OH) 加入 溶液,过滤
2
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
HCl HSO 加入适量氯化钡溶液,过滤
2 4
CuSO HSO 加入足量的 或氢氧化铜粉末,过滤
4 2 4
KNO KSO 加入适量的硝酸钡溶液,过滤
3 2 4
CaCl HCl 加入足量的 固体,过滤
2
NaNO AgNO 加入适量的氯化钠溶液,过滤
3 3
考向01 气体的除杂
【例1】除去下列各物质中混有的少量杂质,所用试剂及操作方法如下表,能完成提纯的是
序号 物质 杂质 所用试剂和操作方法
A H HCl 通过足量的AgNO 溶液,干燥
2 3
B NaNO 溶液 NaSO 加入过量的Ba(NO ) 溶液,过滤
3 2 4 3 2
C NaCl固体 NaCO 加入足量水溶解,过滤
2 3
D 铁粉 Fe O 加入适量的稀盐酸,过滤
2 3
A.A B.B C.C D.D
【变式1-1】除杂是化学学习和生产中常见的现象,下列除杂方法可行的是
A.除去二氧化锰粉末中混有少量的碳粉——加水、过滤
B.除去硝酸钾中混有的少量氯化钠——蒸发结晶
C.除去硫酸钠溶液中混有少量的碳酸钠——加氯化钡溶液、过滤
D.除去CO 中混有少量的O——通过灼热的铜网
2 2
【变式1-2】下列除去杂质的方法中,错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B 盐酸 稀硫酸 适量BaCl 、过滤
2
C FeCl 溶液 CuCl 过量铁粉、过滤
2 2
D 二氧化碳 一氧化碳 点燃
考向02 液体的除杂
【例2】除去下列物质中的少量杂质,所选试剂和操作方法正确的是
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
选项 物质 少量杂质 所用试剂和操作方法
A 氯化钙溶液 盐酸 加入过理的大理石,过滤
B 锌 硫酸铜 溶解、过滤、洗涤、干燥
C 氯化钾 二氧化锰 溶解、过滤
D 氧化钙 石灰石 高温锻烧至不再产生气体
【变式2-1】除去下列物质中的少量杂质,所选用的方法正确的是
选项 物质 杂质 除杂方法
A CO CO 通入氢氧化钠溶液
2
B N O 将混合气体通过灼热的木炭
2 2
C CuO C 加入足量的稀盐酸,过滤
D ZnCl 溶液 CuCl 加入足量的锌粉,过滤
2 2
A.A B.B C.C D.D
【变式2-2】除去下列物质中的杂质,选用试剂和方法均正确的是
选项 物质 杂质(少量) 试剂和方法
A 氯化钾 氯酸钾 加入少量二氧化锰粉末,加热
B 稀硫酸 稀盐酸 加入过量的氯化钡溶液,过滤
C 氯化钙溶液 氢氧化钙 加入稍微过量的稀盐酸,蒸发
D 碳酸钾 硫酸钾 加入过量的硝酸钡溶液,过滤
考向03 固体的除杂
【例3】下列除杂方法正确的是
A.除去氧化钙中少量的碳酸钙:加适量的水
B.除去铁粉中少量的氧化铁:高温时通入足量的一氧化碳
C.除去二氧化碳中少量的一氧化碳:点燃使其燃烧
D.除去氢氧化钠溶液中少量的碳酸钠:滴加适量的氯化钙溶液
【变式3-1】为除去下列物质中的杂质(括号内为杂质),选用试剂和操作方法都正确的是
序号 物质 操作方法
A Fe(Fe O) 加入过量稀盐酸,过滤
2 3
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B CO 气体(O) 将混合气体通过灼热的碳粉
2 2
C CaCO 固体(CaCl ) 加水溶解,过滤,洗涤,干燥
3 2
D NaCl溶液(MgCl ) 加入过量的NaOH溶液,过滤
2
A.A B.B C.C D.D
【变式3-2】除去下列物质中的少量杂质,所选用的试剂及操作方法正确的是
选项 物质 杂质 试剂 操作方法
A FeCl 溶液 CuCl 溶液 过量铁粉 过滤
3 2
B CuO C 足量氧气 充分灼烧
C CuSO Fe 水 溶解、过滤
4
D CaO 大理石 无 高温煅烧
20