文档内容
陕西省西安中学高 2025 届高三第一次质量检测考试
化学试题
(时间:75分钟 满分:100分 命题人:马文哲)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cl-35.5 Mn-55 Zn-65
一、选择题(本题共16小题,每小题3分,共48分。每小题只有一个选项符合题
目要求。)
1. 化学在生活、生产、科研等方面发挥着重要作用。下列说法错误的是( )
A.水质检验员在自来水出厂前会对水中的SO 2-、Cl-、微生物等进行检测和分析
4
B.胶态磁流体治癌术是将磁性物质制成胶体粒子,这种粒子的直径范围是
1~100nm
C.丹霞地貌的岩层因含FeO而呈现红色
D.用于制造“何尊”的青铜和举世轰动的“超级钢”均属于合金
2.下列分子或离子在指定的分散系中能大量共存的一组是( )
A.银氨溶液:Na+、K+、NO -、HCO -
3 3
B.C(Fe2+)=1mol/L的溶液中:K+、NH +、MnO -、SO 2-
4 4 4
C.水电离的C(H+)=1×10-13mol·L-1的溶液中:K+、Na+、Cl-、I-
D.高锰酸钾溶液:Na+、H+、SO 2-、葡萄糖分子
4
3. N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.在标准状况下,2.24L CH Cl中含有0.1N 个分子
3 A
B.100mL 18.4mol/L 浓硫酸与足量锌反应时,生成的SO 分子数目为0.92 N
2 A
C.丙烯和环丙烷组成的42g混合气体中所含氢原子数为6N
A
D.0.1mol 肼(N H )含有的孤电子对数为0.2N
2 4 A
4. 下列离子方程式书写正确的是( )
A.向NaClO溶液中通入过量CO :ClO-+CO +H O=HClO+HCO -
2 2 2 3
B.向NH HCO 溶液中滴加足量NaOH溶液:HCO -+OH-=CO 2-+H O
4 3 3 3 2
C.Cl 通入水中:Cl +H O=2H++Cl-+ClO-
2 2 2
D.铅酸蓄电池放电时的负极反应:PbO +2e-+4H++SO 2-=PbSO +2H O
2 4 4 2
5. 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正
确的是( )
实验目的 方案设计 现象 结论
验证NaCl、 取少量混合溶液于试管中,加 则混合溶
若上层清
A Na SO 混合溶液 入过量Ba(NO ) 溶液,静置, 液中含有
2 4 3 2
液变浑浊
中的 向上层清液中滴加AgNO 溶液 Cl-
3
第一次质量检测化学试题 第 1 页 共8页
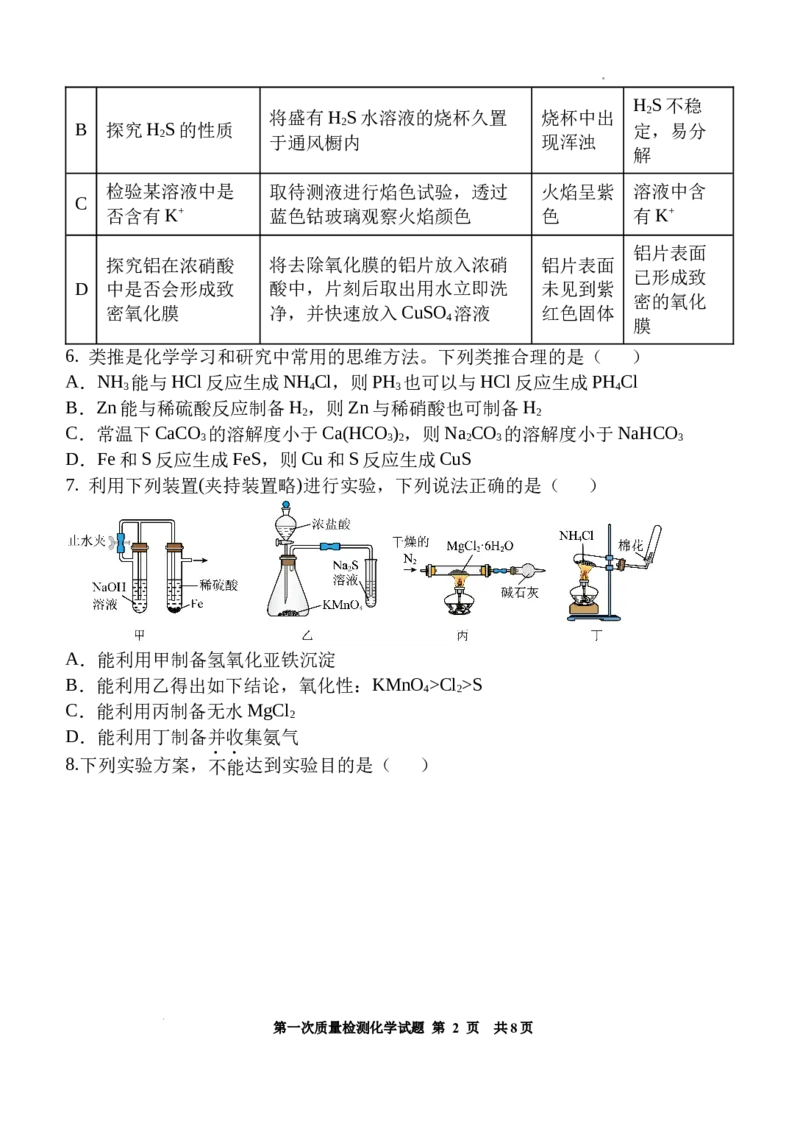
学科网(北京)股份有限公司H S不稳
将盛有H S水溶液的烧杯久置 烧杯中出 2
B 探究H S的性质 2 定,易分
2 于通风橱内 现浑浊
解
检验某溶液中是 取待测液进行焰色试验,透过 火焰呈紫 溶液中含
C
否含有K+ 蓝色钴玻璃观察火焰颜色 色 有K+
铝片表面
探究铝在浓硝酸 将去除氧化膜的铝片放入浓硝 铝片表面
已形成致
D 中是否会形成致 酸中,片刻后取出用水立即洗 未见到紫
密的氧化
密氧化膜 净,并快速放入CuSO 溶液 红色固体
4 膜
6. 类推是化学学习和研究中常用的思维方法。下列类推合理的是( )
A.NH 能与HCl反应生成NH Cl,则PH 也可以与HCl反应生成PH Cl
3 4 3 4
B.Zn能与稀硫酸反应制备H ,则Zn与稀硝酸也可制备H
2 2
C.常温下CaCO 的溶解度小于Ca(HCO ) ,则Na CO 的溶解度小于NaHCO
3 3 2 2 3 3
D.Fe和S反应生成FeS,则Cu和S反应生成CuS
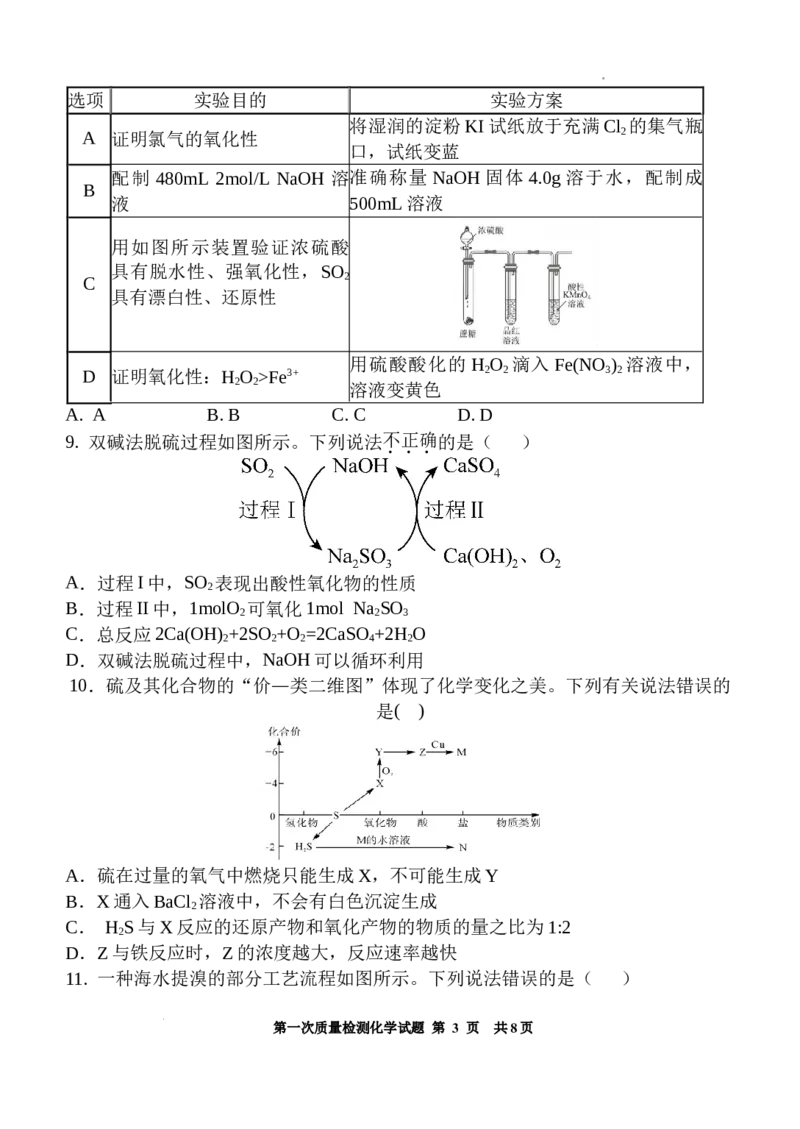
7. 利用下列装置(夹持装置略)进行实验,下列说法正确的是( )
A.能利用甲制备氢氧化亚铁沉淀
B.能利用乙得出如下结论,氧化性:KMnO >Cl >S
4 2
C.能利用丙制备无水MgCl
2
D.能利用丁制备并收集氨气
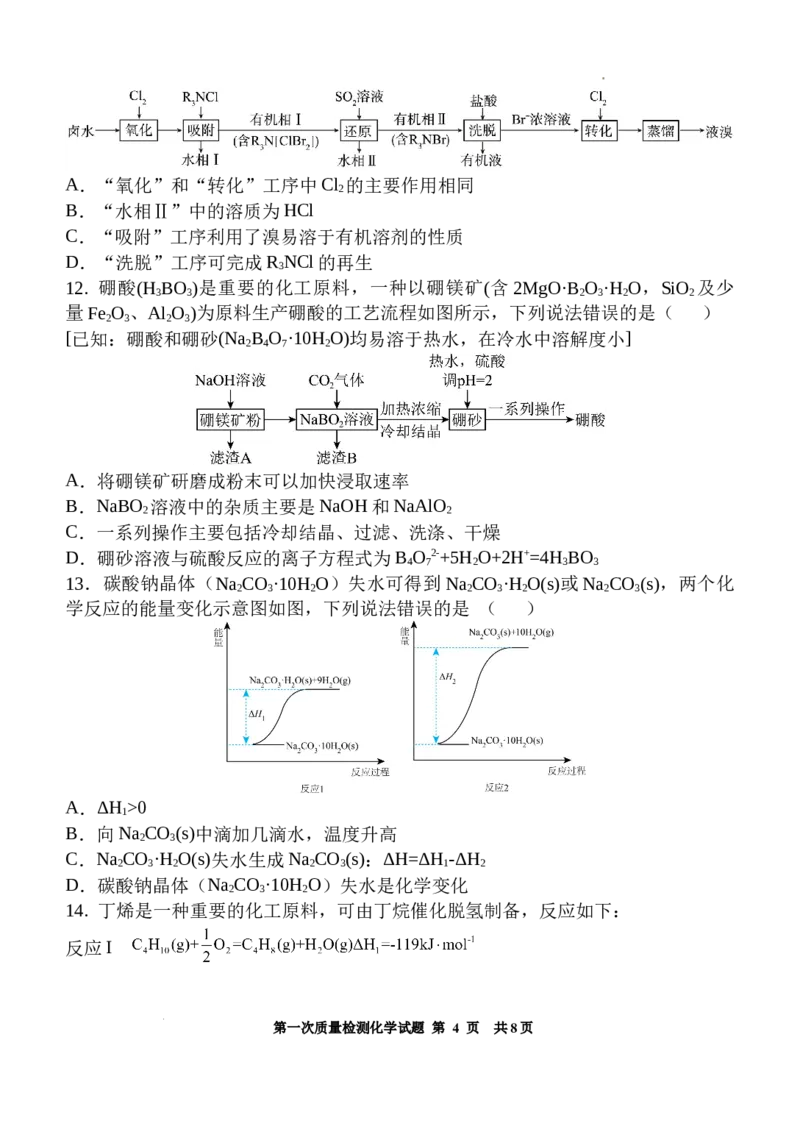
8.下列实验方案,不能达到实验目的是( )
第一次质量检测化学试题 第 2 页 共8页
学科网(北京)股份有限公司选项 实验目的 实验方案
将湿润的淀粉KI试纸放于充满Cl 的集气瓶
A 证明氯气的氧化性 2
口,试纸变蓝
配制 480mL 2mol/L NaOH 溶准确称量 NaOH 固体 4.0g 溶于水,配制成
B
液 500mL溶液
用如图所示装置验证浓硫酸
具有脱水性、强氧化性,SO
C 2
具有漂白性、还原性
用硫酸酸化的 H O 滴入 Fe(NO ) 溶液中,
D 证明氧化性:H O >Fe3+ 2 2 3 2
2 2 溶液变黄色
A. A B. B C. C D. D
9. 双碱法脱硫过程如图所示。下列说法不正确的是( )
A.过程I中,SO 表现出酸性氧化物的性质
2
B.过程II中,1molO 可氧化1mol Na SO
2 2 3
C.总反应2Ca(OH) +2SO +O =2CaSO +2H O
2 2 2 4 2
D.双碱法脱硫过程中,NaOH可以循环利用
10.硫及其化合物的“价—类二维图”体现了化学变化之美。下列有关说法错误的
是( )
A.硫在过量的氧气中燃烧只能生成X,不可能生成Y
B.X通入BaCl 溶液中,不会有白色沉淀生成
2
C. H S与X反应的还原产物和氧化产物的物质的量之比为1:2
2
D.Z与铁反应时,Z的浓度越大,反应速率越快
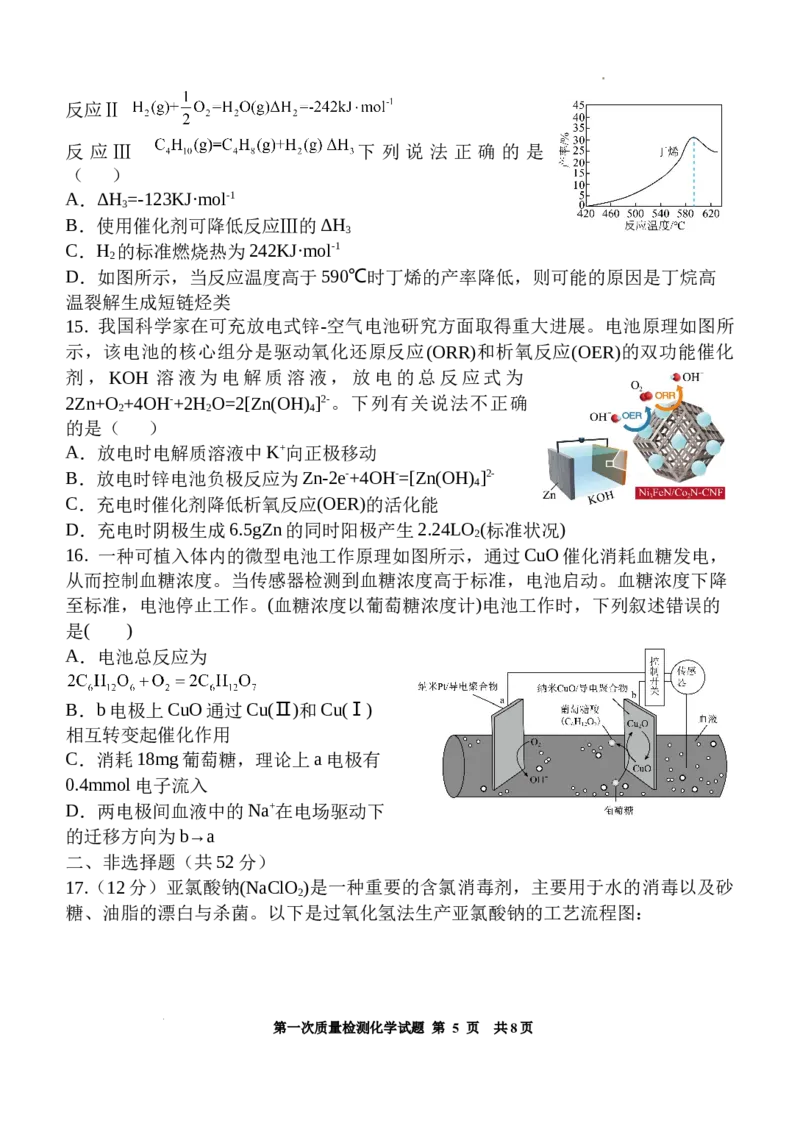
11. 一种海水提溴的部分工艺流程如图所示。下列说法错误的是( )
第一次质量检测化学试题 第 3 页 共8页
学科网(北京)股份有限公司A.“氧化”和“转化”工序中Cl 的主要作用相同
2
B.“水相Ⅱ”中的溶质为HCl
C.“吸附”工序利用了溴易溶于有机溶剂的性质
D.“洗脱”工序可完成R NCl的再生
3
12. 硼酸(H BO )是重要的化工原料,一种以硼镁矿(含2MgO·B O ·H O,SiO 及少
3 3 2 3 2 2
量Fe O 、Al O )为原料生产硼酸的工艺流程如图所示,下列说法错误的是( )
2 3 2 3
[已知:硼酸和硼砂(Na B O ·10H O)均易溶于热水,在冷水中溶解度小]
2 4 7 2
A.将硼镁矿研磨成粉末可以加快浸取速率
B.NaBO 溶液中的杂质主要是NaOH和NaAlO
2 2
C.一系列操作主要包括冷却结晶、过滤、洗涤、干燥
D.硼砂溶液与硫酸反应的离子方程式为B O 2-+5H O+2H+=4H BO
4 7 2 3 3
13.碳酸钠晶体(Na CO ·10H O)失水可得到Na CO ·H O(s)或Na CO (s),两个化
2 3 2 2 3 2 2 3
学反应的能量变化示意图如图,下列说法错误的是 ( )
A.ΔH >0
1
B.向Na CO (s)中滴加几滴水,温度升高
2 3
C.Na CO ·H O(s)失水生成Na CO (s):ΔH=ΔH -ΔH
2 3 2 2 3 1 2
D.碳酸钠晶体(Na CO ·10H O)失水是化学变化
2 3 2
14. 丁烯是一种重要的化工原料,可由丁烷催化脱氢制备,反应如下:
反应I
第一次质量检测化学试题 第 4 页 共8页
学科网(北京)股份有限公司反应Ⅱ
反 应 Ⅲ 下 列 说 法 正 确 的 是
( )
A.ΔH =-123KJ·mol-1
3
B.使用催化剂可降低反应Ⅲ的ΔH
3
C.H 的标准燃烧热为242KJ·mol-1
2
D.如图所示,当反应温度高于590℃时丁烯的产率降低,则可能的原因是丁烷高
温裂解生成短链烃类
15. 我国科学家在可充放电式锌-空气电池研究方面取得重大进展。电池原理如图所
示,该电池的核心组分是驱动氧化还原反应(ORR)和析氧反应(OER)的双功能催化
剂,KOH 溶液为电解质溶液,放电的总反应式为
2Zn+O +4OH-+2H O=2[Zn(OH) ]2-。下列有关说法不正确
2 2 4
的是( )
A.放电时电解质溶液中K+向正极移动
B.放电时锌电池负极反应为Zn-2e-+4OH-=[Zn(OH) ]2-
4
C.充电时催化剂降低析氧反应(OER)的活化能
D.充电时阴极生成6.5gZn的同时阳极产生2.24LO (标准状况)
2
16. 一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,
从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降
至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)电池工作时,下列叙述错误的
是( )
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)
相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有
0.4mmol电子流入
D.两电极间血液中的Na+在电场驱动下
的迁移方向为b→a
二、非选择题(共52分)
17.(12分)亚氯酸钠(NaClO )是一种重要的含氯消毒剂,主要用于水的消毒以及砂
2
糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
第一次质量检测化学试题 第 5 页 共8页
学科网(北京)股份有限公司已知:①NaClO 的溶解度随温度升高而增大,适当条件下可结晶析出产品
2
NaClO ·3H O ②纯ClO 易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2 2 2
(1)发生器中鼓入空气的作用可能是_______。
a. 将SO 氧化成SO ,增强酸性 b. 将NaClO 还原为ClO
2 3 3 2
c. 稀释ClO 以防止爆炸
2
(2)吸收塔内发生反应的化学方程式为 。
(3)吸收塔中为防止 NaClO 被还原成 NaCl,所用还原剂的还原性应适中。除
2
H O 外,还可以选择的还原剂是_______(填序号)。
2 2
a. Na O b.Na S c.FeCl
2 2 2 2
(4)从滤液中得到NaClO ·3H O粗晶体的实验操作依次是 (填序号)。
2 2
a.蒸馏 b. 蒸发 c.灼烧 d.过滤 e.冷却结晶
(5)某学习小组用碘量法测定粗产品中亚氯酸钠的含量,实验如下:
a. 准确称取所得亚氯酸钠样品 m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶
体,再滴入适量的稀硫酸,充分反应,将所得混合液配成 250mL待测溶液。(已
知:ClO -+4I-+4H+=2H O+2I +Cl-)
2 2 2
b.移取25.00 ml待测溶液于锥形瓶中,加几滴淀粉溶液,用 c mol/L Na S O 标准液
2 2 3
滴定至终点,重复2次,测得平均值为V mL。(已知:I +2S O 2-=2I-+S O 2-)
2 2 3 4 6
①达到滴定终点时的现象为 。
②该样品中NaClO 的质量分数为___(用含m、c、V的代数式表示,结果化成最
2
简)
18.(14分)HNO 及AgNO 是中学化学常用试剂,某兴趣小组设计如下实验探究试
3 3
剂性质。
Ⅰ. HNO 的强氧化性
3
采用下列装置,对浓硝酸与木炭的反应进行探究。请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸
入三颈烧瓶中,并塞紧瓶塞,滴加浓硝酸,三颈烧瓶中反应的化学方程式是
。
第一次质量检测化学试题 第 6 页 共8页
学科网(北京)股份有限公司(2)从实现的功能上来说,装置B的名称是 。
( 3 ) 装 置 C 中 盛 有 足 量 Ba(OH) 溶 液 , C中 可 能 观 察 到 的 现 象 是
2
,Ba(OH) 溶液 (填“能”或“不能”)用Ca(OH) 溶液代替。
2 2
(4)装置D中收集到无色气体,部分同学认为是 NO,还有部分同学认为是 O 。
2
假设装置内空气已排净,D瓶中收集的气体仅为产物。下列对该气体的检验方法合
适的是 (填字母)。
A.将试剂瓶取出,放在通风条件良好的桌上敞口观察试剂瓶内气体的颜色是否变红
B.将润湿的蓝色石蕊试纸伸入试剂瓶内,观察试纸是否变红
C.将带火星的木条伸入试剂瓶中,观察木条是否复燃
Ⅱ.AgNO 的热稳定性
3
受热易分解,用如图装置加热固体,试管内有红
棕色气体生成,一段时间后,在末端导管口可收
集到无色气体a。
(5)若B中只生成一种盐,则 AgNO 受热分解
3
的化学方程式为
。
(6)上述实验装置存在的安全隐患为 。
19.(14分)我国明确提出2060年实现“碳中和”。因此将CO 转化为高附加值化
2
学品成为重要研究课题。请根据所学知识,回答下列问题。
(1)已知相关化学键的键能数据如下表:
化学键
E/ 436 414 464 326 803
则 CO (g)+3H (g)=CH OH(g)+H O(g) ΔH= KJ·mol-1。
2 2 3 2
(2)利用污泥燃烧产生的还原性气体(NH 、CO等)可还原烟气中的NO 。CO还原
3 x
NO的反应历程中相对能量变化如图1所示:
图1
该历程中最大能垒(活化能)
KJ·mol-1,该步骤的化学方程式是 。
(3)多晶Cu可高效催化CO 甲烷化,电解
2
CO 制备CH 的原理示意图如图2所示。电解
2 4
第一次质量检测化学试题 第 7 页 共8页
学科网(北京)股份有限公司过程中温度控制在10℃左右,持续通入CO 。阴、阳极室的KHCO 溶液的浓度基
2 3
本保持不变。
①多晶Cu作 (填“阴”或“阳”)极,阳极上发生的电极反应式是
。
②阴离子交换膜中传导的离子是 ,移动方向是 (填“从左向
右”或“从右向左”)。 图2
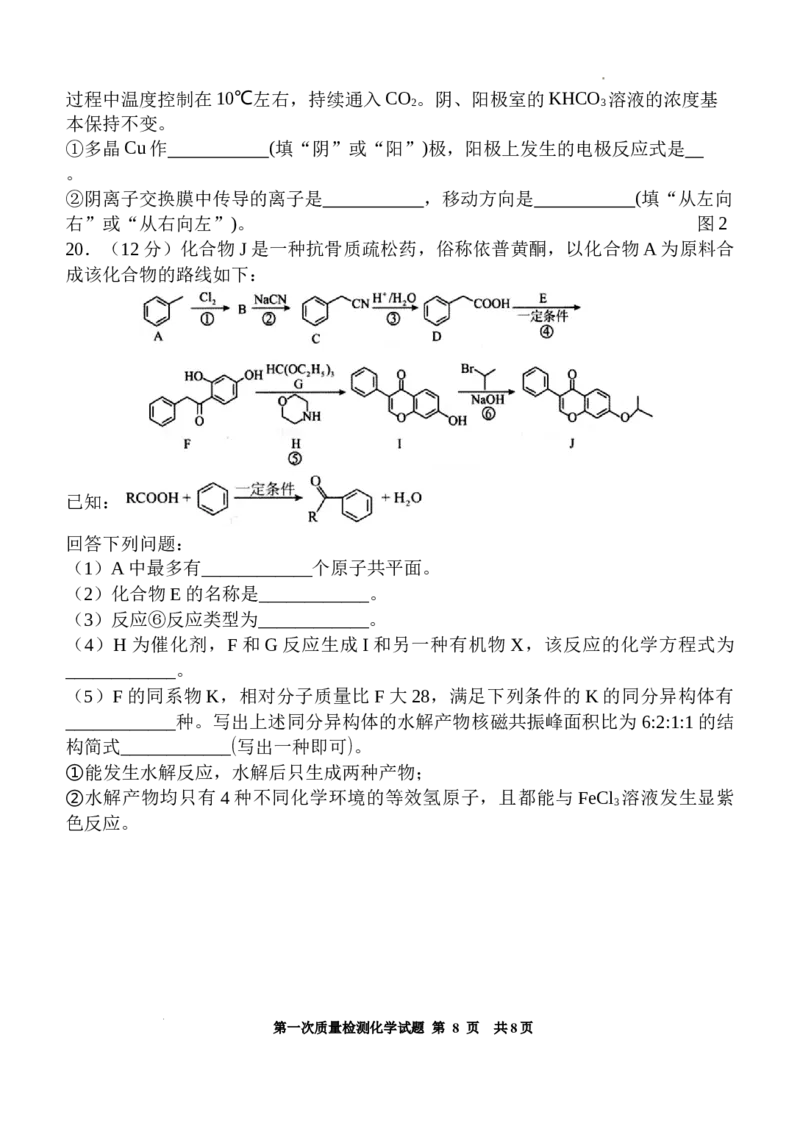
20.(12分)化合物J是一种抗骨质疏松药,俗称依普黄酮,以化合物A为原料合
成该化合物的路线如下:
已知:
回答下列问题:
(1)A中最多有____________个原子共平面。
(2)化合物E的名称是____________。
(3)反应⑥反应类型为____________。
(4)H为催化剂,F和G反应生成I和另一种有机物X,该反应的化学方程式为
____________。
(5)F的同系物K,相对分子质量比F大28,满足下列条件的K的同分异构体有
____________种。写出上述同分异构体的水解产物核磁共振峰面积比为 6:2:1:1的结
构简式____________(写出一种即可)。
①能发生水解反应,水解后只生成两种产物;
②水解产物均只有4种不同化学环境的等效氢原子,且都能与FeCl 溶液发生显紫
3
色反应。
第一次质量检测化学试题 第 8 页 共8页
学科网(北京)股份有限公司