文档内容
A.向NaClO溶液中通入少量SO :2ClO-+SO +H O===2HClO+SO
哈师大青冈实验中学 2024—2025 学年度高三期中考试 2 2 2
B.1molCl 通入含1molFeI 的溶液中:2Fe2++2I-+2Cl ===2Fe3++4Cl-+I
2 2 2 2
化学试题 C.AlCl 溶液中加入过量的浓氨水:Al3++4NH ·H O===[A1(OH) ]- +4NH
3 3 2 4
D.用过量 溶液吸收废气中的
可能用到的相对原子质量:H 1 7 P31 C12 N14 O16 23
S32
6. 易水解,实验室利用 固体配制490mL 溶液。下列说法
35.5 40 56 119
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只 正确的是
有一项是符合题目要求的。 A.配制溶液时500mL容量瓶需要干燥
1.2024年6月25日14时7分,“嫦娥六号”返回器准确着陆于内蒙古四子王旗预定区 B.配制溶液过程中,玻璃棒只起到引流的作用
域,工作正常,这标志着探月工程“嫦娥六号”任务取得圆满成功,实现世界首次月球
C.需用托盘天平称量110.7g 固体
背面采样返回。下列有关说法正确的是
A.制作“嫦娥六号”光学望远镜的高致密碳化硅特种陶瓷属于传统无机非金属材料 D.溶解 固体时需要用浓盐酸代替蒸馏水
B.“嫦娥六号”探测器的壳体材料主要为铝合金,其强度大于纯铝
的
C.“嫦娥六号”所带回的月壤可以通过红外光谱测得所含有的元素种类 7.工业上制备下列物质 生产流程合理的是
D.“嫦娥六号”探测器所使用国产芯片的主要成分为晶体二氧化硅
A.工业制硫酸:硫铁矿 SO SO H SO
2.下列物质按胶体、纯净物、电解质、氧化物的顺序组合的一组为 2 3 2 4
A.氨水、稀盐酸、硫酸、干冰 B.泥水、生石灰、氯化铜、碳酸钠
B.由NaCl制漂白粉:饱和食盐 Cl 漂白粉
2
C.淀粉溶液、蒸馏水、硝酸钾、二氧化硫 D.雾、胆矾、铁、漂白粉
3.下列有关物质的性质和用途说法不正确的是 C.从海水中提取镁:海水 MgO Mg
A.利用高纯单质硅的半导体性能,可以制成光电池
D.工业合成硝酸:N NO NO HNO
2 2 3
B.石灰石在高温下的分解产物可与SO 反应,可用于减少燃煤烟气中的SO
2 2
8.化合物b有美容护肤功效,其合成反应如图所示。下列说法正确的是
C.Na O 与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
A.b的苯环上一氯代物共有5种
D.二氧化硅导电能力强,可用于制造光导纤维
B.a属于芳香烃
4.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.18 g D O和18 g H O中含有的质子数均为10N C.a和b均既能和 溶液反应,又能和 溶液反应
2 2 A
B.常温常压下,124gP 中所含P—P键数目为4N
4 A
D.a、b及苯乙烯均不可以使酸性 溶液褪色
C.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2N
A
D.密闭容器中2 mol NO与1 mol O 充分反应,产物的分子数为2N
2 A 9.下列实验方案能达到实验目的(或所得结论正确)的是
5.下列离子方程式正确的是
化学试题 第 1 页 共 6 页
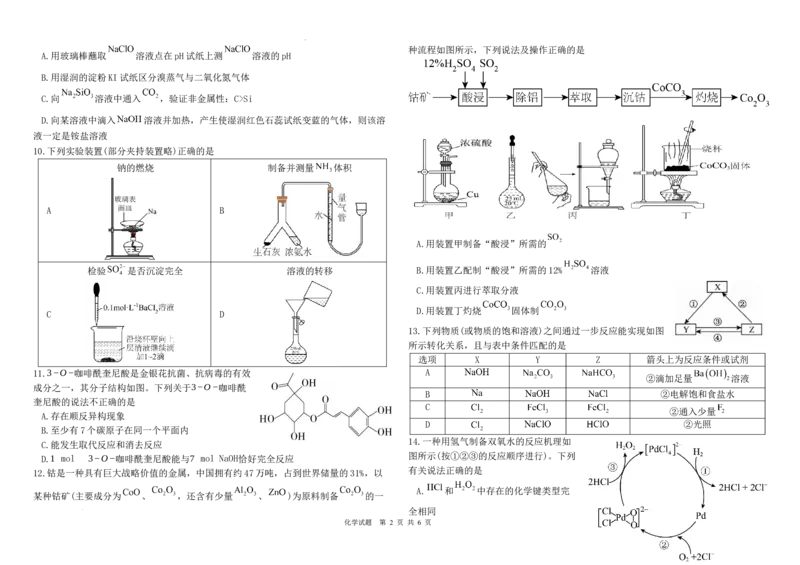
学科网(北京)股份有限公司种流程如图所示,下列说法及操作正确的是
A.用玻璃棒蘸取 溶液点在pH试纸上测 溶液的pH
B.用湿润的淀粉KI试纸区分溴蒸气与二氧化氮气体
C.向 溶液中通入 ,验证非金属性:C>Si
D.向某溶液中滴入 溶液并加热,产生使湿润红色石蕊试纸变蓝的气体,则该溶
液一定是铵盐溶液
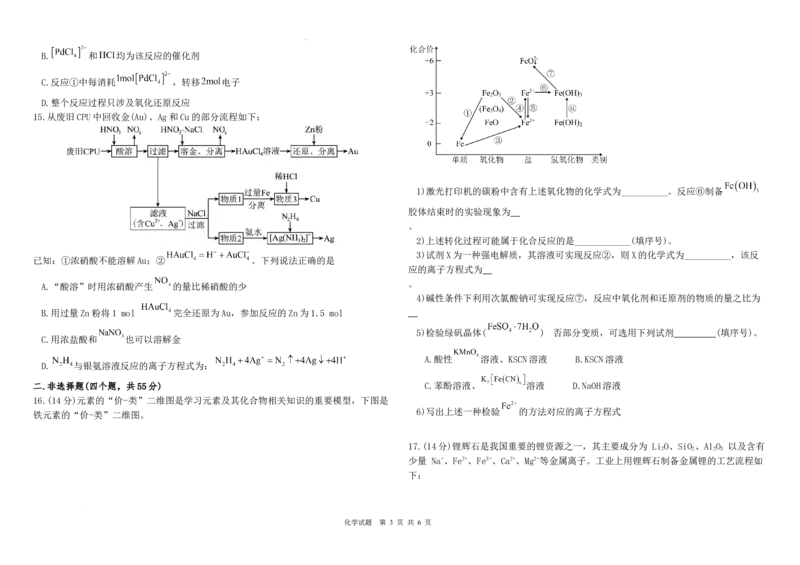
10.下列实验装置(部分夹持装置略)正确的是
钠的燃烧 制备并测量 体积
A B
A.用装置甲制备“酸浸”所需的
检验 是否沉淀完全 溶液的转移 B.用装置乙配制“酸浸”所需的12% 溶液
C.用装置丙进行萃取分液
D.用装置丁灼烧 固体制
C D
13.下列物质(或物质的饱和溶液)之间通过一步反应能实现如图
所示转化关系,且与表中条件匹配的是
选项 X Y Z 箭头上为反应条件或试剂
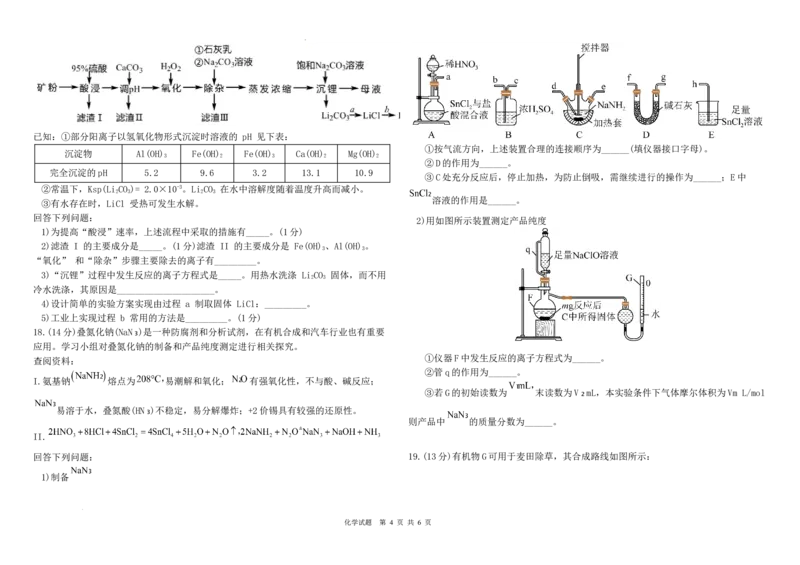
11.3−O−咖啡酰奎尼酸是金银花抗菌、抗病毒的有效 A
②滴加足量 溶液
成分之一,其分子结构如图。下列关于3−O−咖啡酰
B ②电解饱和食盐水
奎尼酸的说法不正确的是
C
②通入少量
A.存在顺反异构现象
D ②光照
B.至少有7个碳原子在同一个平面内
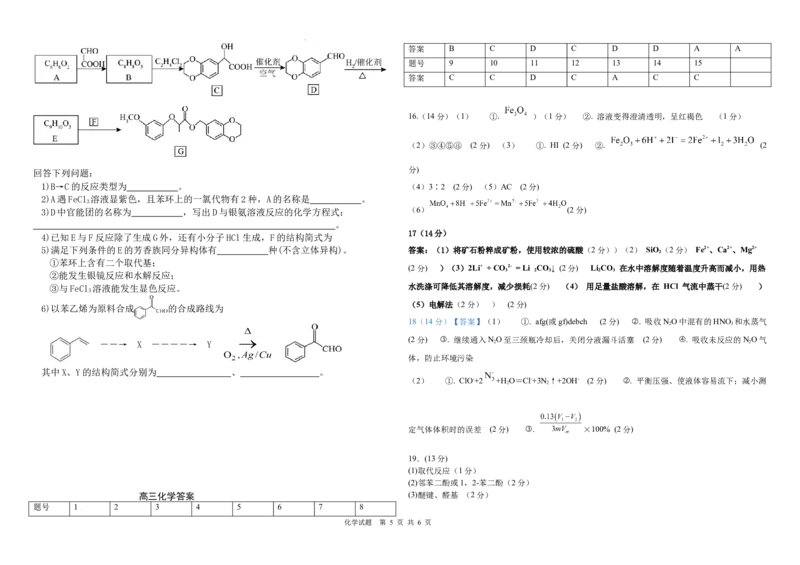
14.一种用氢气制备双氧水的反应机理如
C.能发生取代反应和消去反应
D.1 mol 3−O−咖啡酰奎尼酸能与7 mol NaOH恰好完全反应 图所示(按①②③的反应顺序进行)。下列
有关说法正确的是
12.钴是一种具有巨大战略价值的金属,中国拥有约47万吨,占到世界储量的31%,以
A. 和 中存在的化学键类型完
某种钴矿(主要成分为 、 ,还含有少量 、 )为原料制备 的一
全相同
化学试题 第 2 页 共 6 页
学科网(北京)股份有限公司B. 和 均为该反应的催化剂
C.反应①中每消耗 ,转移 电子
D.整个反应过程只涉及氧化还原反应
15.从废旧CPU中回收金(Au)、Ag和Cu的部分流程如下:
1)激光打印机的碳粉中含有上述氧化物的化学式为__________。反应⑥制备
胶体结束时的实验现象为
。
2)上述转化过程可能属于化合反应的是____________(填序号)。
3)试剂X为一种强电解质,其溶液可实现反应②,则X的化学式为__________,该反
已知:①浓硝酸不能溶解Au;② 。下列说法正确的是
应的离子方程式为
。
A.“酸溶”时用浓硝酸产生 的量比稀硝酸的少
4)碱性条件下利用次氯酸钠可实现反应⑦,反应中氧化剂和还原剂的物质的量之比为
B.用过量Zn粉将1 mol 完全还原为Au,参加反应的Zn为1.5 mol
是
5)检验绿矾晶体( ) 否部分变质,可选用下列试剂 (填序号)。
C.用浓盐酸和 也可以溶解金
A.酸性 溶液、KSCN溶液 B.KSCN溶液
D. 与银氨溶液反应的离子方程式为:
二.非选择题(四个题,共55分) C.苯酚溶液、 溶液 D.NaOH溶液
16.(14分)元素的“价-类”二维图是学习元素及其化合物相关知识的重要模型,下图是
6)写出上述一种检验 的方法对应的离子方程式
铁元素的“价-类”二维图。
17.(14分)锂辉石是我国重要的锂资源之一,其主要成分为 Li O、SiO 、Al O 以及含有
2 2 2 3
少量 Na+、Fe2+、Fe3+、Ca2+、Mg2+等金属离子。工业上用锂辉石制备金属锂的工艺流程如
下:
化学试题 第 3 页 共 6 页
学科网(北京)股份有限公司已知:①部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
①按气流方向,上述装置合理的连接顺序为______(填仪器接口字母)。
沉淀物 Al(OH) Fe(OH) Fe(OH) Ca(OH) Mg(OH)
3 2 3 2 2
②D的作用为______。
完全沉淀的pH 5.2 9.6 3.2 13.1 10.9
③C处充分反应后,停止加热,为防止倒吸,需继续进行的操作为______;E中
②常温下,Ksp(Li CO )= 2.0×10-3。Li CO 在水中溶解度随着温度升高而减小。
2 3 2 3
溶液的作用是______。
③有水存在时,LiCl 受热可发生水解。
回答下列问题:
2)用如图所示装置测定产品纯度
1)为提高“酸浸”速率,上述流程中采取的措施有_____。(1分)
2)滤渣 I 的主要成分是_____。(1分)滤渣 II 的主要成分是 Fe(OH) 、Al(OH) 。
3 3
“氧化” 和“除杂”步骤主要除去的离子有_________。
3)“沉锂”过程中发生反应的离子方程式是_____。用热水洗涤 Li CO 固体,而不用
2 3
冷水洗涤,其原因是_____________________。
4)设计简单的实验方案实现由过程 a 制取固体 LiCl:_________。
5)工业上实现过程 b 常用的方法是_________。(1分)
18.(14分)叠氮化钠(NaN )是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要
₃
应用。学习小组对叠氮化钠的制备和产品纯度测定进行相关探究。
①仪器F中发生反应的离子方程式为______。
查阅资料:
②管q的作用为______。
I.氨基钠 熔点为 易潮解和氧化; 有强氧化性,不与酸、碱反应;
③若G的初始读数为 末读数为V mL,本实验条件下气体摩尔体积为Vm L/mol
₂
易溶于水,叠氮酸(HN )不稳定,易分解爆炸;+2价锡具有较强的还原性。
₃
则产品中 的质量分数为______。
II.
回答下列问题: 19.(13分)有机物G可用于麦田除草,其合成路线如图所示:
1)制备
化学试题 第 4 页 共 6 页
学科网(北京)股份有限公司答案 B C D C D D A A
题号 9 10 11 12 13 14 15
答案 C C D C A C C
16.(14分)(1) ①. )(1分) ②. 溶液变得澄清透明,呈红褐色 (1分)
(2)③④⑤⑧ (2分) (3) ①. HI (2分) ②. (2
分)
回答下列问题:
1)B→C的反应类型为 。 (4)3∶2 (2分) (5)AC (2分)
2)A遇FeCl 溶液显紫色,且苯环上的一氯代物有2种,A的名称是 。
3
3)D中官能团的名称为 ,写出D与银氨溶液反应的化学方程式: (6) (2分)
。
17(14分)
4)已知E与F反应除了生成G外,还有小分子HCl生成,F的结构简式为
5)满足下列条件的E的芳香族同分异构体有 种(不含立体异构)。 答案:(1)将矿石粉粹成矿粉,使用较浓的硫酸(2分))(2) SiO (2分) Fe2+、Ca2+、Mg2+
2
①苯环上含有二个取代基;
(2分) )(3)2Li+ + CO 2- = Li CO ↓ (2分) LiCO 在水中溶解度随着温度升高而减小,用热
3 2 3 2 3
②能发生银镜反应和水解反应;
③与FeCl 溶液能发生显色反应。 水洗涤可降低其溶解度,减少损耗(2分) (4) 用足量盐酸溶解,在 HCl 气流中蒸干(2分) )
3
(5)电解法(2分) ) (2分)
6)以苯乙烯为原料合成 的合成路线为
18(14分)【答案】(1) ①. afg(或gf)debch (2分) ②. 吸收NO中混有的HNO 和水蒸气
2 3
(2分) ③. 继续通入NO至三颈瓶冷却后,关闭分液漏斗活塞 (2分) ④. 吸收未反应的NO气
――→ X ――――→ Y 2 2
体,防止环境污染
其中X、Y的结构简式分别为 、 。
(2) ①. ClO-+2 +H O=Cl-+3N ↑+2OH- (2分) ②. 平衡压强、使液体容易流下;减小测
2 2
定气体体积时的误差 (2分) ③. ×100% (2分)
19.(13分)
(1)取代反应(1分)
(2)邻苯二酚或1,2-苯二酚(2分)
高三化学答案 (3)醚键、醛基 (2分)
题号 1 2 3 4 5 6 7 8
化学试题 第 5 页 共 6 页
学科网(北京)股份有限公司+2[Ag(NH )]OH +2Ag↓+3NH+H O(2分)
3 2 3 2
(4) (2分)
(5)6(2分)
(6) (1分) (1分)
化学试题 第 6 页 共 6 页
学科网(北京)股份有限公司