文档内容
黑龙江省实验中学2024-2025学年度高三学年上学期第三次月考考试
化学学科试卷
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H-1 C-12 O-16 Cu-64
一、选择题(每道小题只有一个正确选项。每题3分,共45分)
1.化学与生活生产密切相关,下列说法不正确的是( )
A. 向TiCl 中加入大量的水,同时加热,促进水解趋于完全,所得沉淀经过滤、焙烧得到TiO
4 2
B. 晶体硅光伏发电将太阳能转化为电能为亚冬会场馆供电
C. 用NaCO 与Al (SO ) 两种溶液制作泡沫灭火剂
2 3 2 4 3
D. 空间站存储器所用的材料石墨烯与C 互为同素异形体
60
2.N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.1.0LpH=2的HSO 溶液中H+的数目为0.02N
2 4 A
B.电解法粗铜精炼,阳极减重6.4g,外电路中通过电子的数目为0.20 N
A
C.常温下,1L0.1mol/L的CHCOONa溶液中,CHCOO-的数目为0.1 N
3 3 A
D.1molCl 与足量的NaOH溶液完全反应后,溶液中ClO-、Cl-和HClO的总数为2N
2 A
3. 下列离子方程式正确的是( )
A.向氨水中滴入少量硝酸银溶液:Ag+ + 2NH ·H O===Ag(NH )++ 2HO
3 2 3 2 2
B.0.1mol·L-1 KHC O 的水解方程式:HC O- + HO C O2- + HO+
2 4 2 4 2 2 4 3
C.NaSO 溶液中加入稀硫酸:SO+ SO 2- + 4H+===2SO ↑ + S↓ + HO
2 2 3 2 4 2 2
D.将少量SO 通入NaClO溶液:SO + HO + ClO- === HSO - + HClO
2 2 2 3
4.下列说法正确的是( )
① ② ③ ④
A.图①由MgCl ·6H O制取无水MgCl 固体
2 2 2
B.图②操作可排出盛有KCr O 溶液滴定管尖嘴内的气泡
2 2 7
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④测定中和热
5.PtF 是极强的氧化剂,用Xe和PtF 可制备六氟合铂酸氙[XeF]+[Pt F ]-,制备方式如图所示。下列说
6 6 2 11
法不正确的是 ( )
A.六氟合铂酸氙是离子化合物
B.六氟合铂酸氙中Xe元素的化合价为+2价
C.上述制备过程的催化剂是F-和PtF
D.上述制备过程中属于氧化还原反应的有②③
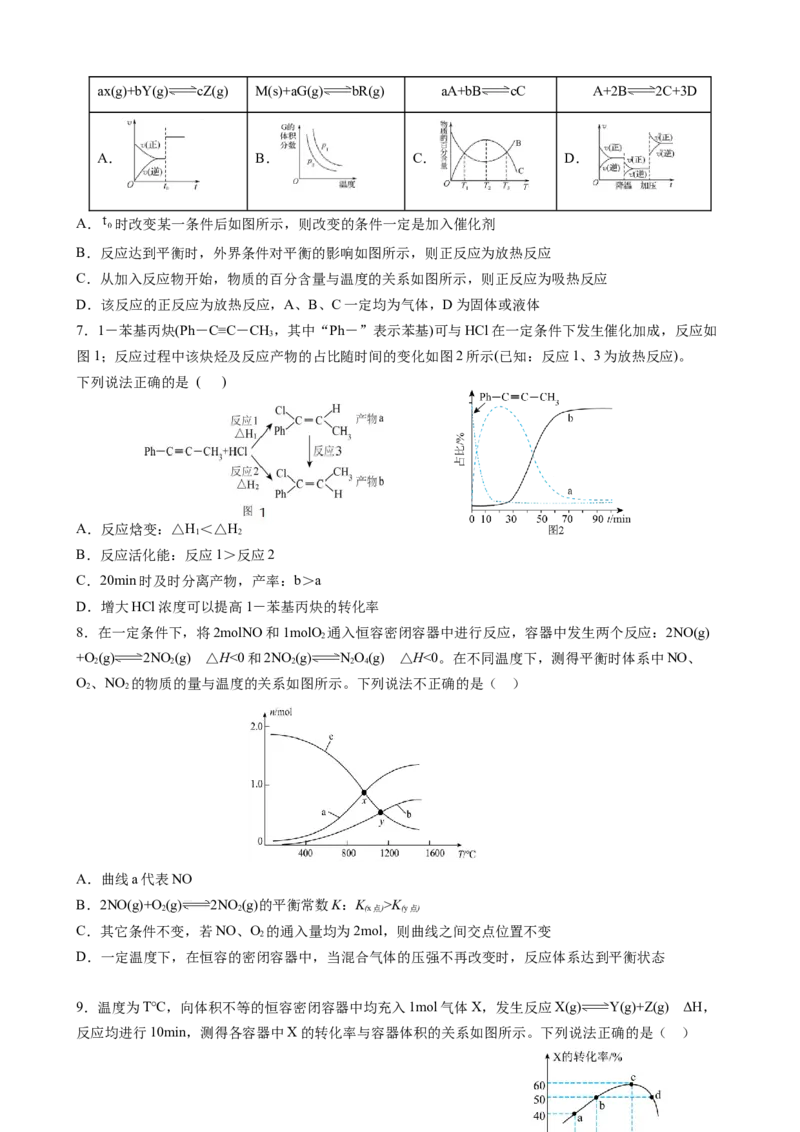
6.根据相应的图象(图象编号与选项一一对应),判断下列相关说法正确的是( )ax(g)+bY(g) cZ(g) M(s)+aG(g) bR(g) aA+bB cC A+2B 2C+3D
A. B. C. D.
A. 时改变某一条件后如图所示,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡的影响如图所示,则正反应为放热反应
C.从加入反应物开始,物质的百分含量与温度的关系如图所示,则正反应为吸热反应
D.该反应的正反应为放热反应,A、B、C一定均为气体,D为固体或液体
7.1-苯基丙炔(Ph-C≡C-CH,其中“Ph-”表示苯基)可与HCl在一定条件下发生催化加成,反应如
3
图1;反应过程中该炔烃及反应产物的占比随时间的变化如图2所示(已知:反应1、3为放热反应)。
下列说法正确的是 ( )
A.反应焓变:△H<△H
1 2
B.反应活化能:反应1>反应2
C.20min时及时分离产物,产率:b>a
D.增大HCl浓度可以提高1-苯基丙炔的转化率
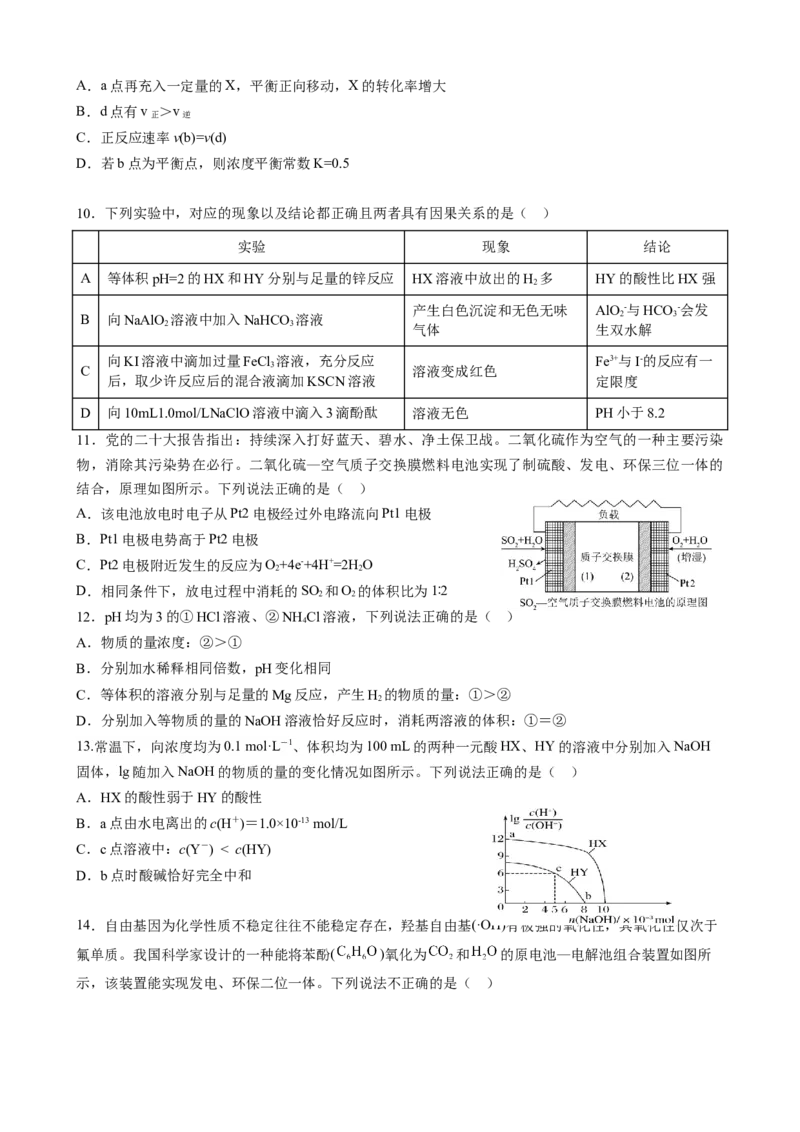
8.在一定条件下,将2molNO和1molO 通入恒容密闭容器中进行反应,容器中发生两个反应:2NO(g)
2
+O (g) 2NO (g) △H<0和2NO (g) NO(g) △H<0。在不同温度下,测得平衡时体系中NO、
2 2 2 2 4
O、NO 的物质的量与温度的关系如图所示。下列说法不正确的是( )
2 2
A.曲线a代表NO
B.2NO(g)+O (g) 2NO (g)的平衡常数K:K >K
2 2 (x点) (y点)
C.其它条件不变,若NO、O 的通入量均为2mol,则曲线之间交点位置不变
2
D.一定温度下,在恒容的密闭容器中,当混合气体的压强不再改变时,反应体系达到平衡状态
9.温度为T℃,向体积不等的恒容密闭容器中均充入1mol气体X,发生反应X(g) Y(g)+Z(g) ΔH,
反应均进行10min,测得各容器中X的转化率与容器体积的关系如图所示。下列说法正确的是( )A.a点再充入一定量的X,平衡正向移动,X的转化率增大
B.d点有v >v
正 逆
C.正反应速率v(b)=v(d)
D.若b点为平衡点,则浓度平衡常数K=0.5
10.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
实验 现象 结论
A 等体积pH=2的HX和HY分别与足量的锌反应 HX溶液中放出的H 多 HY的酸性比HX强
2
产生白色沉淀和无色无味 AlO-与HCO -会发
B 向NaAlO 溶液中加入NaHCO 溶液 2 3
2 3 气体 生双水解
向KI溶液中滴加过量FeCl 溶液,充分反应 Fe3+与I-的反应有一
C 3 溶液变成红色
后,取少许反应后的混合液滴加KSCN溶液 定限度
D 向10mL1.0mol/LNaClO溶液中滴入3滴酚酞 溶液无色 PH小于8.2
11.党的二十大报告指出:持续深入打好蓝天、碧水、净土保卫战。二氧化硫作为空气的一种主要污染
物,消除其污染势在必行。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的
结合,原理如图所示。下列说法正确的是( )
A.该电池放电时电子从Pt2电极经过外电路流向Pt1电极
B.Pt1电极电势高于Pt2电极
C.Pt2电极附近发生的反应为O+4e-+4H+=2H O
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为1∶2
2 2
12.pH均为3的①HCl溶液、②NH Cl溶液,下列说法正确的是( )
4
A.物质的量浓度:②>①
B.分别加水稀释相同倍数,pH变化相同
C.等体积的溶液分别与足量的Mg反应,产生H 的物质的量:①>②
2
D.分别加入等物质的量的NaOH溶液恰好反应时,消耗两溶液的体积:①=②
13.常温下,向浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中分别加入NaOH
固体,lg随加入NaOH的物质的量的变化情况如图所示。下列说法正确的是( )
A.HX的酸性弱于HY的酸性
B.a点由水电离出的c(H+)=1.0×10-13 mol/L
C.c点溶液中:c(Y-) < c(HY)
D.b点时酸碱恰好完全中和
14.自由基因为化学性质不稳定往往不能稳定存在,羟基自由基(·OH)有极强的氧化性,其氧化性仅次于
氟单质。我国科学家设计的一种能将苯酚( )氧化为 和 的原电池—电解池组合装置如图所
示,该装置能实现发电、环保二位一体。下列说法不正确的是( )A.该装置工作时,电流方向为电极b→Ⅲ室→Ⅱ室→Ⅰ室→电极a··· ··· →电极b
B.当电极a上有1molCr(OH) 生成时,c极区溶液呈碱性
3
C.电极d的电极反应为HO - e- = H++·OH
2
D.当电极b上有 生成时,电极c、d两极共产生气体22.4L(标准状况)
15.已知HA的电离常数分别用Ka、Ka 表示,水的离子积常数为K 。25 ℃时,向1 L 0.01 mol·L-1
2 1 2 W
HA溶液中滴加NaOH溶液,溶液中c(HA)、c(HA-)、c(A2-)、c(OH-)、c(H+)的负对数值(-lg c)与pH
2 2
的关系如图所示。下列说法不正确的是( )
A.a线代表的微观粒子是H+
B.HA的Ka=1×10-9
2 2
C.25 ℃时,NaHA溶液中Kw < Ka ·Ka
1 2
D.M点溶液中c(Na+)+c(H+)-c(A2-)=0.01 mol/L
二、填空题(共55分)
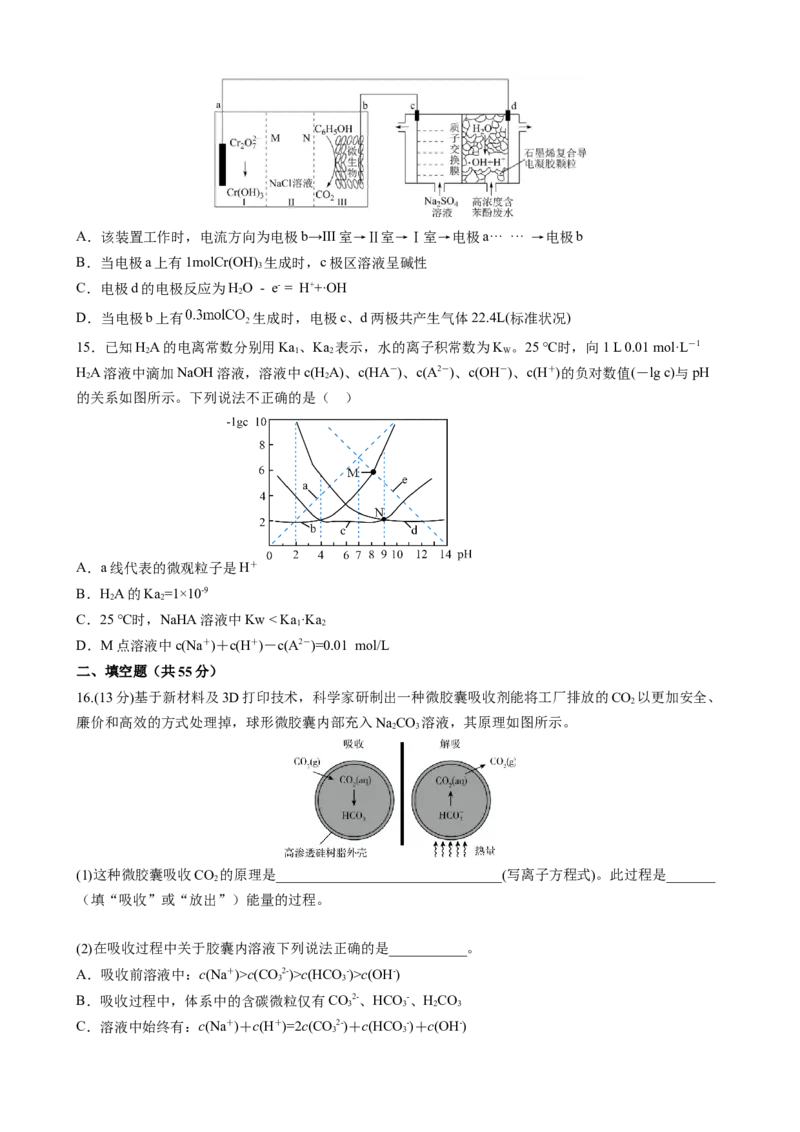
16.(13分)基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的CO 以更加安全、
2
廉价和高效的方式处理掉,球形微胶囊内部充入NaCO 溶液,其原理如图所示。
2 3
(1)这种微胶囊吸收CO 的原理是________________________________(写离子方程式)。此过程是_______
2
(填“吸收”或“放出”)能量的过程。
(2)在吸收过程中关于胶囊内溶液下列说法正确的是___________。
A.吸收前溶液中:c(Na+)>c(CO2-)>c(HCO -)>c(OH-)
3 3
B.吸收过程中,体系中的含碳微粒仅有CO2-、HCO -、HCO
3 3 2 3
C.溶液中始终有:c(Na+)+c(H+)=2c(CO2-)+c(HCO -)+c(OH-)
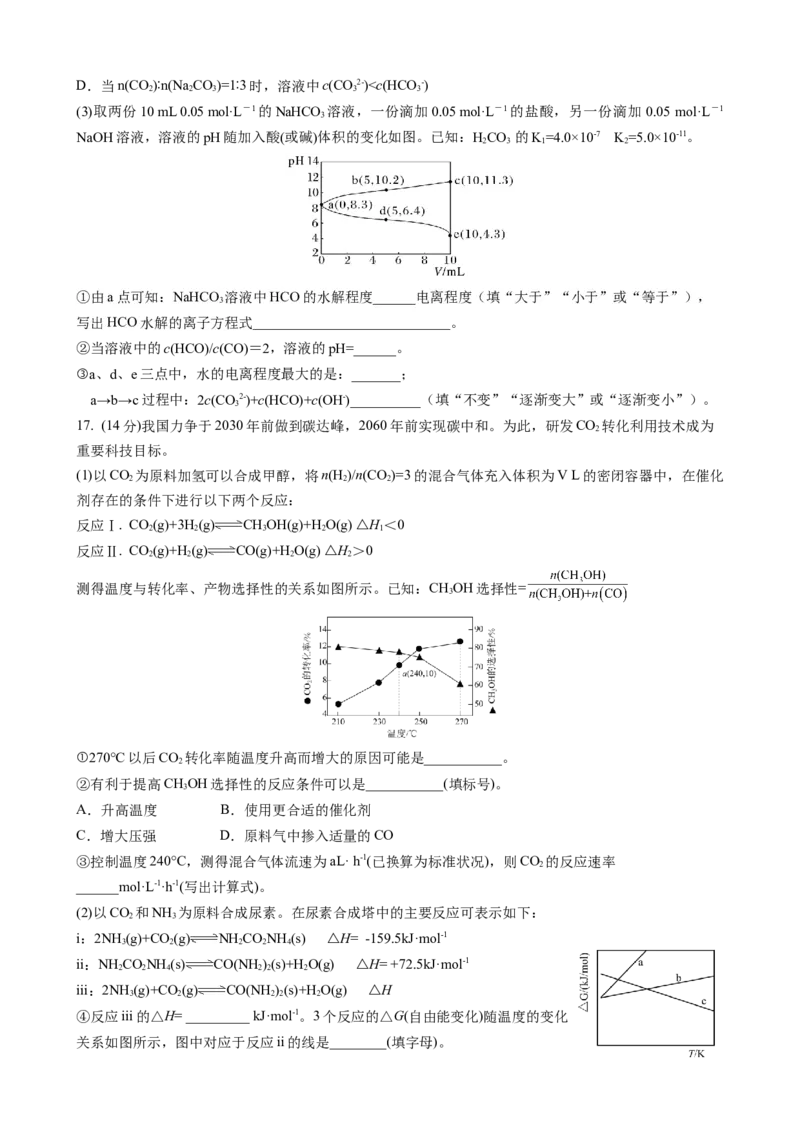
3 3D.当n(CO)∶n(Na CO)=1∶3时,溶液中c(CO2-)